Цель работы
Валидационная оценка методикиопределения глицина и кислоты янтарной в таблетках ноотропного действия методом капиллярного электрофореза.
Материалы и методы исследования
Для исследования использовали образцы таблеток разрабатываемого препарата ноотропного действия «Гинкготропил-форте» (экспериментальная серия от 27.11.14); субстанции глицина с количественным содержанием 99,5% (WIRUD®GL10001, производитель WIRUDGmbH, Германия), кислоты янтарной с содержанием 99,7% (HuanlongFoodAdditivesCorporation, Китай), а также сухие экстракты гинкго двулопастного и лабазника вязолистного [2].
Работа проводилась с использованием системы капиллярного электрофореза Капель 105 (группа компаний Люмэкс, Россия). Рабочие параметры прибора: кварцевый капилляр диаметром 75 мкм, общей длинной 60 см и эффективной длинной 50 см;детектирование осуществляли спектрофотометрически при длине волны равной 200 нм в катодной области капилляра;напряжение +20 кВ, температура опыта 30°С; ввод пробы гидродинамически 150 мБар×с; давление, прикладываемое при анализе 10 мБар.Ведущий электролит0,01 М боратный буферный раствор с рН 9.Для подготовки капилляра и восстановления его поверхности проводили его последовательную промывку водой, 0,5 М раствором кислоты хлористоводородной, водой, 0,5 М раствором натрия гидроксида, водой и затем ведущим электролитом [1–3].
Методика: около 0,2 г (точная навеска) массы растертых таблеток (модельной смеси) помещают в мерную колбу вместимостью 100 мл, растворяют в небольшом количестве воды очищенной в течение 10 минут, доводят объем раствора до метки тем же растворителем и перемешивают. 1 мл полученного раствора центрифугируют в течение 5 минут при 8000 мин-1 и подвергают анализу, прикладывая по ходу эксперимента давление 10 мБар. В аналогичных условиях выполняют анализ растворов стандартных образцов (СО) глицина и кислоты янтарной. Расчет содержания глицина и кислоты янтарной проводили по формуле:
![]()
где: ![]() – площадь исследуемого вещества;
– площадь исследуемого вещества;
![]() – площадь стандартного образца;
– площадь стандартного образца;
![]() – навескастандартного образца, г;
– навескастандартного образца, г;
![]() – навеска испытуемого образца, г;
– навеска испытуемого образца, г;
![]() – средняя масса таблеток, г.
– средняя масса таблеток, г.
Приготовление растворов стандартных образцов и модельных смесей таблеток
Точные навески глицина (0,1000 г) и кислоты янтарной (0,0200 г) помещали в мерную колбу вместимостью 100 мл, растворяли 50–60 мл воды и доводили используемым растворителем до метки.
Для построенияградуировочного графика использовали растворы СО следующих концентраций: глицин – 0,0250%; 0,0500%; 0,1000%; 0,1500%; 0,2000%; кислота янтарная – 0,0050%; 0,0100%; 0,0200%; 0,0300%; 0,0400%.
Модельные смеси таблеток готовили согласно данным, приведенным в таблице 1.
Таблица 1
Состав модельных смесей таблеток
|
Модельная смесь |
Содержание анализируемых веществ |
Содержание других компонентов в модельных смесях |
|
|
Глицин, г |
Янтарная кислота, г |
||
|
1 |
Нет |
Нет |
Экстракт гинкго двулопастного сухого, экстракт лабазника вязолистного сухого и вспомогательных веществ до массы 0,2100 г |
|
2 |
0,0800 |
0,0400 |
|
|
3 |
0,1000 |
0,0200 |
|
|
4 |
0,1200 |
0,0100 |
|
Результаты исследований и их обсуждение
Валидационную оценку разработанной методики устанавливали по показателям: специфичность, линейность, прецизионность и правильность.
Специфичность методики определяли, сравнивая раствор СО глицина и кислоты янтарной с раствором модельной смеси 1(табл. 1) и раствором экспериментальной серии таблеток. Было установлено, что время миграции глицина и кислоты янтарной в экспериментальной серии таблеток соответствует времени СО данных веществ.Присутствующие в экстрактах гинкго и лабазника биологически активные веществаи вспомогательные вещества таблетокне мешают определению глицина и кислоты янтарной (рис. 1, Б). Полученные данные говорят о специфичности методики.

Рис.1. Элетрофореграмы растворов: А – раствор СО глицина(1) и кислоты янтарной(2);
Б – раствор модельной смеси 1; В – раствор экспериментальной серии таблеток
Линейность методикиопределялипо результатам анализа серии растворов СО глицина в интервале концентраций 0,0025–0,2000% и янтарной кислоты 0,0050–0,0400%. На рисунках 2 и 3 представлены графики зависимости площади пика исследуемых веществ от их концентраций в пробе. Полученная зависимость имеет линейный характер и описывается уравнениями регрессии: y = 259,23x + 0,9116 (глицин) и y = 1264,3x - 0,0842 (янтарная кислота). Критерием приемлемости линейности является коэффициент корреляции (r ≥ 0,99), который составил для глицина и кислоты янтарной0,9991 и 0,9990соответственно[5].
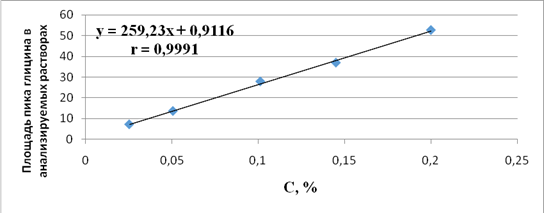
Рис.2. График зависимости площади пика от концентрации глицина в пробе
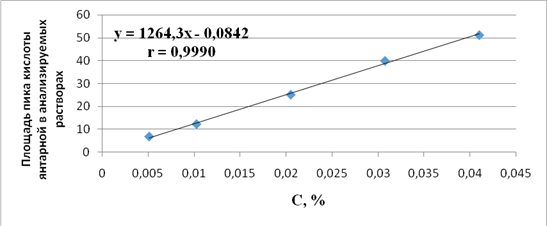
Рис.3. График зависимости площади пика от концентрации янтарной кислоты в пробе
Таким образом, методика валидна по критерию линейность и может быть использована для количественного определения глицина и янтарной кислоты в препарате «Гинкготропил-форте» в указанном диапазоне концентраций.
Для установления прецизионности (сходимости) методики количественного определения глицина и кислоты янтарной, проводили 6 параллельных определений этих компонентов в таблетках «Гинкготропил-форте» экспериментальной серии от 27.11.14. Расчет содержания (г/табл.) проводили с использованием СО. Полученные результаты приведены в таблице 2.
Таблица 2
Результаты оценкипрецизионностиметодики количественного определения
глицина и янтарной кислоты
|
Взято |
Найдено |
|||||
|
Масса таблеток, г |
Глицин |
Кислота янтарная |
||||
|
Площади пиков |
Х, г/табл. |
Метрологические характеристики |
Площади пиков |
Х, г/табл. |
Метрологические характеристики |
|
|
0,2131 0,2096 0,2109 0,2137 0,2082 0,2090 |
22,97 22,67 22,88 22,83 22,15 22,19 |
0,0970 0,1020 0,1000 0,0970 0,0980 0,0980 |
SD = 0,002 RSD= ±1,99% |
25,06 24,98 26,34 26,28 25,95 26,39 |
0,0195 0,0198 0,0201 0,0200 0,0210 0,0200 |
SD = 0,001 RSD= ±2,51% |
Критерий приемлемости, выражаемый через величину относительного стандартного отклонения (RSD,%), составляющий ±1,99% (глицин) и ±2,51% (кислота янтарная), удовлетворяет требованиям по параметру сходимости, что свидетельствует о валидностиданной методики по показателюпрецизионность [5].
Правильность методики определяли путем анализа 9 образцов модельных смесей на трех уровнях концентраций. Оценку правильности проводили по параметру «открываемость»(R, %). Полученные результаты представлены в таблицах 3,4.
Таблица 3
Результаты оценки правильности методики количественного определения глицина в модельной смеси таблеток
|
Глицин |
|||||
|
Уровень |
Навеска*, г
|
Содержание в модельной смеси, г |
Найдено, г |
R,% |
Метрологические характеристики |
|
1 |
0,2013 |
0,0800 |
0,0805 |
100,63 |
SD = 1,33% RSD = ±1,34% |
|
1 |
0,2062 |
0,0800 |
0,0791 |
98,88 |
|
|
1 |
0,2030 |
0,0800 |
0,0802 |
100,25 |
|
|
2 |
0,2036 |
0,1000 |
0,0975 |
97,50 |
|
|
2 |
0,2101 |
0,1000 |
0,0991 |
99,10 |
|
|
2 |
0,2056 |
0,1000 |
0,1017 |
101,70 |
|
|
3 |
0,2068 |
0,1200 |
0,1192 |
99,33 |
|
|
3 |
0,2109 |
0,1200 |
0,1217 |
101,42 |
|
|
3 |
0,2090 |
0,1200 |
0,1205 |
100,42 |
|
Таблица 4
Результаты оценки правильности методики количественного определениякислоты янтарной в модельной смеси таблеток
|
Кислота янтарная |
|||||
|
Уровень |
Навеска*, г
|
Содержание в модельной смеси, г |
Найдено, г |
R,% |
Метрологические характеристики |
|
1 |
0,2013 |
0,0100 |
0,0098 |
98,00 |
SD = 2,88% RSD = ±2,89% |
|
1 |
0,2062 |
0,0100 |
0,0102 |
102,00 |
|
|
1 |
0,2030 |
0,0100 |
0,0099 |
99,00 |
|
|
2 |
0,2036 |
0,0200 |
0,0198 |
99,00 |
|
|
2 |
0,2101 |
0,0200 |
0,0192 |
96,00 |
|
|
2 |
0,2056 |
0,0200 |
0,0210 |
105,00 |
|
|
3 |
0,2068 |
0,0400 |
0,0394 |
98,50 |
|
|
3 |
0,2109 |
0,0400 |
0,0389 |
97,25 |
|
|
3 |
0,2090 |
0,0400 |
0,0410 |
102,50 |
|
*Навески: 1–3 – модельная смесь 2; 4–6 – модельная смесь 3; 7–9 – модельная смесь 4 (см. табл.2)
Полученные результаты свидетельствуют, что значения открываемости для обоих веществнаходятся в пределах для глицина 95–105% и янтарной кислоты 90–107%, что согласно общепринятым рекомендациям свидетельствует о валидности методики по данному показателю [5].
Выводы
Методика определения глицина и кислоты янтарной методом капиллярного электрофореза валидна по показателям: специфичность, линейность, прецизионность, правильность и может быть использована для включения в нормативно-техническую документацию на разрабатываемый препарат в разделы «Подлинность», «Количественное определение» проекта ФСП «Таблетки “Гинкготропил-форте”сублингвальные».
Рецензенты:Лазарян Д.С., д.фарм.н., профессор, зав. кафедрой фармацевтической и токсикологической химии ПМФИ – филиала ГБОУ ВПО ВолгГМУ Минздрава России, г.Пятигорск;
Кодониди И.П., д.фарм.н., доцент кафедры органической химии ПМФИ – филиала ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск.
Библиографическая ссылка
Крылов Н.Н., Сенченко С.П., Компанцева Е.В. ВАЛИДАЦИОННАЯ ОЦЕНКА МЕТОДИКИ ОПРЕДЕЛЕНИЯ ГЛИЦИНА И КИСЛОТЫ ЯНТАРНОЙ В ТАБЛЕТКАХ НООТРОПНОГО ДЕЙСТВИЯ МЕТОДОМ КАПИЛЛЯРНОГО ЭЛЕКТРОФОРЕЗА // Современные проблемы науки и образования. 2015. № 2-2. ;URL: https://science-education.ru/ru/article/view?id=22761 (дата обращения: 18.04.2026).



