Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
THE INFLUENCE OF DEPRESSION ON METABOLIC SYNDROME AND IHD DEVELOPMENT AT PATIENTS OF SENIOR AGE GROUPS
Введение. Метаболический синдром (МС) – комплекс патогенетически взаимосвязанных метаболических и сердечно-сосудистых нарушений, включающих инсулинорезистентность (ИР), нарушение толерантности к глюкозе (НТГ), сахарный диабет (СД), артериальную гипертензию (АГ), сочетающихся с абдоминальным ожирением и атерогенной дислипидемией [1; 4; 7]. В настоящее время установлено, что через 10-20 лет после начала метаболического синдрома развивается и прогрессирует атеросклероз – в дальнейшем возможны такие осложнения, как инфаркт и инсульт. Согласно современным данным, коморбидность депрессии и тревоги с сердечно-сосудистой патологией составляет от 20 до 70% пациентов: у 17-27% пациентов с ишемической болезнью сердца (ИБС), проходящих процедуру коронарной ангиографии, выявляются депрессии, а у больных после инфаркта миокарда (ИМ) депрессии обнаруживаются в 16-45% случаев [9]. Депрессия является таким же важным фактором риска сердечно-сосудистых болезней и их осложнений, в т.ч. и смертности, как и курение, гипертензия, ожирение и гиперхолестеринемия [6; 8]. Смертность при депрессии выше в 2-3 раза. Таким образом, понимание патофизиологических механизмов, которые могут способствовать развитию метаболического синдрома, крайне важно для клинической медицины.
Цель исследования: изучение влияния уровня кортизола на фоне депрессий на распространенность МС и скорость формирования ИБС у пациентов старших возрастных групп.
Материал и методы исследования. Всего было обследовано 189 пациентов с депрессией (I группа) и 216 – без признаков депрессии (II группа) в возрасте от 56 до 79 лет, средний возраст 68,2±8,5 лет, среди них 188 женщин и 217 мужчин. Для выявления распространенности и глубины депрессивных расстройств среди пациентов старших возрастных групп использовалась шкала самооценки Цунга. Среди них были 48 пациентов с легкой формой депрессии (50-59 баллов), 76 человек с умеренной депрессией (60-69баллов), у 65 пациентов по шкале Цунга было 70 баллов и более, что соответствовало выраженной депрессии. Наличие депрессии подтверждалось врачами-специалистами по критериям МКБ10.
Метаболический синдром ставился на основании рабочих критериев экспертов ционального института здоровья США (Adult Treatment Panel III)., 2001 г.: АГ ≥ 130/85 мм рт. ст., объем талии >102 см для мужчин, >89 см для женщин, триглицериды ≥1,69 ммоль/л и/или ХС ЛПВП <1,04 ммоль/л для мужчин, и <1,29 ммоль/л для женщин, глюкоза натощак >6,1ммоль/л.
Уровень кортизола определялся с помощью электрохемилюминесцентного анализатора Elecsys (Hoffmann-La Roche, Швейцария, (норма: утро 171-536 нмоль/л, вечер 64-327 нмоль/л, чувствительность метода – 0,5 нмоль/л).
Основным методом обследования являлся метод клинического анализа. Все пациенты обследовались по методикам, предусмотренным стандартами обследования пациентов с ИБС и МС. При определении дислипидемических нарушений общий холестерин (ОХ), холестерин липопротеидов высокой плотности (ХС ЛПВП), ТГ определяли на биохимическом анализаторе крови CardioChek P•A. Концентрация ХС ЛПНП рассчитывалась нами у пациентов по формуле Фридвальда (Fridwald W., 1972), при условии, что концентрация ТГ в крови не превышает 4,5 ммоль/л. Кроме этого, мы определяли индекс атерогенности, который рассчитывался по формуле: ИА= ОХС/ХС ЛПВП, при этом ИА>5 расценивался нами, согласно рекомендациям ВНОК, как дислипидемия.
Инструментальная диагностика сердечно-сосудистой патологии включала следующие методы исследования: суточное мониторирование ЭКГ по Холтеру, эхокардиографию, компьютерную коронарографию на 16-срезовом мультиспиральном компьютерном томографе (МСКТ) фирмы Siemens Somatom Emocion 16 (Германия) с определением кальциевого индекса по методу Agatson [5], для интерпретации содержания фосфата кальция в бляшках коронарных артерий использовался метод H. Yoon и соавт. (1996) [10].
Статистическая обработка данных проводилась с помощью пакета прикладных программ Statistica for Windous 7.0. Результаты изучения полученных вариационных рядов были представлены в виде средней арифметической величины (М) с учетом средней ошибки средней арифметической (m) – M±m. При определении достоверности полученных результатов использовался критерий Стъюдента. Статистические результаты считались достоверными при p<0,05.
Полученные результаты и их обсуждение. Анализ медицинских карт и данных анамнеза 405 больных позволил сделать вывод о том, что у пациентов на фоне депрессии как МС, так и ИБС прогрессируют значительно быстрее, чем в группе сравнения (рис. 1).
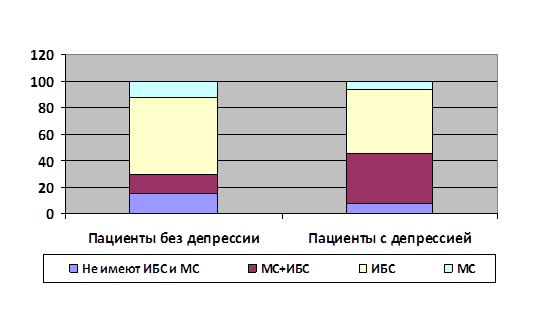
Рис. 1. Доля МС, ИБС и сочетанной патологии в структуре заболеваемости пациентов обследованных групп.
Развитию и прогрессированию МС у пациентов первой группы способствовал тот факт, что на фоне депрессии возникало повышение уровня кортизола, в среднем по группе до 769,5 ± 56,8 нмоль/л,. Известно, что кортизол стимулирует кортизолзависимую липопротеиновую липазу (ЛПЛ) на капиллярах жировых клеток верхней половины туловища, брюшной стенки и висцерального жира (кортизолзависимая жировая ткань). В результате увеличивается отложение жира, развивается гипертрофия жировых клеток и столь характерное абдоминальное ожирение [2], которое у пациентов первой группы наблюдалось у 85 человек (45,0% обследованных), в то время как среди пациентов группы сравнения МС лишь у 26,4% обследованных. Кроме этого, кортизол принимает непосредственное участие в развитии инсулинорезистентности, так как значительно уменьшает чувствительность тканей к действию инсулина. При этом уменьшается инсулинобусловленный транспорт глюкозы в клетки, тормозится пострецепторная утилизация глюкозы, что подавляет активность вторичных мессенджеров инсулина, усиливается распад гликогена в печени, в связи с чем у больных повышается уровень сахара в крови и еще больше усиливаются процессы формирования инсулинорезистентности [3]. По-видимому, эти процессы стали одним из факторов относительного роста диабета II типа по сравнению с нарушением толерантности к глюкозе в структуре МС у пациентов первой группы. Так, соотношение между пациентами с МС, страдающими сахарным диабетом II типа и нарушением толерантности к глюкозе, в первой группе составило 72,5 и 27,5%, а в группе сравнения 36,6 и 63,4% соответственно (р1,2<0,001). Кроме этого, в первой группе чаще встречались сочетанные поражения (МС + ИБС), чем у лиц II группы с нормальным содержанием кортизола (213,6 ± 26,9 нмоль/л) -38,1 и 13,9% (р<0,001), соответственно. Возможно, более частое развитие сочетанных нарушений (МС + ИБС) у лиц первой группы было связано с тем, что избыток инсулина не только усиливает синтез холестерина (ХС), липопротеинов низкой и очень низкой плотности (ЛПНП, ЛПОНП), но и существенно тормозит процессы липолиза. Вызывая существенные количественные и, что немаловажно, качественные изменения липопротеиновых молекул, гиперинсулинемия индуцирует атерогенные изменения липидного спектра крови [3]. Увеличивается количество и чувствительность рецепторов для ЛПНП на клеточных мембранах стенки артерии, что приводит к ускоренному транспорту избытка ХС в сосудистую стенку. Изменения в липидограмме были выявлены у всех пациентов как первой, так и второй групп, однако их выраженность была наибольшей при сочетании МС и ИБС, особенно у лиц на фоне депрессии (табл. 1).
Таблица 1 – Липидный спектр у пациентов (M±m)
|
|
ОХС, ммоль/л |
ХС ЛПВП, ммоль/л |
ХС ЛПНП, ммоль/л |
ИА, ед |
ТГ, ммоль/л |
|||
|
|
|
Муж |
Жен |
Муж |
Жен |
Муж |
Жен |
|
|
I группа: ИБС, n=91 ИБС+МС, n=72
|
6,2±0,1
6,9±0,1 |
0,7±0,03
0,7±0,02 |
1,0±0,02
0,9±0,03 |
4,0±0,2
4,4±0,2 |
3,6±0,2
4,4±0,2 |
8,8±0,3
9,8±0,4 |
6,2±0,2
7,7±0,3 |
3,5±0,2
3,6±0,1 |
|
II группа, ИБС, n=125 ИБС+МС, n=30
|
5,6±0,1*
6,2±0,2** |
0,9±0,04*
0,8±0,02** |
1,15±0,03**
1,1±0,04** |
3,2±0,1
3,9±0,2 |
3,0±0,2
3,6±0,3 |
6,2±0,3
7,6±0,3 |
4,9±0,2
5,6±0,2 |
3,2±0,2
3,3±0,1 |
*р<0,001, **р<0,05 по сравнению с показателями I группы.
Более выраженные изменения липидного спектра у пациентов первой группы привели у них к утяжелению течения ИБС. Структура стабильной стенокардии напряжения (ССТН) по степени тяжести функционального класса (ФК) приведена на рис. 2.
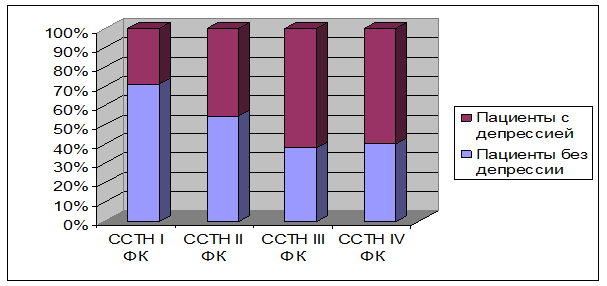
Рис. 2. Структура стабильной стенокардии напряжения у пациентов двух групп по степени тяжести.
Результаты Холтеровского мониторирования ЭКГ показали, что при наличии депрессии у пациентов с ИБС на 15,7% чаще, чем в группе сравнения, в ночное время регистрируется выраженная синусовая аритмия, на 21,1% преходящие синоатриальные или атриовентрикулярные блокады, а также на 24,7% различные нарушения ритма на фоне длительных, до 77,3 + 2,4 мин/сут., периодов ишемии миокарда.
Было установлено, что у пациентов с высоким содержанием кортизола в крови происходит более быстрое формирование кальциноза коронарных артерий, о чем свидетельствовали более высокие показатели кальциевого индекса (КИ), определенные по методу Агатсона у 108 пациентов с ИБС (табл. 2).
Таблица 2 – Показатели индекса кальция по методу Агатсона
|
Количество баллов |
I группа, n=57 |
II группа, n=51 |
||
|
ИБС, n=28 |
ИБС+МС, n=29 |
ИБС, n=24 |
ИБС+МС, n=27 |
|
|
0 |
- |
- |
- |
- |
|
1-10 |
- |
- |
2 (8,3%) |
2 (7,4%) |
|
11-100 |
5 (17,9%) |
3 (10,3%) |
9 (37,5%) |
8 (29,6%) |
|
101-400 |
17 (60,7%) |
18 (62,1 %) |
11 (45,9%) |
14 (51,9 %) |
|
>400 |
6 (21,4%) |
8 (27,6%) |
2 (8,3%) |
2 (11,1%) |
В соответствии с рекомендациями по интерпретации показателей КИ (0 баллов – очень низкий, 1-10 – низкий, 11-100 – умеренный, 101-400 – умеренно высокий и > 400 баллов – высокий риски развития ИБС и сердечно-сосудистых заболеваний) нами было установлено, что присоединение МС к ИБС повышает риск развития сердечно-сосудистых осложнений у пациентов с ИБС в среднем на 5-7%, а при наличии депрессии высокий риск развития сердечно-сосудистых осложнений возрастает как при изолированной ИБС, так и при сочетании МС и ИБС – в 2,5 раза (р<0,001).
Относительный риск развития симптоматики сердечно-сосудистых заболеваний, рассчитанный по методу H. Yoon и соавт., подтвердил полученные ранее результаты (табл. 3).
Таблица 3 – Сравнительные показатели содержания кальция в бляшках коронарных артерий пациентов, включенных в обследование
|
Содержание кальция, мг |
Пациенты с ИБС, % |
Пациенты с ИБС+МС, % |
Риск сердечно-сосудистой патологии (по сравнению с людьми с нулевым уровнем кальция) |
|
I группа, n=57 |
n=28 |
n=29 |
|
|
1-79 |
21,4 |
10,3 |
3:1 |
|
80-399 |
57,1 |
58,7 |
8:1 |
|
>400 |
21,5 |
31,0 |
25:1 |
|
II группа, n=51 |
n=24 |
n=27 |
|
|
1-79 |
37,5 |
17,2 |
3:1 |
|
80-399 |
62,5 |
69,0 |
8:1 |
|
>400 |
- |
13,8 |
25:1 |
Полученные факты подтверждались данными анамнеза обследованных пациентов. Среди больных первой группы инфаркт миокарда (ИМ) перенесли 12,7% обследованных. Из них ИМ с зубцом Q был выявлен более чем у 70% из них. Еще у 6,3% в анамнезе были острые нарушения мозгового кровообращения. В группе сравнения эти показатели составляли 6,0; 46,2 и 2,3% соответстенно (р1,2.3<0,05).
Выводы
1. При наличии депрессии, которая коррелирует (r+0,98) с высоким уровнем кортизола, у лиц старших возрастных групп повышается риск развития сочетанной патологии: ИБС и МС.
2. Гиперкортизолемия приводит к быстрому прогрессированию как МС, так и ИБС и повышает риск развития осложнений со стороны сердечно-сосудистой системы.
Рецензенты:
Сергеев Олег Степанович, доктор биологических наук, профессор, кафедра общей и клинической патологии: патологическая анатомия и патологическая физиология, Самарский государственный медицинский университет, г. Самара.
Лебедева Елена Алексеевна, доктор медицинских наук, профессор, кафедра госпитальной терапии с курсом трансфузиологии, Самарский государственный медицинский университет, г. Самара.
Библиографическая ссылка
Прохоренко И.О., Зарубина Е.Г., Моисеева Т.В. ВЛИЯНИЕ ДЕПРЕССИИ НА ФОРМИРОВАНИЕ МЕТАБОЛИЧЕСКОГО СИНДРОМА И РАЗВИТИЕ ИБС У ПАЦИЕНТОВ СТАРШИХ ВОЗРАСТНЫХ ГРУПП // Современные проблемы науки и образования. 2012. № 6. ;URL: https://science-education.ru/en/article/view?id=7569 (дата обращения: 16.05.2026).



