Востребованность остеотропных материалов в современном мире растет с каждым годом. По данным НИИ ревматологии РАМН, в настоящее время около 2 млн пациентов нуждаются в операциях по замещению костной ткани, а общий объем рынка биоматериалов в Российской Федерации к 2025 г. должен достичь 979 млн рублей [1]. Мировой рынок растет еще более стремительно, и, если, по данным Global View Research, в 2017 г. он оценивался в 83,9 млрд долларов, то ожидается, что к 2025 г. он вырастет примерно в 3 раза – до 240 млрд долларов [2].
Столь значительная потребность в материалах для костной пластики имеет медицинскую основу. Травмы, хирургические вмешательства при опухолевых и воспалительных процессах требуют от врачей поиска новых подходов к замещению дефектов костной ткани или оптимизации процессов остеогенеза, в том числе с использованием специальных материалов [3]. Такими достаточно изученными и применяемыми материалами являются имплантируемые субстанции, изготовленные на основе фосфатов (ФК) или силикатов (СК) кальция. Керамика из ФК обладает способностью индуцировать процессы остеогенеза, так как имеет схожий с натуральной костью состав и может служить каркасом для ее восстановления [4], а нанесение покрытий из ФК, в частности гидроксиапатита (Са10(РО4)6(ОН)2) и трикальция фосфата (Са3(РО4)2), на металлоконструкции для остеосинтеза и эндопротезирования достаточно давно используется в медицинской практике, поскольку позволяет добиться достоверно лучших результатов лечения [5, 6, 7]. Помимо кальцийфосфатных материалов, широкое распространение получили биоактивные стекла, содержащие в составе оксид кремния [8, 9]. Доказано, что они обладают остеоиндуктивными свойствами и способствуют дифференцировке мультипотентных мезенхимальных стволовых клеток в остеобласты, оказывают положительное влияние на формирование основного вещества кости, тем самым стимулируя процессы репаративного остеогенеза [10].
Наряду с составом важна и форма материала, которая должна обеспечивать возможность полного заполнения костного дефекта любой конфигурации и объема. С этой точки зрения более удобны гранулированные материалы, в составе которых присутствуют частицы различных размеров [11].
Резюмируя изложенное, можно заключить, что композитные препараты, содержащие в своем составе фосфаты и силикаты кальция в виде гранул различных размеров, представляются перспективными костнопластическими материалами, требующими дальнейшего изучения.
Цель исследования – экспериментальное изучение ранних общих и местных реакций на имплантацию нового остеопластического материала, включающего различные комбинации фосфата и силиката кальция, при замещении метаэпифизарного костного дефекта.
Материалы и методы исследования
Для достижения поставленной цели необходимо было разработать экспериментальный резорбируемый материал на основе сочетания фосфатов и силикатов кальция, имплантировать его в стандартизированный посттравматический метаэпифизарный костный дефект у лабораторных животных и изучить его влияние на общие и локальные регенераторные процессы.
На первом этапе исследования на базе научной лаборатории стоматологического факультета ФГБОУ ОмГМУ Минзрава России был разработан и получен новый синтетический гранулированный материал с варьируемым содержанием фосфата и силиката кальция, а именно гидроксиапатита (Са10(РО4)6(ОН)2) и волластонита (CaSiO3), и связующего полимера – желатина (в количестве не более 20 масс.%) [2]. Макроскопически материал представляет собой набор сфер различного диаметра (от 0,2 мм до 5 мм) (рис. 1) с открытой пористостью порядка 50% и микротвердостью не менее 17 HV (микротвердость – твердость отдельных участков микроструктуры), эти данные были получены путем измерений по Виккерсу.


а б
Рис. 1. Общий вид гранул: фото образца в чашке Петри (а) и микрофотография, полученная на микроскопе «JCM-5700», JEOL (б)
Для исследования in vivo были выбраны гранулы с пропорцией гидроксиапатита к волластониту 60/40, 50/50 и 40/60 масс.% соответственно, размерами от 0,2 до 1,0 мм. Перед использованием материалы стерилизовали путем автоклавирования при температуре 120°С в течение 30 минут.
Экспериментальное исследование проводилось на 36 кроликах породы Белый великан весом 3800–4200 г с соблюдением принципов гуманности, которые изложены в директивах Европейского сообщества (86/609//ЕЕС) и Хельсинкской декларации, на основании разрешения этического комитета ОмГМУ № 128 от 03.02.2021 г. Всем животным выполнялся стандартизированный дефект метаэпифизарного отдела бедренной кости. Для этого каждому из кроликов в операционной выполнялась в/м седация путем введения препарата «Золетил» в индивидуальной дозировке. С использованием циркулярной пилы в дистальном метаэфипизе бедренной кости формировался прямоугольный дефект кортикального слоя размером 10х5 мм. При помощи инструментария кортикальная пластинка «вдавлена» на глубину до 8 мм (объем сформированной полости составил 400±4 мм3), далее при помощи элеватора выполнялся подъем костного фрагмента, впоследствии, в зависимости от исследуемой группы, в сформированную полость помещался синтетический материал либо зона оставалась интактной. Кортикальная пластинка фиксировалась в материнское ложе, мягкие ткани послойно ушивались (рис. 2).
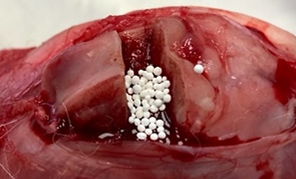
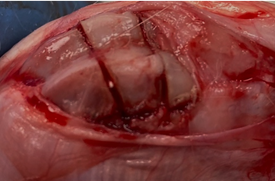
а б
Рис. 2. Вид метаэпифизарного костного дефекта: а – после имплантации биоактивных гранул; б – после закрытия костной полости кортикальной пластинкой
Экспериментальные животные были разделены на 4 группы (по 9 животных в каждой) в зависимости от выбранного соотношения фосфатов и силикатов кальция: 1-я группа (контрольная) – зона дефекта не замещалась материалом, 2-я группа – в зону перелома имплантировался материал, в своем составе содержащий фосфаты и силикаты кальция в соотношении 60/40 масс.% соответственно, 3-я группа – в зону смоделированного дефекта имплантировался материал, в своем составе содержащий фосфаты и силикаты кальция в соотношении 50/50 масс.% соответственно, 4-я группа – в зону перелома имплантировался материал, в своем составе содержащий фосфаты и силикаты кальция в соотношении 40/60 масс.% соответственно.
После моделирования костного дефекта животные находились под ежедневным контролем клинического статуса: оценивались их общее состояние, сохранение аппетита и жажды, температура тела per rectum, опороспособность конечности, заживление послеоперационной раны, наличие или отсутствие отека, гиперемии, повышение локальной температуры оперированной конечности. Лабораторные исследования сыворотки крови всех групп животных выполнялись на 7-е, 14-е и 30-сутки. При биохимическом исследовании крови были проанализированы уровень кальция, фосфора и щелочной фосфатазы, WBC, СРБ. Реакцию костной ткани на имплантацию и динамику репаративных процессов контролировали выполнением рентгенологического исследования на аппарате Toshiba Radrex и мультиспиральной компьютерной томографией (МСКТ), выполненной на аппарате Toshiba Aquilion CXL 128, в сроки 1-е, 14-е и 30-е сутки после операции.
Для забора морфологического материала животные выводились из эксперимента на 14-е и 30-е сутки. С помощью медицинского инструментария и фрезы резецировалась метаэпифизарная часть бедренной кости, включающая область экспериментального костного дефекта. Полученные костные фрагменты помещали в 10%-ный раствор формалина, декальцинировали в 5%-ном растворе азотной кислоты и обезвоживали в спиртах возрастающей крепости (от 60° до 96°), а также в смеси этилового спирта с диэтиловым эфиром (в соотношении 1:1). В последующем образцы заливали в целлоидин, уплотняли под парами хлороформа, после чего из полученных блоков изготавливали срезы толщиной 7–10 мкм, которые окрашивали гематоксилином и эозином и исследовали под микроскопом «XSZ 158T».
При статистическом анализе использовали программные пакеты Microsoft Excel XP и Statsoft Statistica v.10. Сравнение групп лабораторных животных проводили с использованием t-критерия Стьюдента с уровнем достоверности р<0,05. Полученные данные каждой группы оценивали при помощи критерия Шапиро–Уилка; результаты анализа приближаются к 1, то есть данные можно считать достоверными.
Результаты исследования и их обсуждение
Наиболее значимые изменения в клиническом статусе животных были зафиксированы в период с 1-е по 6-е сутки. В 1-е сутки после моделирования дефекта и установки биоактивного материала животные всех исследуемых групп оставались вялыми, мало двигались, не опирались на оперированную конечность. Были зафиксированы снижение аппетита, увеличение потребления жидкости (до 500 мл), средняя температура тела у животных составила 40,03±0,08°C (в норме температура тела составляет 39,0°C), а среднее значение локальной температуры оперированной конечности – 40,5±0,1°С. У всех животных отмечались местная гиперемия, отечность и болезненная реакция на пальпацию оперированной конечности. На 2-е сутки у животных сохранялись снижение аппетита, болевая реакция, однако зона гиперемии уменьшалась, повысилась активность и восстановилась частичная опороспособность. Среднее значение температуры у животных составило 39,8±0,1°С, местной – 40,2±0,1°С. На 3-и сутки у животных восстановились аппетит и двигательная активность, жажда снизилась (объем потребляемой жидкости – 350 мл). Местный отек и болевая чувствительность не регистрировались. Среднее значение температуры тела составило 39,4±0,2°С, местной – 39,6±0,2°С. К 5-м суткам после операции фиксировали только незначительное повышение местной температуры конечности – 39,2±0,1°С, остальные показатели клинического статуса вернулись к дооперационным, с 6-х суток отмечалось полное восстановление клинического статуса у животных всех наблюдаемых групп.
Результаты лабораторных исследований свидетельствовали об однотипной стойкой тенденции к повышению биохимических показателей кальция, фосфора и щелочной фосфатазы в сыворотке крови у всех групп оперированных животных, что подтверждает активацию процессов регенерации. Интегрированные результаты биохимических исследований представлены в таблице.
Некоторые биохимические показатели сыворотки крови у экспериментальных животных в ранние сроки после имплантации
|
Показатель сыворотки крови |
До операции |
Сутки после моделирования дефекта |
Референтный интервал |
||
|
7-е |
14-е |
30-е |
|
||
|
Кальций, mmol\l |
1,60±0,08 |
2,6±0,1 |
3,3±0,1 |
1,9±0,3 |
1,4–3,1 |
|
Фосфор, mmol\l |
1,5±0,1 |
2,0±0,2 |
2,4±0,2 |
2,0±0,6 |
1,3–2,2 |
|
Щелочная фосфатаза, u/l |
7,0±1,2 |
11,8±0,5 |
18,3±0,6 |
12,7±0,3 |
4,1–16,2 |
|
WBC х109/l |
3,5±0,5 |
10,2±0,7 |
6,4±0.3 |
4,1±0,4 |
3,3–11,1 |
|
СРБ mg/l |
0,08±0,08 |
0,76±0,18 |
0,39±0,09 |
0,10±0,03 |
0,08–1,02 |
Полученные результаты свидетельствуют о том, что на протяжении первого месяца эксперимента значения концентраций кальция, фосфора и активности щелочной фосфатазы превышали исходные и референтные значения. К 7-м суткам отмечалось абсолютное увеличение концентрации кальция на 15,4%, фосфора – на 5%, ЩФ – на 23%; на 14-е сутки концентрации кальция были выше на 12,1%, фосфора – на 4,2%, ЩФ – на 12%, на 30-е сутки количества кальция, фосфора, активность щелочной фосфатазы, WBC и СРБ уже находились в границах физиологической нормы. Статистически достоверной разницы при использовании имплантатов с различными массовыми соотношениями фосфата и силиката кальция выявлено не было.
На 14-е сутки выполнялись контрольная рентгенография оперированной конечности в прямой и боковой проекциях, а также МСКТ-исследование, которые подтвердили, что имплантированные гранулы у животных всех экспериментальных групп полностью заполняли послеоперационный костный дефект, миграции гранул не произошло, патологической периостальной реакции, новых зон резорбции костной ткани выявлено не было.
К 30-м суткам после операции наибольшая выраженность остеопластического процесса была отмечена во 2-й экспериментальной группе, где зона дефекта заполнялась материалом, содержащим фосфаты и силикаты кальция в соотношении 60 к 40 масс% соответственно. По данным рентгенографии в посттравматическом костном дефекте у животных этой группы были отмечены признаки резорбции и трансформации имплантированного материала в новообразованную костную ткань. Кроме того, имелись отчетливые признаки сращения остеотомированной кортикальной пластинки бедренной кости с материнским ложем за счет развития костно-пластических процессов в зоне самого посттравматического дефекта (рис. 3).
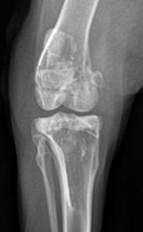
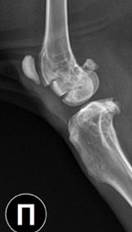
а) б)
Рис. 3. Вид метаэпифизарного костного дефекта на 30-е сутки эксперимента: а – передне-задняя проекция: б – боковая проекция
МСКТ-картина подтверждала полученные клинические и рентгенологические данные. В зоне имплантации остеогенного материала формировалась костная ткань неравномерной плотности, заполняющая посттравматический дефект и имеющая в ряде отделов интимную связь с кортикальным слоем кости. В этих же отделах выявлялись элементы гипертрофической реакции надкостницы и периостальной костной мозоли. В некоторых сканах в отдельных участках костного дефекта, вероятно, в связи с преобладанием рубцовой соединительной ткани, визуализировались отграниченные от интактной кости «пустые» зоны с формированием небольших полостей и начинающимся остеосклерозом их стенок (рис. 4).
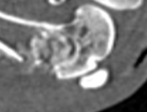
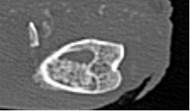
а) б)
Рис. 4. МСКТ срезы метаэпифизарного костного дефекта на 30-е сутки эксперимента: а – сагиттальный срез; б – коронарный срез
Измерение плотности новообразованной ткани в единицах Хаунсфилда (рис. 5) показало, что в зоне имплантируемого вещества к 30-м суткам эксперимента наблюдалось формирование костной ткани, схожей по плотности с окружающей метафизарной костью и соответствующей плотности кости не оперированной контрлатеральной конечности (HU = 250–400 Ед).

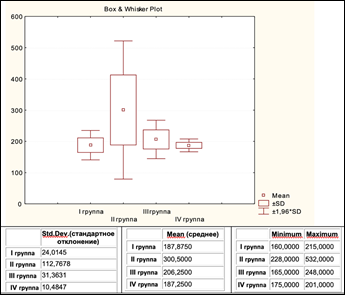
Рис. 5. Распределение плотности новообразованной костной ткани (Hu) в экспериментальных группах
Наибольший разброс показателей плотности, но и наибольшая средняя плотность костного регенерата были зарегистрированы у животных 2-й экспериментальной группы, что, вероятно, свидетельствовало о большей активности репаративных процессов при использовании имплантируемого материала с соотношением фосфата и силиката кальция 60 к 40 масс%.
Гистологическое исследование показало, что в опытных группах, где были имплантированы материалы, имеющие в составе фосфаты и силикаты кальция в соотношении 40 к 60 и 50 к 50 масс%, к 30-м суткам после операции локальная картина была однотипной. В костном дефекте обнаруживались неструктурированные фрагменты имплантируемого материала различной формы и величины с отсутствием макрофагальной реакции. Сам дефект был преимущественно заполнен нежно-волокнистой соединительной тканью с новообразованными полнокровными сосудами капиллярного типа, на границе дефекта и интактной кости определялись единичные активные остеобласты. Иная картина наблюдалась в гистологических образцах 2-й группы при использовании соотношения фосфатов и силикатов кальция в 60 к 40 масс% (рис. 6).
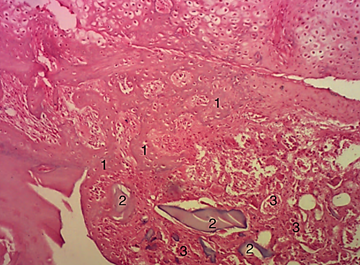
Рис. 6. Гистологический препарат новообразованной костной ткани после имплантации гранул в соотношении 60/40 масс% ФК/СК: 1 – новообразованная кость; 2 – включения имплантируемого вещества; 3 – новообразованные сосуды
Кроме заполняющего дефект массива малодифференцированной соединительной ткани с множественными кровеносными сосудами различных размеров и фрагментами имплантированного материала, визуализировались формирующиеся костные трабекулы, образовывающие среднеячеистую губчатую кость, в межтрабекулярных промежутках которой соединительная ткань приобретала более организованную структуру.
Таким образом, проведенное исследование показало, что использование имплантируемого биодеградируемого материала на основе сочетания фосфатов и силикатов кальция имеет ряд положительных качеств и в отношении переносимости, и в отношении остеоиндуктивности. Первое подтверждалось отсутствием патологических реакций, признаков системного и местного активного воспалительного процесса в раннем и средне-срочном периодах после имплантации. Более того, после заполнения дефекта произошло достаточно быстрое (в течение первых 6 суток) возобновление активности лабораторных животных с восстановлением опороспособности конечности, отмечалось первичное заживление послеоперационной раны с отсутствием признаков продолжительной экссудации. Лабораторные показатели общего анализа крови, СРБ в течение первых 10 суток вернулись к референтным значениям.
Наиболее важной задачей исследования являлось выяснение регенераторного потенциала имплантируемого материала при различных сочетаниях в нем фосфата и силиката кальция. Литературные данные свидетельствуют, что для оптимизации процессов остеогенеза в основном используют материалы, имеющие в своем составе исключительно фосфаты кальция [5, 2, 12] в различных формах, размерах и сочетаниях (с металлами, органическими компонентами и пр.). В зарубежной литературе имеются данные о синтезировании высокотемпературной керамики, сочетающей в себе фосфаты и силикаты кальция в различных пропорциях, но основными недостатками данных веществ являются высокая плотность и отсутствие пористости поверхности, что препятствует процессам активного роста и интеграции новообразованной костной ткани [12]. Однако в ряде исследований показано существенное стимулирующее влияние ионов кремния на процессы остеогенеза, которое носит волнообразный характер и наиболее активно проявляется в процессе минерализации. Было установлено, что на ранних стадиях роста остеоидной ткани содержание в ней кремния крайне невелико, однако с созреванием каллуса его количество постепенно нарастает, достигая более чем 200% от исходного. Методом рентгеноспектрального анализа обнаружено, что в этот период кремний присутствует в участках роста молодой кости и в составе остеобластов в количествах, близких к содержанию кальция, фосфора и магния [9]. В дальнейшем, по мере увеличения в новообразованной кости концентрации кальция до соответствующего зрелому костному апатиту, уровень кремния снова снижается до минимума [3, 2, 13].
В проведенном нами экспериментальном исследовании получены комплексные данные, позволяющие прийти к заключению о перспективности симультанного использования фосфатов и силикатов кальция для замещения костных дефектов. Это подтвердили и данные биохимического исследования крови (повышение значений концентраций кальция, фосфора и активности щелочной фосфатазы), и результаты рентгенологических методов визуализации, отмечающих, что уже к 30-м суткам в зоне имплантации формировалась костная ткань, заполняющая полость сформированного дефекта, с неравномерной, но достаточно высокой средней плотностью в 300,5 ед. Хаунсфилда. Гистологическое исследование подтвердило активацию процессов остеогенеза в зоне костного дефекта с биодеградацией искусственного материала и преимущественным замещением его новообразованной трабекулярной костной тканью. Проводя сравнение и анализ полученных результатов, необходимо отметить, что наибольший потенциал регенераторного воздействия в ранние сроки показала имплантация гранул материала, сочетающего в своем составе фосфаты и силикаты кальция в соотношении 60/40 масс%.
Заключение
По результатам проведенного экспериментального исследования нами было установлено, что предлагаемый синтетический материал не вызывает патологических общих и локальных реакций на имплантацию, а использование комбинации фосфатов и силикатов кальция с целью стимуляции и оптимизации процессов репаративного остеогенеза в соотношении 60/40 масс% соответственно показало лучшие первичные результаты восполнения метаэпифизарного костного дефекта, в отличие от других дозировок, что было подтверждено клиническими, рентгенологическими и гистологическими методами исследования. Таким образом, полученные данные демонстрируют целесообразность дальнейшего изучения механизмов и эффективности применения новых биоактивных имплантатов для замещения дефектов костной ткани.



