Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
MORPHOLOGICAL FEATURES OF THE STRUCTURE OF UNSTABLE ATHEROSCLEROTIC PLATES OF THE CORONARY HEART ARTERIES
Атеросклероз коронарных артерий представляет собой хроническое прогрессирующее заболевание, приводящее к развитию ишемической болезни сердца (ИБС), которая является наиболее частой причиной смерти больных в мире [1].
Для понимания патогенеза и возможных осложнений атеросклероза коронарных артерий (КА) необходимо оценивать строение атеросклеротической бляшки (АБ). Известно, что АБ состоят из трех основных компонентов: 1) клеток, включая гладкомышечные клетки, макрофаги и Т-лимфоциты; 2) экстрацеллюлярного матрикса (ЭКМ), включающего коллаген, эластические волокна, протеогликаны; 3) липидов, которые могут локализоваться внутри- и внеклеточно [2]. Типичная АБ состоит из фиброзной покрышки, представленной плотным коллагеном, гладкомышечных клеток и липидного ядра, содержащего холестерин и его эфиры, а также клеточный детрит, пенистые клетки (нагруженные липидами макрофаги), белки плазмы крови [3–5].
Известно, что в динамике развития АБ могут быть стабильными и нестабильными. АБ, содержащие большие участки, выполненные пенистыми клетками, внеклеточными липидами, а также с тонкой фиброзной покрышкой или покрышкой, содержащей небольшое количество гладкомышечных клеток или кластеры воспалительных клеток, называют нестабильными. Важно подчеркнуть, что понятие «нестабильность АБ» является неоднозначным, подразумевающим, в том числе, нарушение гемодинамической функции коронарной артерии [6–8].
Основными структурными компонентами АБ, сохраняющими целостность стенки коронарной артерии и предупреждающим от воздействия гемодинамических факторов (таких как артериальное давление, белки плазмы крови, вазоспазм), являются фиброзная покрышка и коллаген. В синтезе и деградации коллагена фиброзной покрышки АБ принимают участие гладкомышечные клетки и макрофаги [9–11]. Особое значение придают макрофагам, которые способны продуцировать матриксные металлопротеиназы и их ингибиторы [12, 13]. Воспаление, возникающее в нестабильной АБ, представленное Т-лимфоцитами, может также инициировать деструкцию фиброзной покрышки АБ КА [12]. Все эти вопросы требуют своего обсуждения и оценки роли тех или иных клеточных и экстрацеллюлярных компонентов в морфогенезе нестабильной АБ.
В связи с этим целью исследования послужил анализ морфологических особенностей нестабильных АБ КА сердца.
Материал и методы исследования. Проведено морфологическое исследование нестабильных АБ КА, полученных во время выполнения аутопсий у 20 пациентов. Среди умерших было 12 мужчин и 8 женщин, средний возраст которых составил 67±5 лет. Из истории болезни умерших было известно, что больные поступали в кардиологическое отделение клиники РостГМУ с признаками нестабильной стенокардии (11 случаев), острого инфаркта миокарда (9 случаев).
Исследование проведено в соответствии с Хельсинкской декларацией Всемирной медицинской ассоциации «Этические принципы проведения медицинских исследований с участием человека в качестве субъекта», Федеральным законом от 21.11.2011 г. № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации» (п. 4 ст. 67).
При вскрытии КА обращали внимание на топографию поражения, диаметр артерии, степень выраженности стеноза (в %), размеры АБ, наличие или отсутствие вторичных изменений АБ (тромбоза, кальциноза). Для гистологического, гистохимического исследования вырезали наиболее измененный участок КА с наличием в ней АБ и после фиксации в забуференном 10%-ном растворе формалина, обезвоживания в изопропиловом спирте с использованием гистопроцессора Milestone (Италия), заливки в парафин выполняли гистологические срезы на ротационном микротоме фирмы Leica (Германия). Микропрепараты окрашивали гематоксилином-эозином, пикрофуксином по Ван Гизону, Хочкиссу (ШИК-реакция). Микроскопия и микрофотографирование осуществлялись на микроскопе Leica DM 1000 (Германия) со встроенной фотокамерой.
Для проведения морфометрического анализа применяли программное обеспечение с открытым исходным кодом ImageJ (National Institutes of Health, USA) и фотографии препаратов с увеличением объектива х20 или х40. Во всех случаях проводили измерение общей площади гистологического среза стенки коронарной артерии и ее просвета. Для препаратов, окрашенных гематоксилином-эозином, выполняли измерение суммарной площади липидной инфильтрации, кровоизлияний, отложений солей кальция, новообразованных сосудов, количества клеточных элементов в инфильтрате (пенистых клеток, лимфоцитов). Статистическую обработку полученных результатов осуществляли с помощью статистических инструментов программы MedCalc Statistical Software version 19.1.3. Характер распределения выборочных значений проверили с использованием W-критерия Шапиро–Уилка (p<0,05)
Результаты исследования и их обсуждение
При макроскопическом исследовании КА нами были обнаружены следующие изменения (табл. 1).
Таблица 1
Макроскопическая характеристика коронарных артерий сердца при атеросклерозе средние значения)
|
Топография поражения коронарной артерии |
Диаметр коронарной артерии (мм) |
Cтепень выраженности стеноза (%) |
Размеры АБ (мм) |
Вторичные изменения в АБ |
|
ПКА |
3,1 мм |
42% (±1,53) |
1,6 мм |
нет |
|
ЛКА |
2,2 мм |
75% (±1,84)
|
2,4 мм |
есть |
|
ПМЖВ |
2,3 мм |
80% (±2,38) |
2,5 мм |
есть |
|
ОВ |
1,9 мм |
67% (±1,3)
|
1,9 мм |
нет |
Примечание: ПКА – правая коронарная артерия, ЛКА – левая коронарная артерия, ПМЖВ – передняя ветвь левой коронарной артерии, ОВ – огибающая ветвь левой коронарной артерии. Стандартное отклонение (±).
Как видно из таблицы 1, наиболее выраженные признаки атеросклеротического поражения были в ЛКА в области устья ПМЖВ ЛКА, что сопровождалось развитием выраженного стеноза данных артерий (75%, 80% соответственно), большими размерами АБ, наличием вторичных изменений в бляшке (кровоизлиянием, кальцинозом).
Гистологическое исследование АБ позволило уточнить морфологические особенности их строения. В 8 наблюдениях (40%) в стенках КА обнаруживались нестабильные АБ, представленные крупными атеромами (рис. 1). Атеромы занимали более 2/3 стенки артерии, содержали тонкую фиброзную покрышку с участками резкого истончения коллагеновых волокон. В отдельных участках интимы встречались очаги расслоения и повреждения со скоплением пенистых клеток (макрофагов, наполненных липидами), немногочисленных лимфоцитов.
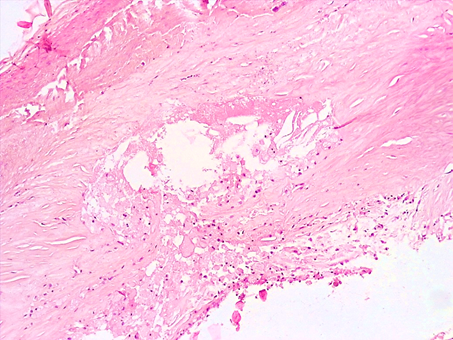
Рис. 1. Нестабильная АБ коронарной артерии сердца: вокруг атеромы отмечаются повреждение интимы артерии со скоплением пенистых клеток (макрофагов), немногочисленных лимфоцитов, резкая атрофия мышечной оболочки. Окраска гематоксилином-эозином. Увеличение х200
В 4 наблюдениях (20%) в стенках КА под истонченной фиброзной покрышкой, представленной тонкими коллагеновыми, имелось скопление пенистых клеток (макрофагов) с очаговым повреждением фиброзной покрышки АБ. Субэндотелиально в стенке КА обнаруживали субэндотелиальное кровоизлияние, представленное лизированными эритроцитами, с деформацией и резким сдавлением мышечной оболочки (рис. 2).
В 4 случаях (20%) просвет КА был резко сужен до 85%, имел вид щелевидного отверстия за счет резко выраженного атероматоза, атерокальциноза (рис. 3). Строение стенок КА было нарушено в связи с отложением липидных масс и крупных депозитов солей кальция, которые локализовались субинтимально, в медии, со сдавлением и выраженной атрофией гладкомышечных клеток. В этих же участках встречались скопления кислых мукополисахаридов (ШИК+), что указывало на повышение сосудистой проницаемости стенок КА.
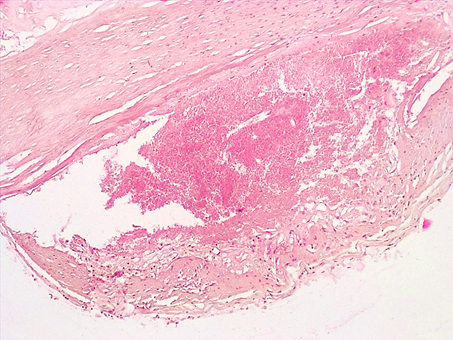
Рис. 2. Нестабильная АБ коронарной артерии сердца: под резко истонченной фиброзной покрышкой имеется интрамуральное кровоизлияние со скоплением пенистых клеток (макрофагов). Окраска гематоксилином-эозином. Увеличение х100
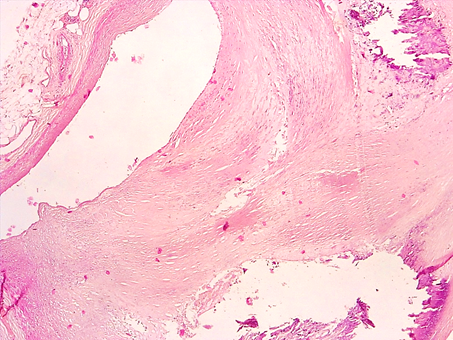
Рис. 3. Нестабильная АБ коронарной артерии сердца: стеноз просвета артерии, атероматоз с крупными депозитами солей кальция в медии, резкая атрофия гладкомышечных клеток. Окраска гематоксилином-эозином. Увеличение х50
В 2 случаях (10%) наблюдали своеобразные морфологические изменения в стенках КА при атеросклерозе. Просветы КА были неравномерно сужены за счет резко утолщенной интимы, содержащей массы липидов, некротизированные клеточные элементы, с резкой атрофией фиброзной покрышки и медии. В глубоких отделах АБ имелись новообразованные тонкостенные сосуды капиллярного типа (рис. 4). Подобный процесс отражает неоангиогенез в связи с возможным формированием сосудов из адвентициальных vasa vasorum, в то время как васкулогенез отражает их развитие в процессе эмбриогенеза.
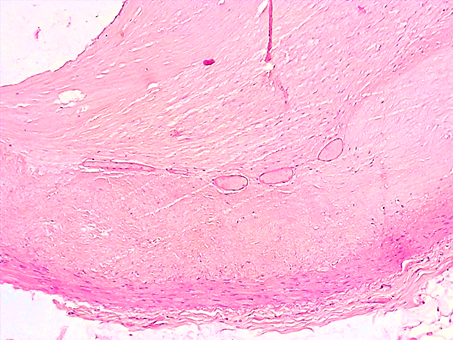
Рис. 4. Нестабильная АБ коронарной артерии сердца: резкое утолщение интимы за счет атероматоза с выраженной атрофией мышечной оболочки. Новообразованные тонкостенные сосуды в бляшке. Окраска гематоксилином-эозином. Увеличение х100
В 2 наблюдениях (10%) в нестабильных АБ имелись признаки хронического воспаления с наличием лимфоцитарной инфильтрации. При этом атерома, представленная массами липидов, занимала на всем протяжении интиму, вовлекала мышечную оболочку с выраженной атрофией гладкомышечных клеток. Лимфоцитарная воспалительная инфильтрация отмечалась как в поверхностных слоях атеромы, так и в глубоких отделах стенки артерии (в медии, адвентиции), распространялась на окружающую жировую клетчатку (рис. 5).
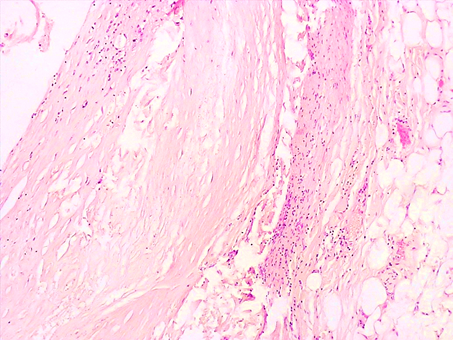
Рис. 5. Нестабильная АБ коронарной артерии сердца: крупная атерома с вовлечением интимы, медии с резкой атрофией мышечной оболочки с окружающей лимфоцитарной инфильтрацией слоев. Окраска гематоксилином-эозином. Увеличение х200
Полученные морфологические данные об особенностях строения нестабильных АБ коронарных артерий сердца обобщены в таблице 2.
Таблица 2
Морфологические особенности строения нестабильных АБ коронарных артерий сердца (средние значения)
|
Тип нестабильной АБ |
S атеромы (%) |
S фиброзной покрышки (%) |
S кальциноза (%) |
S кровоизлияний (%) |
Кол-во пенистых клеток |
Кол-во лимфоцитов |
Кол-во сосудов |
|
С пенистыми клетками |
53 (± 3,43) |
14 (± 2,54) |
– |
– |
44 (± 2,54) |
5,4 (± 2,07) |
– |
|
С кровоизлиянием |
62,4 (± 2,4): |
14 (± 2,25) |
– |
47,6 (± 1,14) |
54,6 (± 3,04) |
– |
– |
|
С кальцинозом |
94 (± 2,23) |
5,2 (± 1,30) |
74,80 (± 3,11) |
– |
– |
– |
– |
|
С неоангиогенезом |
63 (± 2,07) |
4,40 (± 1,14) |
– |
– |
4,40 (± 1,51) |
– |
8,40 (± 1,14) |
|
С хроническим воспалением |
84 (± 2,23) |
5 (± 1,58 |
– |
– |
– |
95,6 (± 3,04) |
– |
Примечание: S – площадь поражения (%); стандартное отклонение (±).
Полученные морфологические данные позволили выделить пять вариантов нестабильных АБ КА сердца: 1) с преобладанием пенистых клеток (макрофагов); 2) с внутристеночным кровоизлиянием в бляшку; 3) с дистрофическими изменениями и кальцинозом бляшки; 4) с признаками неоангиогенеза в бляшке; 5) с хроническим воспалением в бляшке.
Основными морфологическими ориентирами, позволившими выделить данные варианты нестабильной АБ, были: площадь атеромы, площадь фиброзной покрышки, площадь кальциноза, площадь кровоизлияний, количество пенистых клеток (макрофагов), количество лимфоцитов, количество сосудов. Эти данные дополняют ранее выполненные работы, посвященные строению атеросклеротических бляшек различных артерий [3, 4, 6], и помогают по-новому взглянуть на их структурные особенности.
Принимая во внимание, что нестабильная АБ представляет собой патологический процесс в динамике развития, можно полагать, что выделенные морфологические варианты могут указывать на различную роль как клеточных, так и внеклеточных компонентов КА. Важное значение, на наш взгляд, в морфогенезе нестабильной АБ имеют пенистые клетки (макрофаги), которые могут иметь как моноцитарное происхождение, так и возникать путем трансдифференцировки из гладкомышечных клеток [9, 10, 11]. По-видимому, пенистые клетки могут выступать не только в роли фагоцитов, осуществлять захват липидных частиц, но и участвовать в секреции тканевых металлопротеиназ, вызывающих деградацию структуры сосудистой стенки – гладкомышечных клеток, коллагеновых волокон, протеогликанов или цитокинов (интерлейкинов), фактора роста эндотелия сосудов [13].
Возможно, дефицит энзимов фагоцитов при избыточной липидной инфильтрации стенки КА может вызвать апоптоз самих клеток с последующим накоплением солей кальция в стенке. Однако данное положение требует дальнейшего биохимического и молекулярно-генетического исследования.
Заключение
Представленное морфологическое исследование особенностей строения нестабильных АБ КА сердца дополняет представление о прогрессировании атеросклероза.
Выделены пять морфологических вариантов нестабильных АБ: 1) с преобладанием пенистых клеток (макрофагов); 2) с внутристеночным кровоизлиянием в бляшку; 3) с дистрофическими изменениями и кальцинозом бляшки; 4) с признаками неоангиогенеза в бляшке; 5) с хроническим воспалением в бляшке. Нестабильные АБ с дистрофическими изменениями, кальцинозом не сопровождались развитием хронического воспаления в бляшке. Данный морфотип нестабильной АБ может играть существенную роль в развитии стенозирования КА.
Нестабильные АБ с наличием хронического воспаления, неоангиогенеза и внутристеночного кровоизлияния, вероятно, могут иметь значение в генезе расслоения бляшки с последующим тромбообразованием.
Дальнейшее изучение клеточно-межклеточных взаимоотношений
Библиографическая ссылка
Тодоров С.С., Дерибас В.Ю., Сидоров Р.В., Казьмин А.С., Тодоров С.С. МОРФОЛОГИЧЕСКИЕ ОСОБЕННОСТИ СТРОЕНИЯ НЕСТАБИЛЬНЫХ АТЕРОСКЛЕРОТИЧЕСКИХ БЛЯШЕК КОРОНАРНЫХ АРТЕРИЙ СЕРДЦА // Современные проблемы науки и образования. 2021. № 4. ;URL: https://science-education.ru/en/article/view?id=31054 (дата обращения: 22.05.2026).
DOI: https://doi.org/10.17513/spno.31054



