Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
EFFECT OF LICOPID ON INTERLEUKIN-4 LEVEL AND FUNCTIONAL ACTIVITY OF NEUTROPHILS IN PATIENTS WITH TYPE II DIABETES MELLITUS WITH URINARY TRACT INFECTION
Больные, страдающие сахарным диабетом II типа (СД), являются группой высокого риска развития инфекций мочевыводящих путей (ИМП) [1; 2]. Так, заболеваемость ИМП среди пациентов с СД составляет 46,9 на 1000 в сравнении с показателем у пациентов, не имеющих СД - 29,9 на 1000 [3; 4]. Высокий риск развития ИМП у больных СД обусловлен нарушением процессов микроциркуляции, формированием иммуносупрессии, развитием диабетической нефропатии, а также нейропатии мочевого пузыря с нарушением пассажа мочи [3].
Так, почти у 80% больных СД формируется диабетическая нефропатия (ДН), возможным результатом которой является развитие тяжелой почечной недостаточности (ХБП 4-5) [5]. Также к развитию ИМП у больных СД предрасполагают глюкозурия, сниженная антибактериальная активность мочи, нарушение защитной способности нейтрофилов [2; 3].
Огромная роль в развитии СД принадлежит иммунной дизрегуляции и воспалительному процессу, что сопровождается гиперпродукцией провоспалительных цитокинов, которые способствуют формированию инсулинорезистентности, гипергликемии (чаще постпрандиальной), участвуют в развитии микроангиопатии, нефропатии и др. [6; 7]. Это ведет к хронизации ИМП, снижению функции почек, что, в свою очередь, утяжеляет течение СД и ухудшает прогноз заболевания [6]. Огромное влияние на течение ИМП у больных СД оказывает состояние фагоцитов, прежде всего – нейтрофилов, которым принадлежит важная роль в интегративном ответе иммунной системы при инфекционно-воспалительных заболеваниях [8].
Большое значение в связи с этим отводится противовоспалительным цитокинам, в частности интерлейкину 4 (IL4) [6]. IL4 продуцируется Т-хелперами, тучными клетками, базофилами, эозинофилами, стромальными клетками костного мозга и др. [6]. IL4 является ключевым регулятором гуморального и адаптивного иммунитета, оказывает стимулирующее воздействие на пролиферацию и дифференцировку активированных Т- и В-лимфоцитов, синтез антител, повышает активность фагоцитов, синтез колониестимулирующих факторов, лейкопоэз, оказывает выраженное противовоспалительное действие [6].
Все вышеизложенное обосновывает необходимость включения иммуномодуляторов в схемы терапии пациентов, страдающих ИМП на фоне СД [9].
Учитывая этиопатогенетические аспекты развития и течения ИМП у больных СД, в качестве иммуномодулятора был использован ликопид (Лп). Лп стимулирует функциональную активность фагоцитов (ФАН), усиливает антигенпрезентирующую функцию макрофагов, пролиферацию Т- и B-лимфоцитов [10].
Установлена эффективность Лп в лечении заболеваний, сопровождающихся формированием иммуносупрессии [10]. Показано, что применение Лп способствует снижению уровня провоспалительных цитокинов (IL-1ß, IL-6 и TNF–α) [10].
Цель исследования: оценить воздействие Лп на содержание IL4 и ФАН у пациентов, страдающих СД и ИМП.
Материалы и методы исследования
Обследовано 155 чел., распределенных на следующие группы: группа «СД» - больные СД, группа «ИМП» - больные ИМП, группа «СД+ИМП» - больные СД и ИМП, группа «СД+ИМП+Лп» - больные СД и ИМП, получавшие иммуномодулятор Лп (табл. 1). Пациенты с СД, ИМП, СД с ИМП получали терапию в соответствии с действующими стандартами лечения [11; 12], а больные в группе «СД+ИМП+Лп» - дополнительно принимали Лп (10 мг 1 раз в сутки, 10 дней (ООО научно-производственное предприятие «Пептек ЗАО, Россия»)). Также в исследование была включена группа «Здоровые» - без признаков (анамнестических, клинических) СДII, ИМП и других заболеваний (таблица).
Характеристика групп пациентов
|
Показатели |
Здоровые |
СД |
ИМП |
СД+ИМП |
СД+ИМП+Лп |
|
|
|
Абс. (%) |
|
|
|
|
|
|
Количество пациентов (n) |
35 |
31 |
32 |
30 |
27 |
|
|
Пол |
М |
11 (31,4%) |
14 (45,2%) |
15 (42,86%) |
10 (33,3%) |
3 (11,1%) |
|
Ж |
24 (68,6%) |
17 (54,8%) |
20 (57,14%) |
20 (66,7%) |
24 (88,9%) |
|
|
Возраст (лет) |
43,0 [39,0-50,0] |
60,0 [53,0-63,0] |
56,0 [47,0-63,0] |
56,50 [50,0-61,0] |
60,0 [53,0 – 64,0] |
|
|
Индекс массы тела (кг/м2) |
24,80 [22,50-25,80] |
29,60 [27,40-34,90] |
27,05 [23,50-28,60] |
32,0 [28,60-33,50] |
32,65 [29,10-37,0] |
|
|
АД |
сАД |
110 [110,0 – 120,0] |
140 [120,0 – 150,0] |
117 [110,0 – 120,0] |
140 [130,0 – 150,0] |
130 [120,0 – 160,0] |
|
дАД |
70,0 [70,0 – 80,0] |
80,0 [80,0 – 90,0] |
72,5 [70,0 – 80,0] |
80,0 [80,0 – 90,0] |
80,0 [80,0 – 90,0] |
|
|
Стаж СДII (лет) |
- |
9,50 [6,0-12,0] |
- |
9,0 [8,0-11,0] |
6,50 [5,0 – 11,0] |
|
|
Стаж ИМП (лет) |
- |
- |
9,0 [7,0 – 10,0] |
9,0 [7,0 – 11,0] |
9,0 [7,0 – 11,0] |
|
Верификацию диагноза у пациентов осуществляли на основании «Алгоритмов специализированной медицинской помощи больным сахарным диабетом» (8-й выпуск, 2017 г.). Основание: данные анамнеза, результаты клинических и лабораторных исследований (определение базального и суточного уровня глюкозы в сыворотке крови, а также - в суточной порции мочи, содержания HbA1c), консультативные заключения офтальмолога и невролога.
Критерии включения:
|
• возраст |
• старше 18 лет |
|
• диагноз СД II |
• ранее установленный |
|
• лабораторные данные |
• гликемия натощак<7,0 ммоль/л • гликемия постпрандиальная<19,0 ммоль/л • HbA1<7%) |
|
• диагноз ИМП (пиелонефрит) |
• подтвержденный |
Каждый пациент подписывал информированное согласие на включение в исследование и соблюдение этических принципов.
Во всех группах определяли: уровень IL-4 методом иммуноферментного анализа (тест-система ЗАО «Вектор-Бест», г. Новосибирск), интенсивность оксидантного метаболизма нейтрофилов (спонтанный и индуцированный НСТ-тест - НСТсп, НСТинд) и ФАН [13].
Результаты регистрировали на 1-м визите (до лечения), а в группах «СД+ИМП» и «СД+ИМП+Лп» - на 2-м (через 2 недели), 3-м (через 4 недели) и 4-м визитах (через 8 недель лечения).
Статистическую обработку проводили с помощью методов вариационной статистики [14], пакета программ Statistica 10.0. Нормальность распределения данных определяли с использованием критерия Шапиро-Вилка. Оценку значимости различий определяли, вычисляя медиану и межквартильный интервал, дисперсионный анализ - с помощью Н-критерия Краскела-Уоллиса, для множественных сравнений использовали Q-критерий Дана. Критический уровень значимости р для статистических критериев принимали равным 0,05.
Результаты исследования и их обсуждение
Уровень IL4 в группах «СД» и «ИМП» был статистически значимо выше такового в группе «Здоровые» (p=0,00076 и p=0,00053 соответственно) (рис. 1).
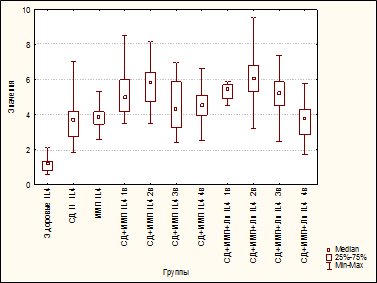 |
Рис. 1. Уровень IL4 (пг/мл) у здоровых, больных сахарным диабетом, больных инфекцией мочевых путей, больных сахарным диабетом и инфекцией мочевых путей, больных сахарным диабетом и инфекцией мочевых путей и получавших ликопид
Как и в предыдущих исследованиях, у больных СД отмечалось снижение интенсивности образования активных форм кислорода (АФК) как в НСТсп, так и в НСТинд (рис. 2) [15]. Это сочеталось с подавлением ФАН: в 3,75 раза по сравнению с группой «Здоровые» (p≤0,00001), и в 3,2 раза – с группой «ИМП» (p≤0,00001) (рис. 2) [15]. Эти результаты согласуются с данными других авторов и подтверждают дисфункциональное состояние фагоцитов у больных СД [7].
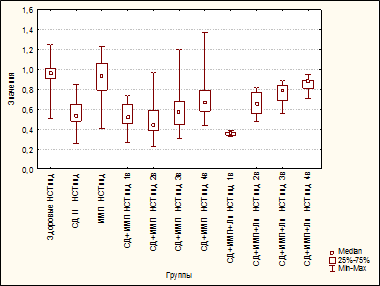 |
Рис. 2. Интенсивность кислородзависимого метаболизма ПМЯЛ в индуцированном НСТ-тесте у здоровых, больных сахарным диабетом, больных инфекцией мочевых путей, больных сахарным диабетом и инфекцией мочевых путей, получавших ликопид
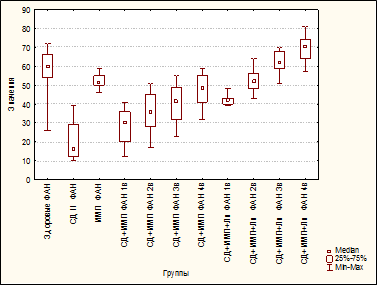 |
Рис. 3. Фагоцитарная активность нейтрофилов у здоровых, больных сахарным диабетом, больных инфекцией мочевых путей, больных сахарным диабетом и инфекцией мочевых путей, больных сахарным диабетом и инфекцией мочевых путей, получавших ликопид
В группе больных СД с ИМП уровень IL4 до лечения (1-й визит) и через 2 недели лечения (2-й визит) был почти в 2 раза выше, чем у больных СД без ИМП (p=0,01205, p=0,00041 соответственно) и в 2 раза ниже, чем у больных ИМП (p=0,00771, p=0,00022 соответственно) (рис. 1). Через 4 и 8 недель от начала лечения уровень IL4 не отличался от такового в группе «СД» (p=1,0000 и p=1,0000). При этом, как и в группе больных «СД», уровень IL4 в группе «СД+ИМП» на все сроки наблюдения был статистически значимо выше, чем в группе «Здоровые» (рис. 1).
Ранее было показано, что в группе «СД+ИМП» идентично изменялась интенсивность образования АФК в НСТсп: сохранялась на уровне таковой в группе «СД», будучи статистически значимо ниже таковой в группах «ИМП» (в т.ч. в остром периоде заболевания) и «Здоровые» вплоть до 4-го визита (рис. 2). К 4-му же визиту интенсивность образования АФК повышалась до уровня показателей в группах «ИМП» и «Здоровые» (рис. 2) [15].
В условиях же индукции интенсивность кислородзависимого метаболизма ПМЯЛ на протяжении первых трех визитов была статистически значимо ниже аналогичных показателей в группах «ИМП» и «Здоровые», оставаясь на одном уровне с показателями в группе «СД». И лишь к 4-му визиту интенсивность образования АФК повышалась, оставаясь почти на 30% ниже таковой в группах «ИМП» и «Здоровые» [15].
Идентично изменялись показатели ФАН: в острый период (1-й визит) ФАН вдвое превышала показатель в группе «СД», оставаясь статистически значимо ниже вплоть до 4-го визита, чем в группах «ИМП» и «Здоровые» (рис. 3) [15]. Только к 8-й неделе от начала терапии уровень ФАН возрастал до уровня такового в группах «ИМП» (p=1,0000) и «Здоровые» (p=0,45198) (рис. 3).
Эти данные свидетельствуют о подавлении микробицидного потенциала ПМЯЛ у больных СДII с ИМП, что существенно снижает результативность терапии и способствует длительному течению ИМП.
В группе больных «СД+ИМП+Лп» уровень IL4 как до лечения (1-й визит), так и в процессе лечения (2-й, 3-й визиты) был статистически значимо выше аналогичного показателя в группах «СД» (p=0,00255, p=0,00002, p=0,03383 на 1, 2 и 3-й визиты) и «ИМП» (p=0,00155, p=0,00001, p=0,02329 на 1, 2 и 3-й визиты) (рис. 1), снижаясь к 4-му визиту до уровня больных СДII без ИМП (p=1,0000) (рис. 1). Динамика уровня IL4 в группе «СД+ИМП+Лп» не имела существенных отличий от таковой в группе «СД+ИМП» (рис. 1).
В группе «СД+ИМП+Лп» интенсивность образования АФК в НСТсп как до лечения, так и через 2 недели не превышала показателей у больных СД без ИМП, значимо превышая ее на 3-й и 4-й визиты (p=0,00133, p≤0,00001 - на 3-й и 4-й визиты) (рис. 2). И, напротив, в начале наблюдения интенсивность образования АФК в группе «СД+ИМП+Лп» была статистически значимо ниже таковой в группах «ИМП» (p≤0,00001, p=0,00005 - на 1-й и 2-й визиты) и «Здоровые» (p≤0,00001, p=0,00018 - на 1-й и 2-й визиты), повышаясь на 3-й и 4-й визиты до уровня показателей в группах «ИМП» (p=0,24825, p=1,0000 соответственно) и «Здоровые» (p=0,48912, p=1,0000 соответственно) (рис. 2). Вместе с тем динамика показателей НСТсп в группе «СД+ИМП+Лп» не имела отличий от показателей в группе «СД+ИМП».
В условиях же индукции применение Лп обеспечило повышение интенсивности образования АФК на 3-й и 4-й визиты до уровня в группе «Здоровые» (p=0,61042, p=1,0000), статистически значимо превышая уровень образования АФК в НСТинд у больных СД без ИМП (p=0,00714 и p≤0,00001 соответственно) (рис. 2).
Изменение показателей оксидантного метаболизма ПМЯЛ в группах «СД+ИМП+Лп» и «СД+ИМП» выявило, что на 2-й и 3-й визиты, интенсивность образования АФК в группе «СД+ИМП+Лп» превышала таковую в группе «СД+ИМП» более чем на 20% (p=0,04766 и p=0,01488 соответственно) (рис. 2). Через 8 недель от начала терапии интенсивность образования АФК в группе «СД+ИМП+Лп» превышала таковую в группе «СД+ИМП» почти на 20%, не достигая, однако, статистической значимости (рис. 2). Это свидетельствует о значительном улучшении микробицидного потенциала нейтрофильных гранулоцитов у больных СДII с ИМП, получавших Лп, и предполагает большую результативность антимикробной и противовоспалительной терапии.
Включение Лп в стандартную схему лечения ИМП у больных СД привело к статистически значимому увеличению ФАН в сравнении с группой «СД» - начиная со 2-й недели (p=0,02257, p≤0,00001 - на 2, 3 и 4-й визиты) (рис. 3). В сравнении с группой «ИМП» показатели ФАН на первых трех визитах в группе «СД+ИМП+Лп» не отличались, а к 4-му визиту – статистически значимо превышали их (p=0,00257) (рис. 3).
Следует подчеркнуть, что уже через 2 недели от начала терапии в группе «СД+ИМП+Лп» показатели ФАН были статистически значимо выше таковых в группе «СД+ИМП» (p=0,00137 через 2 недели и p≤0,00001 – через 4 и 8 недель) (рис. 3). Более того, начиная со 2-го визита фагоцитарная активность в группе «СД+ИМП+Лп» достигала уровня таковой в группе «Здоровые» (p=1,000 – на 2-й и 3-й визиты, p=0,16170 – на 4-й визит) (рис. 3).
Полученные данные согласуются с известной способностью Лп повышать неспецифическую резистентность, фагоцитарную и бактерицидную способность фагоцитов, а также с его эффективностью в лечении гнойно-воспалительных и гнойно-септических заболеваний [10].
Резюмируя, можно отметить, что добавление Лп к стандартной схеме лечения больных СД с ИМП способствовало нормализации уровня IL4, восстановлению биоцидного потенциала и увеличению поглотительной активности нейтрофильных гранулоцитов.
Результаты исследования позволяют заключить, что добавление Лп к стандартной терапии ИМП у больных СД корректирует иммунный дисбаланс и существенно улучшает функциональное состояние нейтрофильных гранулоцитов.
Выводы
1. У больных в группе «СД» выявлено повышение уровня IL4, снижение функциональной активности нейтрофилов (фагоцитарная способность, микробицидный потенциал).
2. У больных в группе «СД+ИМП» на фоне стандартной терапии наблюдается высокий уровень IL4, подавление кислородзависимого метаболизма и фагоцитарной активности нейтрофилов.
3. Включение ликопида в стандартную терапию больных СД с ИМП не изменяет уровень IL4, восстанавливает микробицидную способность и повышает фагоцитарную активность нейтрофильных гранулоцитов.
Библиографическая ссылка
Алибаева Г.Ф., Моругова Т.В., Насыртдинова А.Д. ВЛИЯНИЕ ЛИКОПИДА НА УРОВЕНЬ ИНТЕРЛЕЙКИНА-4 И ФУНКЦИОНАЛЬНУЮ АКТИВНОСТЬ НЕЙТРОФИЛОВ У БОЛЬНЫХ САХАРНЫМ ДИАБЕТОМ 2 ТИПА С ИНФЕКЦИЕЙ МОЧЕВЫХ ПУТЕЙ // Современные проблемы науки и образования. 2021. № 1. ;URL: https://science-education.ru/en/article/view?id=30519 (дата обращения: 02.06.2026).
DOI: https://doi.org/10.17513/spno.30519



