Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
MULTIDISCIPLINARY APPROACH IN SURGICAL TREATMENT OF COLORECTAL CANCER IN PATIENTS WITH SENIOR AND SENIOR AGE WITH HIGH OPERATIONAL ANESTHESIA RISK
Колоректальный рак представляет одну из основных проблем современной клинической онкологии. Анализ публикаций последних лет свидетельствует о неуклонной тенденции роста заболеваемости колоректальным раком (КРР) во всем мире [1; 2]. Ежегодно в мире регистрируют более 1 200 000 больных раком ободочной и прямой кишки и 639 000 смертей в результате прогрессии заболевания. По статистике онкологической заболеваемости, колоректальный рак занимает одно из лидирующих мест во всех экономически развитых странах мира, составляя 10-15% от общего количества больных раком [3; 4]. По последним данным, эта патология занимает третье место в структуре заболеваемости и второе место в структуре смертности от онкологических причин в большинстве развитых стран, в том числе в России [5; 6]. Ежегодно наблюдается увеличение заболеваемости на 2,3% и смертности на 3,4% [7]. Прогнозируется, что в первой половине XXI века колоректальный рак прочно займет первое место в структуре онкологических заболеваний [8].
При КРР хирургический подход является основным компонентом современного эффективного лечения и единственным способом радикального удаления опухоли [9; 10].
В настоящее время возрастает частота плановых оперативных вмешательств при КРР у лиц пожилого и старческого возраста с выраженной сопутствующей патологией [11; 12]. Последнее связано с развитием медицинских технологий и демографическим процессом старения населения. Между тем, по мнению экспертов международного общества гериартрической онкологии (SIOG), частый неудовлетворительный результат лечения данной группы пациентов связан с неоптимальной оценкой периоперационных рисков при наличии значимых сопутствующих заболеваний [13; 14]. Исходы хирургического лечения больных пожилого и старческого возраста КРР в случаях вовремя и адекватно компенсированных нехирургических нозологий сопоставимы с результатами подобной тактики у пациентов до 60 лет.
Тревожным фактором является высокий уровень летальности на первом году жизни после установления диагноза, обусловленный тем, что при первичном обращении пациентов к врачу запущенные формы рака (III-IV стадии) уже имеют более 70% пациентов, страдающих раком ободочной кишки, и более 60% пациентов с установленным раком прямой кишки, при этом хирургическому лечению подвергается лишь около 40% от всех больных [15; 16].
По-прежнему предпринимаются попытки поиска простого универсального и достоверного показателя, способного в скрининговом режиме оценить вероятность наиболее значимых сердечно-сосудистых осложнений при не кардиальных хирургических вмешательствах. Известен способ прогнозирования осложнений со стороны сердечно-сосудистой системы в ближайшем послеоперационном периоде путем анализа анамнестических, клинико-инструментальных и лабораторных факторов риска с построением шкал, таких как APACHE II, III, SOFA, SAPS I, II, MODS и др. Также применяются дополнительные характеристики коморбидного статуса, в частности модифицированный индекс Charlson, индекс сосуществующих болезней ICED (Index of Co-Existent Disease) и др. [17].
Перечисленные шкалы и индексы в большинстве случаев не имеют четких количественных критериев и не учитывают в должной степени особенностей возрастных нормативов функциональных показателей, особенно у пациентов старших возрастных групп, тем самым не всегда адекватно прогнозируя развитие острой левожелудочковой недостаточности в раннем послеоперационном периоде. В связи с этим весьма перспективным видится разработка и внедрение в клиническую практику дополнительных эхокардиографических критериев, в частности индекса Tei, способствующих повышению точности прогнозирования возможной острой левожелудочковой недостаточности у пациентов, перенесших оперативное лечение по поводу колоректального рака. Данный метод в кардиологической практике является относительно простым, неинвазивным, информативным и высоковоспроизводимым способом определения скрытых гемодинамических нарушений, тем самым позволяя эффективно прогнозировать послеоперационные осложнения со стороны сердечно-сосудистой системы.
Цель исследования. Улучшить результаты хирургического лечения колоректального рака у больных пожилого и старческого возраста путем применения разработанного алгоритма периоперационного ведения больных с высоким операционно-анестезиологическим риском.
Материал и методы. Проанализированы результаты обследования и хирургического лечения 172 пациентов колоректальным раком. Больные были представлены в возрасте от 61 до 96 лет. Все пациенты были распределены на две группы. В первую – основную - группу (86 человек) вошли лица, средний возраст которых составил 75,1+8,0 лет. В этой группе применялся расширенный алгоритм периоперационного ведения пациентов: вся когорта больных оценивалась специалистами мультидисциплинарной бригады, дополнительно включавшей кардиолога и специалиста по функциональной диагностике с последующим расчетом индекса Tei. Вторую - контрольную - группу (86 человек) составили пациенты, средний возраст которых был 75,6+8,4 года. В этой группе не применялся разработанный алгоритм диагностики. В основную группу пациентов вошли: мужчин - 45, женщин - 41, в контрольную - 33 и 53 соответственно. В целом доля мужчин в этих группах составляла 45,3%, женщин 54,7%. По возрастным категориям всех пациентов разделили на: пожилой возраст (61-75 лет) – 96 чел., старческий (76-90 лет) – 69 чел. и долгожителей (90 лет и старше) – 7 чел. (табл. 1).
Таблица 1
Распределение обследованных пациентов по возрастным группам
|
Возрастные группы (лет) |
Группы наблюдения |
Всего |
||||
|
Основная |
Контрольная |
|||||
|
Абс. |
% |
Абс. |
% |
Абс. |
% |
|
|
61-75 |
48 |
55,8 |
43 |
50,0 |
91 |
52,9 |
|
76-90 |
35 |
40,7 |
34 |
39,5 |
69 |
40,1 |
|
90 и ст. |
3 |
3,5 |
4 |
4,7 |
7 |
4,1 |
|
Итого |
86 |
100,0 |
86 |
100,0 |
172 |
100,0 |
У всех пациентов как основной, так и контрольной группы был отягощенный полиморбидный фон (табл. 2), в среднем на одного пациента приходилось два и более заболеваний, а также высокий операционно–анестезиологический риск по шкале МНОАР, соответственно 7,1+1,1 и 6,7+1,1 балла.
Таблица 2
Частота случаев сопутствующей патологии у пациентов наблюдаемых групп
|
Сопутствующая патология |
Контрольная группа |
Основная группа |
|
Стабильная стенокардия напряжения |
44 (51,2%) |
32 (37,2%) |
|
Атеросклеротический кардиосклероз |
80 (93,0%) |
82 (95,3%) |
|
Постинфарктный кардиосклероз |
23 (26,7%) |
10 (11,6%) |
|
Гипертоническая болезнь I-III ст. |
86 (100%) |
86 (100%) |
|
Хроническая сердечная недостаточность |
47 (54,7) |
36 (41,9%) |
|
ОНМК в анамнезе |
15 (17,4%) |
12 (13,9%) |
По локализации опухолевого процесса пациенты были представлены двумя группами: злокачественное новообразование ректосигмоидного соединения - имелось более чем у половины обследованных больных контрольной группы (54,6%) и злокачественное новообразование прямой кишки - в основной группе у 60,5% пациентов.
Среди клинических особенностей пациентов обеих групп обращали на себя внимание характеристики болевого абдоминального синдрома. У 109 человек из всех обследованных данная симптоматика по субъективной оценке воспринималась в качестве «наиболее значимой». При этом сами боли, их локализация, характер и интенсивность были различными, с превалированием как в основной - 59,0%, так и в контрольной группе - 50,1% схваткообразных болей.
Инструментальная часть клинико-функционального исследования дополнительно включала расчет Tei-индекса. В процессе эхокардиографического исследования трансторакально из верхушечного доступа в 5-камерном сечении в режиме постоянно-волновой доплерографии одновременно регистрировали трансмитральный и трансаортальный потоки. Миокардиальный индекс (Tei-индекс) рассчитывается как сумма периодов изоволюметрического сокращения (IVCT) и изоволюметрического расслабления (IVRT), отнесенная ко времени изгнания (ET) по формуле Теi= (IVCT+IVRT) / ЕТ. В норме Tei-индекс для левого желудочка составляет 0,36 ± 0,04. Данный показатель оценивали в предоперационном периоде, на 1-е сутки и 10-11-е сутки послеоперационного периода, как общепринятые временные реперные точки, в наибольшей степени отражающие возможные потенциально неблагоприятные клинические периоды ухудшения состояния пациентов с возможным развитием сердечно-сосудистых осложнений.
При величине миокардиального индекса дисфункции сердца более 0,79 у пациентов диагностировались клинико-инструментальные предикторы развития острой левожелудочковой сердечной недостаточности. Указанные значения Tei-индекса свидетельствовали об удельном повышении систолической составляющей в кардиоцикле, удлинение которой снижало эффективность сократимости левого желудочка, являясь непосредственной потенциальной причиной развития левожелудочковой сердечной недостаточности. Больные с подобными значениями Tei-индекса были отнесены нами в «группу риска». Дальнейшая кардиотропная фармакологическая коррекция позволяла профилактировать возможные сердечно-сосудистые осложнения.
Статистическая обработка полученных результатов, в процессе выполнения работы, проводилась с использованием системы STATISTICA for Windows (версия 7). Сравнение частотных характеристик (пол, осложнения, сопутствующая патология) качественных показателей проводилось с помощью непараметрических методов Йетса (для малых групп), критерия Фишера.
Результаты. После реализации стандартного предоперационного диагностического общепринятого алгоритма, включающего в себя как лабораторные (клинический анализ крови, показатели биохимического анализа крови, анализ крови на гепатиты, кровь на ВИЧ и сифилис, определение группы крови и резус-фактора, общий анализ мочи), так и функциональные методы исследования (ЭКГ, рентгенография органов грудной клетки и ультразвуковое исследование органов брюшной полости), всем больным основной группы дополнительно рассчитывался индекс Tei. Перед операцией из 86 пациентов 27 имели показатели Tei-индекса, превышающие референтные – от 0.41 до 0,89. Данный «разброс» потребовал дифференцированного подхода к коррекции возможных сердечно-сосудистых осложнений. Пороговым значением индекса, в наибольшей степени отражающим риск развития острой левожелудочковой сердечной недостаточности, в раннем послеоперационном периоде – на 1-е сутки - оказался показатель 0,79. Подобное повышение миокардиального индекса наблюдалось у 16 пациентов. Отметим, что наиболее частыми клиническими проявлениями, сопутствовавшими значимому возрастанию Tei-индекса, являлись гипертензивные состояния (67%), реже ишемия миокарда (52%) либо их сочетание (38%). Проведенная патогенетическая кардиотропная терапия позволила компенсировать указанные изменения, и на 10-11-е сутки после операции только у 4 больных Tei-индекс превышал значение 0,41. Указанные данные представлены в таблице 3.
Таблица 3
Динамика Tei-индекса у пациентов основной группы в периоперационном периоде
|
Период измерения |
Величина индекса Tei |
|
|
0,36 ± 0,04 |
0,41-0,89 |
|
|
До операции |
59 |
27 |
|
На 1-е сутки |
70 |
16 |
|
На 10-11-е сутки |
82 |
4 |
С учетом приведенных данных в группе больных «высокого риска» дополнительная превентивная кардиотропная фармакологическая коррекция проводилась в процессе всего послеоперационного лечения по результатам мониторирования Tei-индекса в указанных ранее реперных точках: на 1-е сутки и 10-11-е сутки после операции.
Таким образом, пациенты основной группы имели существенное преимущество в профилактике риска развития сердечно-сосудистых осложнений в периоперационном периоде над контрольной группой, что в последующем позволило расширить операбельность и тем самым увеличить количество радикальных операций (табл. 4).
Таблица 4
Структура выполненных оперативных вмешательств
|
Исходы |
Контрольная группа |
Основная группа |
Итого |
|
Брюшно-промежностная экстирпация |
13 (15,12%) |
50 (58,14%) |
63 |
|
Передняя резекция |
12 (13,95%) |
17 (19,77%) |
29 |
|
Операция по типу Гартмана |
16 (18,6%) |
14 (16,28%) |
30 |
|
Выведение стомы |
43 (50,0%) |
5 (5,81%) |
48 |
|
Прочие |
2 (2,33%) |
0 |
2 |
При анализе числа послеоперационных осложнений в обеих группах после использования способа прогнозирования ближайших послеоперационных осложнений со стороны сердечно-сосудистой системы у больных, перенесших радикальное оперативное лечение (92 пациента, из них основная группа - 67 человек и контрольная - 25 человек) по поводу колоректального рака, установили, что наибольший процент осложнений встречался в контрольной группе и составил 12,0% (11 пациентов), а в основной – 7,6% (7 пациентов). Указанные данные представлены в таблице 5.
Таблица 5
Сердечно-сосудистые послеоперационные осложнения у пациентов, оперированных радикально (n=92)
|
Исходы |
Контрольная группа (n=25) |
Основная группа (n=67) |
|
ОИМ |
4 (16,0 %) |
2 (2,9%) |
|
ТЭЛА |
2 (8,0%) |
1 (1,5%) |
|
Нарушения сердечного ритма |
3 (12,0%) |
2 (2,9%) |
|
Острая сердечная недостаточность |
2 (8,0%) |
2 (2,9%) |
При сравнительном анализе было выявлено, что в обеих группах первое место по структуре хирургических осложнений занимают гнойно-воспалительные осложнения в области хирургического вмешательства, а именно: нагноение со стороны лапаротомной раны встречалось в основной группе у 3 (3,5%) пациентов, в контрольной у 5 (5,8%) пациентов и было связано с операцией Гартмана и выведением колостомы. Со стороны промежностной раны в основной группе отмечены 3 (3,5%) серомы глухого шва промежности и 4 (4,7%) нагноения в области промежности, при тампонировании пресакрального пространства. Второе место по частоте встречаемости заняло внутрибрюшное кровотечение. У пациентов основной группы оно составило 2,3% (2 человека) (передняя резекция и брюшно- промежностная экстирпация). В контрольной - 4,7% (4 человека), из них двум (две передние резекции) пациентам была выполнена релапаротомия. В структуре послеоперационных осложнений также встречалась ранняя спаечная непроходимость, в обеих группах было по 1 (1,2%) случаю устранения ранней спаечной тонкокишечной непроходимости. Обоим пациентам была выполнена релапаротомия. У остальных 77 (89,5%) пациентов основной и у 72 (83,6%) контрольной группы послеоперационный период протекал гладко (рисунок).
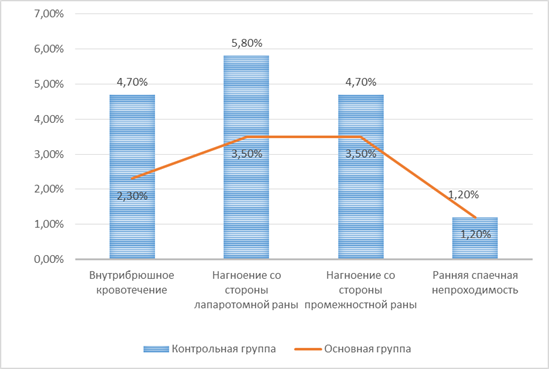
Послеоперационные осложнения зоны хирургического вмешательства
При этом послеоперационная летальность всех оперированных пациентов (n=172) составила 5,8% (5 пациентов) в основной группе и 25,5% (22 пациента) в контрольной.
При сравнительном анализе причин летального исхода пациентов обеих групп (n=172) первое место по частоте встречаемости занимает полиорганная недостаточность. Так, в контрольной группе она составила 11,6% (10 человек), а в основной 3,5% (3 человека). Из 10 пациентов контрольной группы четырем была выполнена передняя резекция прямой кишки, одному - брюшно-промежностная экстирпация, а пяти пациентам выполнялось выведение сигмостомы в качестве паллиативного метода лечения. Всем трем пациентам основной группы выполнялся разный объем оперативного лечения: одному пациенту была выполнена передняя резекция прямой кишки, второму - операция по типу Гартмана, третьему - выведение сигмостомы, все три пациента были оперированы по поводу верхне- и среднеампулярного рака прямой кишки. Несмотря на проводимую фармакологическую терапию и профилактику осложнений со стороны сердечно-сосудистой системы, в послеоперационном периоде мы столкнулись с летальностью от острого инфаркта миокарда и тромбоэмболии легочной артерии: по 1 пациенту (1,3%) в основной группе и 5 (5,8%) и 7 (8,1%) пациентов в контрольной (табл. 6).
Таблица 6
Причины летального исхода в исследуемых группах
|
Причина летального исхода |
Контрольная группа (n=86) |
Основная группа (n=86) |
|
ПОН |
10 (11,6%) |
3 (3,5%) |
|
ОИМ |
5 (5,8%) |
1 (1,2%) |
|
ТЭЛА |
7 (8,1%) |
1 (1,2%) |
Заключение
Таким образом, мультидисциплинарный подход с использованием дополнительных функционально-диагностических инструментальных методов исследования, в частности доплерэхокардиографии с расчетом Tei-индекса, позволяет спрогнозировать развитие ранней левожелудочковой недостаточности в периоперационном периоде. Это дает возможность оптимизировать хирургическое лечение колоректального рака у пациентов старшей возрастной группы с высоким полиморбидным фоном, скорректировать сердечно-сосудистый риск и тем самым увеличить операбельность и снизить количество послеоперационных осложнений.
Библиографическая ссылка
Павелец К.В., Лобанов М.Ю., Шишликова Ю.С., Русанов Д.С. МУЛЬТИДИСЦИПЛИНАРНЫЙ ПОДХОД В ХИРУРГИЧЕСКОМ ЛЕЧЕНИИ КОЛОРЕКТАЛЬНОГО РАКА У БОЛЬНЫХ ПОЖИЛОГО И СТАРЧЕСКОГО ВОЗРАСТА С ВЫСОКИМ ОПЕРАЦИОННО- АНЕСТЕЗИОЛОГИЧЕСКИМ РИСКОМ. // Современные проблемы науки и образования. 2018. № 5. ;URL: https://science-education.ru/en/article/view?id=27908 (дата обращения: 16.05.2026).
DOI: https://doi.org/10.17513/spno.27908



