В структуре детской заболеваемости и смертности одно из ведущих мест занимают пневмонии. В связи с этим ВОЗ объявила пневмонию основной причиной детской смертности и провозгласила «Глобальный план действий по профилактике пневмонии и борьбе с ней» (2015). Актуальна эта проблема и в странах СНГ в связи с ростом частоты, тяжести клинического течения и исхода заболевания у детей раннего возраста [1-3].
Общеизвестно, что этиологическая структура пневмоний изменчива, имеет явную региональную зависимость, и тяжесть клинического течения у детей раннего возраста во многом зависит от совокупности влияния модифицируемых и не модифицируемых факторов риска [4; 5]. Однако нет данных об особенностях этиологической структуры и клинических особенностях внебольничных пневмоний (ВП) у детей раннего возраста из многодетных семей.
Цель исследования
Определить этиологические и клинико-лабораторные особенности внебольничных пневмоний у детей раннего возраста из многодетных семей.
Материал и методы исследования
Всего полное клинико-лабораторное обследование проведено у 179 больных ВП детей раннего возраста. Больные дети были разделены на 2 группы:
1. Основная (1-я) группа - 118 детей с пневмонией из многодетных семей.
2. Контрольная (2-я) группа - 61 больной ребёнок из малодетных семей.
К многодетным отнесены семьи, имеющие 4 и более детей, к малодетным – до 4 детей.
При клинической оценке были использованы ключевые критерии оценки тяжести ВП у детей в зависимости от возраста, предлагаемые академиком Чучалиным А.Г. с соавт. (2015). Классификация тяжести пневмонии, наличие опасных признаков и степень дыхательной недостаточности оценивались по карманному справочнику «Оказание стационарной помощи детям» [6; 7]. Детям проводились общеклинические анализы, рентгенография органов грудной клетки, иммунологическое исследование субпопуляций лимфоцитов с использованием моноклональных антител.
Концентрации IgG, IgM, IgA в сыворотке крови определялись методом радиальной иммунодиффузии. При изучении чувствительности пневмопатогенов к антибактериальным препаратам определялась МИК - минимальная ингибирующая концентрация антибиотика. Чем ниже МИК, тем более силен антибиотик по отношению к выявленным микроорганизмам.
Атипичная микрофлора изучена методами ПЦР с использованием ПЦР–амплификатора «Bio-Rad» и «Rotor-Gene Q» в режиме реального времени (Real-Time ПЦР) и ИФА с использованием тест-систем Vector Best (г. Новосибирск) на фотометре BioRad-680 (США) и иммуноферментном анализаторе (ImmunoChem-2100).
Статистический анализ данных выполнен с использованием программ «SPSS 16». Достоверность разности относительных показателей закодирована следующими кодами: * - р<0,05 (95,0%); ** - р<0,01 (99,0%); *** - р<0,001 (99,9%).
Результаты исследования и их обсуждение
Установлено, что в нашем регионе в этиологической структуре ВП у детей раннего возраста в целом и по группам достоверно (р<0,001) преобладает грамположительная флора (рис. 1).
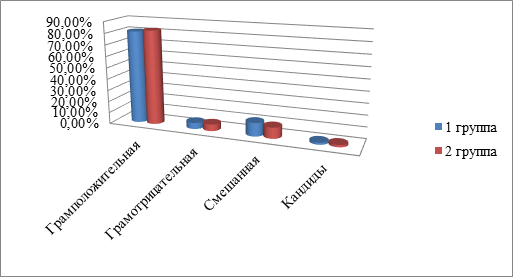
Рис. 1. Этиоструктура ВП у детей исследованных групп
Из грамположительной флоры практически в равных соотношениях высеиваются стрептококки и стафилококки (р>0,05) (табл. 1).
Таблица 1
Характеристика этиологической микрофлоры у больных
|
Флора |
163 |
100% |
|
1. Грамположительная флора |
133 |
81,60%*** |
|
Streptococcus |
76 |
57,14% |
|
Штаммы: - pneumonia - pyogenes - viridans |
31 8 37 |
40,79%** 10,53% 48,68%** |
|
Staphylococcus |
57 |
42,86% |
|
Штаммы: - epidermidis - aureus - hemoliticus |
3 20 34 |
5,26 35,08 59,66** |
|
2. Грамотрицательная |
9 |
5,52% |
|
Из них: - гемофильная палочка - энтеробактерии - кишечная палочка |
5 3 1 |
55,55% 33,33% 11,11% |
|
Смешанная флора |
18 |
11,04% |
|
Кандиды |
3 |
1,84 |
Примечание: * - р<0,05 (95,0%); ** - р<0,01 (99,0%); *** - р<0,001 (99,9%).
Стрептококки представлены патогенными и не патогенными штаммами в равных соотношениях (р>0,05). Из стафилококков чаще (94,74%, р<0,001) высеваются патогенные штаммы: Staphylococcus hemoliticus и реже (р<0,01) - Staphylococcus аureus. Грамотрицательная флора в основном представлена Haemofilus influenza, реже - Enterobacter и Escherichia coli. Существенные различия выявляются при сравнительном изучении этиологической структуры ВП по группам (рис. 2).
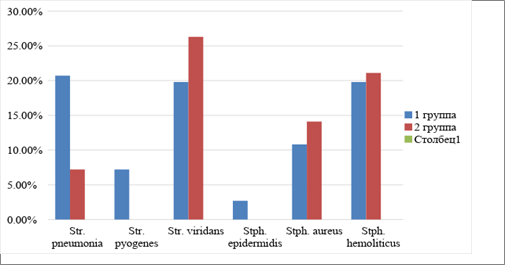
Рис. 2. Сравнительная этиоструктура ВП у больных детей
Наиболее патогенные штаммы стрептококков чаще определяются в основной группе (р<0,001). Из стафилококков патогенные штаммы высеваются в обеих группах практически с одинаковой частотой (р>0,05). В то же время роль атипичной микрофлоры в этиологии ВП у детей раннего возраста не значительна (табл. 2).
Таблица 2
Данные ПЦР и ИФА на атипичную микрофлору у больных ВП детей
|
Группа |
1-я группа |
2-я группа |
||
|
|
ПЦР |
ИФА (Ig G) |
ПЦР |
ИФА (Ig G) |
|
Chlamydia pneumonia |
2 (10%) |
2 (10%) |
- |
- |
|
Chlamydia trachomatis |
- |
- |
- |
- |
|
Mycoplasma pneumonia |
1 (5,0%) |
- |
- |
- |
|
Mycoplasma hominis |
- |
|
- |
|
|
CMV |
3 (15%) |
3 (15%) |
1 (6,6%) |
1 (6,6%) |
|
HSVI |
1 (5,0%) |
2 (10%) |
1 (6,6%) |
1 (6,6%) |
|
HSVI I |
- |
|
- |
|
|
Toxoplasma gondii |
- |
3 (15%) |
- |
2 (13,3%) |
|
Ureaplasma |
|
сомн. 2 (10%) полож. 1 (5%) |
|
1 (6,6%) |
Методы ПЦР и ИФА дают почти идентичные результаты, что позволяет нам рекомендовать метод ИФА как более доступный и менее затратный.
Выявлена высокая резистентность пневмопатогенов почти ко всем пенициллинам. Чувствительность сохранена только к оксациллину, амоксиклаву и ампициллин сульбактаму. Из цефалоспоринов наиболее высокая чувствительность отмечается к цефалоспоринам 2-го и 3-го поколения, из аминогликозидов - к амикацину, из макролидов – к эритромицину. Высокочувствительны к пневмопатогенам практически все антибиотики резерва.
Установлено, что у больных из многодетных семьей отмечается более отягощённый анамнез заболевания: длительное амбулаторное лечение (более 6–9 дней), самолечение и поздняя госпитализация больных, в основном по линии СМП в тяжёлом состоянии (р<0,001).
При изучении особенностей клинического течения установлено, что у больных из многодетных семей чаще отмечаются опасные для жизни симптомы: снижена активность сосания груди или из бутылочки, отмечаются судороги и нарушение сознания (р<0,001). У них более выражены симптомы тяжёлой дыхательной недостаточности: тахипноэ или брадипноэ/апноэ, кряхтящее дыхание, выраженное втяжение грудной клетки и диффузный цианоз (р<0,01). Более часты легочные и внелегочные осложнения (р<0,01). А ателектазы наблюдаются только у детей основной группы. В этой же группе в 1,75 раза выше уровень летальных случаев.
На рентгенограмме у них более обширны (р<0,001) воспалительные изменения в лёгких (рис. 3).
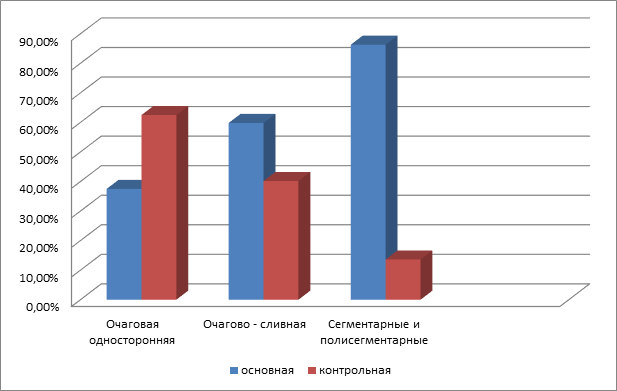
Рис. 3. Рентгенологические данные у детей исследованных групп
У больных детей основной группы достоверно чаще (р<0,001) отмечается ЖДА вплоть до тяжёлой степени, высокий лейкоцитоз (р<0,01), нейтрофилёз (р<0,01), палочкоядерный сдвиг влево (р<0,001) и значительно ускоренное СОЭ (р<0,001), чем у больных из малодетных семей. Достоверно выше (р<0,05) маркёры воспалительного процесса (табл. 3).
Таблица 3
Показатели С-реактивного белка и прокальцитонина у больных детей
|
Группа |
Основная |
Контрольная |
Всего |
Нормативные показатели |
|
С-реактивный белок |
7,53±0,58* |
5,99±0,92 |
7,02±0,49 |
0-5 мг/мл |
|
Прокальцитонин |
3,14±0,23* |
2,46±0,20 |
3,01±0,19 |
0,5-2 нг/мл |
Значительные различия выявлены при изучении иммунологического статуса у больных основной и контрольной групп (табл. 4).
Таблица 4
Показатели клеточных и гуморальных иммунных реакций у больных
|
Группа |
Основная |
Контрольная |
Всего |
Нормативные показатели |
|
CD3+ |
39,87±1,87*** |
51,54±2,56 |
44,54±1,71 |
58-69% |
|
CD4+ |
29,56±0,94** |
36,85±1,44 |
32,47±0,95 |
38-50% |
|
CD8+ |
22,8±0,92 |
22,0±0,65 |
22,48±0,60 |
18-25% |
|
СД 4/СД 8 |
1,15±0,08* |
1,75±0,15 |
1,17±0,09 |
1,25 – 2,5 |
|
СД19 |
18,98±2,44 |
15,62±1,98 |
17,63±1,66 |
14 - 44 |
|
CD3-HLA-DR |
15,92±1,7* |
10,65±1,46 |
13,83±1,22 |
|
|
Ig A |
0,84±0,02г/л |
1,8±0,33 г/л |
1,17±0,14 г/л |
0,9-4,74 г/л |
|
IgM |
1,59±0,13 г/л |
1,73±0,15 г/л |
1,64±0,09г/л |
0,48-2,5 г/л |
|
IgG |
13,63±0,54 г/л |
12,3±0,73 г/л |
13,09±0,44 г/л |
6,81-16,40 г/л |
Примечание: * - р<0,05 (95,0%); ** - р<0,01 (99,0%); *** - р<0,001 (99,9%).
В основной группе больных детей достоверно снижен уровень CD3+ (р<0,001), CD4+ (р<0,01) и СД4/СД8 (р<0,05). В то же время противовоспалительные медиаторы: Т-лимфоциты-супрессоры (СД8), Т-лимфоциты-киллеры (CD3-HLA-DR) и активированные В-лимфоциты (СД19) находятся на нижней границе нормы. Достоверно снижены уровни Ig A и Ig М (р<0,05).
Следовательно, в генезе развития ВП у детей раннего возраста из многодетных семей играет роль депрессия клеточных и дисфункция гуморальных иммунных реакций, характерные для системных воспалительных процессов, свидетельствующих о неадекватности иммунного ответа, что и обуславливает тяжесть клинического течения и исход заболевания.
Выводы
1. Региональной особенностью этиологической структуры ВП у детей раннего возраста является преобладание (81,6%, р<0,001) грамположительной флоры. У детей из многодетных семей чаще (р<0,01) высеиваются патогенные штаммы стрептококков (St. Pneumonia, St. Pyogenes). Роль атипичной микрофлоры (хламидии, микоплазмы) малозначима.
2. Выявлена высокая резистентность пневматогенных микроорганизмов к пенициллинам, за исключением оксациллина (91-94%, МИК![]() =0,25), амоксиклава (77,7-80%, МИК
=0,25), амоксиклава (77,7-80%, МИК![]() 4,2) и ампициллин сульбактама (60-61%, МИК
4,2) и ампициллин сульбактама (60-61%, МИК![]() 8). Сохраняется высокая чувствительность пневмопатогенов из аминогликозидов - к амикацину, из макролидов – к эритромицину, цефалоспоринам 2-го и 3-го поколения, карбопенемам и другим антибиотикам резерва.
8). Сохраняется высокая чувствительность пневмопатогенов из аминогликозидов - к амикацину, из макролидов – к эритромицину, цефалоспоринам 2-го и 3-го поколения, карбопенемам и другим антибиотикам резерва.![]()
3. Особенностью клинического течения ВП у детей из многодетных семей являются: крайне отягощённый анамнез заболевания, поздняя госпитализация с клиническими симптомами, опасными для жизни. В более тяжелой степени выражены симптомы дыхательной и сердечно-сосудистой недостаточности, симптомы интоксикации. Отмечены более обширные воспалительные инфильтраты в лёгких с наличием легочных и внелегочных осложнений (р<0,001). Более выражены воспалительные изменения крови, показатели С-реактивного белка и прокальцитонина (р<0,001). А также выше частота летальных случаев.
4. Тяжесть клинического течения и исход ВП у детей из многодетных семей обусловлены депрессией клеточных и дисфункцией гуморальных иммунных реакций, характерных для системных воспалительных процессов.
Выводы
1. Региональной особенностью этиологической структуры ВП у детей раннего возраста является преобладание (81,6%, р<0,001) грамположительной флоры. У детей из многодетных семей чаще (р<0,01) высеиваются патогенные штаммы стрептококков (St. Pneumonia, St. Pyogenes). Роль атипичной микрофлоры (хламидии, микоплазмы) малозначима.
2. Выявлена высокая резистентность пневматогенных микроорганизмов к пенициллинам, за исключением оксациллина (91-94%, МИК![]() =0,25), амоксиклава (77,7-80%, МИК
=0,25), амоксиклава (77,7-80%, МИК![]() 4,2) и ампициллин сульбактама (60-61%, МИК
4,2) и ампициллин сульбактама (60-61%, МИК![]() 8). Сохраняется высокая чувствительность пневмопатогенов из аминогликозидов - к амикацину, из макролидов – к эритромицину, цефалоспоринам 2-го и 3-го поколения, карбопенемам и другим антибиотикам резерва.
8). Сохраняется высокая чувствительность пневмопатогенов из аминогликозидов - к амикацину, из макролидов – к эритромицину, цефалоспоринам 2-го и 3-го поколения, карбопенемам и другим антибиотикам резерва.![]()
3. Особенностью клинического течения ВП у детей из многодетных семей являются: крайне отягощённый анамнез заболевания, поздняя госпитализация с клиническими симптомами, опасными для жизни. В более тяжелой степени выражены симптомы дыхательной и сердечно-сосудистой недостаточности, симптомы интоксикации. Отмечены более обширные воспалительные инфильтраты в лёгких с наличием легочных и внелегочных осложнений (р<0,001). Более выражены воспалительные изменения крови, показатели С-реактивного белка и прокальцитонина (р<0,001). А также выше частота летальных случаев.
4. Тяжесть клинического течения и исход ВП у детей из многодетных семей обусловлены депрессией клеточных и дисфункцией гуморальных иммунных реакций, характерных для системных воспалительных процессов.
Библиографическая ссылка
Боконбаева С.Д., Алиева Ж.К. ОСОБЕННОСТИ ЭТИОЛОГИЧЕСКОЙ СТРУКТУРЫ И КЛИНИКИ ВНЕБОЛЬНИЧНЫХ ПНЕВМОНИЙ У ДЕТЕЙ РАННЕГО ВОЗРАСТА ИЗ МНОГОДЕТНЫХ СЕМЕЙ // Современные проблемы науки и образования. 2018. № 4. ;URL: https://science-education.ru/en/article/view?id=27832 (дата обращения: 25.04.2026).



