Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
ANALYSIS OF THE STRESS-STRAIN STATE OF THE SYSTEM UPON THE INSTALLATION OF DENTAL IMPLANTS OF VARIOUS DESIGNS IN TERMS OF BONE ATROPHY OF THE MANDIBLE
Актуальность. Одной из проблем при выборе конструкции дентального имплантата является обеспечение адекватного распределения напряжений в системе кость-имплантат и физиологическое состояние костной ткани. Жизнеспособность костной ткани определяют напряжения и деформации, возникающие при установке дентального имплантата [5]. Наиболее современным и информативным виртуальным методом изучения биомеханики дентального имплантата является трехмерное многофакторное математическое моделирование напряженно-деформированного состояния при разных клинических ситуациях [8,9,10]. Во многих работах изучаются закономерности биомеханики внутрикостных дентальных имплантатов, вводимых в костную ткань после удаления зуба, влияние параметров имплантата на напряженно-деформированное состояние зоны имплантации; реакция костной ткани, окружающей имплантат, на функциональные нагрузки [2,3,6,8,10,11]. Не реже встречаются работы, в которых с помощью методов математического моделирования производится оценка конструкций съемных протезов, опирающихся на имплантаты и биологические ткани полости рта, влияния направления установки имплантатов на прочностные характеристики протезов, распределения нагрузок и вероятности необратимых изменений в костной ткани при ортопедическом лечении [8,11]. Возникающие напряжения в костной ткани характеризуют действия внутренних сил. При жевании (при физиологических нагрузках) эти силы в зубочелюстной системе человека являются физиологическими раздражителями, которые способствуют функционированию и поддержанию обменных процессов в костной ткани, поддерживают баланс между процессами моделирования и ремоделирования. В случае перегрузки или недостаточной степени напряжения, в костной ткани может происходить атрофия и резорбция, что ведет к переимплантиту. Для успешного функционирования остеоинтегрированного имплантата в кости челюсти особую роль играет адекватность передачи нагрузочных сил, к определяющим факторам при этом относятся площадь прямого контакта и направление передаваемых ей нагрузок: чем больше площадь, тем значительнее рассредоточение нагрузки на кость [1,2,3].
Наличие пор в эндооссальной части имплантата способствует глубинному прорастанию костной ткани в металлическую структуру, в результате чего возникает биологическая фиксация имплантата. Для прорастания кости оптимальным является размер пор 100–200 мкм [1,2]. В дентальном имплантате из нетканого титанового имплантата со сквозной пористостью получали поры в имплантате диаметром от 120 до 200 мкм, что составило 70 ± 10 % пористости [4]. При нагрузке имплантата в виртуальном режиме полученные результаты показателей величины и характера распределения участков с повышенным напряжением в костной ткани позволяют провести высокоточную диагностику и планирование этапа имплантации и ортопедических процедур. На этапе разработки имплантата анализ экспериментальной модели напряженно-деформированного состояния обеспечивает возможность коррекции параметров конструкции имплантата. Цель исследования. Целью нашей работы было математическое обоснование оптимальной конструкции дентального имплантата, функционирующего в условиях атрофии костной ткани. Материалы и методы. Для решения поставленной задачи были использованы методы математического моделирования и пакет для конечно-элементного анализа ANSYS (ANSYS, Inc). С позиции механики деформируемого твердого тела система имплантат-костная ткань представляет собой неоднородную трехмерную задачу. Неоднородность задачи обусловлена тем, что необходимо учитывать различие в механических характеристиках металлоконструкций (дентальный имплантат, накостная пластина), компактной и губчатой кости. Если свойства металлоконструкций (стальных или из титановых сплавов) для рассматриваемых величин нагрузок можно принять линейно упругими, то механические свойства компактной и губчатой кости только приближенно можно рассматривать как нелинейно упругие. Восстановление исходной формы после снятия нагрузки (свойство упругости) для костной ткани происходит, но с некоторой задержкой по времени. Описание напряженного состояния твердого тела в трехмерном случае происходит с использованием тензора (или таблицы размером 3х3) напряжений ![]() (i, j=1, 2, 3) и деформаций
(i, j=1, 2, 3) и деформаций ![]() (i, j=1, 2, 3). Из 9 компонент тензора только 6 являются независимыми функциями координат, т.е. изменяются от точки к точке. Каждая компонента тензора напряжений соответствует величине внутренних усилий в твердом теле, направленных перпендикулярно площадкам в системе координат XYZ. Решение подобных по сложности задач аналитическим способом встречает на своем пути труднопреодолимые математические трудности, в связи с чем используют численные методы, хорошо развитые и активно используемые в последнее время, в частности метод конечных элементов (МКЭ). Основная идея МКЭ состоит в том, что область задачи на первом этапе разбивается на меньшие, и решение вычисляется для каждого участка (но так, чтобы в промежуточных точках решения совпадали). Построение геометрической модели нижней челюсти вели с использованием средств, заложенных в пакет анализа ANSYS. Геометрические размеры сечения челюсти, полученные при помощи компьютерной томографии (КТ), с незначительной идеализацией импортировали в ANSYS и на них выстраивали модель челюсти. На втором этапе было проведено разбиение модели на конечные элементы. Производили оптимизацию конечно-элементной сетки: выполняли сгущение сетки в областях (зона контакта винтов с костной тканью), где возможно значительное изменение напряжений (концентрация напряжений). Было создано несколько моделей (рис.3) с различной степенью детализации (от 20 до 200 тыс. элементов), из которых была выбрана оптимальная, состоящая из 50 тысяч конечных элементов, которая позволяет оперативно проводить конечно-элементный расчёт (в пределах1–4 часов) и в то же время обеспечивает приемлемую точность. В ходе исследования были построены конечно-элементные модели, описывающие распределение напряжений в нижней челюсти при установке дентальных имплантатов трех видов. Конечно-элементные модели построены на основе данных КТ нижней челюсти пациента с признаками атрофии костной ткани. 3-D модели включали в себя кортикальную и губчатую костные ткани, цилиндрический внутрикостный имплантат, цилиндрический внутрикостный имплантат и накостную мини пластину, фиксированную винтами, втулку из НТМСП, штифт-распорку и абатмент. Размеры внутрикостных частей имплантатов составили: диаметр 3,5 мм, длина 5 мм. На двух моделях имитировали применение внутрикостного цилиндрического и внутрикостно-накостного имплантатов. Моделировали установку имплантатов в проекции отсутствующих 6, 7 зубов. На третьей модели имитировали функционирование дентального внутрикостно-накостного имплантата (ДВНИ) со втулкой из нетканого титанового материала со сквозной пористостью (НТМСП), разработанного на кафедре челюстно-лицевой хирургии и стоматологии СамГМУ (патент на полезную модель №162614 от 01.06.2016 г.). После построения конечноэлементной модели нижней челюсти задавали физико-механические свойства для рассматриваемых материалов, учитывая, что реологические соотношения для биологических материалов носят сложный, нелинейный характер. Величину модуля Юнга для костной ткани принимали равной 13,7 ГПа, а коэффициент Пуассона 0,3 [7]. После построения математической модели к ней были приложены граничные условия и нагрузки. Нагрузки принимали 2-х видов: вертикальная 200 Н и горизонтальная 20 Н. Указанные величины наиболее часто использовались другими авторами. Они являются усредненными значениями действующих значений и поэтому удобны для сравнения. Затем был проведён расчёт напряженно-деформированного состояния для трех вариантов конструкции имплантата: стандартный внутрикостный, внутрикостно-накостный имплантат и внутрикостно-накостный имплантат со втулкой из нетканого титанового материала.
(i, j=1, 2, 3). Из 9 компонент тензора только 6 являются независимыми функциями координат, т.е. изменяются от точки к точке. Каждая компонента тензора напряжений соответствует величине внутренних усилий в твердом теле, направленных перпендикулярно площадкам в системе координат XYZ. Решение подобных по сложности задач аналитическим способом встречает на своем пути труднопреодолимые математические трудности, в связи с чем используют численные методы, хорошо развитые и активно используемые в последнее время, в частности метод конечных элементов (МКЭ). Основная идея МКЭ состоит в том, что область задачи на первом этапе разбивается на меньшие, и решение вычисляется для каждого участка (но так, чтобы в промежуточных точках решения совпадали). Построение геометрической модели нижней челюсти вели с использованием средств, заложенных в пакет анализа ANSYS. Геометрические размеры сечения челюсти, полученные при помощи компьютерной томографии (КТ), с незначительной идеализацией импортировали в ANSYS и на них выстраивали модель челюсти. На втором этапе было проведено разбиение модели на конечные элементы. Производили оптимизацию конечно-элементной сетки: выполняли сгущение сетки в областях (зона контакта винтов с костной тканью), где возможно значительное изменение напряжений (концентрация напряжений). Было создано несколько моделей (рис.3) с различной степенью детализации (от 20 до 200 тыс. элементов), из которых была выбрана оптимальная, состоящая из 50 тысяч конечных элементов, которая позволяет оперативно проводить конечно-элементный расчёт (в пределах1–4 часов) и в то же время обеспечивает приемлемую точность. В ходе исследования были построены конечно-элементные модели, описывающие распределение напряжений в нижней челюсти при установке дентальных имплантатов трех видов. Конечно-элементные модели построены на основе данных КТ нижней челюсти пациента с признаками атрофии костной ткани. 3-D модели включали в себя кортикальную и губчатую костные ткани, цилиндрический внутрикостный имплантат, цилиндрический внутрикостный имплантат и накостную мини пластину, фиксированную винтами, втулку из НТМСП, штифт-распорку и абатмент. Размеры внутрикостных частей имплантатов составили: диаметр 3,5 мм, длина 5 мм. На двух моделях имитировали применение внутрикостного цилиндрического и внутрикостно-накостного имплантатов. Моделировали установку имплантатов в проекции отсутствующих 6, 7 зубов. На третьей модели имитировали функционирование дентального внутрикостно-накостного имплантата (ДВНИ) со втулкой из нетканого титанового материала со сквозной пористостью (НТМСП), разработанного на кафедре челюстно-лицевой хирургии и стоматологии СамГМУ (патент на полезную модель №162614 от 01.06.2016 г.). После построения конечноэлементной модели нижней челюсти задавали физико-механические свойства для рассматриваемых материалов, учитывая, что реологические соотношения для биологических материалов носят сложный, нелинейный характер. Величину модуля Юнга для костной ткани принимали равной 13,7 ГПа, а коэффициент Пуассона 0,3 [7]. После построения математической модели к ней были приложены граничные условия и нагрузки. Нагрузки принимали 2-х видов: вертикальная 200 Н и горизонтальная 20 Н. Указанные величины наиболее часто использовались другими авторами. Они являются усредненными значениями действующих значений и поэтому удобны для сравнения. Затем был проведён расчёт напряженно-деформированного состояния для трех вариантов конструкции имплантата: стандартный внутрикостный, внутрикостно-накостный имплантат и внутрикостно-накостный имплантат со втулкой из нетканого титанового материала.
Результаты исследования и их обсуждение. В результате получено распределение значений напряжений и деформаций как в текстовой, так и в графической формах. На рис. 1, 2 и 3 приведены виды из рассматриваемых случаев нагружения для величины усилия в области моляра 200 и 20 Н. Цвета на модели соответствуют найденным величинам напряжений. Нами изучена общая картина напряженно-деформированного состояния кортикального слоя, губчатого слоя, напряжения в области апекса имплантата для трех вариантов конструкции при вертикальной нагрузке в 200 Н. Максимальные эквивалентные напряжения в эксперименте в костной ткани для внутрикостного цилиндрического имплантата составили 5,1Мпа, для внутрикостно-накостного имплантата 4,6 МПа, для внутрикостно-накостного имплантата со втулкой из НТМСП 2,8 МПа. При вертикальной нагрузке равнораспределенное напряжение в большей степени концентрируется в области витков имплантата, расположенных в кортикальной кости. При вертикальной нагрузке происходит снижение максимальных значений напряжений в конечно-элементных моделях нижней челюсти при моделировании установки внутрикостно-накостного имплантата со втулкой из НТМСП на 45,09 % по сравнению с внутрикостным цилиндрическим имплантатом и на 39,1 % по сравнению с внутрикостно-накостным имплантатом за счет введения в конструкцию дополнительной стабилизирующей накостной мини пластины и втулки из НТМСП.
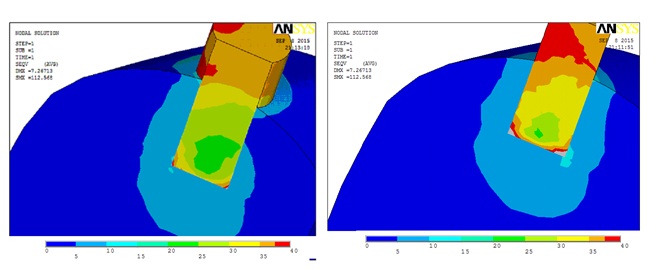
Рис. 1. Распределение интенсивности напряжений в нижней челюсти для вертикальной и горизонтальной нагрузок, стандартный внутрикостный имплантат
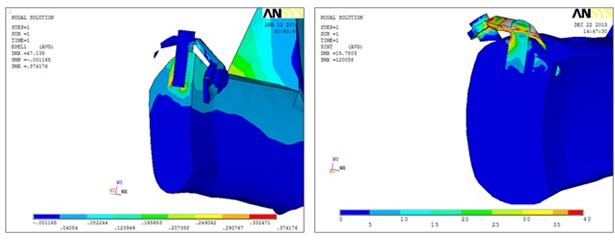
Рис. 2. Распределение интенсивности деформаций в нижней челюсти для горизонтальной и вертикальной нагрузок, внутрикостно-накостный имплантат
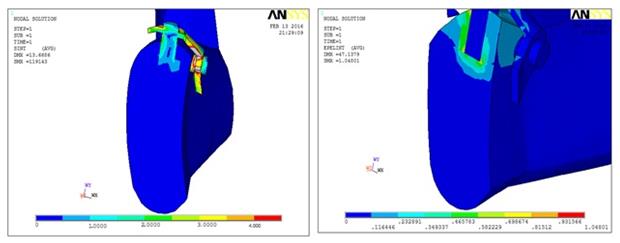
Рис. 3. Распределение интенсивности напряжений в нижней челюсти для горизонтальной и вертикальной нагрузки, внутрикостно-накостный имплантат со втулкой из НТМСП
Помимо вертикальной, имплантат еще испытывает и горизонтальную (неосевую) нагрузку, которая по данным отечественных и зарубежных исследователей оказывает наибольшее воздействие на напряженно-деформированное состояние костной ткани. Этот факт напрямую влияет на выбор конструкции дентального имплантата, а также на планирование и конструирование ортопедической конструкции. При анализе максимальных напряжений в костной ткани, развивающихся при горизонтальной нагрузке, мы рассматривали общую картину напряженно-деформированного состояния для трех вариантов конструкции. При исследовании перемещений при горизонтальной нагрузке 20 Н максимальное значение напряжений для внутрикостного цилиндрического имплантата составило 1,04 МПа, для внутрикостно-накостного имплантата 0,87 МПа, для внутрикостно-накостного имплантата со втулкой из НТМСП 0,48 МПа. Максимальные напряжения концентрировались в витках с противоположной стороны приложенной нагрузки. При горизонтальной нагрузке происходит снижение максимальных значений напряжений в конечно-элементных моделях нижней челюсти при моделировании установки внутрикостно-накостного имплантата со втулкой из НТМСП на 53,8 % по сравнению с внутрикостным цилиндрическим имплантатом и на 44,8 % по сравнению с внутрикостно-накостным имплантатом за счет введения в конструкцию дополнительной стабилизирующей накостной мини пластины и втулки из НТМСП. В результате проведенного анализа видно, что при вертикальной и горизонтальной нагрузке и введении в конструкцию дополнительных элементов, таких как дополнительная накостная пластина и установленная втулка из НТМСП, снижается напряжение в системе в целом. Цилиндр-втулка из НТМСП дополнительно обладает демпферными свойствами, способствует прорастанию вглубь пор имплантата костной ткани. Это дает основание считать, что имплантат выдержит большую окклюзионную нагрузку близкую или равную нативному зубу, по сравнению с классическими винтовыми цилиндрическими имплантатами, и обеспечит долговременное, полноценное функционирование и стабильность имплантата в условиях атрофии костной ткани. Эти исследования позволили изменить подходы к моделированию конструкции дентального имплантата, функционирующего в условиях атрофии костной ткани. Выводы. Использование имплантатов с поддерживающей пластиной и втулкой из нетканого титанового материала приводит к значимому снижению действующих напряжений в костной ткани челюсти от приложенной нагрузки в условиях атрофии костной ткани. С точки зрения процессов биомеханики конструкция дентального внутрикостно-накостного имплантата со втулкой из НТМСП обоснована и может являться приоритетной при ортопедическом лечении больных с отсутствием зубов в условиях атрофии костной ткани.
Библиографическая ссылка
Монаков Д.В. АНАЛИЗ НАПРЯЖЕННО-ДЕФОРМИРОВАННОГО СОСТОЯНИЯ СИСТЕМЫ ПРИ УСТАНОВКЕ ДЕНТАЛЬНЫХ ИМПЛАНТАТОВ РАЗЛИЧНЫХ КОНСТРУКЦИЙ В УСЛОВИЯХ АТРОФИИ КОСТНОЙ ТКАНИ НИЖНЕЙ ЧЕЛЮСТИ // Современные проблемы науки и образования. 2017. № 1. ;URL: https://science-education.ru/en/article/view?id=26141 (дата обращения: 13.05.2026).



