Известно, что длительное стрессорное воздействие способно оказывать существенное влияние на показатели гомеостаза всего организма, в поддержании которого важную роль играет печень. При этом развивающиеся стресс-индуцированные изменения метаболических процессов отражаются на функциональном состоянии данного органа как за счет мобилизации его резервов, так и вследствие повреждающего воздействия целого ряда факторов, в том числе активных метаболитов кислорода [12; 15]. Необходимо отметить, что при различных видах стрессорного воздействия важную роль для дальнейшего развития стрессорной реакции играет эмоционально-негативное напряжение, при котором изменяется метаболизм печеночных ферментов, принадлежащих к семье цитохрома Р450 (CYP) [11] и производных кофермента А [8], развивается стеатоз и неалкогольная жировая болезнь печени [7], запускается апоптоз гепатоцитов [9]. Частой причиной стрессорных реакций является болевое раздражение, вызывающее значительную активацию систем эмоционально-негативного подкрепления.
Модулирующее влияние на выраженность стрессорных сдвигов оказывают стресс-лимитирующие системы организма. К числу регуляторных пептидов, играющих важную роль в функционировании данных механизмов, относится дельта-сон индуцирующий пептид (ДСИП), обладающий анальгетическими [5], стресс-лимитирующими [13], нейромодулирующими [2] и мембраностабилизирующими [14] эффектами.
На основании вышеизложенных данных целью данной работы явилось изучение влияния дельта-сон индуцирующего пептида при внутрибрюшинном введении на морфологию печени в условиях хронического эмоционально-болевого стресса.
Материал и методы исследования
Эксперименты выполнены на 60 крысах-самцах Вистар массой 310-340 г, разделенных на группы по 10 животных, которые содержались в стандартных условиях вивария со свободным доступом к воде и пище при 12-часовом световом режиме и контролируемой температуре (22±2 °С). Исследования проводили в промежуток времени с 9 до 14 часов.
Все исследования проводились с соблюдением принципов Хельсинкской декларации о гуманном отношении к животным и в соответствии с решением регионального этического комитета.
В работе использовали дельта-сон индицирующий пептид, имеющий формулу (NH2)Trp-Ala-Gly-Gly-Asp-Ala-Ser-Gly-Glu(COOH), синтезированный в НИИ химии Санкт-Петербургского государственного университета. Пептид растворяли в физиологическом растворе и вводили внутрибрюшинно за 60 мин до начала каждого стрессорного воздействия в дозах 40, 120, 360 и 1080 мкг/кг массы тела. Контрольным животным вводили эквивалентные объемы физиологического раствора из расчета 1 мл на 1 кг массы тела. Интактные животные не получали стрессорного воздействия, на протяжении эксперимента им вводили объемы физиологического раствора, эквивалентные таковым у контрольных стрессированных крыс.
Хронический эмоционально-болевой стресс создавали электрокожным раздражением лап попарно сгруппированных животных в камере с электрифицированным решетчатым полом. С помощью программируемого электростимулятора на пол камеры в течение 30 минут подавались импульсы тока силой 0,2-0,3 mА продолжительностью 5 секунд с межимпульсным интервалом 15 секунд в течение 5 дней подряд [6; 10].
Животных выводили из эксперимента путем обескровливания под эфирным наркозом. При заборе органов осуществляли взвешивание печени и с учетом массы животного вычисляли индекс ее относительной массы («печень/тело»). Для этого рассчитывали отношение массы органа к массе тела соответствующего животного и умножали полученный результат на 1000.
После выведения животных из эксперимента для морфологического исследования атравматично забирали печень. Для фиксации кусочков изучаемых органов использовали формалин 10% в фосфатном буфере, затем проводили заливку тканей в парафин, готовили гистологические срезы толщиной 6-7 мкм и окрашивали гематоксилином и эозином.
Морфологическое исследование гистологических препаратов проводили на микроскопе Nikon Eclipse Ci со штатной цифровой цветной камерой. Морфологическую оценку состояния печеночной ткани осуществляли на основе морфометрического исследования гистологических срезов [4]. При помощи калиброванной окулярной сетки определяли следующие показатели: число митозов (ЧМ), число двухъядерных клеток (ЧДК), число целых ядросодержащих клеток (ЧК) и число точек пересечения сетки (ЧСТ), не попадающих на срезы гепатоцитов и их ядер. По результатам этих измерений рассчитывали: показатель паренхиматозной плотности (ПП=1-ЧСТ/Nузл) функциональной клеточной массы (ФКМ=(ЧК/Sсет)*ПП*100000), характеризующий паренхиматозно-стромальные отношения в единице объема ткани; показатель ядерной массы (ЯМ=(ЧК+ЧДК)/Sсет)*ПП*100000), отражающий ядерно-цитоплазматические отношения в единице объема ткани; индекс массы двухъядерных клеток (ИМДК=((ЧДК/ЧК)/Sсет)*ПП*100000), свидетельствующий о степени реализации восстановительных резервов единицы объема печеночной ткани; масс-митотический индекс (ММИ=((ЧМ/ЧК)/Sсет)*ПП*100000), показывающий пролиферативную активность единицы объема печеночной ткани; показатель функционального кариоклеточного индекса (ФККИ=ЯМ/ФКМ), характеризующий количество ядерного материала в клетке единицы объема печеночной ткани; показатель средней площади среза гепатоцитов (СПСГ=(Sсет/ЧК)*ПП), пропорциональной его функциональной активности.
Характер распределения признаков в статистической выборке определяли с использованием критерия Колмогорова-Смирнова. Значимость полученных результатов оценивали с помощью непарного параметрического t-критерия Стьюдента и непараметрического критерия Манна-Уитни в зависимости от типа распределения признаков. Статистическую обработку проводили с использованием программного пакета MS Excel и программной среды вычислений R [3]. Результаты считали достоверными при p<0,05.
Результаты исследования и их обсуждение
Как видно из таблицы, хронический эмоционально-болевой стресс вызывал у животных существенное изменение показателей морфологического состояния печени. Так, у стрессированных крыс по сравнению с интактными наблюдалось достоверное снижение функциональной клеточной массы (на 15%, p<0,005) (рисунок), что свидетельствует о развитии полнокровия, застойных явлений и холестаза в ткани печени. Хронический стресс также вызывал повышение показателя ядерной массы (на 16%, p<0,01), что указывает на развитие дегенеративных и деструктивных процессов в печеночной ткани. Повышение масс-митотического индекса на 66% (p<0,05) отражает увеличение текущей (относительно кратковременной) интенсивности функционирования и снижение глубины репаративных резервов. Повышение средней площади среза гепатоцита при стрессе на 26% (p<0,001) не имеет самостоятельного значения в морфологической оценке ткани печени, так как оно не сопровождалось одновременным увеличением индекса массы двухъядерных клеток.
Дисперсионный анализ выявил достоверные различия при сравнении исследуемых показателей внутри всех исследуемых групп животных для всех анализируемых показателей (p<0,01-0,005), кроме паренхиматозной плотности.
Влияние ДСИП на показатели восстановительных процессов печени и относительную массу органов при хроническом эмоционально-болевом стрессе (M±m)
|
Группа Показатель |
Интактные животные |
Действие стресса |
||||
|
Контроль |
Введение ДСИП в дозе: |
|||||
|
40 |
120 |
360 |
1080 мкг/кг |
|||
|
ФКМ |
88,2±3,0 |
74,7±2,91 |
88,3±4,3* |
95,6±5,3* |
82,5±1,7* |
95,6±5,0* |
|
ЯМ |
97,3±3,9 |
81,6±3,31 |
96,9±4,9* |
107,8±107,8* |
91,3±2,1* |
103,9±5,3* |
|
ИМДК |
0,17±0,02 |
0,16±0,01 |
0,16±0,01 |
0,22±0,02* |
0,17±0,01 |
0,15±0,01 |
|
ММИ |
0,010±0,001 |
0,017±0,0021 |
0,016±0,002 |
0,014±0,002 |
0,014±0,002 |
0,007±0,001* |
|
ПП |
0,52±0,01 |
0,54±0,01 |
0,53±0,01 |
0,54±0,02 |
0,50±0,01* |
0,55±0,01 |
|
ФККИ |
1,10±0,01 |
1,09±0,01 |
1,10±0,00 |
1,13±0,01* |
1,11±0,01 |
1,09±0,01 |
|
СПСГ |
312,6±8,2 |
394,7±12,41 |
323,7±6,3* |
311,0±9,6* |
299,9±6,7* |
316,0±6,2* |
|
Индекс «Печень/тело» |
34,9±0,9 |
38,6±1,11 |
32,2±1,0* |
34,1±0,8* |
32,9±0,8* |
30,9±0,7* |
Примечание: * – р < 0,05-0,001 по сравнению с контрольной группой крыс, подвергавшихся стрессу;
1 – р < 0,05-0,001 по сравнению с интактной группой крыс, не подвергавшихся стрессу.
Во всех использованных дозах ДСИП вызывал увеличение сниженных под действием стресса показателей. Так, при введении пептида в наименьшей используемой дозе 40 мкг/кг функциональная клеточная масса увеличивалась на 18% (p<0,05), ядерная масса – на 19% (p<0,05). Увеличение дозы до 120 мкг/кг сопровождалось усилением эффектов пептида, что проявлялось в возрастании функциональной клеточной массы на 28% (p<0,01) и ядерной массы на 32% (p<0,001). Повышение дозы ДСИП до 360 мкг/кг вызывало сходные по направленности эффекты, однако их выраженность была наименьшей среди всех подопытных групп животных: функциональная клеточная масса повышалась на 10% (p<0,05), а ядерная масса – на 12% (p<0,05). При увеличении вводимой дозы пептида до 1080 мкг/кг его влияние на морфометрические показатели снова существенно возросло: функциональная клеточная масса увеличилась на 28% (p<0,001), а ядерная масса – на 27% (p<0,01) по сравнению с показателями контрольной группы. Полученные данные свидетельствуют об уменьшении под действием ДСИП выраженности дегенеративных и деструктивных процессов, вызванных стрессорным воздействием, а также о снижении полнокровия, застойных явлений, холестаза в печеночной ткани. Кроме того, в дозах 120 и 1080 мкг/кг отмечалась тенденция к активации пролиферативных процессов и нарастанию интенсивности функционирования ткани печени.
Также при введении в дозе 40 мкг/кг пептид вызывал снижение средней площади среза гепатоцита на 18% (p<0,001), в дозе 120 мкг/кг – на 21% (p<0,001), в дозе 360 мкг/кг – на 24% (p<0,001) и в дозе 1080 мкг/кг – на 20% (p<0,001). Однако указанные изменения в данном случае не могут быть использованы для морфологической оценки ткани печени, так как они не сопровождались одновременным повышением масс-митотического индекса.
Наряду с вышеуказанным выраженным действием ДСИП в отдельных подопытных группах имели место и менее значительные эффекты. Так, в дозе 120 мкг/кг пептид по сравнению с контрольной группой увеличивал индекс массы двухъядерных клеток на 39% (p<0,05) и функциональный кариоклеточный индекс на 3% (p<0,01), что может отражать активацию восстановительных процессов и накопление репаративных резервов. В дозе 360 мкг/кг у стрессированных животных ДСИП вызывал небольшое, но достоверно значимое снижение паренхиматозной плотности (на 8%, p<0,05), которая характеризует паренхиматозно-стромальное соотношение. После введения пептида в дозе 1080 мкг/кг отмечено снижение масс-митотического индекса на 58% (p<0,01), что свидетельствует о повышении глубины репаративных резервов при снижении интенсивности функционирования гепатоцитов.
Также в условиях хронического эмоционально-болевого стресса наблюдалось увеличение относительной массы печени на 11% (p<0,05) (таблица), что может являться следствием застойных явлений в данном органе. Пептид нивелировал отмеченный сдвиг, снижая данный показатель после введения в дозах 40, 120, 360 и 1080 мкг/кг соответственно на 17% (p<0,001), 12% (p<0,01), 15% (p<0,001) и 20% (p<0,001). Дисперсионный анализ также показал наличие достоверных изменений в показателях относительной массы печени.
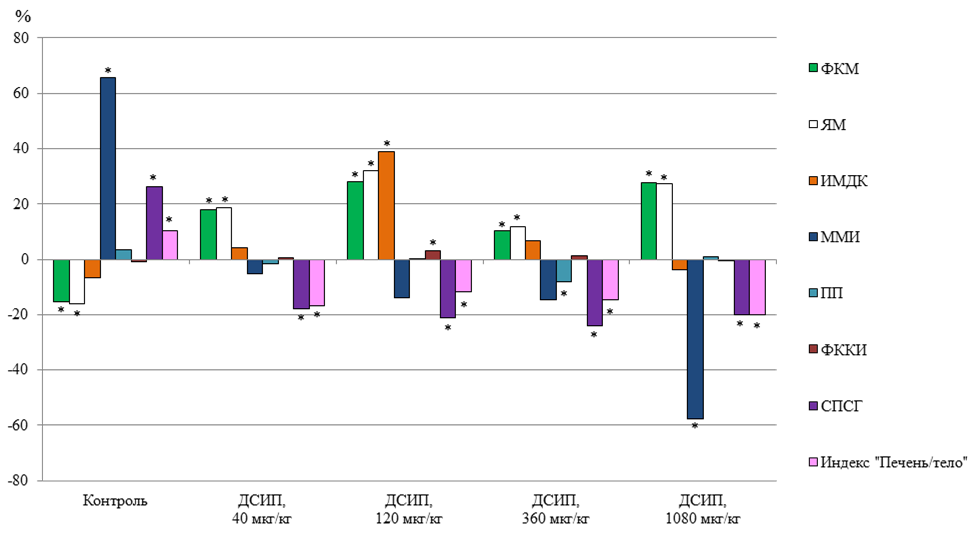
Морфометрические показатели печени у животных различных групп в условиях хронического эмоционально-болевого стресса
Примечание: на представленной диаграмме животные контрольной группы сравниваются с интактными, а подопытные группы – с контрольной; * – достоверность полученных результатов – p<0,05-0,001.
Заключение
На основании полученных данных можно заключить, что хронический эмоционально-болевой стресс по результатам морфометрического исследования печени вызывал развитие дегенеративных и деструктивных процессов, сопровождающихся полнокровием, застойными явлениями и холестазом в печеночной ткани, а также увеличение текущей (относительно кратковременной) интенсивности функционирования гепатоцитов и снижение глубины репаративных резервов. Введение ДСИП стрессированным животным в дозах 40, 120, 360 и 1080 мкг/кг вызывало уменьшение выраженности дегенеративных и деструктивных процессов, снижение полнокровия, застойных явлений и холестаза. Кроме этого, после введения ДСИП в дозах 120 и 1080 мкг/кг отмечалась тенденция к активации пролиферативных процессов и нарастанию интенсивности функционирования ткани печени. У стрессированных животных наблюдалось увеличение относительной массы печени по сравнению с интактными животными, что может быть вызвано, в том числе, развитием застойных явлений в данном органе. Данный показатель снижался после введения пептида во всех исследуемых дозах, нивелируя отмеченный стресс-индуцированный сдвиг.
Таким образом, результаты морфометрического исследования печени у стрессированных крыс на фоне введения ДСИП свидетельствуют о его стресс-лимитирующем действии, проявившемся в ослаблении или полном нивелированнии вызванных стрессом изменений изученных морфофункциональных показателей. В основе наблюдавшихся эффектов пептида может находиться как его влияние на развитие эмоциональных и болевых реакций, так и периферическое действие [1].



