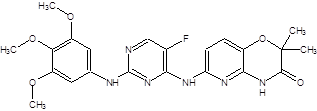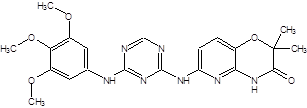Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
STUDYING OF ELECTROPHORETIC BEHAVIOUR OF NEW SYK-KINASE INHIBITORS IN THE CONDITIONS OF THE MICELLAR ELECTROKINETIC CHROMATOGRAPHY
В настоящее время при разработке лекарственных средств (ЛС) предназначенных для лечения ревматоидного артрита (РА), а также ряда онкологических заболеваний, все большее внимание уделяется соединениям, действие которых нацелено на протеинкиназы, в частности митоген-активированную фосфокиназу p38 (p38 МАРК), селезеночную тирозинкиназу (Syk) и янус-киназу (JAK). Однако, клинические испытания показали достоверную эффективность в лечении РА и некоторых онкологических заболеваний только ингибиторов Syk- и JAK-киназ. В частности, можно отметить такие ЛС как фостаматиниб (ингибитор SYK-киназы) и тофацитиниб (ингибитор JAK-киназы), клинические испытания которых уже показали высокую эффективность в сочетании с удовлетворительной безопасностью [2].
Поэтому, разработка новых ЛС направленных на ингибирование данных видов протеинкиназ является актуальной задачей современной медицины и фармации. Следует также сказать, что разработка новых ЛС требует наличие надежных методов оценки их качества. На сегодняшний день одним из перспективных методов анализа является капиллярный электрофорез, обладающий высокой эффективностью, экспрессностью и экономичностью исследований. Метод уже входит в ведущие мировые фармакопеи, а также активно развивается в отечественной фармацевтической отрасли.
Цель работы: с использованием капиллярного электрофореза разработать методику анализа новых ингибиторов Syk-киназы (шифр MT-Syk-00 и MT-Syk-03).
Материалы и методы исследования
В работе использовали фармацевтические субстанции (в виде свободного основания) веществ (табл. 1), представляющие собой производные диаминодиазина и диаминотриазина и являющиеся ингибиторами Syk-киназы (лабораторные шифры MT-Syk-00 и MT-Syk-03), для лечения РА и ряда онкологических заболеваний.
Таблица 1
Формулы ингибиторов SYK-киназы MT-SYK-00 и MT-SYK-03
|
Шифр соединения |
Структурная формула |
|
MT-SYK-00 |
|
|
MT-SYK-03 |
|
Данные фармацевтические субстанции были предоставлены опытным производством компании ООО «Молекулярные Технологии». В работе использовались субстанции, с содержанием действующих веществ не менее 99,8%
Для определения веществ был использован метод капиллярного электрофореза. Измерения проводились на приборе Капель 105 (группа компаний «Люмэкс», г. Москва). В работе использовался термостатируемый кварцевый капилляр с рабочей длиной 65 см и диаметром 75 мкм. Температура опыта составила 20 0С и напряжение 20 кВ (блок положительной полярности).
Результаты исследования и их обсуждение
Учитывая слабоосновный характер веществ, эксперимент необходимо было проводить в условиях мицеллярной электрокинетической хроматографии (МЭКХ) [1]. При этом в качестве ведущего электролита использовали раствор натрия тетрабората декагидрата с концентрацией 2 мг/мл и добавкой додецилсульфата натрия, концентрация которого варьировалась от 10 до 20 мг/мл. Ввод пробы осуществляли гидродинамически 150 мБар•с. Детектирование осуществляли спектрофотометрически при 254 нм. Для обработки хроматограмм была использована программа «Мультихром».
В результате было показано, что оба вещества мигрируют в одно и то же время, при этом увеличение концентрации додецилсульфата натрия до 20 мг/мл не приводило к улучшению разделения. Полученная в данных условиях электрофореграмма представлена на рисунке 1.
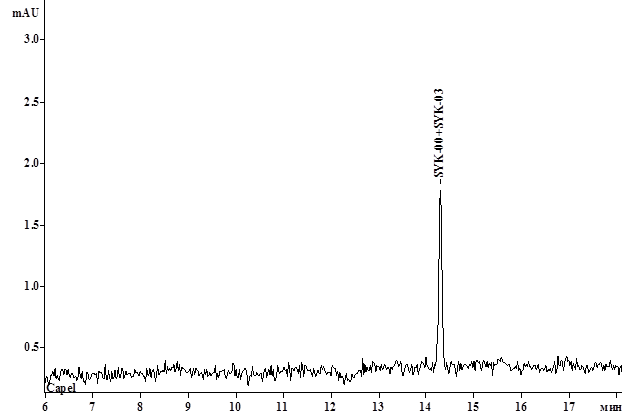
Рис. 1. Электрофореграмма модельной смеси MT-SYK-00 и MT-SYK-03 в условиях МЭКХ (концентрация додецилсульфата натрия 20 мг/мл)
Данный факт можно объяснить близкими значениями их гидрофобности, в результате чего константа их распределения между мицеллярной (псевдостационарной) фазой и фазой раствора одинакова.
В ряде случаев для повышения степени разделения компонентов в МЭКХ используют добавку метанола к ведущему электролиту. В этом случае удается повлиять на гидрофобные взаимодействия между анализируемым компонентом и мицеллой, а также на подвижность электроосмотического потока и собственную электрофоретическую подвижность аналита и соответственно повысить селективность анализа [3,5]. Поэтому, на следующем этапе работы осуществляли добавку метанола, содержание которого в ведущем электролите составило 10%. Результаты представлены на рисунке 2.
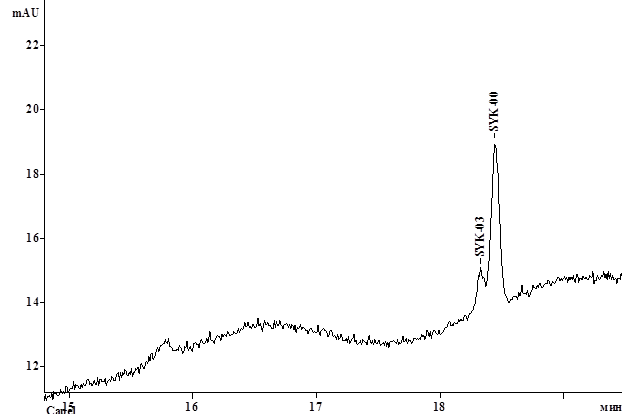
Рис. 2. Электрофореграмма модельной смеси MT-SYK-00 и MT-SYK-03 в условиях МЭКХ (концентрация додецилсульфата натрия 10 мг/мл) с добавкой метанола
Полученные данные свидетельствуют об улучшении параметров разделения изучаемых веществ, что позволяет проводить качественную их оценку. В то же время для количественного определения полученного разделения не достаточно. Также необходимо отметить, что дальнейшее повышение концентрации метанола (до 20%) в составе ведущего электролита значительно увеличивало время анализа, что также является не желательным эффектом. Кроме того, использование органического модификатора приводило к низкой воспроизводимости времен миграции обоих веществ, что не позволяет использовать данные условия анализа для контроля их качества.
Еще одним важным модификатором в МЭКХ является мочевина [4]. Связано это с тем, что за счет образования клатратов мочевины удается повлиять на коэффициент распределения, что, в свою очередь, также может приводить к улучшению селективности анализа. В связи с этим на заключительном этапе оптимизации условий разделения новых ингибиторов SYK-киназы осуществляли добавку мочевины к ведущему электролиту. При этом ее содержание в буфере составляло от 10 до 40% (от 100 до 400 мг/мл) (рис. 3).
а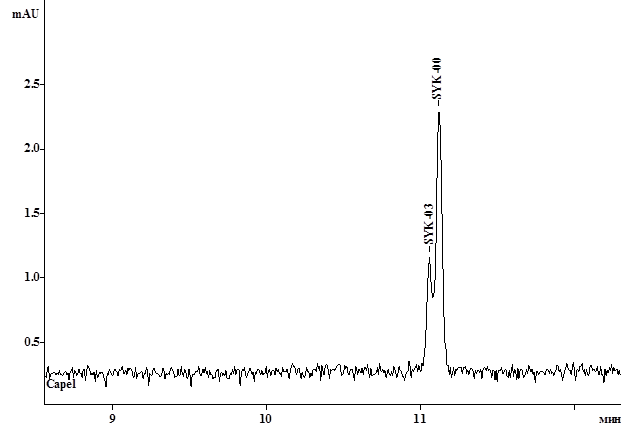
б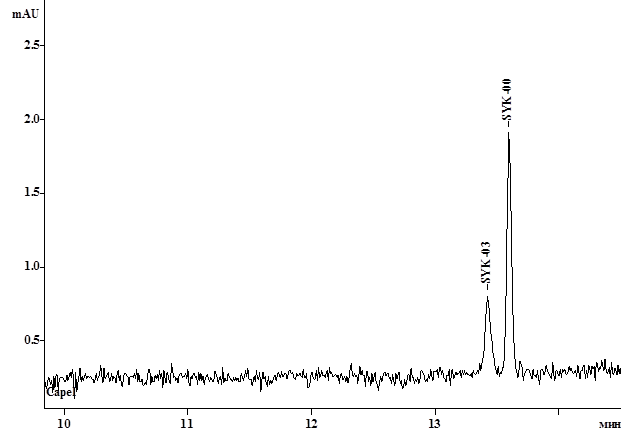
Рис.3. Электрофореграмма модельной смеси MT-SYK-00 и MT-SYK-03 в условиях МЭКХ (концентрация додецилсульфата натрия 10 мг/мл) с добавкой мочевины: a – 20%, b – 40%
В результате было показано, что только при концентрации мочевины в 40% в ведущем электролите удается достичь приемлемых параметров разделения анализируемых веществ. Полученные параметры пиков веществ приведены в таблице 2.
Таблица 2
Параметры пиков MT-SYK-00 и MT-SYK-03, полученные в условиях МЭКХ с добавкой мочевины
|
Шифр соединения |
Эффективность, ТТ |
Асимметрия |
Разрешение между пиками |
|
MT-SYK-03 |
400 000 |
1,2 |
2,38 |
|
MT-SYK-00 |
580 000 |
1,2 |
Параметры разделения, а также характеристики обоих пиков свидетельствуют о приемлемости выбранных условий анализа, что позволяет использовать их для дальнейшей разработки методик количественного определения новых ингибиторов SYK-киназы в лекарственных препаратах.
Выводы
В результате изучения электрофоретического поведения новых ингибиторов SYK-киназы (шифр MT-SYK-00 и MT-SYK-03) в условиях МЭКХ выбраны оптимальные условия их анализа. При этом разделения веществ удалось достичь при использовании в качестве ведущего электролита раствора натрия тетрабората декагидрата с концентрацией 2 мг/мл и добавками додецилсульфата натрия (10 мг/мл) и мочевины (400мг/мл).
Рецензенты:
Компанцева Е.В., д.фарм.н., профессор кафедры фармацевтической и токсикологической химии ПМФИ – филиала ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск.
Оганесян Э.Т., д.фарм.н., профессор, зав. кафедрой органической химии ПМФИ – филиала ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск.
Библиографическая ссылка
Сенченко С.П., Чилов Г.Г., Новиков Ф.Н. ИЗУЧЕНИЕ ЭЛЕКТРОФОРЕТИЧЕСКОГО ПОВЕДЕНИЯ НОВЫХ ИНГИБИТОРОВ SYK-КИНАЗЫ В УСЛОВИЯХ МИЦЕЛЛЯРНОЙ ЭЛЕКТРОКИНЕТИЧЕСКОЙ ХРОМАТОГРАФИИ // Современные проблемы науки и образования. 2014. № 4. ;URL: https://science-education.ru/en/article/view?id=14115 (дата обращения: 07.06.2026).