Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
FLUORESCENT INDICATORS OF LIVING TUMOR CELLS OF SQUAMOUS EPITHELIUM BEFORE AND AFTER RADIOTHERAPY IN PATIENTS WITH SQUAMOUS CELL CARCINOMA OF THE ORAL CAVITY
Введение. Основным методом лечения местно распространенных процессов плоскоклеточного рака слизистой оболочки полости рта (ПРСПР) является лучевая терапия, при проведении которой число рецидивов достигает 50% случаев (Г.А. Гинзбург и соавт.) [2].
Сонодинамическая терапия с помощью локального ультразвука средней интенсивности в сочетании с химиотерапией и/или соносенсибилизатором позволяет увеличить биодоступность лечебных препаратов к опухоли, усилить повреждающее действие на опухоль (Андронова Н.В. и соавт.) [1]; Kim H.J. et al. [10]. Однако еще не доказаны механизмы взаимодействия с клеточными структурами цитостатиков, введенных в ткани с помощью ультразвукового воздействия.
Изучение электрической неоднородности клеточной взвеси, обусловленной различной величиной мембранных потенциалов живых клеток, способствует пониманию взаимодействия этих клеток с разными ионами (например, цитостатиками, антибиотиками), а также оценке влияния и действия на клетки электромагнитных полей и радиации. Высокие потенциальные возможности использования потенциалозависимых флуорохромов АНС и ДСМ были доказаны в работах О.В. Тарнопольской (2012) [6-8]; Г.К. Максимова (2012) [3], Е.М. Непомнящей (2012) [4], А.И. Шихляровой (2013) [9].
Цель. Изучить изменения, происходящие в опухолевых клетках больных (ПРСПР) при химиолучевом лечении с использованием локальной УЗ-химиотерапии.
Материалы и методы. Изучали опухолевые клетки биоптатов 11 больных 3-4 стадии ПРСПР, получавших расщепленным курсом ДГТ в режиме ускоренного фракционирования (1,2+1,2 Гр с интервалом 5 часов) и локальную химиотерапию цисплатином, проводимую в интервале между отдельными фракциями разовой дозы с использованием УЗ-воздействия (патент № 2488412 от 03.02.2012) [5]. Исследовали биопсийный материал до лечения и после очаговой дозы 40 Гр и суммарной дозы цитостатика 45 мг.
Из биоптата ПРСПР, не более 30 мин после удаления, размером 3×4 мм, получали клеточную взвесь путем измельчения скальпелем на стекле в 100 мкл забуференного физраствора. Концентрация клеток в ней составляла 5±3×104 клеток. Каждую клеточную взвесь от одного больного делили на три части. Одну часть витально окрашивали флуорохромом АНС, вторую - ДР, третью - ДСМ. Флуоресцентный зонд-катион ДСМ использовали в конечной концентрации 20 мкМ, АНС – 40 мкМ, ДР – 50 мкМ. Препараты живых клеток после 10-20 минутной инкубации с флуорохромами при температуре 22-25 °С под покровным стеклом исследовали под микроскопом Axio Imager M2, Zeiss. Захват изображения (модуль MosaiX) производили цветной цифровой камерой AxioCam HRc, а интерактивные измерения проводили с помощью программного обеспечения AxioVision, rel.4.8., измеряя в среднем до 100 клеток опухоли в каждой пробе и все попавшие при этом в поле зрения лейкоциты, в основном сегментоядерные нейтрофилы и лимфоциты. Флуорохром ДСМ был синтезирован в НИИ физической и органической химии при ЮФУ. АНС был поставлен фирмой Serva. Длина волны возбуждения и ДСМ, и ДР составляла 480 нм, а волны эмиссии - 520 нм. Для АНС эти параметры – 375 и 480 нм. При микросъемке строго соблюдали одинаковое разрешение и экспозицию для каждого флуорохрома в сравниваемых пробах для обеих групп (до и после лечения). Данные измерений клеток сохраняли в приложении AxioVision, rel.4.8 в файле, совместимом с Excel (Microsoft Office-2003), которые затем сводили в общие электронные таблицы и статистически обрабатывали с помощью Statistika 6.0. Клетки опухоли измеряли одним инструментом – «Outline», а лейкоциты – другим: «Circle Out-In», массив показателей сортировали по инструменту измерения, и тем самым отделяли показатели клеток опухоли от лейкоцитов. Яркость клеток суммировали по трем каналам (RGB). Для оценки различий (р-уровень) применяли как параметрические показатели (среднее и стандартное отклонение, t-test Стьюдента), так и непараметрические – критерий Вилкоксона.
Результаты. Флуорохром-анион АНС окрашивает живые клетки голубым свечением, концентрируется на мембране, не проникает в ядро, поскольку мембрана ядра заряжена отрицательно и в силу этого не пропускает анион АНС. Если в данной окраске ядро прокрашено и светит ярче цитоплазмы, то эта клетка мертвая [9]. На рис. 1 (А, Б, В, Г, Д) показаны поля зрения клеточной взвеси ПРСПР, окрашенные АНС. На рис. 2 и 3 живые клетки в окраске ДСМ и ДР, соответственно. Флуорохромы-катионы легко проникают в ядра клеток, делая ядро зачастую ярче цитоплазмы.
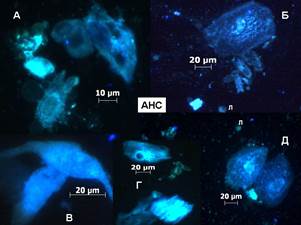
Рис. 1 (А, Б, В, Г, Д). Поля зрения препарата клеточной взвеси плоскоклеточного рака полости рта человека, окраска АНС. Имеет место клеточный и ядерный полиморфизм. Видим неоднородность по яркости флуоресценции АНС, связанного с клетками. Л – лейкоциты (клетки биоптата больных до лечения).
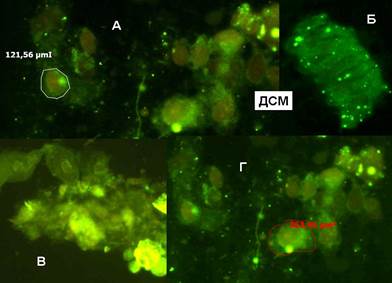
Рис. 2 (А, Б, В, Г). Поля зрения препарата клеточной взвеси ПРСПР, флуорохром ДСМ. После лечения. В данном случае ядра плохо прокрашены по сравнению с оранжевыми ядрами клеток аденокарциномы предстательной железы [6].
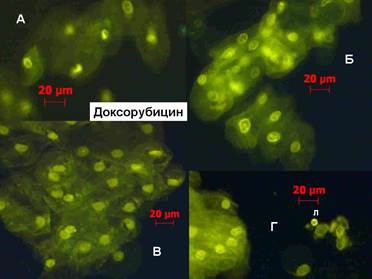
Рис. 3 (А, Б, В, Г). Поля зрения препарата клеточной взвеси ПРСПР, флуорохром доксорубицин. Больные после лечения. Л – лейкоциты. Ядра клеток интенсивно набрали доксорубицин.
В таблице 1 представлены полученные цитометрические результаты для группы 1 – «До лечения», а в таблице 2 - для группы 2 «После лечения», окраска ДСМ. Измеряли размеры клеток и яркость флуоресценции. Такие же таблицы были созданы для флуорохромов АНС и ДР. В таблицу 3 сведены данные по средним для групп значениям цитометрических показателей для трех флуорохромов; представлен уровень статистической значимости различий между группами «р», рассчитанный по критерию Стьюдента (параметрический) и по критерию Вилкоксона (непараметрический).
Таблица 1. Цитометрические показатели клеток опухоли ПРСПР больных ДО лечения. Флуорохром ДСМ.
|
Группа 1, больные до лечения (n=11) |
||||||
|
Номер больного |
Клетки опухоли |
Лейкоциты в опухоли |
||||
|
N |
S± ст. откл. (мкр кв.) |
Br ± ст. откл. (отн. ед.) |
Nlе |
Dle± ст. откл. |
Brle ± ст. откл. |
|
|
1 |
116 |
199±119 |
39±7 |
58 |
8,6±1,8 |
73±36 |
|
2 |
82 |
134±62 |
42±7 |
77 |
8,6±1,1 |
45±7 |
|
3 |
118 |
232±126 |
86±36 |
61 |
9,2±2,9 |
82±35 |
|
4 |
60 |
156±73 |
21±6 |
29 |
8,5±1,4 |
24±9 |
|
5 |
70 |
363±216 |
52±2 |
88 |
8,1±1,2 |
18±2 |
|
6 |
96 |
412±242 |
45±11 |
65 |
9,8±1,3 |
57±30 |
|
7 |
97 |
212±90 |
25±12 |
66 |
8,8±1,4 |
27±10 |
|
8 |
98 |
302±104 |
42±10 |
67 |
8,6±1,5 |
50±22 |
|
9 |
99 |
286±145 |
12±4 |
68 |
9,0±1,6 |
22±13 |
|
10 |
75 |
187±140 |
32±15 |
42 |
9,1±1,5 |
28±14 |
|
11 |
85 |
296±147 |
44±16 |
24 |
8,0±1,8 |
42±15 |
|
СРЕДНЕЕ → |
253±87 |
40±19 |
|
8,8±0,5 |
42±22 |
|
Таблица 2. Цитометрические показатели клеток опухоли ПРСПР больных ПОСЛЕ лечения. Флуорохром ДСМ.
|
Номер больного |
Клетки опухоли |
Лейкоциты в опухоли |
||||
|
N |
S (мкр кв.) |
Br (отн. ед.) |
Nlе |
Dle± ст. откл. |
Brle (отн. ед.) |
|
|
1 |
131 |
214±91 |
40±16 |
33 |
8,7±1,7 |
23±5 |
|
2 |
50 |
156±73 |
21±6 |
29 |
8,5±1,4 |
24±9 |
|
3 |
60 |
363±216 |
12±2 |
40 |
8,1±1,2 |
14±2 |
|
4 |
96 |
402±142 |
25±11 |
15 |
9,8±1,3 |
35±10 |
|
5 |
48 |
452±400 |
20±12 |
45 |
9,3±1,3 |
15±4 |
|
6 |
94 |
144±69 |
27±4 |
26 |
7,2±0,9 |
37±7 |
|
7 |
95 |
194±70 |
15±5 |
27 |
7,2±1,0 |
20±9 |
|
8 |
96 |
294±71 |
35±9 |
19 |
9,2±1,1 |
29±10 |
|
9 |
97 |
280±72 |
24±12 |
27 |
8,2±1,2 |
23±6 |
|
СРЕДНЕЕ → |
277±110 |
24±9 |
|
8,5±0,9 |
24±8 |
|
Таблица 3. Сравнение средних цитометрических показателей клеток опухоли плоскоклеточного рака слизистой полости рта (ПРСПР) и лейкоцитов, населяющих эту опухоль. Уровни статистического различия между ними.
|
Флуорохром |
Цитометрический показатель |
Больные ДО ЛЕЧЕНИЯ |
Больные ПОСЛЕ ЛЕЧЕНИЯ |
р-уровень (Т-Тест Стьюдента) |
р-уровень (Wilcoxon-test), |
|
|
ДСМ |
(S), мкр кв. |
253±87 |
277±110 |
р=0,577 |
р=0,441 |
|
|
Яркость (Br), отн. ед. |
40±19 |
24±9 |
р=0,038 |
р=0,086 |
||
|
(D le), мкр |
8,8±0,5 |
8,5±0,9 |
р=0,380 |
р=0,554 |
||
|
Яркость (Brle), отн. ед. |
42±22 |
24±8 |
р=0,030 |
р=0,038 |
||
|
АНС |
(S), мкр кв. |
227±61 |
210±44 |
р=0,499 |
р=0,953 |
|
|
Яркость (Br), отн. ед. |
71±28 |
61±10 |
р=0,349 |
р=0,678 |
||
|
(D le), мкр |
8,6±1,1 |
7,7±0,5 |
р=0,037 |
р=0,0,21 |
||
|
Яркость (Brle), отн. ед. |
37±10 |
44±10 |
р=0,164 |
р=0,173 |
||
|
ДР |
(S), мкр кв. |
248±83 |
292±106 |
р=0,308 |
р=0,374 |
|
|
Яркость (Br), отн. ед. |
31±8 |
30±10 |
р=0,855 |
р=0,859 |
||
|
(D le), мкр |
8,7±0,5 |
8,8±0,7 |
р=0,629 |
р=0,753 |
||
|
Яркость (Brle), отн. ед. |
36±13 |
30±12 |
р=0,255 |
р=0,441 |
||
Обозначения в таблицах: S - средняя площадь клеток; Dle - средний диаметр лейкоцитов; Br - средняя яркость клеток; N - число измеренных клеток; ст. откл. - стандартное отклонение; мкр кв. - микрон квадратный; отн. ед. - относительные единицы. На рис. 4 представлены графики средних значений измеренных показателей (Mean) и стандарнтой ошибки среднего (±SE) для клеток, окрашенных АНС и ДСМ.
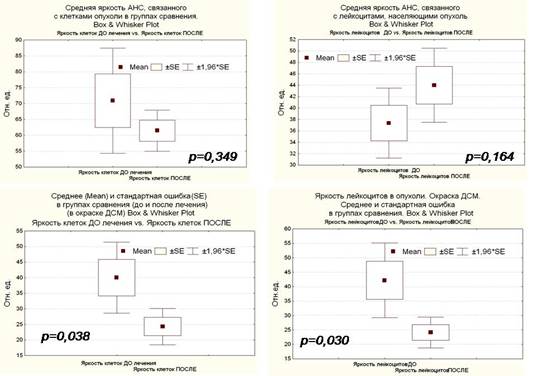
Рис. 4. Разброс флуориметрических показателей клеток ПРСПР у больных до и после лечения.
Обсуждение. Визуализация клеточной взвеси ПРСПР, окрашенной витальными флуорохромами, показывает четкую картину неоднородности по яркости клеток опухоли и лейкоцитов, так же как на других типах опухолевых клеток, о чем сообщалось в работах [3; 4]. Об этом свидетельствуют представленные здесь таблицы и рис. 4. Нами были обнаружены различия в выбранных флуориметрических показателях между группами до и после лечения. Это достоверная разница в средней яркости флуоресценции ДСМ, которая в группе больных после лечения снижена в 1,7 раза (р=0,038). Яркость флуоресценции АНС, связанного с опухолевыми клетками, также несколько снижена у больных после лечения, но не достоверно. На основании исследования, представленного в работе [8], можно объяснить происхождение такого различия. Все больные второй группы получали цисплатин при химиотерапии, а вывод в работе [8] свидетельствует о конкуренции в ядре клеток между ДСМ и цисплатином. Цисплатин занимает места связывания в ядре и не позволяет связаться там молекулам ДСМ, а без этой связи флуоресценции ДСМ не происходит. Отсюда и пониженная яркость целых клеток, и сниженная яркость ДСМ в ядрах этих клеток, например на рис. 2 (Б). Остальные показатели на данном числе испытаний не представили значимой разницы. Можем отметить следующие различия в клеточных картинах ПРСПР в группах до и после лечения: во-первых, до лечения имеет место обилие флоры, расположенной на плоских клетках, да и самой взвеси (рис. 1). После лечения флоры практически нет; во-вторых, имеет место значительное преобладание плоских клеток у больных после лечения, рис. 3.
Выводы. Полученные данные свидетельствуют о том, что снижение яркости флуоресценции ДСМ, связанного с опухолевыми клетками, может быть критерием наличия в клеточной взвеси цисплатина.
Рецензенты:
Каймакчи О.Ю., д.м.н., ассистент кафедры онкологии Ростовского государственного медицинского университета, г. Ростов-на-Дону.
Николаева Н.В., д.м.н., ассистент кафедры онкологии Ростовского государственного медицинского университета, г. Ростов-на-Дону.
Библиографическая ссылка
Розенко Л.Я., Тарнопольская О.В., Шихлярова А.И., Непомнящая Е.М., Крохмаль Ю.Н. ФЛУОРЕСЦЕНТНЫЕ ПОКАЗАТЕЛИ ЖИВЫХ КЛЕТОК ОПУХОЛИ ПЛОСКОГО ЭПИТЕЛИЯ ДО И ПОСЛЕ ХИМИОЛУЧЕВОЙ ТЕРАПИИ У БОЛЬНЫХ ПЛОСКОКЛЕТОЧНЫМ РАКОМ ПОЛОСТИ РТА // Современные проблемы науки и образования. 2013. № 6. ;URL: https://science-education.ru/en/article/view?id=11699 (дата обращения: 02.06.2026).



