Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
STUDYING OF STABILITY OF SALT ADEMETIONINE FROM THE TOLUENSULFONIC ACID
Введение
Адеметионин (S - аденозил – L - метионин) играет важную роль в биохимических процессах в организме человека. Адеметионин производится человеческим организмом и присутствует практически во всех тканях организма. Он важен для образования глутатиона, водорастворимого пептида, помогающего организму бороться со свободными радикалами. Адеметионин также помогает при жировой дистрофии печени, а также играет роль в защите организма от сердечной недостаточности. Является донором метильных групп, что важно для метаболизма. В общем адеметионин повышает уровень функционирования остальных аминокислот в организме. Дефицит адеметионина может стать причиной дисфункции важного гормона – мелатонина, который играет роль в регулировании процесса сна и кардиоритме. Применяется адеметионин при внутрипеченочном холестазе, токсическом поражении печени, в т.ч. алкогольном, лекарственном, вирусном гепатите и т.п. [1].
Однако главным недостатком адеметионина является его неустойчивость при комнатной температуре. Основным продуктом распада адеметионина является метилтиоаденозин (МТА). Процесс распада адеметионина на метилтиоаденозин связан с нуклеофильной атакой карбоксильного углерода на аминокислотный гамма-метилен, который вступает в реакцию с соседним сульфонием. На стабильность адеметионина, помимо температуры, также влияет значение pН. Кислое значение pН предотвращает быстрое разрушение адеметионина до МТА. При высоком значении pН стабильность в растворе низкая и молекула быстро разлагается согласно различным механизмам [2-4].
Добавление растворов различных кислот, солей, а также полианионов и высокомолекулярных веществ к раствору адеметионина приводит к получению стабильных солей адеметионина [5].
В данной статье нами изучена стабильность соли адеметионина с толуолсульфокислотой.
Методики исследования
Субстанцию адеметионина с серной и п-толуолсульфокислотой получали биосинтетическим способом.
Для этого 150 г дрожжей, накопленных в среде Шленка, подвергали лизису, путем добавления 20 мл этилацетата и 100 мл 0,35 Н кислоты серной, перемешивали 2 ч. По окончании лизиса остатки дрожжей отделяли от лизата с помощью центрифугирования. К полученному лизату добавляли 50 мл 5%-ного водного раствора пикролоновой кислоты. Образующийся осадок отстаивали в течение 12 ч, после чего его промывали дважды водой. Полученный таким образом осадок растворяли в 40 мл смеси, состоящей из 0,1 н серной и 0,1 н п-толуолсульфокислоты. К полученному раствору добавляли 40 мл н-бутанола. После разделения органический слой отбрасывали, а к водному добавляли обесцвечивающий уголь и фильтровали. К фильтрату добавляли 80 мл этанола при перемешивании. Образующийся осадок отстаивали и отделяли декантацией. Полученный осадок растворяли в 5 мл 15%-ного раствора п-толуолсульфокислоты в метаноле. К полученному раствору добавляли изопропанол. Сразу образуется белый гигроскопичный осадок, очень легко растворимый в воде и практически не растворимый в основных органических растворителях.
Для полученной субстанции определяли сроки хранения.
В первой серии субстанцию соли адеметионина с толуолсульфокислотой герметично закрывали во флаконах и хранили при температуре 20±2 °С. Вторую серию в герметично закрытых флаконах хранили в термостате при температуре 40 ± 1 °С. В каждой серии проводили количественное определение адеметионина с периодичностью в 90 дней.
Количественное определение адеметионина проводили спектрофотометрическим методом. Спектр поглощения адеметионина в 0,1 M растворе кислоты хлористоводородной приведен на рисунке 1.
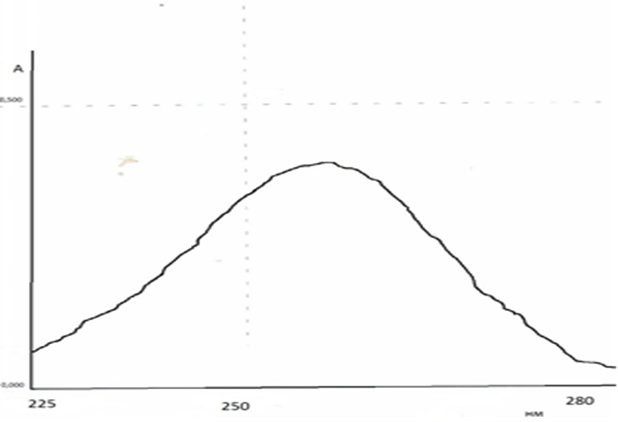
Рис. 1. Спектр поглощения раствора адеметионина в 0,1 M растворе кислоты хлористоводородной.
В спектре поглощения адеметионина имеется одна широкая полоса поглощения с максимумом при 256 нм. Толуолсульфокислота в этой области не имеет светопоглощения и не мешает определению адеметионина. Содержание адеметионина рассчитывали по рабочему стандартному образцу, в качестве которого использовали субстанцию, соответствующую ФС.
Точную навеску соли массой около 0,1 г растворяли в мерной колбе вместимостью 100 мл в 0,1 М кислоте хлористоводородной и доводили до метки той же кислотой. Аликвоту 25 мл переносили в мерную колбу вместимостью 100 мл и доводили до метки 0,1 М кислотой хлористоводородной. Оптическую плотность полученного раствора регистрировали при длине волны 256 нм. Параллельно измеряли оптическую плотность РСО с концентрацией 0,001%.
Расчет содержания адеметионина проводили по формуле:
![]()
где:
![]() ,
,![]() - значение оптической плотности исследуемого и стандартного растворов;
- значение оптической плотности исследуемого и стандартного растворов;
����т - концентрация раствора РСО, %;
а – масса навески исследуемого образца.
Результаты анализа адеметионина, полученные в период хранения, приведены в таблице 1.
Таблица 1. Изменение содержания адеметионина (%) в процессе хранения
|
t, дни T °С |
90 |
180 |
270 |
360 |
450 |
540 |
630 |
720 |
|
20 °С |
41,2 |
41,15 |
41,17 |
41,15 |
41,14 |
41,15 |
41,13 |
41,11 |
|
40 °С |
41,2 |
41,18 |
41,15 |
41,12 |
40,90 |
40,70 |
40,55 |
40,15 |
Приведенные результаты показывают, что при нормальной температуре соль адеметионина с толуолсульфокислотой сохраняет стабильность на протяжении всего срока хранения. Срок наблюдения был 2 года. При температуре 40 °С через 360 суток наблюдается тенденция к снижению содержания адеметионина.
В качестве второго метода контроля стабильности был использован метод ТСХ. Для выявления возможных продуктов деструкции адеметионин был подвержен термическому разложению. Образец субстанции метионина помещали в термостат и выдерживали в течение часа при 100 °С. Далее проводили хроматографирование всех образцов адеметионина: подвергшийся термическому разложению; образцы, заложенные на хранение; фармакопейный образец.
Из всех образцов готовили водные растворы с концентрацией около 0,1%. Хроматографировали в системе этанол : вода : уксусная кислота (65:34:1). После высушивания хроматограммы проявляли в УФ-свете. На хроматограммах проявляется четкое пятно адеметионина с ![]() =0,3. В образце, подвергнутом термическому разложению, проявляется дополнительное пятно с
=0,3. В образце, подвергнутом термическому разложению, проявляется дополнительное пятно с ![]() =0,65. В образцах, хранившихся 2 года при температуре 20 °С и при температуре 40 °С 12 месяцев, дополнительных пятен не появляется. Однако при температуре 40 °C после хранения 13-15 месяцев появляется дополнительное пятно с ����=0,62.
=0,65. В образцах, хранившихся 2 года при температуре 20 °С и при температуре 40 °С 12 месяцев, дополнительных пятен не появляется. Однако при температуре 40 °C после хранения 13-15 месяцев появляется дополнительное пятно с ����=0,62.
Эти результаты показывают, что соль адеметионина с толуолсульфокислотой стабильна не менее 2 лет.
Выводы.
1. Проведено изучение деструкции адеметионина во время хранения при 20 °С и при 40 °С и показано, что адеметионин сохраняет показатели качества в процессе хранения в первом случае в течение 24 месяцев во втором случае – в течение 12 месяцев.
2. Методом ТСХ показано, что после хранения в течение 24 месяцев при 20 °С и 12 месяцев при 40 °С могут появляться продукты деструкции адеметионина.
3. На основании исследования стабильности можно установить срок хранения соли адеметионина с толуолсульфокислотой – 2 года.
Рецензенты:
Компанцев В.А., д.фарм.н., профессор кафедры неорганической химии Пятигорского медико-фармацевтического института, филиала ГБОУ ВПО «ВолгГМУ», г. Пятигорск.
Кодониди И.П., д.фарм.н., доцент кафедры органической химии Пятигорского медико-фармацевтического института, филиала ГБОУ ВПО «ВолгГМУ», г. Пятигорск.
Библиографическая ссылка
Морозов А.В. ИЗУЧЕНИЕ СТАБИЛЬНОСТИ СОЛИ АДЕМЕТИОНИНА С ТОЛУОЛСУЛЬФОКИСЛОТОЙ // Современные проблемы науки и образования. 2013. № 6. ;URL: https://science-education.ru/en/article/view?id=10976 (дата обращения: 27.04.2026).



