Введение
Старение кожи представляет собой комплексный биологический процесс, характеризующийся прогрессирующими структурными и функциональными изменениями в эпидермисе и дерме [1, 2]. Ключевыми звеньями патогенеза являются снижение синтетической активности фибробластов, дезорганизация волокнистых структур дермы (коллагена и эластина), уменьшение содержания гиалуроновой кислоты и нарушение микроциркуляции [3, 4]. Эти изменения клинически проявляются снижением тонуса и тургора кожи, появлением морщин, сухостью и утратой четкого овала лица. В условиях растущего спроса на малоинвазивные, но эффективные методы коррекции возрастных изменений особую актуальность приобретает разработка и внедрение инъекционных тканевых наполнителей разной химической природы [5–7] с доказанным биостимулирующим действием, способных воздействовать на причину, на весь большой многофакторный процесс старения. Поиск безопасных и эффективных биоревитализантов и полирепарантов, сочетающих немедленный эффект увлажнения с пролонгированной стимуляцией эпидермально-дермальных отношений, является одной из приоритетных задач современной эстетической медицины. Одним из перспективных направлений является применение полирепарантов на основе поли-α-гидроксикислот, в частности поли-L-молочной кислоты (ПЛА) [7]. Данное соединение обладает уникальной способностью к контролируемому гидролизу в дерме, инициируя каскад реакций, приводящих к активации фибробластов и вовлечению в ответный процесс цепочки фибробласт – макрофаг – кератиноцит [8–10]. В Российской Федерации зарегистрирован тканевой наполнитель Bellarti® Estilla – пролонгированный биостимулирующий полирепарант, представляющий собой стерильный биоразлагаемый наполнитель в преднаполненном шприце в виде инъекционного геля. Его состав сочетает 1,0% поли-L-молочной кислоты для стимуляции ремоделирования дермы и создания каскада клеточного ответа в структуре дерма – эпидермис и 0,75% гиалуроновой кислоты, обеспечивающей немедленный эффект увлажнения, визуального разглаживания и создающей оптимальную среду для репаративных процессов, что сильно отличает этот наполнитель от инъекционных тканевых наполнителей на основе полимолочной кислоты, предназначенных для стимуляции и последующего синтеза нового коллагена. Несмотря на растущий клинический опыт применения полирепаранта, его механизмы действия на тканевом и клеточном уровне требуют детального и многоуровневого изучения с использованием современных методов доказательной медицины.
Цель исследования – комплексная оценка клинической эффективности и биостимулирующей активности полирепаранта в коррекции возрастных изменений кожи лица.
В задачи работы входило не только документирование клинических результатов с использованием валидированных шкал, но и углубленное изучение его механизмов действия через призму фундаментальной триады доказательств: 1) клинической оценки, 2) гистологического анализа («золотой стандарт»), и 3) клеточно-биологического исследования in vitro, включая оценку функционального состояния фибробластов в трехмерной модели сфероидов. Такая многоуровневая методология позволила получить целостное представление о взаимосвязи между клиническим улучшением, структурной перестройкой эпидермально-дермальных отношений и активацией ключевых клеточных компонентов базисной структуры.
Материал и методы исследования
Настоящее исследование представляет собой международное, проспективное, открытое, нерандомизированное многоцентровое исследование, проведенное в клиниках Российской Федерации и Республики Беларусь. Протокол исследования, а также дизайн и документы, включая форму информированного согласия пациента, были рассмотрены и одобрены Локальным этическим комитетом Медицинского университета «Реавиз» (Протокол №5 от 27.05.2024) в соответствии с Хельсинкской декларацией, национальными нормативными актами и руководством ICH GCP. Главным исследователем выступила С.Л.Первых.
В исследование было включено 79 пациенток в возрасте от 35 до 47 лет. Критериями включения являлись: доминирующий деформационный (гравитационный) тип старения кожи лица, фототип кожи II или III по Фитцпатрику, а также наличие умеренных или выраженных признаков хроно- и фотостарения, соответствующих II–III типу по шкале Глогау. Ключевыми жалобами были снижение тонуса, тургора, увлажненности кожи и наличие статических морщин средней глубины. Критериями исключения являлись острые заболевания на момент включения, острые инфекционные заболевания в течение четырех недель до исследования, сахарный диабет в анамнезе, а также склонность к келоидным рубцам и гиперпигментации, введение инъекционных тканевых наполнителей в течение года до исследования. Всем пациенткам проводилась коррекция возрастных изменений с использованием биостимулирующего полирепаранта пролонгированного действия «Беларти® Эстилла» (Bellarti® Estilla, производитель ООО «Гротекс», Россия), представляющего собой стерильный гель, содержащий 1,0% поли-L-молочной кислоты и 0,75% гиалуроновой кислоты. Препарат вводился интрадермально с использованием папульной техники (с исключением поверхностного введения) в стандартные зоны коррекции лица: верхнюю, среднюю и нижнюю трети, область скул, носогубных складок, область шеи и декольте, кистей рук. Общий курс терапии состоял из трех процедур с интервалом в 1 месяц (±3 дня). Объем вводимого препарата на одну процедуру составлял в среднем 2 мл, конечный объем коррекции определялся индивидуально в зависимости от выраженности возрастных изменений.
Эффективность и биостимулирующая активность оценивались по трем взаимодополняющим уровням:
1. Клинический уровень.Оценка динамики осуществлялась по шкале Глобальной эстетической импрессии (Global Aesthetic Improvement Scale, GAIS) как исследователем, так и самими пациентками через 1 и 3 месяца после завершения полного курса процедур. Дополнительно фиксировался уровень субъективной удовлетворенности пациентов по 5-балльной шкале Лайкерта (где 5 – «полностью удовлетворен», 1 – «совершенно не удовлетворен). На всех этапах проводилась стандартизированная фотофиксация в идентичных условиях (освещение, ракурс, нейтральное выражение лица).
2. Патогистологический уровень (золотой стандарт).С целью объективной оценки реструктурирования дермы у 20 пациенток, давших дополнительное информированное согласие, выполнялась панч-биопсия кожи (диаметр 3 мм) (Apexmed, Индия) в преаурикулярной области до начала лечения и через 3 месяца после последней процедуры. Полученные образцы фиксировались, окрашивались гематоксилином и эозином. Цифровые изображения срезов получали с использованием слайд-сканера Leica Aperio AT2 (Leica Biosystems). Морфометрический анализ проводили в программе ImageJ, патогистологический анализ включал оценку архитектоники эпидермо-дермального соединения (количество и высота дермальных сосочков), плотности и морфологии фибробластов, состояния микроциркуляторного русла и состояния коллагенового матрикса.
3. Клеточно-биологический уровень.Из части биоптатов, полученных до и после лечения, методом эксплантатной культуры выделялись аутологичные фибробласты дермы. Для оценки функционального состояния клеток использовался тест с образованием трехмерных сфероидов. Жизнеспособность, пролиферативная и секреторная активность фибробластов оценивались путем сравнения размеров, плотности и морфологии сфероидов, сформированных в контролируемых условиях in vitro. Сфероиды инкубировали с жизнеспособными красителямиHoechst 33342 (5 мкг/мл) для ядер и CellTracker™ Green CMFDA (1 мкМ)в соответствии с инструкцией производителя (Thermo Fisher Scientific) и сразу визуализировали с помощью инвертированного флуоресцентного микроскопа Leica TCS SP8 с климатической камерой для поддержания условий культивирования. Анализ проводился с помощью световой и конфокальной микроскопии.
Для статистической обработки данных использовали пакет программ IBM SPSS Statistics 23.0. Характеристики представлены в виде медианы (Me) и интерквартильного размаха [Q1; Q3] для количественных показателей и абсолютных (n) и относительных (%) частот – для качественных. Сравнение независимых групп по количественным признакам проводили с использованием U-критерия Манна – Уитни, а для парных измерений – критерия Вилкоксона. Для сравнения качественных показателей применяли критерий χ² (хи-квадрат) Пирсона или точный критерий Фишера, где это было необходимо. Статистически значимыми считали различия при уровне значимости p < 0,05.
Результаты исследования и их обсуждение
Спустя 3 месяца после завершения полного курса терапии полирепарантом была проведена объективная и субъективная оценка его эффективности. Анализ динамики по Глобальной шкале эстетического улучшения (GAIS) показал значительное положительное изменение: 92,4% (73 из 79) пациенток были отнесены к категориям «значительно улучшилось» и «улучшилось» по оценке исследователя. При этом субъективная удовлетворенность пациентов, оцененная с помощью анкетирования, составила 98,5% (78 из 79), что указывает на высокую корреляцию клинического эффекта с ощущениями пациентов. Стандартизированная фотодокументация, предоставленная исследователями из разных клинических центров, визуально подтвердила выраженные изменения (рис.1).
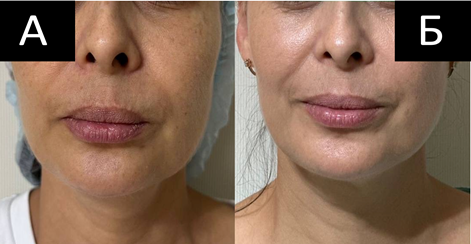
Рис.1. Результаты коррекции средней и нижней третей лица пациентки К., 42 года.
А – исходное состояние, Б – состояние через 3 месяца после курса из трех процедур пролонгированного полирепаранта на основе гиалуроновой и поли-L-молочной кислот.
Примечание: составлен авторами по результатам данного исследования
Были отмечены улучшение контуров средней и нижней третей лица, повышение плотности и увлажненности кожи кистей рук, а также улучшение текстуры и тонуса кожи тела, включая зону декольте, где позитивная динамика наблюдалась уже на 10-й день после процедуры (рис.2).
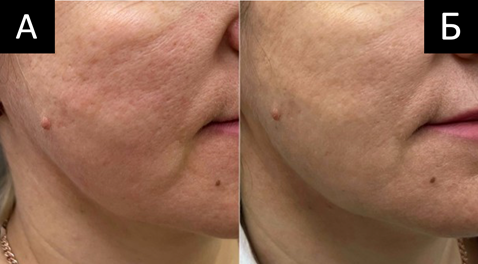
Рис.2. Результаты коррекции средней и нижней третей лица пациентки М., 46 лет.
А – исходное состояние кожи и мягких тканей лица пациентки, Б – состояние через 3 месяца после курса из трех процедур пролонгированного полирепаранта на основе гиалуроновой и поли-L-молочной кислот.
Примечание: составлен авторами по результатам данного исследования
Оценка динамики клинической эффективности проводилась с использованием глобальной шкалы эстетического улучшения (GAIS, Global Aesthetic Improvement Scale) на всех контрольных визитах. Распределение пациентов по категориям улучшения в зависимости от сроков наблюдения представлено в таблице.
Динамика клинической эффективности терапии по глобальной шкале эстетического улучшения (GAIS, Global Aesthetic Improvement Scale) (n=79)
|
Оценка по GAIS
|
Описание улучшения
|
Через 1 месяц
|
Через 3 месяца
|
Ключевая динамика
|
|
+2 |
Значительное улучшение
|
56 пациенток (70,9%) |
71 пациентка (89,9%) |
Увеличение доли на 19,0% |
|
+1 |
Улучшение (Очевидное положительное изменение)
|
23 пациентки (29,1%) |
8 пациенток (10,1%) |
Переход большинства в категорию +2 |
|
0 |
Без изменений (Изменения отсутствуют)
|
0 пациенток (0%) |
0 пациенток (0%) |
|
|
-1/-2 |
Ухудшение (Нежелательные изменения) Доля пациенток с положительным результатом
|
0 пациенток (0%) |
0 пациенток (0%) |
|
|
Итого с улучшением (+1 и +2) |
Доля пациенток с положительным результатом |
79 пациенток (100%) |
79 пациенток (100%) |
100% эффективность в обеих точках оценки |
|
Средний балл |
Сводный количественный показатель
|
+1,71 |
+1,9 |
Статистически значимый рост (р<0,05) |
Примечание: составлена авторами на основе полученных данных в ходе исследования
Субъективная удовлетворенность пациентов, оцененная по 5-балльной шкале Лайкерта, составила в среднем4,7±0,3 балла. При этом 78,5% (n=62) пациентов оценили результат на 5 баллов, 21,5% (n=17) – на 4 балла, и 1,5% (n=1) – на 3 балла. Общая доля удовлетворенных пациентов (оценки 4 и 5 баллов) достигла98,5%.
Сравнительный анализ парных панч-биоптатов кожи, взятых до начала лечения и через 3 месяца после него, выявил статистически значимые структурные изменения на тканевом уровне (рис.3).
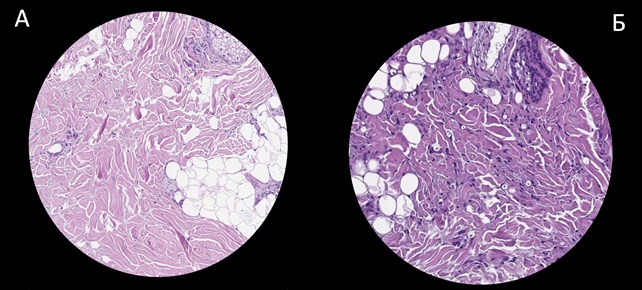
Рис.3. Гистологические изменения кожи периаурикулярной области до и после терапии биостимулирующим полирепарантом. Световая микроскопия.
Окраска гематоксилином и эозином. Увеличение ×200.
А – исходный биоптат. Б – биоптат через 3 месяца после курса. Отмечаются: 1) повышение клеточности дермы за счет активированных фибробластов; 2) усиление васкуляризации.
Примечание: составлен авторами по результатам данного исследования
На гистологических срезах было зафиксировано выраженноеулучшение архитектоники эпидермо-дермального соединения:наблюдалось увеличение количества и высоты дермальных сосочков, что свидетельствовало об увеличении площади контакта между эпидермисом и дермой и улучшении трофики.Микрососудистая сеть дермы претерпела позитивные изменения:отмечалось увеличение плотности капилляров, а также расширение их просвета, что указывает на усиление васкуляризации и улучшение микроциркуляции. Наиболее показательными сталипризнаки активации фибробластов. Количественный анализ выявил увеличение плотности этих клеток на единицу площади дермы. Качественная оценка морфологии показала отчетливый переход фибробластов из уплощенного, неактивного состояния в вытянутую, звездчатую форму с выраженной цитоплазмой, что является классическим гистологическим маркером их синтетической активности. Совокупность этих изменений объективно подтвердила процесс активного ремоделирования дермального матрикса. Однако стоит отметить выраженную лимфогистиоцитарную инфильтрацию, свидетельствующую о воспалительном ответе в зоне введения, требующую дополнительного ИГХ-исследования с определением экспрессии маркеров фибробластов.
Функциональный статус фибробластов, выделенных из биоптатов пациенток, был оценен in vitro с помощью теста образования трехмерных сфероидов. Сравнение культур, полученных до и после курса лечения, продемонстрировало существенные различия (рис.4).
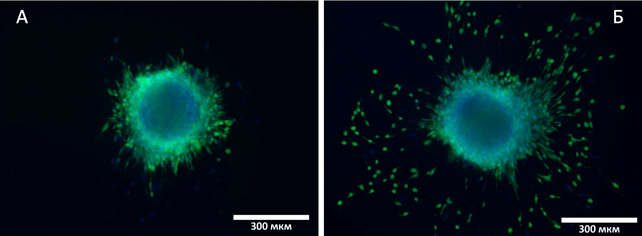
Рис.4. Анализ функциональной активности фибробластов в 3D-культуре сфероидовinvitro. А – контрольный сфероид (клетки до лечения). Б – сфероид после курса терапии (клетки через 3 месяца после лечения). Наблюдаемое увеличение диаметра и плотности сфероида (Б) указывает на усиление пролиферативного потенциала и клеточной кооперации фибробластов на фоне терапии. Масштабная линейка: 300 мкм.
Примечание: составлен авторами по результатам данного исследования
Сфероиды, сформированные фибробластами после лечения, характеризовались значительно большими размерами и более высокой плотностьюпо сравнению с контрольными образцами, что является прямым свидетельством повышения пролиферативной и метаболической активности клеток. Эти данные, полученные в контролируемых лабораторных условиях, служат непосредственным доказательствомповышения синтетической и миграционной активности фибробластовпод воздействием терапии. Результаты клеточно-биологического тестирования соответствовали гистологической картине и клиническим исходам выполненных медицинских манипуляций.
Проведенное исследование продемонстрировало высокую клиническую эффективность пролонгированного полирепаранта на основе поли-L-молочной и гиалуроновой кислот для коррекции возрастных изменений кожи. Полученные данные, интегрирующие клиническую оценку, гистологический анализ и клеточно-биологические тесты, формируют комплексную доказательную базу, раскрывающую не просто симптоматический эффект, а механизм глубокого тканевого ремоделирования за счет активации эпидермально-дермальных взаимодействий. Результаты проведенного исследования вносят вклад в понимание механизмов действия современных полирепарантов, выходящих за рамки классической парадигмы простой биодеградации и стимуляции синтеза коллагена. В настоящее время в научной литературе достаточно полно освещены механизмы дермального ремоделирования, реализуемые при монотерапии препаратами на основе полимолочной кислоты [11–13]. Не менее детально охарактеризованы и пути активации фибробластов под действием гиалуроновой кислоты [14, 15], но вместе с тем вопрос о наличии синергичного эффекта при одновременном применении указанных агентов в фиксированной комбинации, а именно 1% поли-L-молочной и 0,75% гиалуроновой кислот, остается малоизученным, что обусловило необходимость проведения настоящего исследования.
Настоящая работа, применяя трехуровневую систему оценки, фокусируется на изучении влияния данного состава на комплексное восстановление тканевого гомеостаза, в первую очередь через призмунормализации эпидермально-дермальных отношений. Как известно, гиалуроновая кислота обеспечивает не только немедленную коррекцию, но и, выступая в роли лиганда для CD44 рецепторов на кератиноцитах и фибробластах, модулирует их пролиферацию, миграцию и синтетическую активность [16]. В дополнение к ней гидролизируемый до молочной кислоты 1% полилактид инициирует каскад клеточных реакций за счет активации хемотаксиса и последующей миграции как фибробластов, так и макрофагов в зоне введения полирепаранта. Таким образом, субстрат полирепаранта работает синергично: гиалуроновая кислота оптимизирует микросреду и эпидермально-дермальную коммуникацию, а полилактид обеспечивает пролонгированный стимул для направленного ремоделирования дермального матрикса. С учетом вышеуказанного становится очевидным, что гиалуроновая кислота в составе полирепаранта играет ключевую роль не только как увлажняющий агент, но и как модулятор внеклеточного матрикса, создающий благоприятные условия для последующего действия полимолочной кислоты и смещает акцент с активации синтетической активности фибробластов накомплексное ремоделирование эпидермально-дермальной единицы. Полученные данные косвенно подтверждают гипотезу о том, что комбинация полилактида и гиалуроновой кислоты в изучаемых концентрациях может способствовать восстановлению нарушенного при старении диалога между кератиноцитами и фибробластами.
Заключение
В результате применения трехуровневой системы оценки (клинической, гистологической и клеточно-биологической) доказано, что пролонгированный полирепарант на основе полимолочной и гиалуроновой кислот является эффективным средством для коррекции возрастных изменений кожи. Его действие реализуется через запуск физиологического процесса ремоделирования дермы, основанного на восстановлении эпидермо-дермального взаимодействия, активации фибробластов и усилении микроциркуляции. Полученные результаты предоставляют врачам научно обоснованный алгоритм применения препарата и углубляют понимание механизмов ремоделирования в эстетической медицине.
Конфликт интересов
Финансирование
Библиографическая ссылка
Первых С.Л., Гамбарова Л.Д., Герман О.Ю., Баранова И.А., Кукушкина И.В., Корецкая А.В., Маслянцына Е.В., Ломанова Е.А., Беляева А.А., Гинтовт Е.А., Заровский Н.М. ЭФФЕКТИВНОСТЬ И БИОСТИМУЛИРУЮЩАЯ АКТИВНОСТЬ ПРОЛОНГИРОВАННОГО ПОЛИРЕПАРАНТА В КОРРЕКЦИИ ВОЗРАСТНЫХ ИЗМЕНЕНИЙ КОЖИ: РЕЗУЛЬТАТЫ ОТКРЫТОГО МНОГОЦЕНТРОВОГО ИССЛЕДОВАНИЯ С КЛИНИЧЕСКОЙ, ГИСТОЛОГИЧЕСКОЙ И КЛЕТОЧНО-БИОЛОГИЧЕСКОЙ ОЦЕНКОЙ (3D-СФЕРОИДЫ) // Современные проблемы науки и образования. 2026. № 5. ;URL: https://science-education.ru/ru/article/view?id=34573 (дата обращения: 29.04.2026).
DOI: https://doi.org/10.17513/spno.34573



