Введение
Почти все пациенты, перенесшие ампутацию, страдают от «фантомных ощущений» [1]. Фантомный болевой синдром (ФБС) развивается с высокой частотой в зависимости от временного периода. В течение первой недели после ампутации ФБС возникает у 84% пациентов и через полгода усиливается до 90% [2]. Кроме того, усиление ФБС наблюдается и через 12 месяцев [3]. Известно, что для лечения ФБС широко применяется фармакотерапия, методы регионарной анестезии и физиотерапии [4; 5]. В настоящее время, несмотря на увеличение пациентов, страдающих ФБС, нет четких рекомендаций по методам лечения в раннем послеоперационном периоде. Физиотерапевтическое лечение поврежденной конечности низкоинтенсивным лазерным излучением (НИЛИ) уменьшает воспаление и отек, способствует заживлению и уменьшает проявления ФБС [6; 7]. Особенно актуальным представляется сочетание различных терапевтических методов, позволяющих повысить их эффективность без появления побочных эффектов.
Цель исследования: оценить эффективность комплексного лечения ФБС НИЛИ, блокадой периферических нервов и их сочетанием.
Материалы и методы исследования
Проведено одноцентровое когортное ретроспективно‑проспективное исследование с участием 90 пациентов мужского пола, у которых диагностировано посттравматическое постампутационное развитие ФБС в одной нижней конечности.
Критерии включения: посттравматическое постампутационное развитие ФБС в одной нижней конечности.
Критерии исключения: непереносимость медикаментозной терапии, отказ от выполнения блокады периферических нервов, досрочное завершение протокола исследования (менее 180 дней).
Участники были распределены следующим образом:
- группа № 1, контрольная (n=30): базовая терапия согласно рекомендациям по предотвращению ФБС при ампутации конечности [8], комплексная медикаментозная терапия, включавшая габапентин (300 мг 3 раза в день) и амитриптилин (25 мг/сут.). Обезболивающая терапия подбиралась индивидуально с учётом интенсивности болевого синдрома. Для пациентов с невысокой интенсивностью боли использовались нестероидные противовоспалительные препараты, при сильных болевых ощущениях назначались опиоидные анальгетики. Применяемая терапевтическая стратегия сочетала нейромодулирующий эффект антиконвульсантов и антидепрессантов с индивидуализированным обезболиванием, корректируемым в зависимости от особенностей течения болевого синдрома;
- группа № 2 (n=30) - медикаментозную терапию дополняли методом НИЛИ в комбинации с блокадой нервов. Методика НИЛИ предусматривала 10 ежедневных сеансов с воздействием на болевые зоны и анатомические точки выхода седалищного и большеберцового нервов (с учётом локализации ампутации). Использовали аппарат «Лазмик» (излучающая головка ЛО3, зеркальная насадка ЗН‑50) со следующими параметрами:
· длина волны: λ=904 нм;
· импульсная мощность: 10–15 Вт;
· частота импульсов: 80–150 Гц;
· продолжительность облучения каждой зоны: 1,5–2 мин. (согласно протоколу при невропатии седалищного нерва) [9, с. 120].
Блокаду нервов выполняли по следующим принципам:
· седалищного (при ампутации бедра) - подъягодичным доступом либо ниже паховой связки (в зависимости от локализации боли);
· большеберцового (при ампутации голени/стопы) - подколенным доступом.
Под ультразвуковым контролем после визуализации нерва в его область вводили 20 мл физиологического раствора, содержащего ропивакаин 200 мг, дексаметазон 4 мг, адреналин 2,5 мкг. Блокаду нерва выполняли трехкратно с интервалом 3 дня;
- группа № 3 (n=30) лечение было аналогично группе 2 без НИЛИ. Клиническую характеристику ФБС в группах сравнения оценивали на 1-й и 14-й день госпитализации с применением следующих шкал:
· визуально‑аналоговой шкалы (ВАШ) [10];
· диагностического опросника нейропатической боли (DN‑4) [11];
· вопросника боли Pain Detect (PD) [12];
· госпитальной шкалы тревоги и депрессии (ГШТД) [13].
После прохождения курса лечения и выписки из стационара каждый участник исследования на протяжении 180 последовательных дней ежедневно самостоятельно проводил оценку выраженности болевого синдрома, фиксируя результат по шкале ВАШ.
Статистический анализ. Статистическая обработка данных осуществлялась с применением программного пакета StatTech версии 4.9.2 (разработка ООО «Статтех», Российская Федерация). Количественные переменные описывались с использованием медианы (Me) в сочетании с указанием нижнего (Q1) и верхнего (Q3) квартилей. Категориальные данные описывались с указанием абсолютных значений и процентных долей. Для оценки различий между тремя и более независимыми группами по количественному признаку применялся непараметрический критерий Краскела ‑ Уоллиса. В случае выявления статистически значимых различий выполнялись апостериорные попарные сравнения с использованием критерия Данна и коррекции Холма для контроля частоты ошибок первого рода. При статистической обработке категориальных данных использовали критерий χ2 Пирсона. Анализ проводили на основе многопольных таблиц сопряжённости, позволяющих оценить взаимосвязь между категориальными переменными. При необходимости проведения множественных сравнений применялась поправка Холма к критерию χ 2. Оценка вероятности наступления изучаемого события во времени проводилась с помощью метода Каплана ‑ Мейера. Для построения прогностической модели, позволяющей оценить вероятность определённого исхода, применялся метод логистической регрессии. Пороговое значение уровня статистической значимости было установлено на уровне p<0,05.
Результаты исследования и их обсуждение
Исследуемые группы были сопоставимы по антропометрическим характеристикам. Возраст пациентов 1, 2 и 3-й групп составил 24,50 (22,00 – 28,75), 25,00 (22,00 – 27,75) и 25,50 (22,00 – 31,00) лет соответственно (p=0,630). Анализ клинических особенностей течения послеампутационного периода не выявил статистически значимых различий между исследуемыми группами (табл. 1).
Таблица 1
Клинико-анатомическая характеристика послеампутационного периода
|
Клинико-анатомические показатели |
Группа |
p |
|||
|
1 |
2 |
3 |
|||
|
Уровень ампутации |
Нижняя треть |
8 (26,7) |
9 (30,0) |
9 (30,0) |
0,898 |
|
Средняя треть |
10 (33,3) |
9 (30,0) |
12 (40,0) |
||
|
Верхняя треть |
12 (40,0) |
12 (40,0) |
9 (30,0) |
||
|
Длительность госпитализации >21 дня |
нет |
14 (46,7) |
13 (43,3) |
15 (50,0) |
0,875 |
|
да |
16 (53,3) |
17 (56,7) |
15 (50,0) |
||
|
Инфекционные осложнения |
нет |
17 (56,7) |
14 (46,7) |
17 (56,7) |
0,669 |
|
да |
13 (43,3) |
16 (53,3) |
13 (43,3) |
||
|
Первичное наложение жгута >2 ч |
нет |
12 (40,0) |
13 (43,3) |
13 (43,3) |
0,955 |
|
да |
18 (60,0) |
17 (56,7) |
17 (56,7) |
||
|
Количество ПХО >3 раз |
нет |
14 (46,7) |
7 (23,3) |
11 (36,7) |
0,166 |
|
да |
16 (53,3) |
23 (76,7) |
19 (63,3) |
||
|
Формирование культи >14 дней |
нет |
14 (46,7) |
15 (50,0) |
16 (53,3) |
0,875 |
|
да |
16 (53,3) |
15 (50,0) |
14 (46,7) |
||
Примечание: категориальные данные описаны с указанием абсолютных значений и процентных долей - n (%). Составлено автором на основе полученных данных в ходе исследования.
Клинические проявления ФБС во всех группах исследования появились одновременно (p=0,785), спустя 2 суток от момента ампутации. При оценке состояния пациентов в 1-й и 14-й дни от момента госпитализации по опросникам DN-4, PD значимых отличий между сравниваемыми группами не получено. По ГШТД выраженность ФБС на 14-й день от момента госпитализации была ниже в группе 2 (табл. 2).
Таблица 2
Тяжесть ФБС по оценочным шкалам
|
Показатели |
Группы исследования |
Me |
Q₁ – Q₃ |
n |
р |
|
DN-4, 1-й день госпитализации, баллы |
1 |
7,00 |
6,00 – 7,00 |
30 |
0,783 |
|
2 |
6,50 |
6,00 – 7,00 |
30 |
||
|
3 |
7,00 |
6,00 – 7,00 |
30 |
||
|
DN-4, 14-й день госпитализации, баллы |
1 |
4,00 |
3,00 – 4,00 |
30 |
0,149 |
|
2 |
4,00 |
3,00 – 4,00 |
30 |
||
|
3 |
4,00 |
4,00 – 4,00 |
30 |
||
|
PD, 1-й день госпитализации, баллы |
1 |
33,00 |
31,00 – 34,75 |
30 |
0,735 |
|
2 |
32,00 |
31,00 – 34,00 |
30 |
||
|
3 |
33,00 |
31,00 – 35,00 |
30 |
||
|
PD, 14-й день госпитализации, баллы |
1 |
15,00 |
13,00 – 17,00 |
30 |
0,740 |
|
2 |
15,50 |
11,25 – 17,00 |
30 |
||
|
3 |
16,00 |
13,00 – 17,00 |
30 |
||
|
ГШТД, 1-й день госпитализации, баллы |
1 |
7,50 |
7,00 – 9,00 |
30 |
0,258 |
|
2 |
7,50 |
7,00 – 8,00 |
30 |
||
|
3 |
8,00 |
7,00 – 9,00 |
30 |
||
|
ГШТД, 14-й день госпитализации, баллы |
1 |
5,00 |
4,00 – 6,00 |
30 |
0,014* |
|
2 |
4,00 |
3,00 – 5,00 |
30 |
||
|
3 |
4,50 |
4,00 – 5,00 |
30 |
Примечание: * - критерий Краскела – Уоллиса. Составлено автором на основе полученных данных в ходе исследования.
Исходно у всех участников исследования регистрировался интенсивный болевой синдром: медиана интенсивности боли по ВАШ составляла 7–7,5 балла. На старте лечения статистически достоверных различий между группами не обнаружено (p=0,064). Однако к 7‑му дню от начала терапевтических мероприятий были выявлены значимые межгрупповые отличия (табл. 3).
Таблица 3
Значения интенсивности болевого синдрома по ВАШ от начала до 180-го дня лечения
|
День от начала лечения |
Группы исследования |
Me |
Q₁ – Q₃ |
n |
p |
|
3 |
1 |
7,00 |
6,00 – 7,75 |
30 |
0,423 |
|
2 |
6,00 |
5,00 – 7,75 |
30 |
||
|
3 |
6,50 |
6,00 – 8,00 |
30 |
||
|
7 |
1 |
6,00 |
5,25 – 7,00 |
30 |
0,041* |
|
2 |
5,00 |
4,00 – 6,00 |
30 |
||
|
3 |
6,00 |
5,00 – 7,00 |
30 |
||
|
14 |
1 |
6,00 |
5,00 – 7,00 |
30 |
< 0,001* |
|
2 |
4,00 |
3,25 – 5,00 |
30 |
||
|
3 |
5,50 |
4,25 – 6,75 |
30 |
||
|
30 |
1 |
5,00 |
5,00 – 6,00 |
30 |
< 0,001* |
|
2 |
4,00 |
3,00 – 4,75 |
30 |
||
|
3 |
4,50 |
4,00 – 6,00 |
30 |
||
|
60 |
1 |
5,00 |
4,00 – 6,00 |
30 |
< 0,001* |
|
2 |
3,00 |
2,00 – 4,00 |
30 |
||
|
3 |
4,00 |
4,00 – 5,00 |
30 |
||
|
90 |
1 |
4,00 |
4,00 – 5,00 |
30 |
< 0,001* |
|
2 |
2,00 |
2,00 – 3,75 |
30 |
||
|
3 |
4,00 |
3,00 – 4,75 |
30 |
||
|
120 |
1 |
4,00 |
3,00 – 4,75 |
30 |
< 0,001* |
|
2 |
2,00 |
1,00 – 3,00 |
30 |
||
|
3 |
3,00 |
2,25 – 4,00 |
30 |
||
|
150 |
1 |
3,00 |
2,25 – 4,00 |
30 |
< 0,001* |
|
2 |
2,00 |
1,00 – 2,00 |
30 |
||
|
3 |
3,00 |
2,00 – 4,00 |
30 |
||
|
180 |
1 |
3,00 |
2,00 – 4,00 |
30 |
< 0,001* |
|
2 |
1,00 |
1,00 – 2,00 |
30 |
||
|
3 |
2,00 |
1,00 – 4,00 |
30 |
Примечание: * - критерий Краскела – Уоллиса.
Составлено автором на основе полученных данных в ходе исследования.
С 7-го по 180-й день исследования выраженность болевого синдрома была ниже во 2-й группе и уже к 60-му дню от начала лечения характеризовалась как легкий болевой синдром. Значимые различия между группами 1 и 3 установлены только на 30-й день, в других точках исследования болевой синдром хоть и был ниже в группе 3 по сравнению с группой 1, но различия не были статистически значимыми. Со 150-го дня от начала лечения большинство пациентов характеризовали ФБС как слабый.
Для оценки времени, которое требуется для снижения выраженности болевого синдрома менее 4 баллов (слабый болевой синдром) по шкале ВАШ, был выполнен анализ методом Каплана - Мейера (рис. 1).
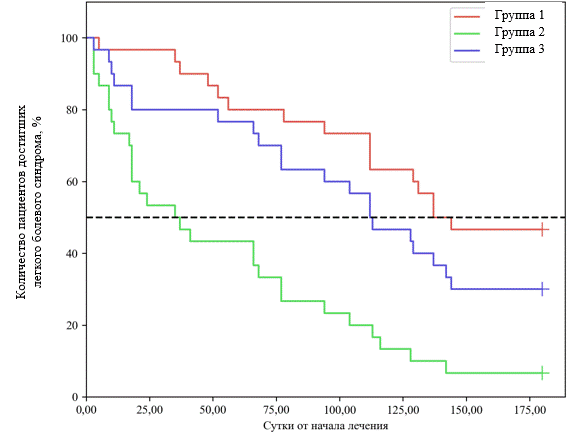
Рис. 1. Предсказательная значимость ВАШ для определения вероятности снижения болевого синдрома до легкой степени тяжести. Пунктирная линия – 50% пациентов достигли уровня ВАШ ≤ 4 балла (легкий болевой синдром).
Составлено автором на основе полученных данных в ходе исследования
Проведенный анализ показал, что медиана срока снижения выраженности болевого синдрома до легкого в группе 1 составила 137 дней, в группе 2 – 35 дней, в группе 3 – 112 дней от момента начала лечения.
Учитывая полученные различия между группами по ГШТД на 14-й день от начала лечения (табл. 1), был выполнен статистический анализ методом бинарной логистической регрессии для определения предсказательной значимости шкалы DN-4, PD и ГШТД в уменьшении болевого синдрома до легкой степени тяжести на 90-й день от момента госпитализации. Статистически значимой оказалась шкала DN-4. При увеличении показателя DN-4 в 1-й день госпитализации на 1 балл вероятность снижения выраженности болевого синдрома по ВАШ до легкой степени тяжести уменьшалась в 2,667 раза (обратная зависимость). При увеличении показателя DN-4 на 14-й день госпитализации на 1 балл вероятность снижения выраженности болевого синдрома по ВАШ до легкой степени тяжести уменьшалась в 2,381 раза (обратная зависимость) (рис. 1). Таким образом, чем меньше баллов по шкале DN-4 набрал пациент, тем выше вероятность снижения выраженности болевого синдрома до легкой степени тяжести к 90-му дню от начала лечения.
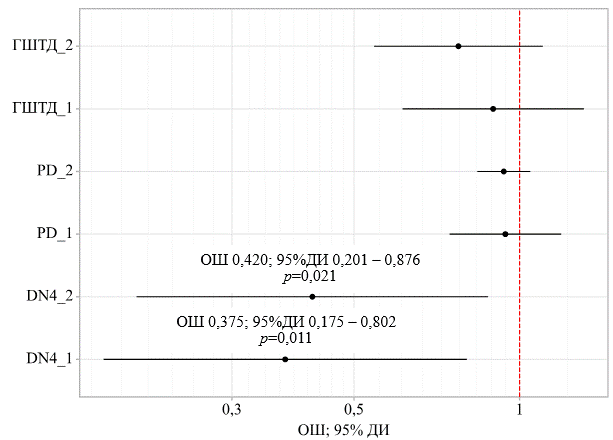
Рис. 2. Бинарная логистическая регрессия предсказательной способности шкал оценки ФБС к 90-му дню от начала лечения. Составлено автором на основе полученных данных в ходе исследования
Несмотря на то, что в клинических рекомендациях по лечению ФБС особое внимание уделяется его профилактике, до наступления этапа ампутации конечности [8] результаты проведенного исследования показали, что на момент госпитализации выраженность ФБС по ВАШ составляла ≥ 7 баллов, что соответствует сильному болевому синдрому. Кроме того, в связи с прогнозируемой эпидемией хронической боли в развитых странах крайне важно разработать экономически эффективные и безопасные методы лечения болезненных состояний, которые позволят пациентам вести активную жизнь [7]. Включение физиотерапии, а именно НИЛИ, в протоколы лечения ФБС на ранней стадии может снизить интенсивность и продолжительность симптомов.
Результаты исследования показали, что в группах с сочетанием методики медикаментозного лечения с НИЛИ с блокадой периферических нервов выраженность боли была меньше. В ходе анализа времени, необходимого для достижения уровня лёгкого болевого синдрома (оценка по ВАШ ≤ 3 балла), были определены медианные сроки наступления данного события в каждой группе. Установлено, что в группе 2 желаемый уровень боли достигался в среднем через 35 дней после начала терапии, в группе 3 - через 112 дней, а в группе 1 - лишь через 137 дней (рис. 1). Таким образом, эффективность лечения была выше во 2-й и 3-й группах.
Пациентам 3-й группы, кроме базовой медикаментозной терапии, выполняли проводниковую анестезию с УЗИ-навигацией, что, по мнению ряда исследователей, повышает эффективность проводимой терапии [14]. Значимое снижение выраженности ФБС было достигнуто к 60-му дню от начала лечения, в других точках исследования выраженность болевого синдрома была также ниже, но без статистической значимости.
Во 2-й группе начиная с 7-го дня от старта лечения установлены существенные различия в первую очередь с пациентами из 1-й группы, а на 14-й день и с пациентами из 3-й группы (табл. 3). Кроме того, эффективность физиотерапевтического лечения косвенно подтверждается результатами оценки состояния пациентов по ГШТД. В группе 2 на 14-й день от начала лечения показатели ГШТД были значимо ниже по сравнению с группой 1 (табл. 2). Несмотря на существенную разницу в количестве набранных баллов между группами, нельзя сделать однозначный вывод о снижении проявлений тревоги и депрессии у пациентов 2-й группы, так как количество набранных баллов в обеих группах (< 7 баллов) не свидетельствует о клинически выраженной депрессии или тревоге.
Учитывая полученные различия между группами исследования по ГШТД был выполнен статистический анализ всего массива данных, полученных в исследовании методом бинарной логистической регрессии для определения предсказательной способности шкал DN-4, PD и ГШТД уменьшения болевого синдрома до легкой степени тяжести на 90-й день от момента госпитализации (рис. 2). Статистически значимой оказалась шкала DN-4. Увеличение показателя DN-4 на 1 балл снижало вероятность «легкой боли» в 2,5 раза. Согласно данным ряда исследований, в последние годы достигнут значительный прогресс в разработке методов визуализации боли. Это открывает перспективы для существенного снижения частоты осложнений, ассоциированных с данным патологическим процессом. Вместе с тем проблема болевого синдрома сохраняет высокую актуальность, что обусловливает необходимость углублённого изучения диагностических подходов и совершенствования методик оценки его интенсивности [15].
Настоящее исследование имеет определённые ограничения, связанные с особенностями сформированной выборки. В исследование были включены исключительно мужчины молодого возраста, не имеющие сопутствующих заболеваний, способных оказать значимое влияние на результаты. Анализируя эффективность применения НИЛИ, важно принимать во внимание комплекс факторов: помимо непосредственного физиологического воздействия на нервные структуры в области повреждённой конечности, следует оценить и иные потенциальные механизмы влияния метода. Существует вероятность наличия психотерапевтического эффекта, который может влиять на результаты исследования. Психологический фактор может играть значительную роль в процессе лечения. У пациента наблюдается снижение эмоционального напряжения, возникающее вследствие доверительных отношений с лечащим врачом и его профессиональных рекомендаций во время сеансов НИЛИ, что может оказывать положительное влияние на интенсивность проявления ФБС и способствовать уменьшению его выраженности.
Выводы
1. Включение НИЛИ в протокол лечения ФБС способствует снижению выраженности болевого синдрома по шкале ВАШ на 7-й день от начала лечения.
2. Преимущества сочетания НИЛИ с другими методами лечения ФБС определяются вплоть до 180-го дня от начала лечения.
3. Снижение выраженности болевого синдрома до показателей легкой степени тяжести в комплексном лечении ФБС при сочетании с методикой НИЛИ наступает на 60-й день.
4. Наиболее существенной предсказательной значимостью в отношении выраженности ФБС на поздних сроках лечения обладает шкала DN-4.
Конфликт интересов
Финансирование
Библиографическая ссылка
Ткаченко Е.В. РОЛЬ НИЗКОИНТЕНСИВНОГО ЛАЗЕРНОГО ИЗЛУЧЕНИЯ В ЛЕЧЕНИИ ФАНТОМНОГО БОЛЕВОГО СИНДРОМА: ОДНОЦЕНТРОВОЕ КОГОРТНОЕ ИССЛЕДОВАНИЕ // Современные проблемы науки и образования. 2026. № 4. ;URL: https://science-education.ru/ru/article/view?id=34562 (дата обращения: 13.05.2026).
DOI: https://doi.org/10.17513/spno.34562



