Введение
Широкое применение инъекционных тканевых наполнителей (ИТН) в современной эстетической медицине демонстрирует увеличение количества процедур с их использованием как в мире, так и на территории Российской Федерации [1]. Параллельно с расширением практики использования ИТН отмечается прогрессирующий рост количества осложнений, среди которых особое место занимают гранулематозные реакции [2; 3]. Несмотря на декларируемую безопасность ИТН, практически все химические группы наполнителей способны индуцировать гранулемообразование [4-6].
Особую актуальность приобретает проблема отсроченных осложнений при применении ИТН на основе полимолочной кислоты (ПМК) в связи с относительно недавним внедрением этой группы препаратов в клиническую практику и, по-видимому, более высокой долей гранулематозных осложнений, развивающихся после применения ИТН данной группы. Существенная вариабельность данных о частоте развития гранулем (от 1,2% до 52%), отсутствие унифицированных диагностических критериев и патогенетически обоснованных методов лечения создают значительные трудности в ведении данной категории пациентов [7-9].
Современные подходы к терапии гранулем подразумевают широкое применение инъекционных форм кортикостероидов [10; 11], которые позволяют достаточно быстро купировать воспалительный процесс, однако их использование не всегда приводит к полному регрессу патологического процесса. В случаях, когда кортикостероидная терапия оказывается недостаточно эффективной или противопоказана, в качестве альтернативы назначаются инъекции цитостатиков [12; 13], механизм действия которых направлен на подавление пролиферативной активности фибробластов и лимфогистиоцитарной реакции. При отсутствии ответа на консервативную терапию, а также при формировании крупных, эстетически выраженных и фиброзно измененных гранулем, методом выбора нередко становится хирургическое иссечение [14], которое, однако, сопряжено с риском, сопровождающим любое оперативное вмешательство, и не является гарантов отсутствия рецидивов.
Несмотря на существование нескольких терапевтических стратегий, каждая из перечисленных методик характеризуется нестабильной и трудно прогнозируемой эффективностью и высокой частотой рецидивов после проведенного лечения и, по данным литературы, может достигать 30%. Дополнительным серьезным ограничением является высокий риск развития системных и локальных побочных эффектов [15], которые могут возникать как на фоне фармакотерапии, так и в результате хирургического вмешательства, что требует разработки более безопасных альтернатив.
Отсутствие стандартизированных протоколов коррекции и предиктивных маркеров развития осложнений диктует необходимость поиска новых патогенетически ориентированных методов лечения. В связи с этим перспективным направлением представляется использование аутологичной богатой тромбоцитами плазмы, обладающей комплексным регенераторным, противовоспалительным и иммуномодулирующим потенциалом. Проведенное авторами экспериментально-клиническое исследование направлено на оценку эффективности аутологичной плазмы в коррекции гранулематозных осложнений после введения ИТН на основе ПМК и разработку алгоритма диагностики и лечения данной патологии.
Цель исследования
Оценка эффективности аутологичной богатой тромбоцитами плазмы в терапии гранулем, индуцированных введением инъекционных тканевых наполнителей на основе полимолочной кислоты, в эксперименте и клинической практике.
Материалы и методы исследования
Авторами проведено комбинированное экспериментально-клиническое исследование, включающее эксперимент на лабораторных животных (одобрен комиссией по биоэтике МГУ, протокол № 157-д-з от 21.12.2023) и проспективный анализ клинических случаев. Исследование было одобрено локальным этическим комитетом ФГАОУ ВО «РНИМУ им. Н.И. Пирогова» (протокол заседания № 224 от 19 декабря 2022 года).
В экспериментальной части исследования для создания модели гранулемы у лабораторных животных были использованы половозрелые самцы мышей (30 особей) линии BALB/c, согласно принципам 3R (Replacement, Reduction, Refinement) ARRIVE guidelines 2.0., в возрасте 8-10 недель с массой тела 19-21 г, полученные из питомника Федерального государственного бюджетного научного учреждения «Федеральный исследовательский центр Институт цитологии и генетики Сибирского отделения Российской академии наук» (ИЦиГ СО РАН) (статус SPF). Животных содержали в стандартных условиях вивария (температура 22±2 °C, влажность 50–60%, 12/12-часовой световой цикл) со свободным (неограниченным) доступом к воде и стандартному корму.
Гранулематозная реакция индуцировалась однократным введением ИТН на основе ПМК путем введения в подкожную клетчатку дорзальной области у животных. В дизайне эксперимента животные были разделены на 3 группы (n=10 в каждой): группа контроля, группа плазмотерапии, группа терапии кортикостероидами (раствор бетаметазона). В протоколе лечения использовалось введение аутологичной плазмы (после забора крови животного из подчелюстной вены в микроцентрифужную пробирку, центрифугирования и отбора отсепарировавшейся плазмы) и кортикостероидов 1 раз в 7 дней трехкратно в область развившейся гранулемы. После гуманного выведения животных из эксперимента проводили гистологическое и иммуногистохимическое исследование биоптатов с оценкой плотности воспалительного инфильтрата, количества гигантских клеток и выраженности фиброза.
В клиническую часть проспективного исследования было включено 25 пациенток с верифицированными гранулемами после введения ИТН на основе ПМК персистенции более 6 месяцев (от 6 до 18, в среднем – 12 мес.), что также являлось основным критерием включения. Права пациенток были соблюдены в полном соответствии с Хельсинкской декларацией: информированное добровольное согласие на использование материала в научных целых, участие в исследовании и использование медицинских данных, включая публикацию в обезличенной форме, было получено от каждой участницы до начала исследования. Отказ от участия не влиял на качество стандартной терапии.
Критериями исключения являлись наличие в анамнезе системных, аутоиммунных, воспалительных, онкологических заболеваний; проведение в области образования гранулем процедур лазерной терапии, криодеструкции или инъекций кортикостероидов/цитостатиков (5-фторурацила) в течение 6 месяцев, предшествующих включению в исследование. Клиническое обследование пациенток с фотофиксацией (Canon EOS 250D Kit 18-55mm IS STM, Япония) состояния области гранулемообразования в сочетании с ультразвуковым исследованием мягких тканей на сканерах (Canon Aplio i800, Япония и Siemens Acuson Sequoia, Германия) линейными датчиками с центральной частотой 17-18 МГц являлись основой клинической диагностики и контроля регресса патологического процесса. Первичная биопсия (панч-биоптат Apexmed Slim, Индия) диаметром 3 мм гранулем с последующей гистологической верификацией является обязательной в рамках установки диагноза «гранулемы мягких тканей», повторный забор материала был обусловлен необходимостью понимания механизма регресса на фоне терапии, что невозможно сделать неинвазивными методами клинического подхода. Биопсия выполнялась опытным специалистом с использованием анестезии, риск осложнений был минимален. Морфологический материал обрабатывали стандартным методом: образцы фиксировали в 10%-ном нейтральном формалине, обезвоживали в спиртах возрастающей концентрации и заливали в парафин. Гистологические срезы кожи толщиной5 мкмокрашивали рутинными красителями - гематоксилином и эозином - для последующего сканирования (Hamamatsu NanoZoomer S360, Япония) и анализа в системе (Digital Pathology, Российская Федерация). Протокол лечения включал применение аутологичной богатой тромбоцитами плазмы по запатентованной авторами методике (патент № 2814006). Инъекции выполнялись в очаги гранулем с интервалом 7 дней, всего 3 процедуры. Для статистической обработки использовали пакет SPSS23.0. Применяли критерии Манна - Уитни, Вилкоксона и хи-квадрат. Различия считались статистически значимыми при p<0,05.
Результаты исследования и их обсуждение
В экспериментальной части исследования после выведения животных на 60-е сутки из эксперимента был произведен патоморфологический анализ гранулем и окружающих тканей, продемонстрировавший статистически значимые различия между группами. В группе контроля (без терапии) выявлялись классические гранулемы инородных тел с плотным лимфогистиоцитарным инфильтратом (плотность 4850±320 клеток/мм²), многочисленными гигантскими клетками инородных тел (9±3 в поле зрения при увеличении ×400) и выраженным периферическим фиброзом (площадь фиброза 38,5±4,2%).
В группе кортикостероидной терапии отмечалось умеренное уменьшение воспалительной инфильтрации (плотность клеток 3520±285 клеток/мм²; p<0,05 против контроля) при сохранении значительного фиброзного компонента (площадь фиброза 31,8±3,5%; p>0,05 против контроля). Количество гигантских клеток составляло 6±2 в поле зрения (p<0,05 против контроля). Наиболее выраженные положительные изменения наблюдались в группе плазмотерапии, где отмечалось достоверное уменьшение плотности клеточного инфильтрата до 2150±180 клеток/мм² (p<0,001 в сравнении с контролем и p<0,01 - с кортикостероидами), снижение количества гигантских клеток до 5±2 в поле зрения (p<0,001 в сравнении с обеими группами) и значительное уменьшение площади фиброза до 19,8±2,7% (p<0,01 в сравнении с контролем и p<0,05 - с группой с кортикостероидами). Различия между группой плазмотерапии и контроля были статистически значимы (p<0,001). Важным аспектом являлось отсутствие рецидивов гранулем в группе плазмотерапии в течение 60 дней наблюдения, в то время как в группе кортикостероидной терапии отмечался рецидив у 40% животных.
Таким образом, экспериментальная часть исследования продемонстрировала выраженную эффективность аутологичной плазмы в коррекции гранулематозных осложнений, проявляющуюся в достоверном уменьшении воспалительной инфильтрации, подавлении фиброгенеза и стойком регрессе образований.
В клинической части проспективного исследования для объективной оценки динамики регресса гранулем использовался комплексный подход, включающий в себя клиническую оценку (с фотофиксацией) (рис. 1), ультразвуковое исследование мягких тканей в области гранулемы и патоморфологический анализ.
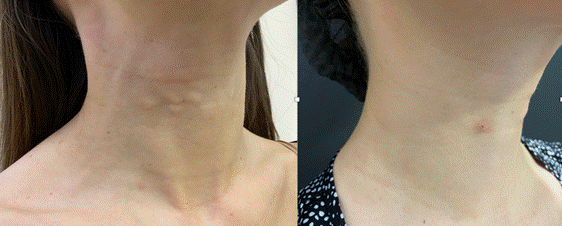
Рис. 1. Осложнение после введения инъекционного тканевого наполнителя на основе полимолочной кислоты: гранулемы области шеи. Слева: вид до лечения (через 8 месяцев после введения инъекционного тканевого наполнителя). Справа вид после (через 1 месяц после курса лечения - 3 инъекции аутологичной богатой тромбоцитами плазмотерапии). Составлено авторами по результатам данного исследования
При клиническом ранжировании объема гранулемы (0-3) использовались следующие критерии: 0 - отсутствие пальпируемого и видимого образования; 1 - легкое уплотнение, не определяющееся визуально; 2 – видимое умеренное уплотнение, определяющееся визуально; 3 – видимое выраженное, значительно деформирующее кожу уплотнение.
Согласно оценке клинической эффективности, проведение трех инъекций аутологичной богатой тромбоцитами плазмы привело к значительному улучшению клинической картины у всех пациенток: отмечено уменьшение гиперемии, объема и пальпаторной плотности образований уже после второй процедуры. Ультразвуковое исследование мягких тканей в области гранулемы объективно подтвердило уменьшение ее площади. Сравнение показателей до и после лечения с помощью критерия Вилкоксона выявило статистически значимую положительную динамику (p < 0,001).
Для объективной количественной оценки динамики состояния гранулем и перифокальных мягких тканей до и после лечения оценивали локализацию, глубину, линейные размеры (длина, ширина, глубина), эхогенность, количество и плотность цветовых картограмм потоков в режиме цветового доплеровского кодирования (ЦДК), рассчитывали объем образований (гранулем) по формуле. Оценка данных параметров производилась до курса терапии и спустя 1 месяц (сразу после завершения курса терапии). Повторная оценка проводилась по тем же параметрам, в той же проекции. Для уменьшения межоператорских ошибок все ультразвуковые исследования осуществлялись опытным специалистом, данные фиксировались в цифровом архиве. Результаты ультразвукового исследования до и после лечения наглядно продемонстрировали признаки регресса гранулем. При исходных УЗИ визуализировались гипоэхогенные или смешанной эхогенности образования неоднородной структуры, по большей мере - с нечеткими относительно ровными и неровными контурами, расположенные в дерме и/или подкожной жировой клетчатке (рис. 2).
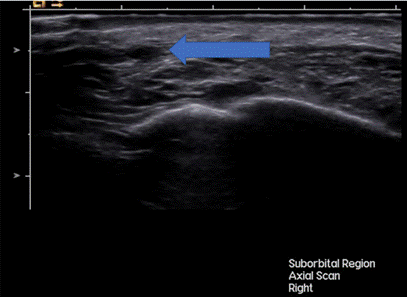
Рис. 2. Ультразвуковая картина гранулемы инфраорбитальной области до проведения курса плазмотерапии. Составлено авторами по результатам данного исследования
Синей стрелкой указано овоидное неоднородно гипоэхогенное образование с относительно ровными нечеткими контурами (аппарат Siemens Acuson Sequoia, линейный датчик 17 МГц, режим серой шкалы (B-режим)).
Средний наибольший исходный размер составил 8,4 ± 2,1 мм. В режиме ЦДК в 68% гранулем регистрировался периферический или интранодулярный тип распределения цветовых картограмм потоков различной степени интенсивности, что могло соответствовать сосудистым реакциям вследствие воспалительного процесса.
После курса плазмотерапии УЗ-картина гранулем существенно изменилась (рис. 3): наблюдалось статистически значимое (p < 0,001) уменьшение линейных размеров и объема образований.
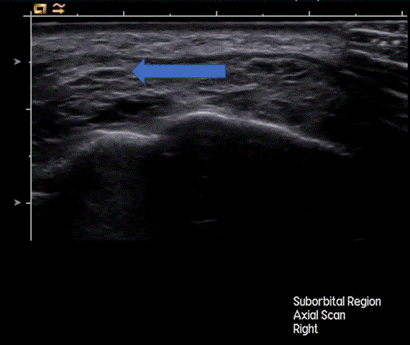
Рис. 3. Ультразвуковая картина регресса гранулемы инфраорбитальной области после проведения курса аутологичной плазмотерапии (через 1 месяц).
Составлено авторами по результатам данного исследования
Наблюдается уменьшение размеров, доли гипоэхогенного компонента. Образование стало более однородным, эхогенность его в целом повысилась, контур стал четким, ровным, гиперэхогенным - признаки замещения воспалительного инфильтрата фиброзной тканью. Средний размер гранулемы сократился до 2,5 ± 1,8 мм (уменьшение на 70,2%). В 72% случаев гранулемы полностью регрессировали, а на контрольном УЗИ определялись лишь минимальные изменения структуры и эхогенности тканей (в виде локальных неоднородно гиперэхогенных участков) без признаков наличия цветовых картограмм потоков внутри и непосредственно перифокально, которые могли трактоваться как соответствующие фиброзным изменениям. В оставшихся случаях образований отмечалось повышение эхогенности внутреннего содержимого, четкости, ровности и эхогенности контуров и полное исчезновение признаков наличия цветовых картограмм потоков при ЦДК, что могло отражать трансформацию активной гранулемы в стадию фиброза и ремоделирования.
Таблица 1
Динамика гранулем на фоне терапии аутологичной богатой тромбоцитами плазмой, по данным клинического и ультразвукового исследования (n=25)
|
Параметр для оценки |
До плазмотерапии (исходный уровень) |
После курса плазмотерапии (через 1 месяц) |
Уровень значимости, р |
|
Объем гранулемы при клинической оценке, среднее значение ± стандартное отклонение |
2,4 ± 0,5 балла |
0,7 ± 0,6 балла |
< 0,001 |
|
Количество гранулем, разрешившихся полностью (объем = 0 баллов) |
0 (0%) |
18 (72%) |
< 0,001 |
|
Максимальный длинник гранулемы по данным УЗИ |
8,4 ± 2,1 мм |
2,5 ± 1,8 мм |
p < 0,001 |
Примечание: составлено авторами на основе полученных данных в ходе исследования.
Представленные данные (табл. 1) в обобщенном виде демонстрируют высокую эффективность метода терапии аутологичной богатой тромбоцитами плазмой. Статистически значимое уменьшение среднего размера гранулемы более чем на 70% и их полное разрешение в 72% случаев обосновывает целесообразность применения плазмотерапии в качестве метода лечения данного осложнения после введения ИТН на основе ПМК.
Однако наиболее информативное подтверждение эффективности введения плазмы, обогащенной тромбоцитами, получено при сравнительном гистологическом анализе биоптатов, полученных до и после курса лечения. Характерной особенностью патоморфологической картины (рис. 4) гранулем после введения ИТН на основе ПМК является большое количество клеток инородного тела со специфическими включениями.
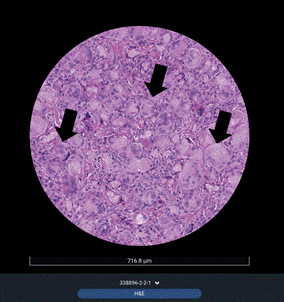
Рис. 4. Патоморфологические изменения в гранулеме дермы области шеи пациентки К., 42 лет (фиксация материала в 10%-ном нейтральном формалине, парафиновый срез 5 мкм), до курса плазмотерапии. Световая микроскопия. Окраска гематоксилином и эозином. Увеличение ×200. Репрезентативный биоптат до лечения. Визуализируется классическая гранулема инородного тела с плотным лимфо-гистиоцитарным инфильтратом, многочисленными гигантскими клетками инородных тел (черные стрелки) с округлыми включениями (соответствуют морфологии частиц инъекционного тканевого наполнителя). Составлено авторами по результатам данного исследования
Ключевым результатом клинического этапа работы явилось подтверждение способности аутологичной обогащенной тромбоцитами плазмы индуцировать обратное развитие гранулематозной ткани (рис. 5).
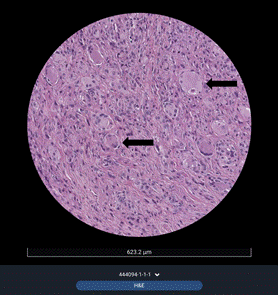
Рис. 5. Регресс патоморфологических изменений в гранулеме дермы области шеи пациентки К., 42 лет (фиксация материала в 10%-ном нейтральном формалине, парафиновый срез 5 мкм), после курса плазмотерапии. Световая микроскопия.
Окраска гематоксилином и эозином. Увеличение ×200. Отмечается резкое снижение плотности клеточного инфильтрата, уменьшение количества гигантских клеток, уменьшение количества и объема самих частиц ТИН на основе ПМК.
Составлено авторами по результатам данного исследования
Данные морфометрического анализа полностью коррелировали с визуальными наблюдениями и представлены в таблице 2.
Таблица 2
Сравнительные результаты патоморфологической морфометрии до и после лечения аутологичной богатой тромбоцитами плазмой
|
Параметр |
До лечения (n=25) |
После лечения (n=25) |
Уровень значимости, р |
|
Плотность клеточного инфильтрата |
478 ± 30 кл/мм² |
218 ± 19 кл/мм² |
<0,001 |
|
Количество гигантских клеток (в поле зр. ×200) |
10 ± 2 |
5 ± 1 |
<0,001 |
Примечание: составлено авторами на основе полученных данных в ходе исследования. Данные представлены в виде среднего значения ± стандартное отклонение; для сравнения показателей в динамике использован критерий Вилкоксона.
Как демонстрирует таблица 2, после курса плазмотерапии было зафиксировано достоверное (p<0,001) уменьшение ключевых патоморфологических параметров: плотности воспалительного инфильтрата более чем в 2 раза и количества гигантских клеток инородного тела. Процедуры инъекций аутологичной плазмы хорошо переносились всеми пациентами. Не было зарегистрировано ни одного случая серьезных нежелательных явлений, таких как аллергические реакции, инфекционные осложнения или признаки выраженной фиброзной трансформации. Отмечались ожидаемые преходящие явления: легкая гиперемия и отечность в зоне инъекции, самостоятельно разрешавшиеся во всех случаях в течение 24-48 часов после введения.
Заключение
Проведенное экспериментально-клиническое исследование подтвердило высокую эффективность и безопасность применения обогащенной тромбоцитами аутологичной плазмы для коррекции гранулематозных осложнений, индуцированных инъекциями ИТН на основе ПМК.
В экспериментальной части работы установлено, что воздействие аутоплазмы сопровождается достоверным уменьшением воспалительной инфильтрации и подавлением фиброгенеза, резорбции частиц ПМК, что клинически выражается в стойком регрессе патологических образований. Клинические наблюдения пациентов с персистирующими гранулемами подтвердили экспериментальные данные: применение разработанного протокола терапии обеспечило не только объективный регресс осложнений (верифицированный инструментальными и гистологическими методами), но и отличный профиль безопасности.
Полученные результаты позволяют рассматривать аутологичную богатую тромбоцитами плазму как эффективный и патогенетически обоснованный метод выбора для терапии гранулематозных осложнений после контурной пластики препаратами ПМК.
Дальнейшее изучение иммунологических и генетических маркеров, позволяющих прогнозировать индивидуальный риск развития гранулематозных осложнений при планировании контурной пластики для их предотвращения, а также разработки превентивных стратегий коррекции и лечения, остается актуальной частью продолжающихся авторами исследований и позволит расширить понимание механизмов развития данного патологического процесса, а также разработать систему профилактики и лечения таких осложнений.
Конфликт интересов
Библиографическая ссылка
Первых С.Л., Карпова Е.И., Лелюк В.Г. ЭФФЕКТИВНОСТЬ ОБОГАЩЕННОЙ ТРОМБОЦИТАМИ АУТОЛОГИЧНОЙ ПЛАЗМЫ В КОРРЕКЦИИ ГРАНУЛЕМАТОЗНЫХ ОСЛОЖНЕНИЙ ПОСЛЕ ВВЕДЕНИЯ ИНЪЕКЦИОННЫХ ТКАНЕВЫХ НАПОЛНИТЕЛЕЙ НА ОСНОВЕ ПОЛИМОЛОЧНОЙ КИСЛОТЫ: ЭКСПЕРИМЕНТАЛЬНО-КЛИНИЧЕСКОЕ ИССЛЕДОВАНИЕ // Современные проблемы науки и образования. 2026. № 4. ;URL: https://science-education.ru/ru/article/view?id=34542 (дата обращения: 21.04.2026).
DOI: https://doi.org/10.17513/spno.34542



