Введение
Протеинкиназы, являясь ключевыми компонентами клеточных сигнальных путей, участвуют в регуляции гомеостаза (рост, пролиферация, апоптоз) и тесно связаны с процессами онкогенеза, что делает их перспективными мишенями для таргетной терапии онкологических заболеваний [1-3]. В частности, низкомолекулярные ингибиторы тирозинкиназы (ИТК) рецептора эпидермального фактора роста (EGFR), характеризующегося гиперэкспрессией или активирующими мутациями при различных типах опухолей, успешно применяются в клинической практике на протяжении нескольких десятилетий [4]. К таким препаратам относятся гефитиниб (ZD1839), эрлотиниб (CID176870), осимертиниб (AZD9291) и другие соединения, демонстрирующие высокую эффективность в терапии немелкоклеточного рака лёгкого (НМРЛ) [5; 6].
На российском фармацевтическом рынке представлены зарубежные оригинальные ИТК EGFR и их дженерики. В то же время разработка отечественных оригинальных таргетных препаратов является приоритетной частью стратегии развития фармацевтической отрасли РФ, направленной на обеспечение лекарственной независимости [7]. К настоящему времени зарегистрирована одна оригинальная российская фармацевтическая субстанция – алофаниб (RPT835), прошедшая первую фазу клинических испытаний и представляющая собой аллостерический низкомолекулярный ингибитор рецептора фактора роста фибробластов 2 типа (FGFR 2) [8].
Актуальность разработки новых ИТК EGFR также обусловлена проблемой резистентности. У большинства пациентов первоначальный ответ на ИТК EGFR сменяется развитием устойчивости, что приводит к прогрессированию заболевания [9]. Установленные механизмы резистентности к ИТК EGFR можно подразделить на две категории. К первой относится непосредственное изменение в целевом белке, например в результате потери сенсибилизирующей мутации (T790M) или возникновения вторичных мутаций EGFR (C797S, L718Q, G724S и др.), ко второй – альтернативная активация внутриклеточных сигнальных путей, вызванная, например, хромосомными аберрациями (амплификация Met/HER2) или мутациями (KRAS/BRAF/PIK3CA), а также фенотипическая трансформация опухоли [10; 11].
Поиск и создание новых противоопухолевых препаратов сопряжены с годами работы, высокими затратами, а также с высоким риском неудачи [12]. Однако методы компьютерного моделирования позволяют оптимизировать выявление перспективных молекул-кандидатов среди различных классов соединений [13-15]. Для разработки новых ИТК EGFR особый интерес представляет скрининг гетероциклических соединений, в частности пиримидина и его производных [16-18]. В сотрудничестве с Пятигорским медико-фармацевтическим институтом был проведён in silico скрининг 17 соединений. На основании экспериментальных значений константы ингибирования (Ki) киназного центра EGFR отобрано новое производное пиримидина: 4-{2-[2-(2-гидрокси-3-метоксифенил)-винил]-6-метил-4-оксо-5-фенил-4H-пиримидин-1-ил}-бензсульфамид (далее PMSoVn). Предварительные расчёты с использованием методов молекулярного докинга (Auto Dock GPU) и молекулярной динамики (GROMACS, BioEurica) выявили структурные особенности PMSoVn, обеспечивающие высокое сродство к внутриклеточному домену EGFR. В подтверждение in silico данных необходимо исследование противоопухолевой активности соединения в опытах in vitro.
Цель исследования – оценка противоопухолевой активности соединения PMSoVn в отношении клеточных линий НМРЛ человека А549 и NCI-H1299.
Материалы и методы исследования
Соединение PMSoVn (рис. 1) стабилизировали 1-этенилпирролидин-2-оном (поливинилпирролидон (ПВП), (ГОСТ ФС 42-1194-98)); полученная мелкодисперсная коллоидная смесь была прозрачной, слабо-жёлтого цвета, не имела запаха и растворялась в воде.
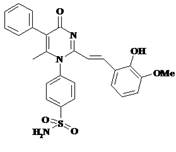
Рис. 1. Структурная формула 4-{2-[2-(2-гидрокси-3-метоксифенил)-винил]-6-метил-4-оксо-5-фенил-4H-пиримидин-1-ил}-бензсульфамида (PMSoVn)
Клеточные линии и условия культивирования
В эксперименте использовали клеточные линии НМРЛ человека А549 (EGFR дикий тип, KRAS G12S) и NCI-Н1299 (EGFR дикий тип, p53-null). Культивирование проводили в полной питательной среде на основе DMEM (Service Bio, Китай) с добавлением 10% фетальной бычьей сыворотки (Hy Clone, США), 1% неосновных аминокислот (Gibco, США), 1% глутамина («Биолот», Россия) и 1% гентамицина («Биолот», Россия) во влажной атмосфере с 5,0% СО2 при температуре 37°С. После достижения логарифмической фазы роста клетки высевали в 96-луночные планшеты (5х103клеток на лунку) и культивировали в течение 24 часов для адгезии.
Оценка жизнеспособности клеток (МТТ-тест)
Цитотоксическое действие PMSoVn оценивали с использованием колориметрического МТТ-теста (3-[4,5-диметилтиазол-2-ил]-2,5-дифенилтетразолия бромид, МТТ) в соответствии с методологией, описанной Kumar et al. [19]. После 24 часов культивирования среду в опытных лунках заменяли на свежую, содержащую PMSoVn в концентрациях: 22,47; 11,23; 5,62; 2,81; 1,40; 0,70; 0,35; 0,18; 0,088; 0,044 и 0,022 µМ. В контрольные лунки добавляли среду, содержащую ПВП в концентрации, эквивалентной его содержанию в опытных лунках. Планшеты инкубировали в течение 24, 48 и 72 часов. После указанной обработки в каждую лунку вносили 20 мкл рабочего раствора МТТ (5 мг/мл в фосфатном буфере) и инкубировали 2 часа для образования формазана. Затем среду в лунках удаляли и добавляли 100 мкл диметилсульфоксида для солюбилизации кристаллов формазана. Оптическую плотность измеряли на планшетном ридере Infinite® M NanoPlus (Tecan, Швейцария) при длине волны 540 нм. Каждый вариант эксперимента включил 16 повторов, выполненных в трёх независимых сериях.
Жизнеспособность клеток в каждой лунке рассчитывали по формуле: жизнеспособность (%)=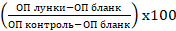 , где ОП лунки – оптическая плотность лунок, ОП контроль – среднее значение оптической плотности в контрольных лунках, ОП бланк – оптическая плотность лунок без клеток. Нормализованные значения выражали в процентах относительно контроля. Усреднённые результаты представлены как среднее арифметическое ± стандартное отклонение (M±SD) для трёх независимых серий опыта (n=3).
, где ОП лунки – оптическая плотность лунок, ОП контроль – среднее значение оптической плотности в контрольных лунках, ОП бланк – оптическая плотность лунок без клеток. Нормализованные значения выражали в процентах относительно контроля. Усреднённые результаты представлены как среднее арифметическое ± стандартное отклонение (M±SD) для трёх независимых серий опыта (n=3).
Значения IC50 (концентрация полумаксимального ингибирования) вычисляли с использованием логистической регрессионной модели в онлайн-калькуляторе QuestGraph™IC50 Calculator (AAT bioquest, Inc., США) [20]. Результаты представлены как среднее арифметическое ± стандартное отклонение (M±SD) для трёх независимых серий опыта (n=3).
Оценка апоптоза/некроза
Для анализа форм клеточной гибели применяли двойное окрашивание клеток аннексином V-PE и DAPI. Клетки Н1299 обрабатывали PMSoVn (12,5 µМ) в течение 24 и 72 часов. В контрольные лунки добавляли среду, содержащую ПВП в концентрации, эквивалентной его содержанию в опытных лунках. Клеточную суспензию готовили согласно инструкции к набору реагентов для детекции апоптоза (Кат. № ALAP-100, Nano Entek, Корея). Окрашенные аннексином V-PE/DAPI образцы в объёме 25 мкл помещали на слайд ADAMII и анализировали на флуоресцентном анализаторе ADAMII LS (Nano Entek, Корея). Результаты представлены как среднеарифметическое значение и стандартное отклонение (M±SD) для трёх независимых серий опыта (n=3).
Статистическую обработку полученных данных проводили с использованием пакета программ Microsoft Excel 2016 (Microsoft, США) и Statistiсa 6.0 (StatSoft, Inc). Нормальность распределения оценивали с помощью критерия Шапиро-Уилка. Для множественных сравнений применяли однофакторный ANOVA с апостериорным тестом Даннета относительно контроля, для парных сравнений применяли двусторонний t-критерий Стьюдента. Различия считали статистически значимыми при уровне достоверности 95% (p<0,05).
Результаты исследования и их обсуждение
Соединение PMSoVn не проявляло значимого цитотоксического действия в отношении клеток линии А549 при всех трёх вариантах инкубации. Так, выживаемость клеток после 48 часов культивирования с PMSoVn в концентрациях 11,23 и 22,47 µМ сохранялась на уровне 87,32±15,79% и 87,87±10,74% соответственно. При экспозиции в течение 72 часов максимальное ингибирование роста А549 не превышало 22%. Соответственно значение IC50 не установлено (рис. 2).
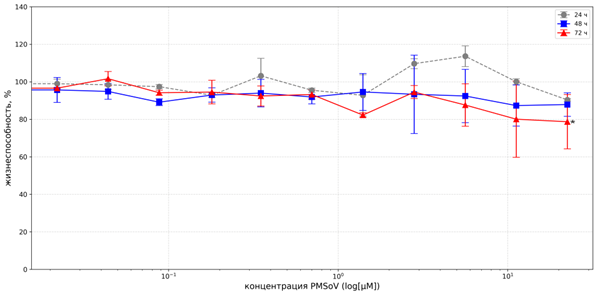
Рис. 2. Цитотоксическое действие PMSoVn на клетки линии А549 в MTT-тесте после инкубации в течение 24, 48 и 72 часов
Примечание: * уровень статистической значимости различий по сравнению с контролем p<0,05. Каждая точка данных представлена как среднеарифметическое значение (M) и стандартное отклонение (±SD).
Источник: составлено авторами на основе полученных данных в ходе исследования.
В отношении линии NCI-H1299 соединение проявляло время- и дозозависимый цитотоксический эффект. Результаты МТТ-теста при 24 часах инкубации продемонстрировали отсутствие 50% торможения роста клеток (рис. 3). Кроме того, на графике наблюдалось увеличение показателя жизнеспособности клеток (в диапазоне доз 0,35-5,62 µМ), что, однако, не имело статистически значимых различий относительно контроля.
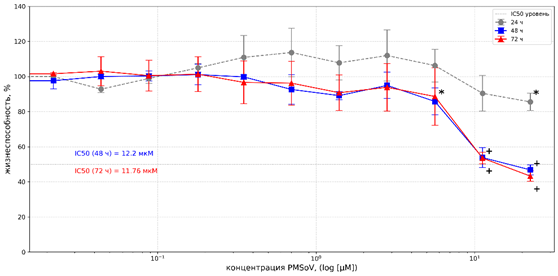
Рис. 3. Цитотоксическое действие PMSoVn на клетки линии NCI-H1299 в MTT-тесте после инкубации в течение 24, 48 и 72 часов
Примечание: * и + уровень статистической значимости различий по сравнению с контролем при p<0,05 и p<0,0001 соответственно. Каждая точка данных представлена как среднеарифметическое значение (M) и стандартное отклонение (±SD).
Источник: составлено авторами на основе полученных данных в ходе исследования.
После 48 часов инкубации жизнеспособность клеток снижалась до 53,81±5,6% и 46,82±2,82% при концентрациях 11,23 и 22,47 µМ соответственно, со значением IC50 в пределах 12,2±3,74 µМ. Увеличение времени экспозиции до 72 часов незначительно повышало эффективность воздействия, снизив значение IC50 до 11,76±2,2 µМ (рис. 3). Отсутствие эффекта при 24 часах экспозиции и значимое снижение жизнеспособности к 48–72 часам свидетельствует о накопительном эффекте действия PMSoVn.
Для оценки гибели клеток культуру H1299 инкубировали с PMSoVn в дозе, близкой к IC50 (12,5 µМ). Эффект PMSoVn через 24 часа инкубации характеризовался снижением количества живых клеток с 92,60% до 77,41% (p<0,01), увеличением в 3 раза уровня некроза (с 4,92% до 14,76%, p<0,01) и раннего апоптоза (с 2,08% до 6,14%, p<0,01), повышением уровня позднего апоптоза более чем в 4 раза (с 0,39% до 1,69%, p<0,01) (табл. 1, рис. 4).
Влияние PMSoVn на гибель клеток линии NCI-Н1299 (M±SD)
|
Параметр |
24 часа |
72 часа |
||
|
Живые (%) |
контроль |
PMSoVn |
контроль |
PMSoVn |
|
92,61±2,27 |
77,41±2,86* |
92,8±11,23 |
49,93±0,92** †† |
|
|
Ранний апоптоз (%) |
2,08±0,88 |
6,14±1,16* |
3,09±1,22 |
11,37±1,13** † |
|
Поздний апоптоз (%) |
0,39±0,36 |
1,69±0,22* |
0,28±0,09 |
3,94±0,87*† |
|
Некроз (%) |
4,92±1,95 |
14,76±1,87* |
3,83±0,88 |
35,37±1,19** †† |
Примечание: данные в таблице представлены как среднеарифметическое значение (M) и стандартное отклонение (±SD). Уровень статистической значимости различий: по сравнению с контролем в те же сроки *p<0,01 и **p<0,001; по сравнению с эффектом PMSoVn через 24 часа † p<0,01 и †† p<0,001.
Источник: составлено авторами на основе полученных данных в ходе исследования.
Через 72 часа доля живых клеток снижалась на 46,2% (р<0,001) по сравнению с контролем (92,8±11,23) и на 35,5% по сравнению с показателем через 24 часа (p<0,01). При этом доля клеток в некрозе увеличивалась в 9 раз (р<0,001) по сравнению с контролем и более чем в два раза относительно показателя при инкубации 24 часа (р<0,01). Ранний апоптоз повышался относительно контроля в 3,7 раза (р<0,001) и инкубации 24 часа (на 85,5%; p<0,01). Поздний апоптоз вырос вдвое по сравнению с 24 часами (р<0,01) и в 14 раз по сравнению с контролем (р<0,001).
Из представленных данных видно, что PMSoVn через24 часа стимулирует все формы клеточной гибели NCI-Н1299. Увеличение продолжительности инкубации до 72 часов усиливает цитотоксическое действие соединения, сокращая долю живых клеток вдвое. При всех вариантах инкубации гибель клеток происходит преимущественно путём некроза, с дополнительной индукцией раннего и позднего апоптоза.
Таким образом, данные МТТ-теста свидетельствуют о различной чувствительности А549 (рис. 2) и NCI-H1299 (рис. 3) к цитотоксическому действию PMSoVn. Для клеток линии NCI-H1299 была установлена умеренная кумулятивная цитотоксичность со значениями IC50 в пределах 12,2±3,74 µМ (48 часов) и 11,76±2,2 µМ (72 часа). Результаты, полученные авторами, согласуются с данными о цитотоксической активности осимертиниба (производное пиримидина) в отношении NCI-H1299 (IC50~10 µМ) [21] и аналогичны результатам оценки цитотоксичности потенциальных ингибиторов EGFR дикого типа на основе пиридо[2,3-d]пиримидин-4(3H)-она, отобранных из ряда соединений, в отношении А549 (IC50 в диапазоне 7,23-16,2 µМ) [22]. Для А549 50% ингибирования роста клеточной популяции в тестируемом диапазоне доз получено не было. Однако для этой линии клеток показатели IC50 стандартных ИТК EGFR могут иметь высокие значения, в частности IC50 гефитиниба может достигать 18,9-32,0 µМ [23-25].
Низкая, по сравнению с NCI-H1299, чувствительность клеток линии А549 к исследуемому соединению может быть обусловлена особенностями её генетического профиля (KRAS G12S), поскольку известно, что наличие мутаций KRAS может влиять на устойчивость к ИТК EGFR [26; 27]. В частности, сообщалось, что у больных аденокарциномой лёгких мутации KRAS (G12X, G13С) ассоциировались с устойчивостью к ИТК EGFR хиназолинового ряда (гефитиниб/эрлотиниб) [28]. В клеточных же линиях НМРЛ (PC-9 и NCI-H1975), чувствительных к осимертинибу, развивалась резистентность к препарату после возникновения мутации KRAS G12V [29]. У мышей линии Balb/c nude ксенографт А549 использовался для моделирования опухоли, устойчивой к гефитинибу [30].
Результаты, полученные на клеточных линиях НМРЛ с различными механизмами резистентности к ИТК EGFR, обосновывают возможность дальнейшего изучения PMSoVn как потенциального ингибитора тирозинкиназы EGFR, на чувствительных к ИТК EGFR иммортализованных клеточных линиях НМРЛ человека, в частности PC-9 (Ex19del E746-A750), H820 (Ex19del E746-E749/T790M), NCI-H1975 (L858R/T790M) и др., а также исследований на первичных культурах клеток рака лёгкого [31].
Заключение
Предварительная оценка нового производного пиримидина-4(1H)-она (PMSoVn) выявила избирательную противоопухолевую активность в отношении клеточной линии НМРЛ NCI-H1299. Клетки линии А549 оказались малочувствительными к соединению. Умеренный цитотоксический эффект PMSoVn проявлялся в дозо- и времязависимом режиме с IC50~12 µМ, сопровождаясь индукцией как некроза, так и апоптоза. Отсутствие значимой активности в отношении А549, вероятно, связано с наличием мутации KRAS, ассоциированной с резистентностью к ингибиторам EGFR. Для установления точных механизмов действия, селективности и выявления направлений структурной оптимизации PMSoVn с целью повышения его эффективности требуются дополнительные исследования.
Конфликт интересов
Библиографическая ссылка
Кит О.И., Франциянц Е.М., Кодониди И.П., Каплиева И.В., Алексеев Э.К., Глушко А.А., Качесова П.С., Филиппова С.Ю., Межевова И.В., Чиряпкин А.С., Шихлярова А.И., Шалашная Е.В., Волкова В.Л. ПРОТИВООПУХОЛЕВАЯ АКТИВНОСТЬ НОВОГО ПРОИЗВОДНОГО ПИРИМИДИНА-4(1H)-ОНА В МОДЕЛЯХ НЕМЕЛКОКЛЕТОЧНОГО РАКА ЛЕГКИХ IN VITRO // Современные проблемы науки и образования. 2025. № 3. ;URL: https://science-education.ru/ru/article/view?id=34141 (дата обращения: 29.04.2026).
DOI: https://doi.org/10.17513/spno.34141



