Введение
Первые двадцать лет XXI века ознаменовались уверенной тенденцией к снижению заболеваемости туберкулезом как в мире, так и особенно быстрыми темпами – в России. На фоне ухудшения общей эпидемической ситуации по туберкулезу в большинстве стран мира в результате пандемии COVID-19, в России продолжилось ее улучшение [1]. Эпидемическая ситуация по туберкулёзу в 2022 году оставалась стабильной. Показатель заболеваемости туберкулёзом, как и в 2021 году, остался на уровне 31,0 на 100 000 населения. Большинство заболевших туберкулёзом составляют мужчины – 68,2%. Смертность от туберкулёза в 2021 году составила 4,3 на 100 000 населения. Показатели заболеваемости туберкулёзом и смертности от него достигли исторического минимума. Распространённость туберкулёза среди гражданского населения также снизилась до исторического минимума и составила 58,5 на 100 000 населения. Распространённость туберкулёза с бактериовыделением составила 26,6%; среди бактериовыделителей 56,9% составляют больные туберкулёзом с множественной лекарственной устойчивостью возбудителя [2]. Благодаря успехам российской фтизиатрической службы ВОЗ в 2021 году исключила Российскую Федерацию из списка стран с высоким бременем туберкулеза [3].
Активно внедряются в практику инновационные препараты и методы лечения туберкулёза. Тем не менее туберкулез (ТБ) с множественной лекарственной устойчивостью (МЛУ) в настоящее время представляет одну из основных проблем, влияющих на возможность искоренения ТБ. Несмотря на снижение уровня заболеваемости ТБ в мире в целом, ТБ с МЛУ продолжает расти [4]. По данным официальной статистики, на конец 2022 года в РФ доля МЛУ среди впервые выявленных составила 37%, при этом доля ШЛУ среди МЛУ составила 22,3%. Применение с 2015 года новых противотуберкулезных препаратов привело к повышению эффективности лечения больных с МЛУ МБТ, достигшей в РФ в 2022 году 54,2%, однако уровень целевых показателей ВОЗ в 80% остаётся не реализованным.
Лечение туберкулеза предполагает использование комбинации противотуберкулезных препаратов, многие из которых вызывают нежелательные побочные реакции различной степени тяжести. Для повышения эффективности и безопасности лечения больных туберкулезом большое значение имеет рациональное использование всех методов комплексной терапии, в том числе патогенетических [5], с применением адъювантных препаратов. В российских клинических рекомендациях «Туберкулез у взрослых» (2024) им уделяется большое внимание, в частности рекомендуется применение глутамил-цистеинил-глицина динатрия – препарата, созданного в 1994 г. в РФ [6; 7].
Цель исследования
Целью исследования явилась оценка эффективности и безопасности применения глутамил-цистеинил-глицина динатрия как адъюванта при лечении туберкулеза легких с ЛЧ и ЛУ возбудителя МБТ.
Материалы и методы исследования
Проведено ретроспективное исследование с анализом медицинской документации пациентов ГБУЗ ЯО «ЯОКТБ», находящихся на стационарном лечении. В исследование включено 127 пациентов (n=127) с различными формами туберкулеза органов дыхания, которые были распределены на 4 группы: 1-я группа (n=35) – пациенты с лекарственной чувствительностью микобактерий туберкулеза (ЛЧ МБТ), получающие стандартную схему лечения; 2-я группа (n=37) – пациенты с ЛЧ МБТ, получающие стандартную схему лечения в сочетании с глутамил-цистеинил-глицина динатрием; 3-я группа (n=27) – пациенты с множественной лекарственной устойчивостью микобактерий туберкулеза (МЛУ МБТ), получающие стандартную схему лечения; 4-я группа (n=28) – пациенты с МЛУ МБТ, получающие стандартную схему лечения в сочетании с глутамил-цистеинил-глицина динатрием.
Группы пациентов сопоставимы по полу, возрасту, социальному статусу, группам и формам туберкулеза. По формам процесса среди ЛЧ ТБ преобладали пациенты с инфильтративной и диссеминированной формами туберкулеза легких в равных соотношениях, среди ЛУ ТБ преобладали диссеминированные формы. Во всех группах преобладали неработающие мужчины в возрасте 30-60 лет (табл. 1).
У большинства пациентов до начала лечения зафиксированы симптомы интоксикации в виде потливости, слабости, температуры. Также большинство из них имели жалобы на кашель и одышку. Динамика этих симптомов и жалоб оценивалась на протяжении 6 месяцев.
У всех пациентов присутствовало бактериовыделение, до начала лечения у всех пациентов определена чувствительность к изониазиду и рифампицину молекулярно-генетическим методом, которая далее подтверждена культуральными методами. Динамическое микробиологическое исследование выполнялось с помощью стандартных микробиологических методов: прямая люминесцентная микроскопия и посевы на плотные питательные среды.
Рентгенологически у всех пациентов имелись полости распада до начала лечения и оценивалось их закрытие на протяжении 10 месяцев.
Таблица 1
Распределение групп
|
|
ЛЧ |
ЛЧ + Glu |
ЛУ |
ЛУ + Glu |
|
Распределение по формам туберкулеза (абс.) |
||||
|
Очаговый |
2 |
2 |
- |
- |
|
Инфильтративный |
14 |
14 |
8 |
8 |
|
Диссеминированный |
14 |
15 |
14 |
16 |
|
Фиброзно-кавернозный |
- |
1 |
3 |
2 |
|
Казеозная пневмония |
5 |
5 |
2 |
2 |
|
Всего пациентов |
35 |
37 |
27 |
28 |
|
Распределение по полу (%) |
||||
|
Мужской |
80 |
95 |
93 |
96 |
|
Женский |
20 |
5 |
7 |
4 |
|
Распределение по социальному статусу (%) |
||||
|
Работающие |
22,9 |
29,7 |
22,2 |
14,3 |
|
Неработающие |
68,6 |
67,6 |
74,1 |
82,1 |
|
Пенсионеры |
8,5 |
2,7 |
3,7 |
3,6 |
|
Распределение по возрасту (%) |
||||
|
18-30 |
5,7 |
10,8 |
11,1 |
3,6 |
|
31-44 |
45,7 |
43,2 |
44,4 |
57,1 |
|
45-60 |
42,9 |
40,5 |
40,7 |
35,7 |
|
61 и старше |
5,7 |
5,5 |
3,8 |
3,6 |
|
Распределение по группам (%) |
||||
|
Впервые выявленные |
94,3 |
83,8 |
77,7 |
67,9 |
|
Из контингентов |
5,7 |
16,2 |
18,5 |
25 |
|
Рецидив |
- |
- |
3,8 |
7,1 |
Примечание: Glu - глутамил-цистеинил-глицина динатрия.
Больным 1-й и 2-й групп назначался стандартный режим лекарственно чувствительного туберкулеза (HREZ), коррекция схемы проводилась с учетом побочных реакций и переносимости в некоторых случаях. Больным 2-й и 3-й групп назначался режим МЛУ, преШЛУ и ШЛУ в зависимости от полученных данных о спектре устойчивости с преобладанием Bq Lzd Cs Fq PAS/Dlm/Pt/Cap [7].
В составе комплексной терапии пациентам 2-й и 4-й групп глутамил-цистеинил-глицина динатрия вводился внутримышечно по 60 мг 1 раз в сутки в первые 10 дней - ежедневно, далее по 60 мг 1 раз в сутки через день – 20 инъекций.
У всех пациентов ежемесячно оценивался общий анализ крови (ОАК) и биохимический анализ крови (БАК) по каждому показателю отдельно, и при наличии отклонений оценивались сроки нормализации этих показателей.
В ходе исследования оценивалась эффективность лечения по показателям исчезновения клинических признаков заболевания, прекращения бактериовыделения и сроков закрытия полостей распада [8].
Результаты исследования и их обсуждение
В таблице 2 рассмотрены симптомы интоксикации и респираторные жалобы у пациентов исследуемых групп с указанием сроков купирования этих отклонений.
Таблица 2
Исчезновение клинических признаков туберкулеза, %
|
|
Группа |
1м |
2м |
3м |
4м |
5м |
6м |
Признак сохраняется после 6 мес. лечения |
|
Потливость |
ЛЧ, 66% |
35 |
61 |
78 |
91 |
100 |
- |
- |
|
ЛЧ+Glu, 71% |
65 |
85 |
96 |
96 |
96 |
100 |
- |
|
|
ЛУ, 76% |
44 |
61 |
78 |
94 |
94 |
100 |
- |
|
|
ЛУ+Glu, 61% |
59 |
94 |
100 |
- |
- |
- |
- |
|
|
Слабость |
ЛЧ, 57% |
25 |
30 |
45 |
80 |
100 |
- |
- |
|
ЛЧ+Glu, 84% |
65 |
90 |
100 |
- |
- |
- |
- |
|
|
ЛУ, 78% |
24 |
38 |
52 |
86 |
100 |
- |
- |
|
|
ЛУ+Glu, 76% |
50 |
82 |
86 |
100 |
- |
- |
- |
|
|
Температура |
ЛЧ, 49% |
35 |
59 |
82 |
100 |
- |
- |
- |
|
ЛЧ+Glu, 38% |
64 |
79 |
100 |
- |
- |
- |
- |
|
|
ЛУ41% |
27 |
64 |
73 |
100 |
- |
- |
- |
|
|
ЛУ+Glu, 29% |
50 |
88 |
100 |
- |
- |
- |
- |
|
|
Кашель |
ЛЧ, 71% |
- |
- |
12 |
24 |
32 |
48 |
52 |
|
ЛЧ+Glu, 70% |
- |
23 |
38 |
58 |
62 |
69 |
31 |
|
|
ЛУ, 63% |
- |
- |
- |
6 |
6 |
29 |
71 |
|
|
ЛУ+Glu, 64% |
- |
6 |
22 |
22 |
22 |
56 |
44 |
|
|
Одышка |
ЛЧ, 34% |
8 |
17 |
25 |
50 |
58 |
58 |
42 |
|
ЛЧ+Glu, 41% |
20 |
40 |
53 |
73 |
73 |
87 |
13 |
|
|
ЛУ, 52% |
- |
7 |
7 |
36 |
43 |
50 |
50 |
|
|
ЛУ+Glu, 43% |
- |
- |
10 |
20 |
50 |
50 |
50 |
У большинства пациентов исследуемых групп до начала лечения отмечалась потливость: 1-я группа - 23 человека (66%), 2-я группа – 26 человек (71%), 3-я группа - 18 человек (67%), 4-я группа – 17 человек (61%). Исчезновение данного симптома к концу 1-го месяца лечения отмечено быстрее на 30% во 2-й группе по сравнению с 1-й и на 14% быстрее в 4-й по отношению к 3-й. К концу 3 месяца лечения потливость исчезла в 96/100% случаев при использовании глутамил-цистеинил-глицина динатрия в группах и ЛЧ/ЛУ, в то время как без него данный симптом сохранялся и до 5/6 месяца лечения соответственно.
Слабость отмечали в 1-й группе – 20 человек (57%), во 2-й группе – 31 человек (84%), в 3-й группе – 21 человек (78%), в 4-й группе – 22 человека (76%). С применением глутамил-цистеинил-глицина динатрия ускорилось купирование слабости на 41% при ЛЧ и на 26% при ЛУ. В последующие месяцы также сохранялась тенденция к более быстрому купированию этого симптома с применением глутамил-цистеинил-глицина динатрия.
Температура отмечалась реже: 1-я группа – 6 человек (49%), 2-я группа - 14 человек (38%), 3-я группа – 11 человек (41%), 4-я группа - 8 человек (29%). Однако купирование этого симптома также происходило быстрее с применением глутамил-цистеинил-глицина динатрия на 35/23% соответственно. При этом темпы нормализации температуры в группах ЛЧ/ЛУ и ЛЧ+Glu/ЛУ+Glu соразмерны друг другу.
Кашель отмечался в 1-й группе у 25 человек (71%), во 2-й группе у 26 (70%), в 3-й группе у 17 (63%), в 4-й группе у 18 (64%) человек. К 3-му месяцу лечения кашель купирован на 26/22% быстрее во 2-й и 4-й группах по сравнению с 1-й и 3-й соответственно. А по истечении 6 месяцев лечения кашель сохранялся на 21/27% меньше в тех же группах.
Одышка встречалась в 1-й группе у 12 (34%), во 2-й группе у 15 (41%), в 3-й группе у 14 (52%), в 4-й группе у 12 (43%) человек. К концу 3-го месяца лечения одышка купирована на 28/18% быстрее у пациентов, принимающих глутамил-цистеинил-глицина динатрия в группах ЛУ/ЛЧ соответственно (рис. 1).
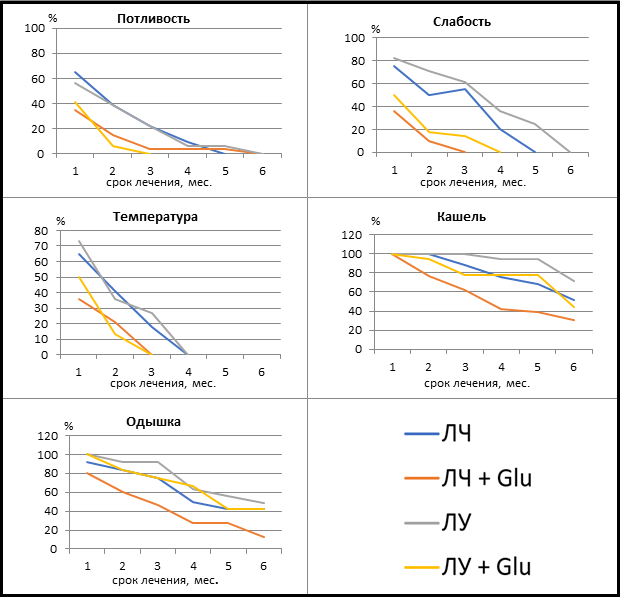
Рис. 1. Исчезновение клинических признаков туберкулеза, %
В ходе исследования оценивались показатели общего анализа крови до лечения, через 2, 4 и 6 месяцев лечения. Динамика показателей представлена в таблице 3.
Таблица 3
Нормализация показателей ОАК, %
|
Нормализация показателей в ОАК у пациентов с ЛЧ и с ЛЧ + Glu в % |
||||||||||
|
Показатель |
2 мес. лечения |
4 мес. лечения |
6 мес. лечения |
Сохранение отклонений после 6 мес. лечения |
Отрицательная динамика |
|||||
|
ЛЧ |
ЛЧ + Glu |
ЛЧ |
ЛЧ + Glu |
ЛЧ |
ЛЧ + Glu |
ЛЧ |
ЛЧ + Glu |
ЛЧ |
ЛЧ + Glu |
|
|
Эритроциты |
13 |
20 |
51 |
53 |
64 |
73 |
36 |
27 |
- |
- |
|
Гемоглобин |
20 |
20 |
30 |
47 |
70 |
74 |
20 |
26 |
10 |
- |
|
Лейкоциты |
- |
20 |
8 |
44 |
47 |
80 |
31 |
8 |
22 |
12 |
|
Тромбоциты |
5 |
33 |
15 |
53 |
20 |
66 |
43 |
27 |
37 |
7 |
|
СОЭ |
16 |
13 |
35 |
45 |
45 |
71 |
48 |
26 |
7 |
3 |
|
с/я |
40 |
42 |
47 |
79 |
54 |
95 |
20 |
- |
26 |
5 |
|
Лимфоциты |
38 |
30 |
57 |
56 |
76 |
82 |
24 |
13 |
- |
5 |
|
Моноциты |
29 |
42 |
47 |
75 |
71 |
83 |
6 |
- |
23 |
17 |
|
Нормализация показателей в ОАК у пациентов с ЛУ и с ЛУ + Glu в % |
||||||||||
|
Показатель |
2 мес. лечения |
4 мес. лечения |
6 мес. лечения |
Сохранение отклонений после 6 мес. лечения |
Отрицательная динамика |
|||||
|
ЛУ |
ЛУ + Glu |
ЛУ |
ЛУ + Glu |
ЛУ |
ЛУ + Glu |
ЛУ |
ЛУ + Glu |
ЛУ |
ЛУ + Glu |
|
|
Эритроциты |
7 |
38 |
40 |
53 |
53 |
68 |
27 |
23 |
20 |
9 |
|
Гемоглобин |
- |
7 |
36 |
43 |
63 |
57 |
18 |
43 |
19 |
- |
|
Лейкоциты |
22 |
23 |
33 |
62 |
44 |
85 |
28 |
15 |
28 |
- |
|
Тромбоциты |
- |
- |
18 |
38 |
36 |
63 |
27 |
13 |
37 |
24 |
|
СОЭ |
4 |
10 |
17 |
34 |
25 |
77 |
63 |
23 |
12 |
- |
|
с/я |
37 |
36 |
69 |
91 |
74 |
100 |
16 |
- |
10 |
- |
|
Лимфоциты |
26 |
7 |
42 |
27 |
63 |
87 |
26 |
13 |
11 |
- |
|
Моноциты |
19 |
9 |
38 |
45 |
50 |
81 |
- |
- |
50 |
19 |
Снижение количества эритроцитов наблюдалось в 1-й группе - 23%, 2-й группе - 41%, 3-й группе - 56%, 4-й группе - 46% от общего числа пациентов в группах. Нормализация показателя ко 2-му месяцу лечения с глутамил-цистеинил-глицин динатрием больше на 7/31% по ЛЧ/ЛУ группам, на 9/4% меньше сохранение отклонений и отрицательная динамика у пациентов 4-й группы меньше на 11% по сравнению с 3-й группой.
Восстановление уровня гемоглобина во 2-й группе быстрее, чем в 1-й, а также в 3-й группе быстрее, чем в 4-й, к 4 месяцам лечения на 17/7%. Сохранение отклонения и отрицательная динамика чаще отмечены у пациентов без глутамил-цистеинил-глицин динатрия.
Нормализация уровня тромбоцитов быстрее проходила во 2-й и 4-й группах по отношению к 1-й и 3-й группам, сохранение отклонения и отрицательная динамика больше в 1-й и 3-й группах на 16/14% и 30/13% соответственно.
Отрицательная динамика по показателям количества эритроцитов, гемоглобина и тромбоцитов показывает частоту побочных реакций на противотуберкулезные препараты, влияющие на ростки кроветворения. В группах, получающих глутамил-цистеинил-глицин динатрия, эти цифры значительно ниже. А среди тех, у кого имелись отклонения по данным параметрам, нормализация этих показателей происходила быстрее с глутамил-цистеинил-глицин динатрием.
Отклонения в ОАК по показателям количества лейкоцитов, уровня СОЭ и изменениям в лейкоцитарной формуле встречались чаще у пациентов с распространенными формами процесса. И у всех пациентов, получающих глутамил-цистеинил-глицин динатрия, нормализация этих показателей проходила быстрее.
Нормализация количества лейкоцитов к 6 месяцам лечения больше на 33/41% в 3-й и 4-й группах, сохранение отклонения и отрицательная динамика больше в 1-й и 3-й группах.
Нормализация СОЭ быстрее на 26/52% во 2-й и 4-й группах. Нормализация лейкоцитарной формулы также выше до 40% во 2-й и 4-й группах к 6 месяцам лечения.
В целом комбинированная противотуберкулезная терапия, проводимая в сочетании с глутамил-цистеинил-глицина динатрием, реже сопровождается нежелательными явлениями, связанными с побочными эффектами противотуберкулезных препаратов. Назначение глутамил-цистеинил-глицин динатрия больным с уже развившимся медикаментозным поражением печени оказывает определенное лечебное действие и позволяет продолжать специфическую терапию в полном объеме, не прибегая к ее временной отмене [9].
В таблице 4 показаны сроки нормализации отклонений в БАК.
Таблица 4
Нормализация показателей БАК, %
|
Нормализация показателей в БАК у пациентов с ЛЧ и с ЛЧ + Glu в % |
||||||||||
|
Показатель |
2 мес. лечения |
4 мес. лечения |
6 мес. лечения |
Сохранение отклонений после 6 мес. лечения |
Отрицательная динамика |
|||||
|
ЛЧ |
ЛЧ + Glu |
ЛЧ |
ЛЧ + Glu |
ЛЧ |
ЛЧ + Glu |
ЛЧ |
ЛЧ + Glu |
ЛЧ |
ЛЧ + Glu |
|
|
АСТ |
11 |
31 |
11 |
62 |
17 |
70 |
33 |
- |
50 |
30 |
|
АЛТ |
16 |
36 |
16 |
63 |
37 |
81 |
26 |
10 |
37 |
9 |
|
Билирубин |
10 |
58 |
10 |
66 |
10 |
83 |
30 |
9 |
60 |
8 |
|
СРБ |
10 |
19 |
20 |
46 |
39 |
85 |
48 |
15 |
13 |
- |
|
Креатинин |
17 |
50 |
25 |
50 |
33 |
63 |
- |
13 |
67 |
24 |
|
Нормализация показателей в БАК у пациентов с ЛУ и с ЛУ + Glu в % |
||||||||||
|
Показатель |
2 мес. лечения |
4 мес. лечения |
6 мес. лечения |
Сохранение отклонений после 6 мес. лечения |
Отрицательная динамика |
|||||
|
ЛУ |
ЛУ + Glu |
ЛУ |
ЛУ + Glu |
ЛУ |
ЛУ + Glu |
ЛУ |
ЛУ + Glu |
ЛУ |
ЛУ + Glu |
|
|
АСТ |
27 |
30 |
27 |
70 |
27 |
100 |
27 |
- |
46 |
- |
|
АЛТ |
10 |
57 |
30 |
86 |
30 |
100 |
20 |
- |
50 |
- |
|
Билирубин |
17 |
44 |
25 |
77 |
59 |
100 |
8 |
- |
33 |
- |
|
СРБ |
5 |
24 |
24 |
29 |
48 |
100 |
43 |
- |
9 |
- |
|
Креатинин |
- |
17 |
17 |
67 |
17 |
67 |
17 |
- |
66 |
33 |
Частота встречаемости нарушений в БАК по показателям АСТ, АЛТ, билирубин в ходе исследования показала, что среди пациентов, получающих глутамил-цистеинил-глицин динатрия, как среди ЛЧ, так и среди ЛУ достоверно ниже, чем в группах сравнения без него, что доказывает его гепатопротективные свойства.
Нарушение показателей БАК в исследуемых группах наблюдалось в объеме:
- АСТ: 1 гр. – 18 чел. (51.4%), 2 гр. – 13 чел. (35.1%), 3 гр. – 11 чел. (40.7%), 4 гр. - 10 чел. (35.7%);
- АЛТ: 1 гр. – 19 чел. (19.54%), 2 гр. – 11 чел. (29.7%), 3 гр. – 10 чел. (37%), 4 гр. – 7 чел. (25%);
- билирубин: 1 гр. – 10 чел. (28.6%), 2 гр. – 12 чел. (32.4%), 3 гр. – 12 чел. (44.4%), 4 гр. – 9 чел. (32.1%);
- СРБ: 1 гр. - 31 чел. (88.6%), 2 гр. – 26 чел. (70.3%), 3 гр. – 21 чел. (77.8%), 4 гр. – 17 чел. (60.7%);
- креатинин: 1 гр. – 12 чел. (34.3%), 2 гр. – 8 чел. (21.6%), 3 гр. – 6 чел. (22.2%), 4 гр. – 6 чел. (21.4%).
Нормализация показателей АСТ, АЛТ, билирубина ко 2-му месяцу лечения во 2-й и 4-й группах увеличивалась до 48%, отрицательной динамики по всем показателям в этих группах было меньше.
Уровень СРБ был повышен у пациентов с распространенными формами туберкулеза и яркой клинической картиной, к 6-му месяцу лечения СРБ приходил в норму на 46/52% быстрее с использованием глутамил-цистеинил-глицин динатрия при ЛЧ/ЛУ соответственно.
Проводимое исследование уровня общего белка и мочевины явилось статистически незначимым.
Самыми важными в оценке эффективности применения глутамил-цистеинил-глицин динатрия являются показатели прекращения бактериовыделения и закрытие полостей распада. В группе ЛЧ к концу 2-го месяца абациллировано только 32%, в группе ЛЧ+Glu 62%, в группе ЛУ 22%, в группе ЛУ+Glu 28%. Через 3 месяца лечения абациллировано: 1 гр. - 49%, 2 гр. - 76%, 3 гр. - 22%, 4 гр. - 36%. Через 4 месяца лечения абациллировано: 1 гр. - 58%, 2 гр. - 81%, 3 гр. - 41%, 4 гр. - 65%. Через 6 месяцев лечения абациллировано: 1 гр. - 89%, 2 гр. - 92%, 3 гр. - 76%, 4 гр. - 87% (рис. 2).
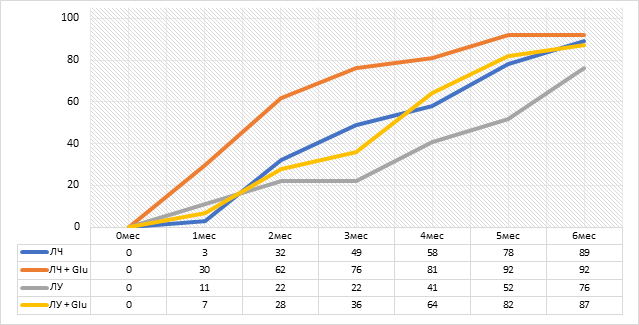
Рис. 2. Абациллирование
Закрытие полостей распада во всех группах проходило медленнее, чем абациллирование, поэтому оценка этого критерия проводилась до 10 месяцев лечения. В результате закрытие полостей распада в группе больных, получавших в схеме лечения глутамил-цистеинил-глицин динатрия, достигнуто в 75/71% случаев с ЛЧ/ЛУ соответственно, а среди пациентов без него 49/48% случаев с ЛЧ/ЛУ соответственно. При этом более значим этот показатель оказался в группе ЛЧ+Glu: через 4 месяца лечения закрытие полостей распада отмечалось на 35% больше, чем в контрольной группе, в то время как аналогичный показатель в группе ЛУ/ЛУ+Glu оказался статистически незначимым на данном этапе оценки результатов. Но в целом за весь период наблюдения (10 месяцев) глутамил-цистеинил-глицин динатрия доказал свою эффективность независимо от наличия лекарственной устойчивости возбудителя (рис. 3).
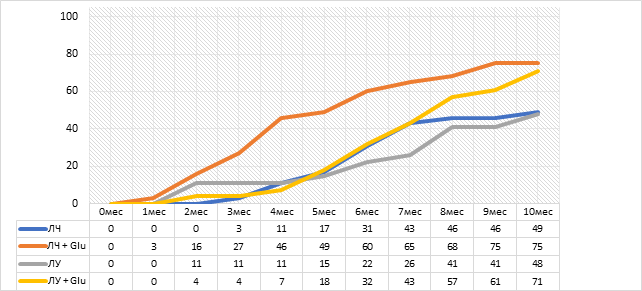
Рис. 3. Закрытие полостей распада
В ходе проведенного анализа ни в одном из случаев применения препарата глутамил-цистеинил-глицин динатрия не отмечено его непереносимости, все пациенты получили его по назначенной схеме.
Статистически значимо улучшаются показатели клинического состояния пациентов. Исчезновение потливости к концу 1-го месяца лечения отмечено быстрее на 30/14% с применением глутамил-цистеинил-глицин динатрия в группах ЛЧ/ЛУ соответственно; ускорилось купирование слабости на 41/26%; нормализация температуры тела происходила быстрее на 35/23%; к 3-му месяцу лечения кашель купирован на 26/22% быстрее, одышка купирована на 28/18% быстрее. Сокращаются сроки нормализации показателей периферической крови. Восстановление уровня гемоглобина быстрее на 17/7%. Нормализация СОЭ быстрее на 26/52%. Нормализация лейкоцитарной формулы также выше до 40% к 6 месяцам лечения. Нормализация показателей АСТ, АЛТ, билирубина ко 2-му месяцу лечения увеличивалась до 48%, отрицательной динамики по всем показателям в этих группах было меньше. Уровень СРБ к 6-му месяцу лечения приходил в норму на 46/52% быстрее с использованием глутамил-цистеинил-глицин динатрия при ЛЧ/ЛУ соответственно. В целом увеличивается % и сроки негативации мокроты, и к 6-му месяцу наблюдения достигают показателей 92% у ЛЧ и 87% у ЛУ пациентов. Сроки закрытия полостей распада сокращаются, через 4 месяца на 35% больше в группе ЛЧ и в целом за период наблюдения до 10 месяцев составляют 75% у пациентов с ЛЧ и 71% у пациентов с ЛУ туберкулезом.
Заключение
Проведенное исследование доказало эффективность включения в комплексное лечение больных туберкулезом легких адъюванта ХТ глутамил-цистеинил-глицина динатрия не только для больных с сохраненной лекарственной чувствительностью возбудителя, но и для резистентных форм туберкулеза легких.
Библиографическая ссылка
Кокорина Н.Н., Проскурякова О.В., Синицын М.В., Виноградова А.С. ЭФФЕКТИВНОСТЬ ПРИМЕНЕНИЯ ГЛУТАМИЛ-ЦИСТЕИНИЛ-ГЛИЦИН ДИНАТРИЯ В ЛЕЧЕНИИ ТУБЕРКУЛЕЗА ЛЕГКИХ С ЛЕКАРСТВЕННОЙ ЧУВСТВИТЕЛЬНОСТЬЮ И УСТОЙЧИВОСТЬЮ ВОЗБУДИТЕЛЯ // Современные проблемы науки и образования. 2025. № 1. ;URL: https://science-education.ru/ru/article/view?id=33952 (дата обращения: 02.05.2026).
DOI: https://doi.org/10.17513/spno.33952



