В процессе поиска веществ, влияющих на ЦНС, важное внимание уделяется целенаправленному синтезу биологически активных соединений (БАС), являющихся агонистами дофаминовых рецепторов. В последнее время, по мере изменения ценза числа пожилых людей в структуре общества, постоянно увеличивается, а болезнь Паркинсона стала настоящей социальной проблемой. На ранних стадиях этой болезни предпочтительно применение агонистов дофаминовых рецепторов, обладающих нейропротекторным действием и способных защищать нейроны от негативного воздействия, а также восстанавливать ранее поврежденные клетки.
В более ранних наших работах было подтверждено нейропротекторное действие ряда производных 4-(3)хиназолинона [4]. По указанной причине значительный интерес вызывает целенаправленный синтез гидрокси- и метоксипроизводных 4-(3)хиназолинона, которые, согласно осуществленному прогнозу, могут обладать дофаминергической активностью.
Материалы и методы.
Прогноз психотропной активности осуществлен с использованием программы PASS (PredictionofActivitySpectraforSubstances). Она позволяет определить вероятность проявления различных фармакологических эффектов прогнозируемыми веществами [6].
Синтез гидрокси- и метоксифенильных производных 4-(3)хиназолинона осуществлялся взаимодействием эквимолекулярных количеств нитрила антраниловой кислоты и соответствующей ароматическойкислоты в среде полифосфорной кислоты (ПФК) в течение 30-40 минут при температуре 100°С.
Противопаркинсоническую активность производных 4-(3)хиназолинона изучали на белых половозрелых крысах-самцах и самках линии Вистар массой 200-250 г (по 9-10 в группах) на модели каталепсии. Каталепсию вызывали введением галоперидола в дозе 1 мг/кг. Исследуемые соединения в дозе 2/10 моль/массы в мг/кг в суспензии с твин-80 (I – 47,6 мг/кг, II – 53,6 мг/кг, III – 53,6 мг/кг, IV – 53,6 мг/кг, V – 56,4 мг/кг), бромокриптин (1,25 мг/кг) вводили внутрибрюшинно одновременно с галоперидолом. Контрольные животные получали один галоперидол в аналогичном режиме. Эксперименты проводили в дневное время.
Животные содержались в стандартных условиях вивария при свободном доступе к воде и пище. Уход, кормление, работа с животными осуществлялись согласно международным рекомендациям о защите позвоночных животных, используемых для экспериментов или в иных научных целях [7].
Определяли выраженность каталепсии путем регистрации (в секундах) длительности удержания животным приданного вертикального положения на опоре («поза лектора»). Оценку выраженности каталепсии (1-й и 2-й результаты – латентный период времени (с), за которое животное убирало, соответственно, одну и вторую лапу) проводили спустя 30, 60, 120, 180 минут после введения солюбилизированных субстанций и раствора препарата сравнения [3]. У самок животных по вагинальным мазкам оценивали стадии эстрального цикла: диэструс ½ и проэструс / эструс [1].
Статистическую обработку результатов проводили, используя стандартные параметрические и непараметрические критерии (t-критерий Стьюдента, критерии Манна–Уитни, Уилкоксона, Крускала-Уоллиса). При проверке данных на нормальность распределения использовался W-критерий Шапиро-Уилка. Проводили относительный сравнительный анализ, сопоставляя опытные данные с контрольными результатами, принятыми за 100%. Для всех видов анализа статистически значимыми считали различия при р<0,05 [2].
Результаты и их обсуждение
Результаты прогноза наиболее перспективных структур, характеризующихся нейропротекторной активностью программой PASS (Pi>50%) приведены в таблице 1.
Таблица 1
Вероятность проявления биологической активности производных
4-(3)хинозолинона
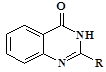
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Из таблицы 1 видно, что все представленные соединения могут проявлять нейропротекторную, бронхолитическую, антиишемической активность и, возможно, являются стимуляторами высвобождения серотонина. В отличие от диметоксипроизводного 4-(3)хиназолинона, содержащие гидроксифенильный фрагмент, могут быть стимуляторами высвобождения дофамина и проявлять кардиопротекторное действие.
Синтез прогнозируемых веществ осуществлялся взаимодействием нитрила антраниловой кислоты с ароматическими альдегидами в среде ПФК по схемеприведенной ниже (рис.1).
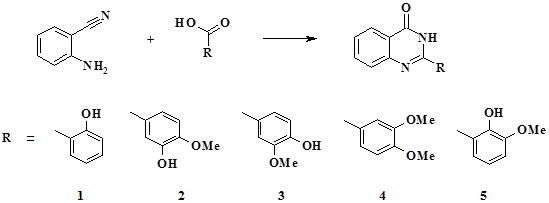
Рис.1. Схема синтеза целевых соединений
Известны немногочисленные подходы к синтезу 2-фенилзамещеных производных хиназолинонов-4, основанные на применении азометиновантраниловой кислоты и ее амида, но все они требуют присутствия окислителя – диацетатаиодозобезола, ацетата меди (II) или даже перманганата калия [5]. Мы предположили, что при взаимодействии нитрила антраниловой кислоты с ароматическими альдегидами в среде ПФК, которая сама проявляет окислительные свойства, приведет к образованию производных 4-(3)хиназолинона в одну стадию.
Необходимо отметить, что успешными оказались лишь синтезы на основе гидрокси- и метоксизамещенных бензойных кислот. Из-за низкой растворимости 2-хлор- и 4-бромбензойных кислот в ПФК реакции с их участием осуществить не удалось.
Образование целевого продукта протекает через стадию формирования промежуточных азометинов. Наибольший выход наблюдается при использовании салициловых альдегидов. Причина, вероятно, заключается в стабилизации плоской структуры интермедиата за счет формирования водородной связи с участием гидрокси-группы и атомаазотав положении 1, и последующим отщеплением молекулы воды. Выходы целевых продуктов варьируют от 30 до 45%. Сравнительно невысокий выход, возможно связан с хорошей растворимостью целевых продуктов в растворе фосфорной кислоты, что само по себе, затрудняет их выделение из реакционной среды.
Анализ результатов фармакологических экспериментов показал, что у самцов все исследованные вещества на 30-й минуте после введения усиливали каталепсию, но сдвиг при этом был статистически значимым для субстанций 15-17, 19 (табл. 2).
Таблица 2
Влияние исследованных производных хиназолинона-4 на каталептогенную активность галоперидола (с) у крыс: самцов и самок (в стадии эстрального цикла проэструс/эструс)
На фоне соединения 15 существенно ослаблялась каталепсия у самок на 120 минуте тестирования. При введении субстанции 16 у самцов только на 180 минуте незначительно ограничивалась интенсивность галоперидоловой каталепсии. Соединение 17 у самцов на 120 минуте после введения ограничивало двигательные нарушения, у самок при этом на 30, 120 и 180 минутах после введения ослаблялась каталепсия, однако сдвиг был статистически значимым на 180 минуте тестирования.
После введения субстанции 18 в сочетании с типичным нейролептиком у самцов на 60 и 180 минуте ограничивалась каталепсия, при этом сдвиг был статистически значим на 60 минуте наблюдения. У самок на 120 и 180 минутах на фоне вещества 18 ослаблялась каталептогенная активность галоперидола, значительнее на 120 минуте эксперимента.
На фоне комбинации галоперидола и субстанции 19 на 60, 120 и 180 минутах после введения ослаблялась выраженность каталепсии, достоверно на 120 и 180 минутах тестирования. У самок на 120 и 180 минутах после введения вещества 19 снижалась интенсивность нейролептической каталепсии, при этом сдвиг на 120 минуте после введения вещества был статистически значимо ниже, чем у самок, получавших один галоперидол, и сопоставим с ослаблением каталепсии у группы самок, получавших галоперидол и препарат сравнения бромокриптин.
Соединения 15, 17-19 оказались интересны в качестве возможных противопаркинсонических средств. Наиболее заметное ослабление галоперидоловой каталепсии отмечалось при использовании веществ 15, 18, 19.
Выводы
Осуществлен прогноз и целенаправленный синтез гидрокси- и метоксифенильных производных 4-(3)хинозолинона, обладающих дофаминергической активностью. Результаты фармакологических исследований в определённой степени подтверждают обоснованность молекулярного конструирования новых агонистов дофаминовых рецепторов.
Работа выполнена в рамках базовой части внутреннего гранта ЮФУ, тема № 213.01-2014/005 на оборудовании ЦКП «Молекулярная спектроскопия»
Рецензенты:
Погребняк А.В., д.х.н., к.фарм.н., профессор кафедры неорганической, физической и коллоидной химии, Пятигорский медико-фармацевтический институт – филиал ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск;
Попова О.И., д.фарм.н., профессор кафедры фармакогнозии, Пятигорский медико-фармацевтический институт – филиал ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск.
Библиографическая ссылка
Овакимян А.Г., Бичеров А.А., Кодониди И.П., Оганесян Э.Т., Манвелян Э.А., Бичеров А.В., Тюрин Р.В., Зайченко С.Б., Манвелян М.М. ПРОГНОЗ, СИНТЕЗ И ИЗУЧЕНИЕ ДОФАМИНЕРГИЧЕСКОЙ АКТИВНОСТИ ГИДРОКСИ- И МЕТОКСИФЕНИЛЬНЫХ ПРОИЗВОДНЫХ 4-(3)ХИНАЗОЛИНОНА // Современные проблемы науки и образования. 2015. № 2-2. ;URL: https://science-education.ru/ru/article/view?id=23168 (дата обращения: 17.05.2026).