Среди новых местных анестетиков амидного ряда видное место занимает мепивакаин, использующийся для инфильтрационной, проводниковой анестезии [2]. Мепивакаин обладает способностью задерживаться в тканях, пролонгируя действие анестезии. При этом отпадает необходимость во введении вазоконстриктора, что делает мепивакаин препаратом выбора для пациентов, страдающих тяжелой сердечно-сосудистой недостаточностью, сахарным диабетом, тиреотоксикозом, бронхиальной астмой и аллергией на препараты, содержащие серу [3].
Однако при определенных условиях (передозировке, индивидуальной непереносимости и т.д.) могут возникать различные осложнения при местном обезболивании [9]. Поэтому для выяснения причины интоксикации лиц, принимавших мепивакаин, решающее значение приобретают результаты химико-токсикологического исследования. В то же время в клинической хирургической практике в ряде случаев возникает потребность в проведении лабораторного анализа препарата в биологических средах.
В литературе наиболее часто встречается информация об использовании в анализе мепивакаина в биологических объектах, прежде всего хроматографических методов (ГЖХ, ВЭЖХ) [8, 9]. Однако в отечественной литературе отсутствуют сведения о применении капиллярного электрофореза (КЭ) для анализа мепивакаина в биологических объектах. Метод КЭ является одним из новых и развивающихся методов разделения сложных смесей, позволяющим анализировать лекарственные средства с высокой эффективностью и экспрессностью, программным обеспечением хода анализа и расчета результатов [5, 7]. КЭ также характеризуется доступностью в приборном отношении (отечественные системы «Капель-105», «Капель-105М» фирмы «Люмекс», г. Санкт-Петербург); малым объемом анализируемой пробы (около 2 мл), отсутствием дорогих и токсичных растворителей.
Важным этапом при количественном определении лекарственных веществ в биологических жидкостях и субстратах (в том числе и моче) методом капиллярного электрофореза являются вопросы пробоподготовки (изолирование из объектов, очистка и концентрирование исследуемых соединений). Наличие в биообъектах различных эндогенных компонентов затрудняет или делает невозможным детектирование искомых соединений в микрограммовых количествах. Кроме того, УФ-спектрофотометрическое детектирование разделенных компонентов происходит непосредственно в кварцевом капилляре, поэтому в определенной степени чувствительность детекции аналита ограничена малой длиной оптического пути, равной внутреннему диаметру капилляра.
При разработке методики количественного определения мепивакаина в моче с использованием капиллярного электрофореза («Капель-105») эти осложняющие проблемы решали тем, что на этапе пробоподготовки для получения в достаточной степени очищенной и сконцентрированной пробы использовали жидкостно-жидкостную экстракцию с последующим реэкстрагированием исследуемого компонента в рабочий электролит, разбавленный водой в 10 раз. При этом перевод исследуемого аналита в рабочий электролит, разбавленный в 10 раз, позволяет в процессе электрофореза в кварцевом капилляре дополнительно осуществить концентрирование пробы за счет явления «стекинга». Данное явление происходит, когда исследуемые ионы аналита пересекают границу, которая разделяет зону низкой проводимости раствора образца и высокой – ведущего электролита. В том случае, если матрица образца имеет значительно более низкую проводимость (обычно за счет разбавления водой), чем ведущий электролит, в зоне образца возникает относительно высокое электрическое поле. Вследствие этого аналит внутри зоны образца движется с более высокой локальной скоростью и, замедляясь на границе с зоной ведущего электролита, концентрируется.
Целью исследования явилось изучение возможности определения мепивакаина в моче капиллярным электрофорезом с использованием отечественной системы для капиллярного электрофореза («Капель-105»).
Материалы и методы исследования
Электрофорез мепивакаина осуществляли с использованием отечественной системы для капиллярного электрофореза («Капель-105»), содержащей кварцевый капилляр с внутренним диаметром 75 мкм, длиной 65 см, встроенный УФ-спектрофотометрический детектор с изменяемой длиной волны от 190 до 380 нм. Запись и обработка данных проводилась с использованием программного обеспечения «Мультихром для Windows» (ЗАО «Амперсенд», Россия).
Условия электрофореза: рабочий электролит (РЭ) — буферный раствор Бриттона—Робинсона (pH 2,3); растворитель пробы (РП) – РЭ, разбавленный в 10 раз водой; ввод пробы — давлением (30 мБар х15 с); положительный электрод со стороны введения РЭ (напряжение: +20 кВ); детектирование в УФ области спектра, 200 нм.
Последовательная промывка капилляра между анализами осуществлялась:
1) по полной схеме (между первым и четвертым анализами): 0,5 М раствором хлористоводородной кислоты – 10 мин, водой очищенной – 10 мин, 0,5 М раствором натрия гидроксида – 10 мин, водой очищенной – 10 мин, РЭ – 10 мин; проведение холостого электрофореза – 15 мин (положительный электрод со стороны введения РЭ, напряжение: +20 кВ);
2) по короткой схеме (между вторым и третьим анализами): РЭ – 10 мин, проведение холостого электрофореза в тех же условиях, как и по полной схеме.
Запись и обработка данных анализа проводилась с помощью программного обеспечения «Мультихром для Windows».
С целью идентификации мепивакаина на электрофореграмме (ЭФГ) нами рассчитано наблюдаемое время миграции в минутах (tm).
Методика количественного определения мепивакаина («Капель-105»)
При количественном определении для подтверждения фактора линейности строили график зависимости фотометрических сигналов (площади пиков) от концентрации мепивакаина на 5 уровнях концентраций его стандартных растворов [1, 4]. Готовили серию стандартного раствора мепивакаина в буферном растворе Бриттона—Робинсона, рН 2,3, разбавленном в 10 раз водой, содержащую от 0,5 до 20 мкг исследуемого анестетика в 1 мл пробы. Электрофоретические исследования полученных стандартных растворов мепивакаина проводили в избранных условиях («Капель-105»). Запись и обработку полученных ЭФГ производили с помощью программного обеспечения «Мультихром для Windows».
Количественное определение мепивакаина в моче
Предварительные исследования по изучению влияния рН среды, природы органического растворителя, кратности экстрагирования на степень экстракции мепивакаина из водных растворов показали, что максимальное количество мепивакаина экстрагируется при трехкратной экстракции хлороформом из щелочной среды (рН 9,0) и соотношением водной и органической фаз 1:1 [6].
Для устранения фонового влияния сопутствующих балластных веществ мочи использовали прием реэкстракции исследуемых компонентов из хлороформных экстрактов в рабочий электролит, разбавленный водой в 10 раз.
Методика. К 1 мл мочи с известным содержанием исследуемого анестетика (модельная смесь) добавляли 25%-ный раствор аммония гидроксида до рН 9,0 (по универсальной индикаторной бумаге) и проводили трехкратную экстракцию хлороформом (1 мл х 3). Эмульсию разрушали центрифугированием (6000 об/мин, 10 мин). Объединенные экстракты упаривали при комнатной температуре в защищенном от света месте. Сухие остатки растворяли в 0,5 мл хлороформа и проводили реэкстракцию 1 мл РП (шейкер, 10 мин). Смесь центрифугировали (6000 об/мин, 10 мин); реэкстракт отделяли, переносили в пробирку типа «эппендорф», осуществляли дегазацию центрифугированием в мини-центрифуге («MiniSpin plus», 10000 об/мин, 5 мин) и использовали для количественного определения мепивакаина по разработанной электрофоретической методике.
Результаты исследования и их обсуждение
Результаты по разработке электрофоретической методики мепивакаина («Капель-105»), представленные в таблице 1, показали, что линейная зависимость фотометрического сигнала от концентрации мепивакаина (от 0,5 до 20 мкг/мл) аппроксимирована линейным уравнением с помощью метода наименьших квадратов, имеющим вид: y = 0,9431x – 0,0338.
Таблица 1
Зависимость фотометрического сигнала от концентрации мепивакаина
(«Капель – 105»)
|
№ п/п |
мепивакаин, мкг/мл |
Фотометрический сигнал |
|||
|
mAU×сек1 |
mAU×сек2 |
mAU×сек3 |
mAU×секср |
||
|
1. |
0,5 |
0,563 |
0,568 |
0,581 |
0,570 |
|
2. |
1 |
0,968 |
0,978 |
0,969 |
0,971 |
|
3. |
5 |
4,796 |
4,716 |
4,716 |
4,743 |
|
4. |
10 |
8,971 |
9,285 |
8,723 |
8,993 |
|
5. |
15 |
13,918 |
13,918 |
14,128 |
13,988 |
|
6. |
20 |
19,125 |
19,034 |
19,150 |
19,103 |
Критерием приемлемости является коэффициент корреляции (r2), который составил 0,9990. Его величина близка к 1, и совокупность данных можно описать прямой линией (рис. 1).
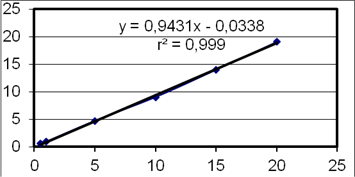
Рис. 1. Калибровочный график для количественного определения мепивакаина методом капиллярного электрофореза («Капель-105»)
Это свидетельствует о том, что электрофоретическая методика валидна по критерию линейности и в данном диапазоне концентраций обеспечивает определение с требуемой правильностью.
Результаты определения мепивакаина в моче представлены в таблице 2.
Таблица 2
Количественное определение мепивакаина в моче методом капиллярного электрофореза («Капель-105»)
|
№ п/п |
Концентрация мепивакаина в моче, мкг/мл |
Определено мепивакаина |
Метрологические характеристики |
|
|
мкг/мл |
% |
|||
|
1. |
20,0 |
13,15 |
65,75 |
S = 0,25
S
[ CV% = 0,38
|
|
2. |
20,0 |
13,02 |
65,10 |
|
|
3. |
20,0 |
13,04 |
65,20 |
|
|
4. |
20,0 |
13,08 |
65,40 |
|
|
5. |
20,0 |
13,10 |
65,50 |
|
|
6. |
контрольный опыт |
- |
- |
|
|
7. |
1,0 |
0,3829 |
38,29 |
S = 1,32
S
[ CV% = 3,56%
|
|
8. |
1,0 |
0,3696 |
36,96 |
|
|
9. |
1,0 |
0,3696 |
36,96 |
|
|
10. |
1,0 |
0,3829 |
38,29 |
|
|
11. |
1,0 |
0,3507 |
35,07 |
|
|
12. |
контрольный опыт |
- |
- |
|
|
13. |
0,5 |
0,2121 |
42,42 |
S = 1,90
S
[ CV% = 4,63
|
|
14. |
0,5 |
0,1913 |
38,26 |
|
|
15. |
0,5 |
0,2074 |
41,48 |
|
|
16. |
0,5 |
0,2159 |
43,18 |
|
|
17. |
0,5 |
0,2027 |
40,54 |
|
|
18. |
контрольный опыт |
- |
- |
|
Как видно из таблицы, при статистической обработке данных, полученных в ходе количественного определения мепивакаина в модельных пробах мочи на трех уровнях концентраций, отражается вполне удовлетворительная сходимость результатов в пределах рекомендуемой аналитической области. Рассчитанное стандартное отклонение среднего результата находится в пределах критерия приемлемости. Методика не отягощена грубой и систематической ошибкой, является правильной и позволяет получать воспроизводимые результаты. Граница определения составила 0,5 мкг, граница обнаружения – 0,1 мкг вещества в 1 мл мочи. При этом условия пробоподготовки биологической жидкости позволяют устранить влияние балластных веществ и эффективно осуществить УФ-спектрофотометрическую детекцию (рис. 2).
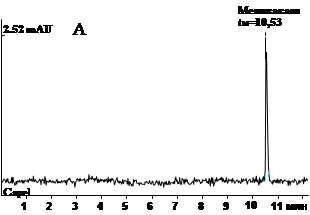

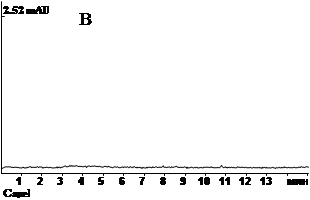
Рис. 2. ЭФГ: А — мепивакаин, выделенный из мочи (1 мкг/мл); Б – мепивакаин-стандарт в РП (1 мкг/мл); В – после пробоподготовки контрольного образца мочи, 1 мл (blank); («Капель-105»)
Заключение
Таким образом, разработанная электрофоретическая методика применима для количественного определения мепивакаина в моче и может быть рекомендована для использования при химико-токсикологических анализах с использованием отечественной эффективной системы для капиллярного электрофореза («Капель-105»).
Рецензенты:
Фурса Н.С., д.фарм.н., профессор, заведующий кафедрой фармакогнозии и фармацевтической технологии ГБОУ ВПО «Ярославский государственный медицинский университет» Минздрава России, г. Ярославль;
Ярыгина Т.И., д.фарм.н., профессор, профессор кафедры фармацевтической химии ФОО ГБОУ ВПО «Пермская государственная фармацевтическая академия» МЗ РФ, г. Пермь.
Библиографическая ссылка
Фомин А.Н., Мерзлякова Ю.А., Смирнова А.В., Алтухова В.В. РАЗРАБОТКА МЕТОДИКИ ОПРЕДЕЛЕНИЯ МЕПИВАКАИНА В МОЧЕ КАПИЛЛЯРНЫМ ЭЛЕКТРОФОРЕЗОМ // Современные проблемы науки и образования. 2015. № 2-2. ;URL: https://science-education.ru/ru/article/view?id=21939 (дата обращения: 18.04.2026).



