Введение
Производные гетероциклических систем, содержащие в качестве заместителей два ароматических остатка, связанные коротким мостиком, известны как соединения, обладающие широким спектром биологической активности [4; 5]. Особое значение имеют соединения, содержащие диарильный фрагмент, связанный линкером с атомом азота в гетероцикле, известные как мощные противовирусные агенты [2; 6]. Однако фармакологический потенциал и подходы к химическому синтезу соединений, содержащих диарильный фрагмент у атома углерода гетероциклического ядра, остаются малоизученными.
Цель исследования
Разработка методов синтеза производных урацила и пиридин-4(3H)-она, содержащих два ароматических остатка, связанных между собой и с положением 6 гетероцикла короткими мостиками.
Материалы и методы исследования
В работе использовались коммерчески доступные растворители и реактивы (Sigma-Aldrich, Merck, Acros Organics).
Спектры ЯМР 1H- и 13С-регистрировали на спектрометре Bruker Avance-400 (400 МГц для 1H-, 100 МГц для 13С) в ДМСО-D6, внутренний стандарт тетраметилсилан (ТМС). Интерпретацию спектров осуществляли с помощью лицензионной программы ACD/HNMR Predictor Pro 3.0 фирмы Advanced Chemistry Development (Канада). Тонкослойную хроматографию выполняли на пластинах Merck TLC Silica gel 60 F254, проявление в УФ-свете с помощью УФ-лампы VL-6.LC (Франция). Температуры плавления измерены в стеклянных капиллярах на приборе Mel-Temp 3.0 (Laboratory Devices Inc., США).
Результаты и их обсуждение
С целью получения структур, содержащих диарильный фрагмент у атома C6 гетероциклического ядра, были проведены конденсации производных 4-[(3-феноксибензил)окси]ацетоуксусного эфира и 4-(дифенилметокси)ацетоуксусного эфира с тиомочевиной, а также солевыми формами S-метилизотиомочевины и гуанидина. Общая схема проведённых реакций представлена на рисунке 1.
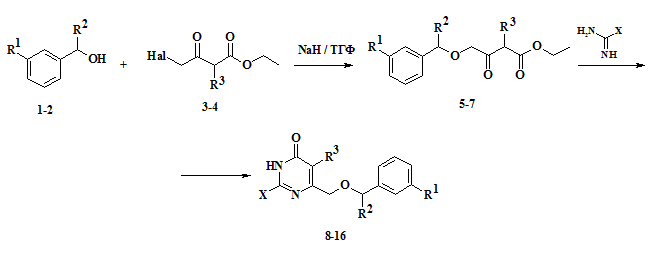
X = SH, SCH3, OH, NH2; R1 = H, PhO; R2 = H, Ph; R3 = H, CH3
Рисунок 1 – Схема синтеза диарильных производных пиримидин-4(3H)-она
Производные этил-4-(бензилокси)-3-оксобутаноата 5-7 были синтезированы путём взаимодействия 3-феноксибензилового спирта (1) и бензгидрола (2) с галогенпроизводными ацетоуксусного эфира 3-4 в присутствии натрия гидрида в среде безводного тетрагидрофурана по известной методике [10]. Этил-4-бром-2-метил-3-оксобутаноат (4) был получен путём бромирования этил-2-метил-3-оксобутаноата молекулярным бромом в среде безводного тетрахлорметана [9].
Продукты конденсации полученных кетоэфиров с 2-кратным избытком тиомочевины в среде метанола в присутствии метилата натрия образовывались с выходами 52-67%.
Циклизация сульфата S-метилизотиурония с этил-3-оксо-4-[(3-феноксибензил)окси]бутаноатом (5) проводилась в присутствии карбоната калия в водно-этанольной среде в течение 48 часов. Выход целевого продукта 11 составил 75% [7].
Конденсация диарилсодержащих кетоэфиров с применением четырёхкратного мольного избытка метилата натрия и двухкратного избытка гуанидина ацетата [1] привела к получению целевых продуктов 12-14 с выходами 56-71%.
Десульфурирование 2-тио-6-{[(3-феноксибензил)окси]метил}урацила (8) проводилось путём кипячения с 10%-ным водным раствором монохлоруксусной кислоты (МХУК) при мольном соотношении тиоурацила и кислоты 1:3 [3]. Однако было обнаружено, что процесс в данных условиях протекает крайне медленно (>48 часов) в связи с низкой растворимостью субстрата и промежуточных продуктов его взаимодействия с МХУК (S-карбоксиметилпроизводного тиоурацила и соответствующего илида) даже при длительном кипячении. Использование в качестве сорастворителя ДМФА позволило сократить время реакции до 16 часов (контроль по ТСХ). Выход продукта 15 составил 73%.
Галогенирование 6-{[(3-феноксибензил)окси]метил}урацила (15) проводилось путём обработки раствором брома в безводном ДМФА в присутствии пиридина в качестве акцептора бромоводорода при температуре 60 °С [8]. Выход продукта бромирования 16 составил 39%, что может быть связано со стерическим влиянием диарилэфирного радикала.
Физико-химические свойства и выходы целевых продуктов представлены в таблице 1.
Таблица 1 – Физико-химические данные диарильных производных пиримидин-4(3H)-она
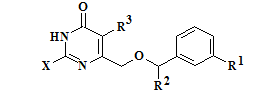
|
Соед. |
X |
R1 |
R2 |
R3 |
Выход, % |
Тпл, °С |
Rf (система)* |
|
8 |
SH |
PhO |
H |
H |
67 |
163-164 |
0,51 (A) |
|
9 |
SH |
PhO |
H |
CH3 |
55 |
150-151 |
0,58 (A) |
|
10 |
SH |
H |
Ph |
H |
52 |
202-204 |
0,65 (A) |
|
11 |
SCH3 |
PhO |
H |
H |
75 |
137-138 |
0,57 (A) |
|
12 |
NH2 |
PhO |
H |
H |
71 |
203,5-204,5 |
0,40 (B) |
|
13 |
NH2 |
PhO |
H |
CH3 |
68 |
213-215 |
0,43 (B) |
|
14 |
NH2 |
H |
Ph |
H |
56 |
218,5-220,5 |
0,50 (B) |
|
15 |
OH |
PhO |
H |
H |
73 |
180-183 |
0,39 (C) |
|
16 |
OH |
PhO |
H |
Br |
39 |
182-183 |
0,72 (C) |
* A – толуол-ацетон 2:1, B – хлороформ-этанол 8:1, C – этилацетат.
Экспериментальная химическая часть
2-Тио-6-{[(3-феноксибензил)окси]метил}урацил (8). К 30 мл абсолютного метанола добавляли 1,15 г (50,00 ммоль) металлического натрия. После полного растворения натрия к полученному раствору метилата натрия в абсолютном метаноле добавляли 3,04 г (40,00 ммоль) тиомочевины и раствор 6,57 г (20,00 ммоль) этил 3-оксо-4-[(3-феноксибензил)окси]бутаноата (5) в 10 мл абсолютного метанола. Полученную смесь нагревали с обратным холодильником с защитой от влаги воздуха в течение 20 часов. Затем реакционную смесь концентрировали в вакууме, к остатку прибавили 50 мл воды и подкислили 0,1 М уксусной кислотой до pH = 5,0, после чего поместили в холодильник на ночь. Выпавший осадок отфильтровали, промыли водой, сушили на воздухе и перекристаллизовали из 35 мл ледяной уксусной кислоты. Получили 4,56 г (выход 67%) продукта в виде светло-жёлтого кристаллического вещества. Rf = 0,51 (толуол-ацетон 2:1). Тпл = 163-164 °С. 1Н ЯМР-спектр (ДМСО-D6, 400 МГц), δ, м.д., J (Гц): 4,27 с (2H, CH2-С6); 4,56 c (2H, CH2 CH2-C1'); 5,81 с (1H, H-5); 6,93-6,95 дд (1H, J = 8,1 и 1,8, H-4'); 6,98-7,05 м (3H, H-2', H-2'', H-6''); 7,09-7,18 м (2H, H-6', H-4''); 7,33-7,44 м (3H, H-5', H-3'', H-5''); 12,30 c (1H, N1-H); 12,41 c (1H, N3-H). 13C ЯМР-спектр (ДМСО-D6, 100 МГц), δ, м.д.: 66,3; 71,8; 102,2; 117,5; 117,8; 118,8; 122,5; 123,6; 130,1; 130,1; 139,9; 153,1; 156,5; 156,8; 161,0; 176,0.
Соединения 9-10 были получены аналогично из соответствующих кетоэфиров.
5-Метил-6-{[(3-феноксибензил)окси]метил}-2-тиоурацил (9). Выход 55%. Rf = 0,58 (толуол-ацетон 2:1). Тпл = 150-151 °С. 1Н ЯМР-спектр (ДМСО-D6, 400 МГц), δ, м.д., J (Гц): 1,77 с (3H, CH3); 4,32 с (2H, CH2-С6); 4,51 c (2H, CH2-С1'); 6,92-6,93 м (1H, H-4'); 6,99-7,00 м (3H, H-2', H-2'', H-6''); 7,10-7,14 м (2H, H-6', H-4''); 7,34-7,39 м (3H, H-5', H-3'', H-5''); 12,05 c (1H, N1-H); 12,39 c (1H, N3-H). 13C ЯМР-спектр (ДМСО-D6, 100 МГц), δ, м.д.: 13,6; 69,5; 75,9; 117,1; 121,76; 122,0; 123,0; 126,9; 127,8; 134,1; 134,3; 144,2; 150,4; 160,7; 161,0; 166,2; 178,2.
2-Тио-6-[(дифенилметокси)метил]урацил (10). Выход 52%. Rf = 0,65 (толуол-ацетон 2:1). Тпл = 202-204 °С. 1Н ЯМР-спектр (ДМСО-D6, 400 МГц), δ, м.д., J (Гц): 4,23 c (2H, CH2); 5,60 c (1H, CH); 5,85 с (1H, H-5); 7,25-7,41 м (10 H, ароматические H); 12,25 c (1H, NH); 12,39 c (1H, NH). 13C ЯМР-спектр (ДМСО-D6, 100 МГц), δ, м.д.: 64,9; 82,7; 101,9; 126,6; 127,6; 128,5; 141,7; 153,3; 161,0; 176,0.
2-(Метилсульфанил)-6-{[(3-феноксибензил)окси]метил}пиримидин-4(3H)-он (11). К смеси 15 мл воды и 15 мл этанола добавили 2,70 г (8,22 ммоль) этил-3-оксо-4-[(3-феноксибензил)окси]бутаноата (5), 3,10 г (16,44 ммоль) сульфата S-метилизотиурония и 4,54 г (32,88 ммоль) калия карбоната. Полученную смесь перемешивали при комнатной температуре в течение 48 часов, после чего осторожно подкислили соляной кислотой до pH = 6,0, выпавший осадок отфильтровали, сушили на воздухе и перекристаллизовали из 30 мл этанола. Получили 2,18 г (выход 75%) продукта в виде белого кристаллического вещества. Rf = 0,57 (толуол-ацетон 2:1). Тпл = 137-138 °С. 1Н ЯМР-спектр (ДМСО-D6, 400 МГц), δ, м.д., J (Гц): 2,43 с (3H, CH3); 4,31 c (2H, CH2-С6); 4,58 c (2H, CH2-С1'); 6,07 с (1H, H-5); 6,91-6,93 дд (1H, J = 8,1 и 2,3, H-4'); 7,00-7,01 м (3H, H-2', H-2'', H-6''); 7,11-7,14 м (2H, H-6', H-4''); 7,35-7,39 м (3H, H-5', H-3'', H-5''). 13C ЯМР-спектр (ДМСО-D6, 100 МГц), δ, м.д.: 17,0; 75,0; 75,7; 121,4; 121,9; 122,9; 126,5; 127,8; 134,2; 134,3; 144,5; 160,7; 161,0.
6-{[(3-феноксибензил)окси]метил}изоцитозин (12). К 30 мл абсолютного метанола добавляли 0,92 г (40,00 ммоль) металлического натрия. После полного растворения натрия к полученному раствору метилата натрия в абсолютном метаноле добавляли 2,39 г (20,00 ммоль) гуанидина ацетата и раствор 3,30 г (10,00 ммоль) этил-3-оксо-4-[(3-феноксибензил)окси]бутаноата (5) в 10 мл абсолютного метанола. Полученную смесь нагревали с обратным холодильником с защитой от влаги воздуха в течение 30 часов. Затем реакционную смесь концентрировали в вакууме, к остатку прибавили 50 мл воды и подкислили 0,1 М уксусной кислотой до pH = 5,0, после чего поместили в холодильник на ночь. Выпавший осадок отфильтровали, промыли водой, сушили на воздухе и перекристаллизовали из смеси 15 мл этанола и 10 мл ДМФА. Получили 2,30 г (выход 71%) продукта в виде мелких лимонно-жёлтых кристаллов. Rf = 0,40 (хлороформ-этанол 8:1). Тпл = 203,5-204,5 °С. 1Н ЯМР-спектр (ДМСО-D6, 400 МГц), δ, м.д., J (Гц): 4,16 с (2H, CH2-С6); 4,54 c (2H, CH2-С1'); 5,60 c (1H, H-5); 6,54 уш.с (2H, NH2); 6,91-6,93 дд (1H, J = 8,0 и 1,6, H-4'); 6,99-7,02 м (3H, H-2', H-2'', H-6''); 7,11-7,15 м (2H, H-6', H-4''); 7,37 к (3H, J = 7,5, H-5', H-3'', H-5''); 10,76 уш. с (1H, NH). 13C ЯМР-спектр (ДМСО-D6, 100 МГц), δ, м.д.: 71,4; 97,7; 117,2; 117,6; 118,8; 122,3; 123,6; 130,0; 130,1; 140,5; 148,5; 149,3; 155,8; 156,6; 156,8.
Соединения 13 и 14 были получены аналогично из гуанидина ацетата и соответствующих кетоэфиров.
5-Метил-6-{[(3-феноксибензил)окси]метил}изоцитозин (13). Выход 68%. Rf = 0,43 (хлороформ-этанол 8:1). Тпл = 213-215 °С. 1Н ЯМР-спектр (ДМСО-D6, 400 МГц), δ, м.д., J (Гц): 1,80 с (3H, CH3); 4,25 с (2H, CH2-С6); 4,50 c (2H, CH2-С1'); 6,32 уш. с. (2H, NH2); 6,90-6,92 дд (1H, J = 8,1 и 1,9, H-4'); 6,97 с (1H, H-2'); 6,99-7,00 д (2H, J = 7,9, H-2'', H-6''); 7,09-7,14 м (2H, H-6', H-4''); 7,33-7,39 м (3H, H-5', H-3'', H-5''). 13C ЯМР-спектр (ДМСО-D6, 100 МГц), δ, м.д.: 13,7; 75,6; 112,9; 121,7; 121,8; 122,9; 126,7; 127,7; 134,0; 134,2; 144,8; 157,7; 160,9; 161,1.
6-[(Дифенилметокси)метил]изоцитозин (14). Выход 56%. Rf = 0,50 (хлороформ-этанол 8:1). Тпл = 218,5-220,5 °С. 1Н ЯМР-спектр (ДМСО-D6, 400 МГц), δ, м.д., J (Гц): 4,10 с (2H, CH2); 5,56 c (1H, H-5); 5,73 c (1H, CH); 6,53 уш. с. (2H, NH2); 7,23-7,41 м (10H, ароматические H); 10,77 уш. с. (1H, NH). 13C ЯМР-спектр (ДМСО-D6, 100 МГц), δ, м.д.: 69,6; 82,3; 97,7; 126,5; 127,5; 128,5; 142,2; 155,7; 163,0; 166,5.
6-{[(3-феноксибензил)окси]метил}урацил (15). К 2,55 г (27,00 ммоль) монохлоруксусной кислоты добавляли 60 мл воды и 20 мл ДМФА. После полного растворения кислоты добавляли 3,08 г (9,00 ммоль) 2-тио-6-{[(3-феноксибензил)окси]метил}урацила (8). Полученную смесь нагревали до кипения с обратным холодильником в течение 16 часов. Образовавшийся осадок отфильтровали, обильно промывая на фильтре водой, сушили на воздухе и перекристаллизовали из смеси 10 мл этанола и 5 мл ДМФА. Получили 2,13 г (выход 73%) продукта. Rf = 0,39 (этилацетат). Тпл = 180-183 °С. 1Н ЯМР-спектр (ДМСО-D6, 400 МГц), δ, м.д., J (Гц): 4,21 с (2H, CH2-С6); 4,54 c (2H, CH2-С1'); 5,48 c (1H, H-5); 6,92-6,94 дд (1H, J = 8,1 и 1,7, H-4'); 6,98-7,06 м (3H, H-2', H-2'', H-6''); 7,09-7,20 м (2H, H-6', H-4''); 7,31-7,44 м (3H, H-5', H-3'', H-5''); 10,83 c (1H, N1-H); 10,94 c (1H, N3-H). 13C ЯМР-спектр (ДМСО-D6, 100 МГц), δ, м.д.: 66,8; 71,7; 97,5; 117,6; 117,8; 118,7; 122,5; 123,6; 130,0; 130,1; 140,0; 151,5; 152,7; 156,6; 156,8; 164,1.
5-Бром-6-{[(3-феноксибензил)окси]метил}урацил (16). В плоскодонную колбу объёмом 250 мл помещали 30 мл безводного ДМФА, 2,60 г (8,00 ммоль) 6-{[(3-феноксибензил)окси]метил}урацила (15) и 0,64 мл (8,00 ммоль) пиридина, предварительно перегнанного над гидроксидом калия. К полученной смеси по каплям при перемешивании добавляли раствор 0,41 мл (8,00 ммоль) брома в 20 мл безводного ДМФА в течение 1 часа. Смесь перемешивали в течение дополнительных 4 часов при 60 °С, после чего добавили 50 мл воды. Полученный осадок отфильтровали, промыли на фильтре водой и перекристаллизовали из смеси 20 мл ДМФА и 10 мл воды. Получили 1,26 г (выход 39%) продукта в виде белого мелкокристаллического вещества. Rf = 0,72 (этилацетат). Тпл = 182-183 °С. 1Н ЯМР-спектр (ДМСО-D6, 400 МГц), δ, м.д., J (Гц): 4,41 с (2H, CH2-С6); 4,55 c (2H, CH2-С1'); 6,93-6,94 дд (1H, J = 8,0 и 1,7 , H-4'); 6,99-7,00 д (2H, J = 7,7, H-2'', H-6''); 7,05 c (1H, H-2'); 7,11-7,15 м (2H, H-6', H-4''); 7,34-7,39 ддд (3H, H-5', H-3'', H-5''); 11,19 c (1H, N1-H); 11,51 c (1H, N3-H). 13C ЯМР-спектр (ДМСО-D6, 100 МГц), δ, м.д.: 71,7; 76,1; 99,9; 122,0; 122,2; 122,9; 127,0; 127,7; 134,3; 144,0; 153,6; 154,4; 160,8; 160,9; 164,3.
Выводы
В ходе проведённой работы осуществлён синтез 9 новых производных пиримидин-4(3H)-она, содержащих диарильный фрагмент, связанный коротким мостиком с положением 6 гетероцикла. Показано, что на выход продуктов оказывает влияние строение диароматического радикала. Полученные соединения представляют интерес как потенциальные противовирусные агенты.
Рецензенты:
Симонян А.В., д.фарм.н., профессор кафедры фармацевтической технологии и биотехнологии Волгоградского государственного медицинского университета, г. Волгоград.
Ганичева Л.М., д.фарм.н., доцент кафедры управления и экономики фармации, медицинского и фармацевтического товароведения Волгоградского государственного медицинского университета, г. Волгоград.
Библиографическая ссылка
Гейсман А.Н., Озеров А.А., Новиков М.С. СИНТЕЗ 6-ДИАРИЛЗАМЕЩЁННЫХ ПРОИЗВОДНЫХ ПИРИМИДИН-4(3H)-ОНА // Современные проблемы науки и образования. 2013. № 6. ;URL: https://science-education.ru/ru/article/view?id=11062 (дата обращения: 02.06.2026).



