Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
EFFECTS OF ACIDIC AMINO ACIDS AND THEIR MIXTURES ON THE WATER COMPONENT IN THEIR TEST SOLUTIONS.
Введение
Аминокислоты относятся к классу органических амфолитов, их молекулы содержат одновременно карбоксильные и аминогруппы. Специфичность каждой аминокислоты определяется строением углеводородного радикала. В частности, глутаминовая кислота является основным возбуждающим нейромедиатором центральной нервной системы. Глутаматэргическая передача опосредована ионотропными глутаматными рецепторами. Глутамат может оказывать эффекты через метаботропные G-белки глутаматного рецептора. Дисфункция данной системы вовлечена в патологию многих заболеваний ЦНС: шизофрения, наркомания, болезнь Паркинсона, болезнь Альцгеймера [10]. Доказано, что аспарагиновая кислота играет важную роль на начальных стадиях развития нервной системы у позвоночных и беспозвоночных. Она в больших количествах вырабатывается в мозге в период эмбрионального развития, а впоследствии ее уровень падает до ничтожных и остаются такими всю жизнь. Получены свидетельства того, что молекулы данной аминокислоты участвуют в процессах обучения и работы памяти у крыс и повышают умственные способности животных. Другими словами, аминокислоты влияют на функциональную активность клетки, свойства биологических мембран отдельных органов и их систем, при этом могут вызвать соответствующие изменения структурного состояния водного компонента биологической системы.
Существуют литературные данные, посвященные изучению влияния аминокислот на структуру воды [9]. Авторы работы [9] используют произведение Уальдена (произведение величины вязкости и проводимости при бесконечном разбавлении раствора) для оценки влияния аминокислот на структуру водной среды. В них показано, что большинство аминокислот обладают умеренной способностью разрушать структуру водных сред, в то время как L-аспарагиновая и L-глутаминовая кислоты проявляют высокую активность в отношении воды. Представляло интерес изучить влияние глутаминовой и аспарагиновой кислот на структурное состояние воды в их водных растворах с использованием ИК- спектроскопии.
Цель работы
Выявить специфику воздействия аспарагиновой, глутаминовой кислот и их смеси на структурное состояние воды в модельных растворах.
Материалы и методы исследования
В качестве исследуемых жидкостей использовали дважды перегнанную деионизованную воду, 1N растворы глутаминовой (Глу) (49449 Sigma, SID 24872908) и аспарагиновой кислот ( A8949 Sigma, SID 24891385).
Для исследования нами применялись аппаратно-программый комплекс «Икар» и ИК- спектрометр с Фурье преобразованием Nicolet IS10.
Анализируемые образцы готовили непосредственно перед снятием спектра в кварцевой посуде, быстрым последовательным десятикратным разбавлением исходных растворов от 101 до 1016 раз. Для проведения спектрометрии использовался аппаратно-программный комплекс «ИКАР», разработанный сотрудниками ТГМА совместно с НИИ-2 МО РФ, представляющий собой девятизональный спектроанализатор. Спектрометр сертифицирован как новый тип измерителя (сертификат № 5745 от 20.11.98г.), который позволяет регистрировать показатели пропускания ИК-излучения после их многократного определения в девяти широких диапазонах в слоях жидкости толщиной 15 мк в кюветах из хлористо-бромистого и йодисто-бромистого таллия (KRS). В процессе анализа в кювету аппаратной части системы помещали 20 мкл полученного раствора и проводили многократные измерения коэффициентов пропускания в течение 30 с [2,3]. За один цикл осуществляли около 300 измерений коэффициентов пропускания и в каждом из девяти диапазонов частот рассчитывали значения дисперсий, характеризующих флуктуацию инфракрасного спектра [6]. Полученные результаты обрабатывались методом линейного дискриминантного анализа в вычислительной среде интегрированной системы расчетов MATLAB (лицензия №1462295). Предварительно было отмечено, что в каждом интервале длин волн наблюдалось нормальное распределение величин флуктуаций. Это дало возможность количественно охарактеризовать состояния воды в присутствии сверхмалых количеств исследуемых веществ по сравнению с эталоном (бидистиллированная вода) с помощью критерия Махаланобиса, учитывающего корреляционные связи между коэффициентами пропускания и их дисперсиями [5]. В результате по величине отношений критерия "эталон – раствор" определяется близость (принадлежность) спектральной характеристики раствора к эталону.
Преобразование Фурье осуществляли с помощью Nicolet IS10 на компьютере в программной среде OMNIC.
Результаты и их обсуждение
На первом этапе работы нами была проведена ИК-спектрометрия с Фурье преобразованием водных 1М растворов глутаминовой и аспарагиновой кислот. Результаты спектрографии представлены на рис.1.
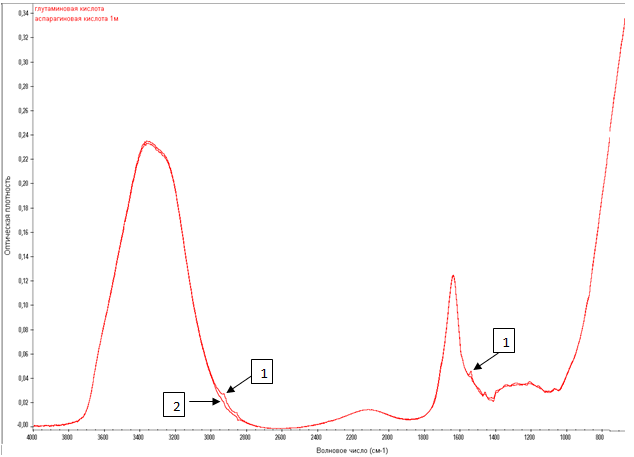
Рис. 1. Огибающие ИК-спектров водных 1N водных растворов глутаминовой кислоты (1), аспарагиновой кислоты (2)
Все изучаемые растворы имеют интенсивную полосу поглощения в области 3000–3600 см-1, характеризующую валентные колебания гидроксильной группы воды [1,4]. В ИК-спектрах водных растворов исследуемых веществ проявляются пики в области около 3100-3150 см-1, что свидетельствует об увеличении энергетики водородной связи и структурировании воды. Установлено уширение полосы поглощения 3440-3220 см-1 и смещение в коротковолновую область спектра. Данное явление объясняется образованием ассоциатов «вода…вода» при участии трех водородных связей в структуре аминокислоты [8]. В водном растворе глутаминовой кислоты наблюдается появление спектральных пиков при волновом числе 2800-2200см-1, что свидетельствует о проявлении взаимодействия ОН-групп воды с аминогруппами. При длине волны 1620см-1 наблюдаются характерные для деформационных колебаний воды пики, не отличающиеся по интенсивности для исследуемых растворов. Таким образом, можно говорить о сходном воздействии данных веществ на водную основу их растворов.
На следующем этапе работы было проведено исследование водного раствора глутаминовой и аспарагиновой кислот, полученного путем смешивания равных количеств 1N растворов исследуемых аминокислот.
В ИК-спектре этой смеси наблюдается наложение спектральных полос исследуемых аминокислот, при этом в спектре не происходило исчезновения полос поглощения, отвечающих одному из компонентов, как и не образовывалось новых спектральных полос, которые характеризовали бы образование новой связи, что говорит об отсутствии химических реакций взаимодействия данных веществ.
Анализ разведенных образцов аминокислот проводили с использованием АПК «ИКАР». Полученные данные показателей пропускания и их дисперсий обрабатывали методами многомерного анализа с вычислением критерия Махаланобиса.
Установлено (рис. 2), что для глутаминовой кислоты анализируемый показатель изменяется волнообразно с достижением максимальных значений при разведении в 109. Разведения раствора аспарагина приводят к постепенному снижению критерия Махаланобиса, для которой минимальное значение исследуемой величины определено при максимальном разведении. Для данных аминокислот установлено, что сходные количественные содержания кислот вызывают однонаправленное изменение структурного состояния водной основы растворов, что подтверждается величинами критерия Махаланобиса. Можно предположить, что в этом случае регистрируется неустойчивое состояние водной основы, которое, согласно литературным данным, возникает в тонких слоях жидкостей [7].
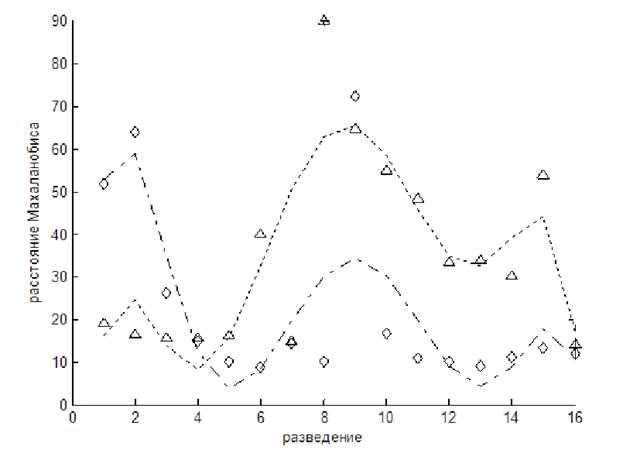
Рис. 2. Графики зависимости и их полиномиальные аппроксимаии расстояния Махаланобиса от разведения (условные обозначения: ![]() и ------ значения и аппроксимационная кривая для глутаминовой кислоты;
и ------ значения и аппроксимационная кривая для глутаминовой кислоты; ![]() и -.-.-.- значения и аппроксимационная кривая для аспарагиновой кислоты)
и -.-.-.- значения и аппроксимационная кривая для аспарагиновой кислоты)
Выводы
Анализ спектральных линий смешанного водного раствора глутаминовой и аспарагиновой кислот подтверждает отсутствие изменения числа частиц за счет взаимодействия исследуемых веществ.
Установлен общий характер изменения структурного состояния водного компонента для кислых аминокислот, при этом для аспарагиновой кислоты это воздействие более выражено. Вероятно, данное явление связано с процессами образования и распада гигантских кластеров, определяющих жидкокристаллическое состояние водных систем.
Рецензенты:
Лапина Галина Петровна, доктор химических наук, профессор, заведующая кафедрой физико-химической экспертизы биоорганических соединений ФГБОУ ВПО «Тверской государственный университет», г. Тверь.
Слюсарь Николай Николаевич, доктор медицинских наук, профессор, профессор кафедры химии и биохимии ГБОУ ВПО Тверская ГМА Минздрава России, г. Тверь.
Библиографическая ссылка
Бутавин Н.Ю., Зубарева Г.М., Волкова Л.Р. ВЛИЯНИЕ КИСЛЫХ АМИНОКИСЛОТ И ИХ СМЕСИ НА ВОДНЫЙ КОМПОНЕНТ МОДЕЛЬНЫХ РАСТВОРОВ. // Современные проблемы науки и образования. 2013. № 3. ;URL: https://science-education.ru/en/article/view?id=9204 (дата обращения: 16.05.2026).



