В основе газофазного способа получения нитрида алюминия лежит взаимодействие субфторида алюминия с азотом [6]. Субфторид алюминия получается за счет взаимодействия трифторида алюминия с металлическим алюминием. Если механизм образования субфторида изучен достаточно подробно и реализуется при получении особо чистого алюминия [3], то процесс газофазного синтеза AlN, состоящий из нескольких стадий, где имеют место побочные реакции с участием жидких, газообразных и твердых фаз, требует дополнительного изучения.
Нельзя также исключать влияния футеровочного материала реакционной камеры на характер высокотемпературных превращений и свойства конечного продукта, нитрида алюминия.
Термодинамический анализ процессов в системе Al-F-N позволяет сделать выводы о возможности прохождения реакций:
AlF3(газ)+2Al(ж)=3AlF(газ) (1)
2Al(ж)+N2(газ)=2AlN(тв) (2)
3AlF(газ)+ N2(газ)=2AlN(тв)+AlF3(газ) (3)
2Al(газ)+ N2(газ)=2AlN(тв) (4)
С этой целью выполнен анализ взаимодействия между компонентами шихты в диапазоне температур 1000-1500 °С не только при давлении, близком к атмосферному [5], но и с учетом реальных давлений паров: AlF3 и AlF. Причем монофторид алюминия имеет большее давление, чем трифторид при одинаковой температуре [2]. Как показывает проведенный анализ, возможны реакции 1, 2, 3.
Наряду с образованием нитрида алюминия по реакции (3) вполне возможно прямое азотирование металлического алюминия в расплавленном состоянии. Нитрид алюминия образует тонкую пленку на расплавленном алюминии и препятствует дальнейшему прохождению реакции. Об этом свидетельствует сравнение молекулярных объемов металлического алюминия (11,35 см3/моль) и нитрида алюминия (12,53 см3/моль), которые различаются между собой менее чем на 15%.
Условия равновесия азотирования алюминия по реакции (4) описываются уравнением ![]() и зависят от двух параметров (температуры и общего давления газовой фазы при постоянном составе газовой фазы или температуры и состава газовой фазы при постоянном общем давлении газовой фазы).
и зависят от двух параметров (температуры и общего давления газовой фазы при постоянном составе газовой фазы или температуры и состава газовой фазы при постоянном общем давлении газовой фазы).
Для реакции (1) условия равновесия определяются уравнением 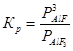 , и константа равновесия определяется двумя параметрами (температуры и общего давления при постоянном составе газовой фазы или температуры и состава газовой фазы при постоянном общем давлении газовой фазы).
, и константа равновесия определяется двумя параметрами (температуры и общего давления при постоянном составе газовой фазы или температуры и состава газовой фазы при постоянном общем давлении газовой фазы).
Для реакции (2) условия равновесия определяются уравнением ![]() , и константа равновесия определяется одним из параметров: температурой или общим давлением газовой фазы.
, и константа равновесия определяется одним из параметров: температурой или общим давлением газовой фазы.
Для реакции (3) условия равновесия определяются уравнением 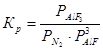 , и константа равновесия зависит от параметров: температуры, общего давления и состава газовой фазы.
, и константа равновесия зависит от параметров: температуры, общего давления и состава газовой фазы.
Анализ приведенных уравнений показывает, что изменение температуры, состава газовой фазы или общего давления в различной комбинации будет сказываться на реакциях получения нитрида алюминия методом газофазного синтеза.
В частности, повышение давления азота приводит к увеличению выхода нитрида алюминия. В таком же направлении будет сказываться повышение температуры, так как равновесное давление AlF увеличивается с ростом температуры [4].
Экспериментальная проверка высказанных положений проводилась на лабораторной установке, состоящей из высокотемпературного реактора с регулируемой температурой, системой напуска и контроля расхода молекулярного азота, системы вакуумирования высокотемпературного реактора. В качестве исходных материалов использовался очищенный вакуумной дистилляцией AlF3, особо чистый азот (ГОСТ 9293-74), металлический алюминий (ТУ 6-09-3742-87).
Кинетика процесса определялась по расходу молекулярного азота. Также фиксировался выход AlN в зависимости от температуры и давления молекулярного азота. Результаты опытов представлены в таблице 1 и 2 и на графиках (рис. 1). Для сравнения приведены расчетные значения.
Таблица 1. Влияние температуры на выход AlN.
|
№ опыта |
Температура, °С |
Количество образовавшегося AlN |
Выход AlN, % |
|
|
Опытное, г |
Теоретическое, г |
|||
|
1 |
1000 |
2,24 |
5,09 |
44 |
|
2 |
1000 |
1,79 |
5,09 |
35,3 |
|
3 |
1050 |
1,61 |
5,09 |
31,6 |
|
4 |
1050 |
2,20 |
5,09 |
43,2 |
|
5 |
1100 |
2,65 |
5,09 |
52,1 |
|
6 |
1100 |
2,38 |
5,09 |
46,8 |
|
7 |
1150 |
4,88 |
5,09 |
95,9 |
|
8 |
1150 |
5,09 |
5,09 |
100,0 |
|
9 |
1200 |
4,50 |
5,09 |
88,4 |
|
10 |
1200 |
5,02 |
5,09 |
98,6 |
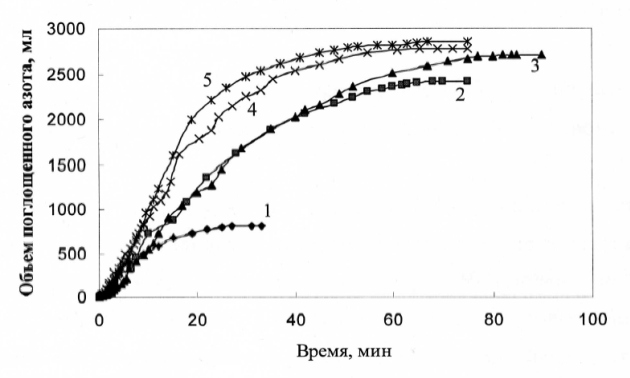
Рис. 1 - Зависимость объема поглощенного азота от времени при температурах:
1 - 1000 °С; 2 - 1050 °С; 3 - 1100 °С; 4 - 1150 °С; 5 - 1200 °С.
Таблица 2. Влияние давления азота на выход AlN.
|
Давление азота, мм рт. ст. |
745 |
335 |
141 |
|
Выход AlN, % |
99,67 |
12,7 |
следы |
Как показывают представленные результаты, повышение температуры начинает заметно сказываться на выходе нитрида алюминия при T > 1150 °С. Уменьшение давления молярного азота снижает выход AlN.
Сегодня процесс газофазного синтеза AlN реализован в виде двух технологических схем на оборудовании, представленном на рисунках 2, 3.
На рис. 2 представлен продольный разрез реакционной камеры, состоящей из трех отдельных секций: испарительной камеры для AlF3 (1), ванны для расплавленного алюминия (2) и камеры для синтеза AlN (3) [1].
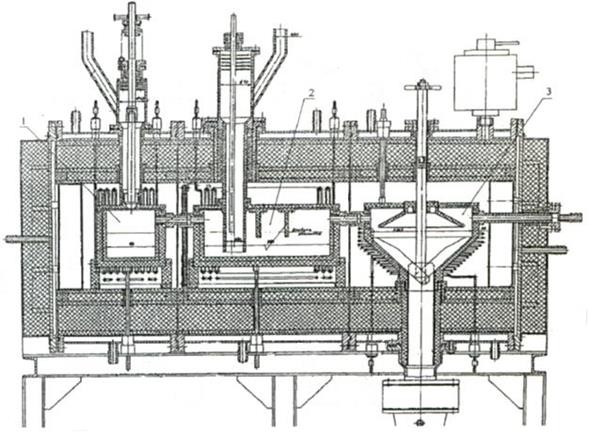
Рис. 2 - Продольный разрез реакционной камеры для получения нитрида алюминия газофазным способом.
На рис. 3 представлен продольный разрез реакционной камеры новой конструкции для получения нитрида алюминия газофазным способом.
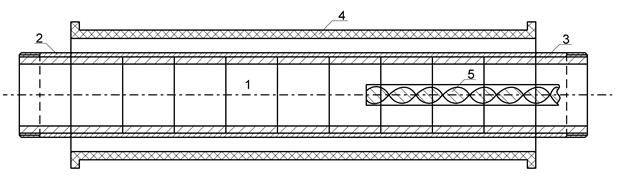
Рис. 3 - Продольный разрез новой конструкции реакционной камеры для получения нитрида алюминия газофазным способом:
1 – общая реакционная зона, 2 – трубчатая реакционная реторта из нержавеющей стали, 3 – составная футеровка из колец, изготовленных из нитрида алюминия, 4 – графитовый нагреватель, 5 – шнек для подачи исходных материалов.
Принципиальное отличие в организации технологического процесса: если в первом случае установка имеет раздельные камеры для проведения частных реакций, то во втором – весь процесс осуществляется в одной камере, где расплавленный алюминий взаимодействует с компонентами шихты, содержащими трифторид алюминия; образовавшийся монофторид алюминия реагирует с азотом с получением нитрида алюминия [8].
Аппаратурное оформление (рис. 2) достаточно сложно в изготовлении и обслуживании, требует использования дефицитных конструкционных и функциональных материалов, что в конечном счете сказывается на стоимости получаемого продукта.
Установка (рис. 3) не только предусматривает синтез AlN в одной камере, но и меняет механизм взаимодействия компонентов.
В объеме камеры компоненты находятся в следующем виде:
1) в газовой фазе: пары AlF3, AlF, Al, N2;
2) на поверхности расплавленного алюминия: хемосорбированный AlF3, AlF, молекулярный азот, частицы AlN. Наличие AlN на поверхности застывшего алюминия подтверждает снимок, сделанный с помощью растрового электронного микроскопа Jeol JSM 6490LV (рис. 4);

Рис. 4 - Электронограмма застывшего Al с частицами AlN на поверхности.
3) в объеме расплавленного алюминия: при захвате частиц AlF3 образуются полости, заполненные парами AlF3, AlF, которые при определенных условиях выходят в объем камеры. Эти данные подтверждает анализ снимков разрезов частиц застывшего алюминия, оставшегося в реакционной зоне после проведения процесса (рис. 5).

Рис. 5 – Снимок частиц застывшего алюминия, оставшихся после проведения процесса получения нитрида алюминия газофазным способом.
На снимке 5, сделанном с помощью растрового электронного микроскопа Jeol JSM 6490LV, видно, что частицы алюминия, оставшиеся после эксперимента, имеют полости, а также покрыты порошкообразным нитридом алюминия;
4) продукт реакции AlN в наносостоянии, агломерированный в частицы от 50 нм до 8 мкм, распределенный по объему реакционной камеры.
Футеровка реакционных камер выполнена из молибдена, графита, спеченного нитрида алюминия, что следует учитывать при получении продукта необходимой чистоты.
Кратко отличие приведенных технологических приемов сводится к следующему:
- возможен захват расплавленным алюминием частиц AlF3 и образование AlF не только на поверхности, но и в объеме расплава;
- хемосорбция AlF3 на поверхности расплавленного алюминия затруднена из-за хемосорбции молекулярного азота и нитрида алюминия в виде отдельных или спекшихся частиц.
Исходя из этих соображений разделение реакционных камер более благоприятно влияет на кинетику процесса получения нитрида алюминия, чем его реализация в одной реакционной камере, если не принимать специальных мер.
Выводы
1. В условиях газофазного синтеза возможно одновременное протекание нескольких процессов, ведущих к образованию AlN.
2. Термодинамический анализ показывает, что изменение основных параметров (температура, давление и состав газовой фазы) позволяет влиять на реакции при газофазном синтезе AlN.
3. Экспериментально подтверждается возможность проведения газофазного синтеза AlN в одной реакционной камере.
4. Предложен механизм взаимодействия компонентов в процессе газофазного синтеза AlN.
5. Показаны особенности двух технологических схем организации газофазного синтеза AlN.
Исследования проведены при поддержке Фонда Президента РФ Научной школы НШ-5669.20123.
Рецензенты:
Бамбуров Виталий Григорьевич, д.х.н., главный научный сотрудник Института химии твёрдого тела УрО РАН, г. Екатеринбург.
Поляков Евгений Валентинович, д.х.н., заместитель директора, заместитель председателя ученого совета, заведующий лабораторией физико-химических методов анализа Института химии твёрдого тела УрО РАН, г. Екатеринбург.



