Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
FISH OIL AUTOXIDATION OXICHEMILUMINESCENCE
В основе множества патологических состояний лежит разрушение липидных структур клеток вследствие свободнорадикального окисления, инициированного активными формами кислорода [7, 8, 13]. Качество пищевых, фармацевтических и технических продуктов, содержащих липиды, также во многом зависит от интенсивности и глубины процессов перекисного (свободнорадикального) окисления липидов [11, 12, 16]. Поэтому разработка экспресс-метода контроля за интенсивностью этих процессов представляется весьма актуальной. Особое внимание привлекает удобный и чувствительный хемилюминесцентный метод, используемый в химии для регистрации кинетики окисления углеводородов и тестирования антиоксидантов [6, 10, 14, 18, 22]. Однако по хемилюминесценции липидов и их аналогов литературные данные отрывочны и носят лишь качественный характер.
Целью настоящей работы является количественное исследование кинетики оксихемилюминесценции липидов и выявление ее механизмов.
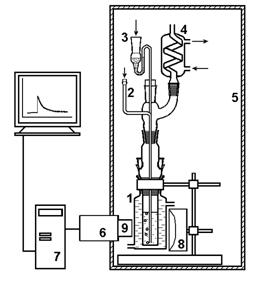
Рис.1. Установка для изучения оксихемилюминесценции в жидкой фазе
МЕТОДИКА И МАТЕРИАЛЫ
Объектом исследования выбран рыбий жир (ТУ Р 71.566.48, Тверская фармацевтическая фабрика), легко окисляющийся вследствие высокой ненасыщенности его липидов и содержащий умеренное количество антиоксидантов [16]. В качестве растворителя использовали хлорбензол (Acros Organics, 99+%). Регистрацию свечения осуществляли при помощи фотоэлектрического умножителя (ФЭУ) в составе модуля Н7467 фирмы Hamamatsu (Япония), работающего в режиме счета фотонов.
Окисление проводили при температуре 30 ¸ 70°С и непрерывном барботировании воздуха на установке, представленной на рис. 1: термостатируемая ячейка-реактор (1), снабженная устройствами для барботажа (2), ввода добавок (3) и обратным холодильником (4) была размещена в светонепроницаемой камере (5) со встроенным модулем Н7467 (6), подключенным к компьютеру (7). Светосбор осуществлялся при помощи параболического зеркала (8) и стеклянного цилиндрического световода (9). Процент светосбора составлял 1.92%, т.е. в фотоумножитель попадало 1.92% полного излучения образца.
В ряде опытов использовали активаторы хемилюминесценции - 9,10-дибромантрацен и Eu3+-1,10-фенантролин-трис(теноил-трифторацетонат) (хелат европия) [2].
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
На рисунках 2-3 приведена кинетика хемилюминесценции растворов рыбьего жира в хлорбензоле при различных температурах и концентрациях. Можно видеть, что все кривые сходны по форме - интенсивность хемилюминесценции снижается по мере увеличения времени инкубации и приближается к определенному квазистационарному уровню, зависящему от исходной концентрации рыбьего жира и температуры опыта. Кривые, полученные при более высоких концентрациях при одной и той же температуре, расположены выше кривых, соответствующих меньшим концентрациям (рис. 3). Увеличение концентрации рыбьего жира приводит к пропорциональному возрастанию интенсивности хемилюминесценции (рис. 3). Это указывает на однотипный характер кинетики в исследованном диапазоне концентраций.
|
|
|
|
Рис. 2. Кинетические кривые хемилюминесценции при окислении раствора (112.5 г/л) рыбьего жира в хлорбензоле. 1 - шум ФЭУ, 2 - хлорбензол
|
Рис. 3. Кинетические кривые хемилюминесценции растворов рыбьего жира в хлорбензоле при температуре 60ºС. 1 - шум ФЭУ. Концентрации: 2 - 0; 3 - 112.5; 4 - 225.0; 5 - 337.5 г/л |
Анализ литературных данных показывает, что в углеводородных системах возможны 2 механизма оксихемилюминесценции:
1) свободнорадикальный, когда при взаимодействии пероксидных радикалов (ROO·) образуется продукт в возбужденном электронном состоянии (*), быстро переходящий в основное состояние с испусканием кванта света [1, 5, 9, 18, 20, 22]
ROO· + ROO· → ROH + R1=O* → R1=O + hν,
2) молекулярный, когда квант света излучается при распаде промежуточного продукта окисления - диоксетана (D) [3, 4, 17, 19],
Реагенты → D → R1=O + R2=O* → R2=O + hν.
В первом случае интенсивность свечения, пропорциональная квадрату концентрации свободных пероксидных радикалов, должна снижаться при введении в систему антиоксидантов, реагирующих с этими радикалами и снижающих их концентрацию.
Известно, что липиды природного происхождения обычно содержат природные антиоксиданты, являющиеся ловушками свободных радикалов [7, 8, 16]. Следовательно, в их присутствии концентрации свободных радикалов незначительны. Поэтому можно отдать предпочтение второму механизму хемилюминесценции. Для доказательства этого на разных стадиях инкубации в исследуемый раствор добавляли высокоэффективный антиоксидант токоферол в концентрациях (2.5 ÷ 36)·10-5 моль/л, способных полностью подавлять свободнорадикальную хемилюминесценцию, возбуждаемую по первому механизму [7, 15, 20]. При этом интенсивность свечения оставалась без изменений, что подтверждает предположение о молекулярном механизме хемилюминесценции.
Учитывая, что квантовый выход фотоумножителя составляет 10%, была вычислена удельная интенсивность хемилюминесценции рыбьего жира (количество фотонов, излучаемое в единицу времени единицей массы жира) в исследованном температурном диапазоне (таблица 1).
Таблица 1. Удельная интенсивность хемилюминесценции раствора рыбьего жира в хлорбензоле
|
Температура, °С |
Удельная интенсивность x 10-3, фотон/(г·с), среднее значение ± стандартное отклонение |
|
|
максимальная (начало опыта) |
минимальная (после 20 мин. инкубации) |
|
|
30 |
91.4 ± 0.006 |
56,4 ± 0.050 |
|
40 |
112 ± 11.4 |
59.3 ± 6.03 |
|
50 |
204 ± 22.9 |
98.4 ± 2.78 |
|
60 |
518 ± 9.21 |
219 ± 11.6 |
|
70 |
786 ± 14.0 |
223 ± 11.8 |
Излучение фотона происходит при переходе молекулы продукта окисления из электронно-возбуждённого состояния (Р*) в основное (Р) по реакции
Р* → Р + фотон.
При этом дожно выполняться соотношение
ΔЕ* = Е* - Ео ≥ hν,
где Ео и Е* - энергии основного и возбужденного состояний, hν - энергия фотона.
Оценка энергии возбужденных состояний возможна благодаря использованию активаторов хемилюминесценции (А) - химически инертных веществ, способных участвовать в переносе электронной энергии по реакции
Р* + А → Р + А*
с последующим излучением фотона [1, 2, 4, 22]
А* → А + фотон.
Нами были использованы два активатора - 9, 10-дибромантрацен (ДБА) и хелат европия (ХЕ), энергии возбужденных состояний которых (ΔЕ*) равны 297 и 243 кДж/моль соответственно[1, 2, 4]. Концентрацию хелата европия варьировали в диапазоне от 9.76·10-5 до 36.4·10-5 моль/л, что соответствовало усилению хемилюминесценции в 7 ÷ 23 раза. Диапазон концентраций ДБА составлял 2.27 ¸ 25 ммоль/л. Это соответствовало усилению хемилюминесценции в 1.27 ÷ 4.4 раза. Эффективный перенос энергии с электронно-возбужденных молекул продуктов окисления (Р*) на молекулы активаторов говорит о том, что энергетические уровни возбужденных состояний продуктов окисления липидов рыбьего жира расположены выше уровней активаторов, т.е.
ΔЕ*Р ≥ ΔЕ*ДБА = 297кДж/моль > ΔЕ*ХЕ = 243кДж/моль.
Возможность многократного усиления хемилюминесценции активаторами показывает, что их квантовый выход люминесценции и время жизни возбужденных состояний много больше, чем у продуктов окисления Р*, имеющих предположительно кетонную природу [1].
Значения интенсивности хемилюминесценции, полученные при одной и той же глубине (по времени) процесса инкубации, но при разных температурах, были использованы для построения графиков температурных зависимостей в координатах ln It ¸ 1/T, где It - интенсивность хемилюминесценции в момент времени t, T - абсолютная температура. Таким образом были получены температурные зависимости хемилюминесценции, соответствующие моментам времени инкубации 60, 120, 180, 300, 480, 780 и 1200с. Коэффициенты корреляции превышали 0.97 и являлись значимыми для уровня Р = 0.0001 согласно t-критерию Стьюдента. Линейные коэффициенты наклона полученных прямых были использованы для вычисления энергии активации, значение которой (± стандартное отклонение) составило 43.8 ± 2.5 кДж/моль. Эта величина близка к значению 41.9 кДж/моль полученному для линоленовой кислоты в работе [21].
По результатам работы можно заключить, что источником хемилюминесценции липидов, содержащих антиоксиданты, являются промежуточные продукты окисления молекулярной природы. Полученные количественные характеристики могут быть использованы для разработки методов мониторинга перекисного окисления липидов и детализации механизмов оксихемилюминесценции, что будет являться предметом дальнейших исследований.
СПИСОК ЛИТЕРАТУРЫ:
- 1. Беляков В.А., Васильев Р.Ф. // В сб. Молекулярная фотоника. Л.: Наука. Ленингр. отд. 1970. С. 70
- 2. Беляков В.А., Васильев Р.Ф., Федорова Г.Ф. // Изв. АН СССР. Сер. физ. 1973. Т.37. №4. С. 747.
- 3. Беляков В.А., Филиппова Т.В., Заседателев С.Ю., Блюмберг Э.А. Хемилюминесценция при окислении непредельных углеводородов // Изв. АН СССР. Сер. хим. 1979. С. 1485-1489.
- 4. Беляков В.А., Васильев Р.Ф., Федорова Г.Ф. // Изв. АН СССР. Сер. хим. 1983. №12. С. 2709-2717.
- 5. Беляков В.А., Васильев Р.Ф., Иванова Н.М., Минаев Б.Ф., Осяева О.В., Федорова Г.Ф. // Изв. АН СССР. Сер. физ. 1987. Т. 51. №3. С. 2709.
- 6. Беляков В.А., Васильев Р.Ф., Федорова Г.Ф. // Кинетика и катализ. 2004. Т. 45. № 3. С. 355.
- 7. Бурлакова Е.Б., Храпова Н.Г. // Успехи химии. 1985. Т. 54. С. 1540.
- 8. Бурлакова Е.Б. //Рос. хим. ж. 2007. Т.51. № 1. С. 3.
- 9. Васильев Р.Ф., Федорова Г.Ф. //Кинетика и катализ. 2004. Т. 45. С. 695.
- 10. Васильев Р.Ф., Наумов В.В., Трофимов А.В., Федорова Г.Ф. //Методы оценки антиоксидантной активности биологически активных веществ лечебного и профилактического назначения. (Под ред. Е.Б. Бурлаковой) М.: Изд-во РУДН. 2005. С. 39.
- 11. Заиков Г.Е. // СОЖ, 2000, №12, с. 48-55.
- 12. Заиков Г.Е. // СОЖ, 2001, №9, с. 50-56.
- 13. Зенков Н.К., Ланкин В.З., Меньщикова Е.Б. Окислительный стресс: Биохимический и патофизиологический аспекты. - М. : МАИК "Наука / Интерпериодика", 2001. 343 С.
- 14. Наумов В.В., Храпова Н.Г. // Кинетика и катализ. 1984. Т. 25. № 3. С. 563.
- 15. Наумов В.В., Васильев Р.Ф. // Кинетика и катализ. 2003. Т. 44. № 1. С. 111.
- 16. Ржавская Ф.М. Жиры рыб и морских млекопитающих. М.: Пищевая промышленность. 1976. 471 С.
- 17. Шарипов Г.Л., Казаков В.П., Толстиков Г.А. Химия и хемилюминесценция 1.2‑диоксетанов. М.: Наука. 1990. 288 С.
- 18. Шляпинтох В.Я., Карпухин О.Н., Постников Л.М. Захаров И.П., Вичутинский А.А., Цепалов В.Ф. Хемилюминесцентные методы исследования медленных химических процессов. М.: Наука. 1966. 300 С.
- 19. Adam W., Trofimov A.V.// The Chemistry of Peroxides, Ed. by Z. Rappoport. Chichester, UK: John Wiley & Sons. 2006. V.2. P. 1171.
- 20. Denisov E.T., Afanas'ev I.B. Oxidation and Antioxidants in Organic Chemistry and Biology. CRC: Har/Cdr edition. 2005. 1024 P.
- 21. Slawson V., Adamson A.W. // Lipids. 1976. V. 11. N. 6. P. 472.
- 22. Vassil'ev R.F. // Progress in reaction kinetics. V. 4. Ed. by G. Porter. Oxford-London-Edinburge-NY: Pregamon Press. 1967. P. 305.
Библиографическая ссылка
Вепринцев Т.Л, Наумов В.В ОКСИХЕМИЛЮМИНЕСЦЕНЦИЯ ПРИ АВТООКИСЛЕНИИ РЫБЬЕГО ЖИРА // Современные проблемы науки и образования. 2007. № 6-2. ;URL: https://science-education.ru/en/article/view?id=809 (дата обращения: 10.06.2026).





