Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
ENZYME PANCREATINE IMMOBILIZATION INTO COMPOSITE MATERIALS AND DEVELOPMENT ON THEIR BASIS TEST-SYSTEMS FOR DETECTION OF CU2+ IONS RESIDUES
Введение
На сегодняшний день проблема загрязнения окружающей среды имеет приоритетное социальное и экономическое значение. Отходы производства: газообразные, жидкие и твердые вещества, поступающие в окружающую среду из различных источников, вызывают деградацию среды обитания и наносят ущерб здоровью населения [5].
В качестве токсикантов, нарушающих жизнедеятельность водных организмов и человека, могут выступать ионы тяжелых металлов. Так в результате прямого окисления сульфидов меди кислородом воздуха или сульфатредуцирующими бактериями происходит загрязнение природных гидросистем токсичными ионами меди. Миграция меди в природных поверхностных и грунтовых водах связана с высокой подвижностью ее иона в сульфатных средах [4]. Источником солей меди могут выступать сельхозугодия, регулярно обрабатываемые медьсодержащими ядохимикатами (например, бордосской жидкостью).
Ферментативные методы анализа являются перспективным направлением в диагностике окружающей среды при проведении эколого-аналитического мониторинга. Высокая селективность и чувствительность к ингибиторам ферментов – загрязнителям окружающей среды является основанием для создания на их основе тест-систем с такими параметрами как: простота и удобство в применении, высокая чувствительность и надежность [3]. Работы по созданию тест-систем на основе иммобилизованных ферментов актуальны и востребованы. Все большее количество ферментов используется при получении уникальных устройств, детектирующих наличие ингибиторов в различных объектах окружающей среды [2].
Цель исследования: разработка тест-системы для обнаружения остаточных количеств ионов меди в объектах окружающей среды на основе высокомолекулярного композиционного материала с иммобилизованным ферментом панкреатином.
Материалы и методы исследования
Для определения амилазной активности растворимого и иммобилизованного фермента панкреатина применяли метод, основанный на использовании в качестве субстрата полисахарида. Суть разработанного метода определения амилазной активности панкреатина состоит в следующем: к 0,1 мл раствора фермента панкреатина (15 мг в 500 мл дистиллированной воды) добавляли 1,6 мл фосфатного буферного раствора (рН 6,9) и термостатировали 30 минут при температуре 37 ℃. Параллельно термостатировали 0,1 %-й раствор крахмала, используемого в качестве субстрата, в 0,9 %-ом растворе хлорида натрия. Для постановки ферментативной реакции к анализируемому раствору панкреатина добавляли 1 мл 0,1 % -го раствора крахмала в 0,9%-ом растворе хлорида натрия, смесь инкубировали в течение 5 минут при температуре 37 ℃. В качестве контроля использовали смесь, в состав которой вместо раствора фермента вносили 0,1мл 0,9 %-го раствора хлорида натрия. Ферментативную реакцию останавливали, добавляя 0,1 мл 1М раствора соляной кислоты. Остаточное количество крахмала оценивали по сине-фиолетовой окраске с раствором йода на ФЭК–КФК-2 при длине волны 670 нм в кювете с толщиной слоя 10 мм. Затем, исходя из оптической плотности, определяли количество крахмала в растворе и рассчитывали удельную активность фермента. Количество расщепленного крахмала определяли по разности экстинкции контрольной и опытной проб с учетом калибровочной кривой в координатах оптическая плотность / количество крахмала (мг).
Активность рассчитывали по формуле:
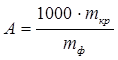 (1)
(1)
мг крахмала/г фермента, где mкр – масса расщепленного крахмала, мг; mф – масса фермента, мг;1000 – единица перевода мг в г.
Для иммобилизации фермента панкреатина в структуру композиционного материала была разработана следующая методика. Готовили 3 %-й раствор метилцеллюлозы в воде, выдерживали в течение 12–15 часов. В полученный коллоидный гель метилцеллюлозы вводили реагент для модификации реологических характеристик, 0,03 %-й водный раствор фермента панкреатина, пластификатор и перемешивали до однородного состояния [1].
Моделирование процесса влияния различных факторов на удельную активность ферментов ацетилхолинэстеразы и панкреатина проводилось с помощью программы Statistic V.6 с привлечением метода искусственные нейронные сети (NeuralNetworks).
Результаты исследования и их обсуждение
В основе тест-системы для обнаружения ионов Cu2+ в объектах окружающей среды лежит ферментативная реакция с участием фермента панкреатина.В связи с этим, создание оптимальных условий при использовании данной тест-системы предполагало исследование таких факторов, как температура, рН буферного раствора, время ингибирования и время ферментативной реакции.
Для анализа использовали пять экспериментальных серий препарата иммобилизованного фермента панкреатина. Исследуемые пробы имели состав: 1 мл 0,1%-го раствора крахмала в 0,9 %-ом растворе хлорида натрия; 1,6 мл фосфатного буферного раствора (рН = 6,9). В одни пробы добавляли по 0,1 мл раствора композиционного материала (композиционный материал массой 36 мг, содержащий фермент панкреатин массой 0,3 мг, растворяли в 10 мл дистиллированной воды). В другие пробы добавляли по 0,1 мл раствора растворимого фермента (15 мг в 500 мл дистиллированной воды). В опытную пробу добавляли 1 мл 0,0001 %-ого раствора CuSO4 в начале реакции, а в контрольную – в конце реакции. Полученные образцы термостатировали 5 минут при температуре 37 ℃.
Полученные данные представлены в таблице 1.
Таблица 1. Оптимизация факторов и анализ активности растворимого и иммобилизованного фермента панкреатина
|
Наименование показателя |
Фермент, иммобилизованный в композиционный материал |
Фермент без носителя |
|
Удельная активность, (мг крахмала/г фермента)×105 |
2,73 |
2,80 |
|
Сохранение удельной активности при иммобилизации, % |
95-98 |
100 |
|
рН |
6,9 |
6,9 |
|
Температура, ℃ |
37 |
37 |
|
Время ингибирования, мин |
30 |
30 |
|
Время ферментативной реакции, мин |
5 |
5 |
Важным аспектом является длительность сохранения каталитической активности ферментного препарата, заключенного в композиции. В этой связи образцы тест-систем хранились в течение 4 месяцев при температурах +4 ℃ и +20 ℃. При этом остаточную активность измеряли один раз в месяц. Для анализа использовали пять экспериментальных серий препарата иммобилизованного фермента панкреатина.
Полученные данные представлены на рисунке 1.
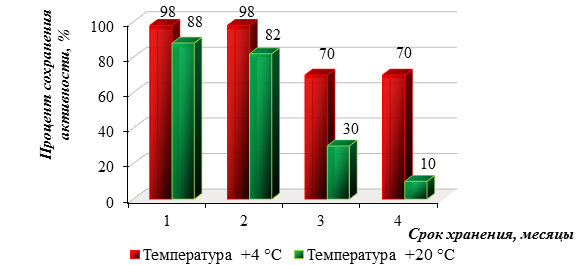
Рисунок 1. Сохранение ферментативной активности панкреатина во времени
Из полученной диаграммы можно сделать вывод: композиции, хранившиеся при температуре +4 ℃, к четвертому месяцу хранения имели стабильный процент сохранения биокаталитической активности, а композиции, хранившиеся при температуре +20 ℃, потеряли 78 % своей удельной активности.
Были проведены исследования по сохранению удельной активности иммобилизованного и растворимого фермента панкреатина во времени при температуре хранения +4 ℃ (рисунок 2).
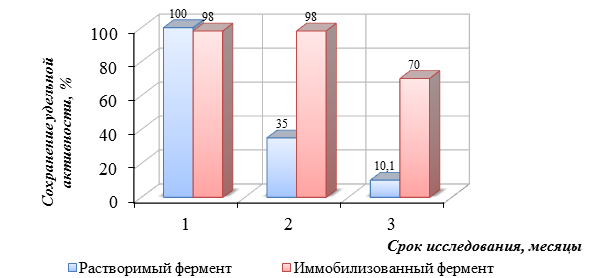
Рисунок 2. Сохранение удельной активности иммобилизованного и растворимого фермента панкреатина во времени
Из графика видно, что к третьему месяцу хранения при температуре +4 ℃ иммобилизованный фермент сохранил 75 % активности, а фермент, находящийся в растворе, сохранил 8,4 % активности.
Полученные данные свидетельствуют о том, что при хранении иммобилизованный фермент предотвращает потерю активности по сравнению с ферментом, находящимся в растворе. Это может являться одним из преимуществ, при разработке тест-системы.
На основании полученных данных была разработана тест-система для обнаружения ионов меди в объектах окружающей среды следующего состава: композиционный материал массой 33 мг с иммобилизованным в его структуру ферментом панкреатином массой 0,003 мг.
Для разработки способа обнаружения меди была составлена модельная система, которая представляла собой образцы воды, содержавшие ионы меди в следующих количествах: 0,25 мкг; 2,5 мкг; 25 мкг; 125 мкг; 250 мкг и 375 мкг. Для анализа использовали шесть экспериментальных серий препарата иммобилизованного фермента панкреатина.
Анализ проводили в следующей последовательности. В анализируемую пробу объемом 2,75 мл помещали композиционный материал массой 33 мг с иммобилизованным ферментом массой 0,003мг и термостатировали 30 минут при +37 ℃. Затем прибавляли 1,6 мл буферный раствор (рН = 6,9) и 1 мл 0,1 %-го раствора крахмала, используемого в качестве субстрата. Смесь инкубировали в течение 5 минут. По истечении времени реакцию останавливали подкисленным раствором индикатора йода (раствор, приготовленный разведением в 50 раз 0,2N раствором соляной кислоты основного раствора, состав которого: 2 г йода, 0,66 г йодида калия в 20 мл воды). Содержание меди определяли количественно на ФЭК-КФК-2 при длине волны 670 нм в кювете толщиной 10 мм.
Полученные данные представлены на рисунке 3.
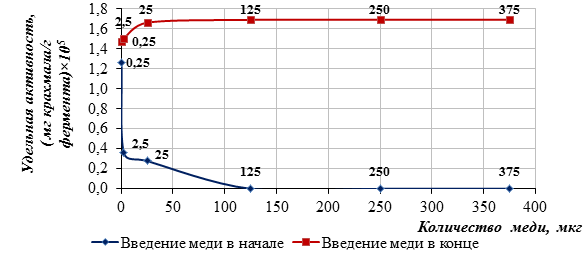
Рисунок 3. Определение ионов Cu2+ с помощью разработанной тест-системы на основе иммобилизованного фермента панкреатина
Анализ полученных данных позволил сделать вывод, что 125 мг меди полностью ингибируют 3 мкг фермента панкреатина. При наличии минимально определяемого количества меди в анализируемом растворе удельная активность иммобилизованного фермента панкреатина снижается на 14 %.
В связи с тем, что в объектах внешней среды наряду с ионами меди присутствуют ионы тяжелых металлов: кадмия, железа, свинца и др., было необходимо провести анализ по влиянию сопутствующих ионов на определение меди с использованием разработанных тест-систем. Концентрация вносимых ионов 10 мкг в 1 мл (рис. 4).
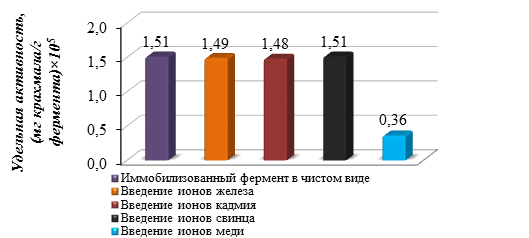
Рисунок 4. Влияние ионов тяжелых металлов на активность иммобилизованного фермента панкреатина
Из графика видно, что определению ионов меди с помощью разработанной тест-системы, не мешают ионы кадмия свинца и железа. Таким образом, данный метод обладает специфичностью в отношении ионов меди.
Заключение
С целью построения тест-системы для обнаружения остаточных количеств ионов меди была проведена иммобилизация фермента панкреатина в композиционные материалы и оптимизированы основные параметры, влияющие на проведение анализа: рН среды – 6,9; температура – 37 ℃; время ингибирования – 30 минут; время постановки ферментативной реакции – 5 минут. На основании результатов исследования установлено, что иммобилизованный фермент панкреатин, хранившийся при температуре +4 ℃, к четвертому месяцу сохранил 70 % каталитической активности, а хранившийся при температуре +20 ℃, потерял 78 % активности. Исследования по сохранению активности фермента во времени показали, что после 3 месяцев хранения фермент в растворе сохранил 10,1 % удельной активности, а иммобилизованный фермент сохранил 70 % удельной активности. На основе полученных данных разработана тест-система с иммобилизованным ферментом панкреатином для детекции ионов меди в объектах внешней среды.
Проведенные исследования показывают, разработанный метод обнаружения ионов Cu2+ с использованием тест-системы на основе фермента панкреатина, иммобилизованного в композиционные материалы, обладает специфичностью и высокой чувствительностью. Диапазон определяемых концентраций с помощью данной тест-системы составляет от 0,02 до 1,45 мг/л. При наличии минимально определяемой концентрации ионов меди удельная активность иммобилизованного фермента снижается на 14 %. Определению меди не мешают сопутствующие ионы кадмия, железа и свинца. Анализ позволяет проводить детекцию меди на уровне предельно допустимой концентрации меди в объектах внешней среды, а также не требует большого объема исследуемой пробы.
Рецензенты:
Орлова Ирина Георгиевна, доктор биологических наук, старший научный сотрудник по специальности, профессор кафедры медицинской биохимии, клинической лабораторной диагностики и фармации ФГАОУ ВПО «Северо-Кавказский федеральный университет», г. Ставрополь.
Лодыгин Алексей Дмитриевич, доктор технических наук, доцент, заведующий кафедрой прикладной биотехнологии ФГАОУ ВПО «Северо-Кавказский федеральный университет», г. Ставрополь.
Библиографическая ссылка
Воробьева О.В., Филиппова А.М., Аванесян С.С. ИММОБИЛИЗАЦИЯ ФЕРМЕНТА ПАНКРЕАТИНА В КОМПОЗИЦИОННЫЕ МА-ТЕРИАЛЫ И СОЗДАНИЕ НА ИХ ОСНОВЕ ТЕСТ-СИСТЕМ ДЛЯ ОБНАРУЖЕНИЯ ОСТАТОЧНЫХ КОЛИЧЕСТВ МЕДИ // Современные проблемы науки и образования. 2012. № 6. ;URL: https://science-education.ru/en/article/view?id=7946 (дата обращения: 16.05.2026).



