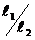Цель исследования - провести квантово-химическое моделирование аминокислотных комплексов кальция и оценить возможность их применения для восполнения дефицита кальция на модели антиортостатической гипокинезии у мышей.
Материалы и методы
Для построения молекулярных моделей аминокислот и их комплексов с кальцием нами использован графический редактор программного комплекса - пакета прикладных программ квантовой химии - Hyper Chem [10]. При построении моделей с пробной геометрией для аминокислот в ряде случаев использована одна из библиотек данного пакета. Оптимизация геометрии осуществлялась в зависимости от нахождения начальной точки относительно ближайшего минимума на поверхности потенциальной энергии (ППЭ) [5]. Построены молекулярные модели для аминокислотных комплексов кальция с аланином, глицином, лейцином, лизином и аргинином с геометрией, оптимизированной полуэмпирическим методом РМ-3. Расчет проводился с применением программного комплекса GAMESS [9].
Комплекс кальция с аминоуксусной кислотой получали смешиванием растворов глицина и хлорида кальция [8].
Эксперимент был выполнен на 54 мышах-самцах линии СВА массой 25-30 г. Для развития у животных остеопороза применяли антиортостатическую силовую разгрузку мышц. Гипокинезию мышц задней конечности создавали с помощью модели [4], заключающейся в вывешивании мышей за хвостовую складку под углом 45° и лишении их опоры на задние конечности. Животные трёх групп содержались на обеднённом белками и кальцием рационе. Первая группа (n=18) служила контролем, второй и третьей группам (по n=18) дополнительно ежесуточно перорально вводился раствор глицината кальция и хлорида кальция соответственно, содержащий 1 мг Са2+ на животное в сутки. Из эксперимента мышей выводили декапитацией на 7 (n=6), 14 (n=6) и 28 (n=6) сутки. Все манипуляции с животными проводили в соответствии с «Правилами проведения работ с использованием экспериментальных животных» (приложение к приказу Минздрава СССР от 12.08.1977 № 755).
Для биохимического исследования в сыворотке крови экспериментальных животных оценивали общее содержание кальция, неорганического фосфата, активность щелочной (ЩФ) и тартрат-резистентной кислой (трКФ) фосфатаз. В бедренных костях мышей определяли содержание кальция, фосфата и оксипролина (ОП). Результаты биохимических показателей сыворотки крови и костной ткани мышей экспериментальных групп сравнивали с показателями животных интактной группы (n=13). Для оценки достоверности различий использовали непараметрический критерий Манна-Уитни (р<0,05). Статистическую обработку результатов осуществляли в макросе программы «Microsoft Excel» «AtteStat» Версия 1.0 [3].
Результаты и их обсуждение
В результате оптимизации геометрии бис-глицинового комплекса кальция была получена модель, геометрические характеристики которой, а также заряды на атомах и порядки связей, определенные по Малликену [1], приведены в таблице 1. Размер комплекса, определенный по максимальным расстояниям между диаметрально противоположными атомами, составляет примерно 7 ангстрем.
|
Таблица 1 Характеристики для связей и атомов в глицине (знаменатель) и бис-глициновом комплексе Ca2+ (числитель) |
||||
|
Связь |
Длина связи, Å |
Порядок связи |
Атом |
Заряд |
|
Ca-O |
2,33 |
0,23 |
Ca2+ |
+0,96 |
|
C-O-(Ca/H) |
1, 28/1,39 |
1,11/0,71 |
O-(Ca)/O(-H) |
-0,41/-0,29 |
|
C=O |
1,28/1.21 |
1,11/1,27 |
OД |
-0,41/-0,12 |
|
C-C(H2) |
1,56/1,55 |
0,73/0,75 |
C(OOCa/H) |
0,25/0,31 |
|
C-N |
1,52/1,48 |
0,71/0,71 |
N |
-0,39/-0,56 |
Из приведенных в таблице 1 данных следует, что при образовании комплекса с кальцием в молекулах глицина происходят изменения, касающиеся только ближайших к атому кальция связей. Связь кальция с атомами кислорода практически ионная. При этом стянутый с атома кальция заряд распределяется между четырьмя атомами кислорода. Суммарное увеличение заряда на них составляет 0,82 заряда электрона.
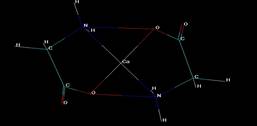
В работе [7] приведена схема бис-глицинового комплекса, в которой ион металла одинаково связан как с кислородом, так и с азотом. Для проверки этого утверждения мы использовали пробную геометрию для бис-глицинового комплекса кальция, соответствующую данной схеме (рис. 1), и далее провели оптимизацию с указанными связями в комплексе. В итоге оптимальная геометрия осталась той же, что и без Ме-N связи, а заселенность этой связи фактически равна нулю. Следовательно, модельное изучение не подтверждает хелатный характер связи иона кальция с атомами азота в данном комплексе.
|
|
|
Рис. 1. Структурная схема бис-глицинового комплекса Са, построенная в соответствии с данными работы [7] |
Практически с начала реализации квантово-химических расчетов обсуждалась возможность определения с их помощью термодинамических функций молекул и их изменения в химических реакциях [5]. Однако подобные расчеты достаточно долго не получали широкого распространения в связи со сложностью и большими затратами машинного времени, необходимого для их реализации. В настоящее время расчет термодинамических функций включен в качестве стандартного блока в пакеты прикладных программ квантовой химии, в частности, такие как Hyper Chem и GAMESS. Опубликованы работы по обоснованию методики этих расчетов (см. например [9]). Однако результаты таких расчетов и до настоящего времени публикуются и обсуждаются недостаточно часто для того, чтобы сделать детальный анализ успешности их реализации.
Методика расчета термодинамических функций молекул, заложенная в пакеты прикладных программ квантовой химии, приведена, например, в работе [1].
Определение равновесной геометрической структуры молекулы и ее колебательного спектра позволяет рассчитать ее основные термодинамические характеристики при заданной температуре - энтальпию (Н), энтропию (S), теплоемкости Cp и CV). Расчеты проводят по формулам:
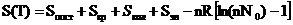 , (1)
, (1)
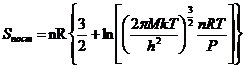 , (2)
, (2)
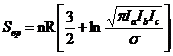 , (3)
, (3)
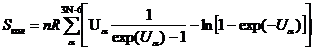 , (4)
, (4)
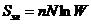 , (5)
, (5)
![]() , (6)
, (6)
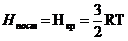 , (7)
, (7)
![]() (для линейных молекул),
(для линейных молекул),
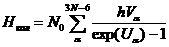 , (8)
, (8)
![]() . (9)
. (9)
Здесь:
![]() , (10)
, (10)
![]() , (11)
, (11)
n- число молей вещества;R - универсальная газовая постоянная; N0- число Авогадро;M - масса молекулы; k- постоянная Больцмана; T температура; P- давление; h- постоянная Планка; Ia- момент инерции; σ число симметрии; Vα - частота колебаний; gα- кратность вырождения колебаний; Wэ- кратность вырождения электронного состояния молекулы (как правило, равна единице);E0 - электронная энергия (получается в квантово-химическом расчете).
Изменение энтальпии в результате химической реакции ![]() (A - реагенты,B - продукты) определяется по формуле:
(A - реагенты,B - продукты) определяется по формуле:
![]() . (12)
. (12)
Два последних члена в этой формуле - поправки на нулевую энергию колебаний (![]() ):
):
![]() . (13)
. (13)
Термодинамические характеристики, рассчитанные по указанной методике, для глицина и комплекса кальция на его основе, приведены в таблице 2.
|
Таблица 2 Термодинамические функции для моделей глицина и его комплекса с кальцием |
||
|
Термодинамическая функция |
Глицин |
Бис-глициновый комплекс Ca |
|
E(0), ккал/моль |
-175148 |
-770042 |
|
E(300), ккал/моль |
-175087 |
-769933 |
|
S(300), ккал/моль·К |
0,0737 |
0,112655 |
|
H(300), ккал/моль |
-175109 |
-769967 |
Проведенный с этими данными расчет теплоты образования ΔH и энтропии образования ΔS комплекса кальция при T=300K по реакции:
2gly + CaCl2 - Ca(gly)2 + 2HCl (14)
дает значения + 78 ккал/моль и - 0,023 ккал/моль·К.
Проведенное модельное исследование показало невозможность образования аминоциальных комплексов с кальцием хелатного типа. Несмотря на то, что линейные размеры молекул аминокислот в изученном ряду возрастают от 5 до 10 ангстрем, размер комплексов примерно одинаков и составляет ≈8Å. Исключение составляет комплекс с аргинином, у которого наряду с компактной частью такого же размера имеется и «хвост».
Аналогичным образом проведены расчеты геометрий комплекса кальция с аланином, лейцином, лизином и аргинином. Данные, обобщенные в таблице 3, показывают, что характер связи Ca в этих комплексах одинаков. Связь практически ионная. В изученном ряду заряд иона кальция закономерно уменьшается; прослеживается тенденция увеличения среднего значения длины Ca-O связи и соответствующего уменьшения ее заселенности. С ростом размера комплексов закономерно возрастает асимметрия Ca-O связей, оцененная по соотношению длин связей и их заселенностей. Ранее в нашей работе [2] было показано, что в случае сеткообразующих оксидов это означает появление тенденции к фрагментации больших молекул. Систематическое изучение комплексов глицина с большим числом металлов [7] также показало уменьшение стабильности комплексов с ростом их асимметрии.
Из данных таблицы 3 следует также, что при синтезе комплексов по реакции типа (13) в изученном ряду наблюдается рост энтальпии реакции и рост изменения энтропии системы в результате реакции.
|
Таблица 3 Сравнительные характеристики аминоацильных комплексов Са2+ по данным полуэмпирического расчета РМ-3 |
|||||
|
|
Глицин |
Аланин |
Лейцин |
Лизин |
Аргинин |
|
Размер комплекса в Å |
7 |
7-7,5 |
8 |
8 |
12 |
|
Заряд атома Са |
0,81 |
0,74 |
0,7 |
0,71 |
0,63 |
|
Средняя длина связи Са-О, Å и средний порядок связи |
2,37/0,21 |
2,38/0,18 |
2,50/0,135 |
2,58/0,11 |
2,47/0,14 |
|
Асимметрия |
1,03 |
1,04 |
1,07 |
1,13 |
1,21 |
|
Асимметрия |
1,08 |
1,28 |
1,7 |
1,75 |
2,22 |
|
- ΔH(300), ккал/моль |
196,8 |
244 |
369 |
386 |
378 |
|
ΔS(300), ккал/моль*K |
-0,0076 |
-0,011 |
-0,033 |
-0,036 |
-0,0491 |
При биохимическом исследовании сыворотки крови и образцов костной ткани экспериментальных животных получили следующие данные.
Повышение концентрации сывороточного кальция на фоне снижения содержания данного элемента в костной ткани животных 1-ой группы свидетельствует о процессах резорбции кости (таблицы 4 и 5). Так как в костной ткани мышей 2-ой группы наблюдалось постепенное накопление кальция на фоне повышения его концентрации в сыворотке крови, то можно предположить, что элемент поступал в кровь не за счет процессов резорбции кости, а из желудочно-кишечного тракта в составе глицината кальция. Следовательно, кальций из комплексного соединения транспортируется в кровяное русло, накапливаясь при этом в костной ткани.
Таблица 4 Основные биохимические показатели сыворотки крови мышей&
|
Показатель, ед. изм. |
№ группы |
Продолжительность эксперимента, сут. |
Интактные животные(n=13) |
||
|
7-е |
14-е |
28-е |
|||
|
трКФ, Ед/л |
1 - контроль, (n =6) 2 - Са(гли)2, (n =6) 3 - СаСl2, (n =6) |
3,4 (1,7;3,7) 2,8 (1,1;4,6) 1,4(0,3;3,3) |
1,5 (1,1;2,3) 7,2* (5,5;8,4) 0,9* (0,5;1,1) |
15,4* (14,6;18,1) 1,5 (0,9;2,1) 4,2 (2,9;5,1) |
3,3(1,7;5,4) |
|
ЩФ, Ед/л |
1 - контроль, (n =6) 2 - Са(гли)2, (n =6) 3 - СаСl2, (n =6) |
103,5*(75,0;116,9) 65,9*(60,4;77,6) 26,3*(24,5;27,9) |
137,3*(128,8;141,6) 97,3* (72,1;107,5) 15,6* (14,5;16,2) |
21,3*(19,3;22,5) 87,6*(80,3;93,8) 16,5*(14,0;18,6) |
164,9(149,6;174,3) |
|
Са2+, ммоль/л |
1 - контроль, (n =6) 2 - Са(гли)2, (n =6) 3 - СаСl2, (n =6) |
2,41*(2,31;2,48) 2,24(2,23;2,26) 2,03(1,83; 2,19) |
2,33*(2,19;2,42) 2,24(2,19;2,33) 2,54*(2,43;2,54) |
2,38*(2,28;2,46) 2,41*(2,41;2,49) 2,45*(2,28;2,47) |
2,12(1,99;2,23) |
|
РО43-, ммоль/л |
1 - контроль, (n =6) 2 - Са(гли)2, (n =6) 3 - СаСl2, (n =6) |
2,52*(2,51;2,54) 1,82*(1,74;2,20) 2,31(2,09;2,48) |
2,73*(2,62;2,98) 2,34(2,29;2,45) 2,50(2,19;2,60) |
2,03(1,96;2,24) 1,17*(1,12;1,21) 1,83*(1,67;1,98) |
2,14(1,97;2,39) |
|
& - В таблице представлены медианы значений М (25 %; 75 %); * - достоверные различия при сравнении интактной группы с экспериментальными животными. |
|||||
В группе № 2 происходило достоверное снижение концентрации фосфата к 28 суткам эксперимента. Данное явление, скорее всего, связано с активным участием неорганической формы фосфата в поддержании нормального функционирования минеральной компоненты костной ткани, тогда как в контрольной группе наблюдалось достоверное увеличение данного показателя на 7 и 14 сутки после начала эксперимента, связанное с интенсивными процессами разрушения костной ткани. При изучении органической составляющей следует отметить увеличение содержания ОП в костной ткани мышей контрольной группы по сравнению с интактной группой, отсутствие существенных изменений в группе животных, которым ежесуточно перорально вводился раствор глицината кальция, и повышение концентрации ОП в большеберцовой кости животных, в рацион которых входил хлористый кальций (таблица 5).
Таблица 5 Основные биохимические показатели костной ткани мышей&
|
Показатель, ед. изм. |
№ группы (по n=6) |
Продолжительность эксперимента, сут. |
Интактные животные(n=13) |
||
|
7-е |
14-е |
28-е |
|||
|
ОП, мг/100 мг |
1(контроль) 2 (Са(гли)2) 3 (СаСl2) |
9,75(8,97;11,22) 10,00(8,46;10,99) 13,22*(12,21;13,41) |
14,17*(13,33; 14,52) 13,73*(13,64; 14,12) 12,53*(12,20;13,21) |
16,15*(14,03;16,48) 10,23(8,95;10,64) 12,01(10,28;13,66) |
10,43 (8,58;10,60) |
|
Са2+, мг/100 мг |
1(контроль) 2 (Са(гли)2) 3 (СаСl2) |
18,04(16,52;18,33) 18,17(16,96;18,81) 16,20(15,18;16,89) |
14,98*(14,89;15,87) 19,01(17,38;19,40) 16,17(15,67;16,68) |
14,30*(13,79;14,37) 18,80*(18,04;18,94) 16,07(15,57;16,29) |
16,20 (15,84;17,98) |
|
РО43-, мг/100 мг |
1(контроль) 2 (Са(гли)2) 3 (СаСl2) |
25,68*(25,46;26,31) 28,14(27,35;28,94) 26,62*(26,47;26,99) |
27,08(25,95;28,53) 25,02*(21,88;27,01) 29,69*(27,75;31,99) |
24,47* (23,81;25,61) 27,80(27,29;28,73) 30,01(27,50;30,31) |
28,76 (27,93;30,39) |
|
& - В таблице представлены медианы значений М (25 %; 75 %); *-- достоверные различия при сравнении интактной группы с экспериментальными животными. |
|||||
Уровень ЩФ в сыворотке крови животных контрольной группы к 28 суткам эксперимента значительно снижался по сравнению с интактной группой, что свидетельствует о преобладании процессов костной резорбции, связанных с нарушением роста и функционирования костной ткани. Введение в пищевой рацион хлорида кальция также значительно снижало активность ЩФ уже к 7-ым суткам эксперимента, данное снижение сохранялось на протяжении всего эксперимента. Уровень ЩФ в сыворотке крови животных 2-ой группы снижался менее интенсивно, на протяжении всего эксперимента не наблюдалось значительных скачков активности фермента. Существенное повышение уровня трКФ к 28 суткам эксперимента в группе № 1 приводило к активизации остеокластов и к угнетению остеобластов, начинали протекать интенсивные процессы костной резорбции. Это подтверждается, как уже было отмечено, возрастанием концентрации кальция и фосфата в сыворотке крови и ингибированием активности ЩФ. Следует отметить, что во 2 и 3-ей группах активность трКФ колебалась незначительно.
Для более полного анализа изменений в системе Са2+-ОП рассчитывали коэффициент Са2+/ОП, позволяющий оценить сдвиги в соотношении минеральной и органической компоненты. Анализ данных показал, что наряду с увеличением содержания ОП в костной ткани 1-ой группы, отмечалось количественное снижение содержания кальция, происходило падение индекса Са2+/ОП. Восполнение кальциевой недостаточности за счёт обогащения пищевого рациона глицинатом кальция сопровождалось достоверным возрастанием содержания кальция в кости на фоне сохранения постоянного значения концентрации ОП. В связи с данным явлением в ходе эксперимента регистрировалось повышение коэффициента Са2+/ОП относительно группы интактных животных. В 3-ей группе животных индекс Са2+/ОП не превышал значения индекса животных группы сравнения.
Заключение
Таким образом, полученные в ходе работы данные указывают на различия в строении аминоацильных комплексов кальция и изученных ранее глициновых комплексов d-элементов. Расчетными методами установлено, что связь в исследуемых соединениях практически ионная, не происходит образования внутрикомплексных соединений (хелатов). Введение в пищевой рацион мышей глицината кальция в количестве 1 мг Са2+ в сутки предупреждает потерю данного элемента костной тканью в условиях антиортостатической разгрузки. Са2+ из комплекса усваивается костной тканью лучше, чем из неорганической соли хлорида кальция. Следовательно, глицинат кальция может найти применение в качестве самостоятельного препарата для восполнения дефицита кальция.
Рецензенты:
- Попков Дмитрий Арнольдович, доктор медицинских наук, заведующий лабораторией коррекции деформаций и удлинения конечностей ФГБУ «РНЦ «ВТО» имени академика Г. А. Илизарова» Минздравсоцразвития России, г. Курган.
- Щудло Наталья Анатольевна, доктор медицинских наук, заведующая клинико-экспериментальной лабораторией реконструктивно-восстановительной микрохирургии и хирургии кисти ФГБУ «РНЦ «ВТО» имени академика Г. А. Илизарова» Минздравсоцразвития России, г. Курган.