Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
MODERN MEDICAL TECHNOLOGIES PATIENTS WITH CHRONIC VIRAL HEPATITIS
Сегодня мировым стандартом в лечении вирусного гепатита С стала комбинированная терапия ИФН и рибавирином. Важно отметить, что свой антивирусный эффект рибавирин оказывает только в присутствии ИФН (монотерапия рибавирином неэффективна), что снижает формирование резистентности HCV к препарату. Хотя у 20-25 % больных на фоне монотерапии рибавирином уровень трансаминаз нормализуется, а после отмены препарата происходит возврат повышенных показателей ферментов.
На сегодняшний день «золотым стандартом» лечения считается терапия с применением интерферона и рибавирина. Рибавирин, аналог нуклеозидов, позволяет добиться снижения уровня аминотрансфераз и уровня РНК вируса только в присутствии интерферона.
По данным специалистов Кокрановской группы [по изучению заболеваний печени (Brok J., et.al., 2005)] анализ 72 протоколов клинических исследований (выборка включала 9991 пациента) с применением интерферона+рибавирина, выявил гистологический и вирусологический ответ у 40 % больных. При этом отмечено множество нежелательных реакций (гематологического, дерматологического, гастроэнтерологического типов), возникших на фоне терапии, негативно сказываясь на качестве жизни пациентов. На выраженные побочные эффекты с отменой препаратов в 56 % случаев, указывают в своих исследованиях T. Nacamura et.al. (2005), Y. Iwasaki.(2006).
В многоцентровых исследованиях (43 научных центра - 832 больных) описан стойкий вирусологический ответ, колеблющийся от 9 до 43 % случаев. У пациентов, не «ответивших» на лечение интерфероном, а применение рибавирина и ИФН-альфа, привело к стойкой ремиссии в 29 % случаев. У больных, не ответивших на первичный курс моно-ИФН-терапии (в 52 % случаев), отмечен рецидив заболевания.
С целью совершенствования терапии A.Tsubota et al. (2004) апробировал, при хроническом гепатите С у больных с 1b генотипом, терапию интерфероном, используя его в высоких дозах (интерферон назначался по 6 млн МЕ ежедневно в течение двух недель, а затем в течение 22-х недель три раза в неделю также по 6 млн МЕ), а рибавирин вводился больным в дозе 800 мг/сутки длительностью 24 недели; получен биохимический ответ у 81 % больных, ранний вирусологический в 66 % случаев, а устойчивый вирусологический ответ сохранился лишь у 19 % больных.
В ряде стран мира, с целью повышения оказания качества медицинской помощи больным с хроническим гепатитом С, приняты стандарты лечения, предусматривающие применение пегилированных интерферонов в комбинации с рибавирином.
По данным I.M.Jacobson et.al. (2005), больные 1 генотипом, не ответившие на монотерапию интерфероном и терапию с рибавирином (321 человек) дали вирусологический ответ лишь в 16 % случаев, а C Camma (2005), получил вирусологический ответ у больных с 1-м генотипом в 54-56 % случаев.
Рандомизированные исследования, проведенные Барбакадзе Г.Г. (2005), позволили установить, что применение пегилированного интерферона с рибавирином (при 1 генотипе) обеспечивает устойчивый вирусологический ответ в 45 % случаев.
Естественное течение хронического вирусного гепатита С характеризуется формированием фиброза печени, прогрессирование которого приводит к развитию цирроза печени. Использование препаратов интерферонового ряда и ненуклеозидных аналогов вероятно способно замедлить прогрессирование фиброза печени и снизить частоту формирования гепатоцеллюлярного рака. Вместе с тем, можно отметить один обнадеживающий факт, что даже при отсутствии биохимического и вирусологического ответа, у больных, получавших интерфероны, отмечается позитивный гистологический ответ, характеризующийся уменьшением выраженности воспалительного процесса в печени. Однако, значительные экономические затраты, связанные с лечением, а также высокая частота развития нежелательных побочных реакций от лечения, снижают приверженность пациентов к терапии.
В этой связи, понятен интерес исследователей, направленный не только на повышение эффективности противовирусной терапии, но и на снижение частоты развития нежелательных явлений, возникающих на фоне лечения. Следует отметить, что более 25 % пациентов, имеющих 1 генотип, «уходят из терапии», а Shiffman M.L. (2006) уверен, что больные с 1 генотипом, имеющие высокую «вирусную нагрузку» и фиброз печени, на терапию не отвечают. T.E.DantzlerP.J. et. al. (2003), Thuiuvath et. al. (2005), убеждены в неэффективности (в 50-60 % случаев) стандартных схем терапии хронического гепатита С, предлагая усилить терапию амантадином с увеличением дозы рибавирина, обосновывая это получением биохимического ответа у 47 %, а вирусологического - у 25-30 % пациентов с сохранением его в 11-13 % случаев.
В исследованиях T.Bizollon et.al., (2005) у больных с генотипом 1 (82 %), с использованием амантадина (200 мг ежедневно в течение 48 недель), получен биохимический ответ в 75 %, а устойчивый вирусологический ответ - в 33 % случаев. Stauber R.E. (2004), считает, что «тройная терапия» длительностью 3 месяца обеспечивает ранний вирусологический ответ в 34 % случаев, с сохранением устойчивого вирусологического ответа только у 15 % больных.
Olveria A., et.al. (2003), включил в комплексную терапию амантадин 39 больным с 1 генотипом, не ответившим на терапию интерфероном и рибавирином. Вирус не выявлялся у 12,8 % больных в течение 48 недель, и у 5,1 % пациентов после 24 недель терапии. Вирусологический ответ получен в 26,3 % случаев, а устойчиво сохранился - у 10,5 % больных.
Существующая противовирусная терапия не обеспечивает ожидаемого терапевтического эффекта, вызывая нежелательные реакции (анемия, депрессия, почечная патология и другие).
В патогенезе HСV-инфекции существенное значение имеет репликативная активность вируса и его взаимодействие с иммунной системой человека, поскольку элиминация вируса обеспечивается адекватным иммунным ответом, а недостаточная интенсивность иммунного воспаления способствует персистенции вируса. Улучшить качество проводимой терапии, с включением в комплекс лечебных мероприятий иммуномодуляторов, модулирующих реакции иммунного ответа (синтез цитокинов) попытались V.K. Rustgi (2005), L. Milazzo (2006),.
Особое значение в медицинской практике приобрело лечение хронического гепатита С, при котором блокада системы интерферона имеет серьезные последствия и сильно ограничивает (затрудняет) терапевтические подходы. Что достигается лечением хронического гепатита С препаратами интерферона и рибавирином? Снижение «вирусной нагрузки?» Но эта «вирусная нагрузка возникает в результате длительной поддержки пороговой репликации путем перестройки иммунной системы и, особенно, баланса цитокинов.
Даже если не предавать значения полученной у 40 % больных резистентности к препаратам интерферона, то сроки лечения у хорошо отвечающих на терапию пациентов позволяют говорить, что современная терапия гепатита С, с точки зрения стратегии экспрессии вирусного генома, при длительном применении нуждается в корректировке.
Вирус гепатита С не дает прямого цитопатического эффекта, цитолиз гепатоцитов не связан с активной репродукцией вируса, или действием его белков на клеточные функции. Репликация РНК обеспечивает эффективную индукцию активности протеинкиназы (PKR), определяющей функциональный ответ клеток на действие интерферона, оказывающего прямое действие на репликацию РНК вируса гепатита С. Если с рибавирином можно обсуждать опосредованные влияния на вирусную репродукцию, то для амантадина существует только одна мишень среди вирусных белков, это белок р7, являющийся аналогом гриппозного белка М2. Препараты адамантанового ряда, действуя как блокаторы вирусспецифических ионных каналов, не позволяют выявить в его структуре адамант связывающие сайты, но другие производные этой группы, могут оказаться более эффективны в подавлении функции белка р7 вируса гепатита С. Большие перспективы связываются с соединениями борадаматана, которые связываются с CD81-рецепторами, специфичными для гепатита С на клетках печени.
Основываясь на изменениях в структуре гена белка NS5a (являющегося ключевым в жизненном цикле и патогенности вируса гепатита С), показано, что белок является прямым ингибитором дс-РНК зависимой протеинкиназы PKR, подавляет индукцию противовирусной защиты к интерферонам. В структуре белка NS5a идентифицирован домен («область детерминации чувствительности к интерферону» - ISDR), который детерминирует связывание белка NS5a с протеинкиназой PKR, блокируя ферменты. Резистентность к интерферону реализуется через связывание белка NS5a с PKR, блокируя процесс трансляции, в результате не происходит индуцированной интерфероном остановки трансляции, а вирусная РНК эффективно транслируется в инфицированных клетках, что имеет принципиальное значение для развития репликативного цикла вируса.
Возвращаясь к белку NS5a, необходимо сказать, что он приводит к нарушению окислительного фосфорилирования в митохондриях и усилению генерирования свободных радикалов, за счет освобождения кальция из эндоплазматического ретикулума в цитоплазму, вызывая активацию транскрипционного фактора NF-kb, который обрывается при добавлении антиоксидантов. Но активация NF-kb может обеспечить антиапоптический эффект в развитии инфекционного процесса и приводить к трансформации гепатоцитов.
Развитие воспалительного процесса в печени и презентация вирусных антигенов на поверхности гепатоцитов приводит к активации иммунных реакций, направленных на лизис зараженных клеток. При персистенции вируса постоянная презентация вирусных антигенов активно поддерживает иммунный ответ Т-лимфоцитов, поддерживая деструктивный процесс, в котором участвуют как СD 8+, так и CD4+ - Т-лимфоциты, определяющие эрадикацию вируса или переход инфекции в стадию персистенции. Иммунный ответ, контролируемый CD4+-лимфоцитами, подразделяется на тип 1 (Th-1) и тип 2 (Th-2). Th-2 продуцируют ИЛ-4 и ИЛ-10, синтезирующих специфические антитела, осуществляющие контроль за Th-1-иммунным ответом.
Функции ИЛ-10 детально исследованы в связи с анализом природы резистентности к интерферонотерапии. Развитие иммунного ответа, контролируемого ИЛ-10, связано с Th2-клетками, что сопровождается активной секрецией этими клетками и ИЛ-4, и ИЛ-10. Последний подавляет синтез и ИЛ-1, и ИЛ-6, и ФНО, данное обстоятельство не принимается во внимание при исследовании резистентности к интерферонам 1-го типа при проведении интерферонотерапии, а именно дисбаланс между Th-1и Th-2 ответом, при инфекции, вызванной вирусом гепатита С, ответственен за прогрессивное течение заболевания и отсутствие элиминации возбудителя. Преобладание Th-1-ответа приводит к усилению воспалительно-некротического компонента, активируя фиброз, а сильный Th-2-ответ является основой для развития хронического персистентного инфекционного процесса.
Таким образом, повышенный синтез Th-1-цитокинов необходим для активной защиты от инфекции, вызванной вирусом гепатита С, а Th-2-цитокины, подавляя иммунные реакции, усиливают возможность перехода острого инфекционного процесса в хронический, при этом становится очевидным, что оценка типа иммунного ответа является основой не только для прогноза течения заболевания, но и для адекватной терапии.
Понимание негативных функций ИЛ-10 и противостояния вируса гепатита С интерферонотерапии ставит вопрос о поиске других подходов к улучшению лечения гепатита С (разработка селективных ингибиторов ИЛ-10 для повышения эффективности терапии, улучшения качества проводимой терапии с включением в комплекс лечебных мероприятий иммуномодуляторов, модулирующих реакции иммунного ответа, воздействием на иммунокомпетентные клетки с индукцией синтеза цитокинов.
L.Milazzo (2006), не ответившим на терапию интерфероном и рибавирином больным, применял талидомид, модулирующий CD8+ лимфоциты, блокирующий ФНО. Автор выявил корреляцию цитолиза и активности ФНО.
Лечение, особенно хронической формы, гепатита С требует индивидуального подхода, поскольку характер патологического процесса у конкретного пациента определяется возрастом, сопутствующей патологией, длительностью заболевания, генотипом вируса, уровнем «вирусной нагрузки», наличием и выраженностью нежелательных реакций на препараты, связанные с проводимой терапией, что немаловажно по экономическим возможностям больного.
Перспективы применения индукторов интерферона более значительны, чем применение препаратов интерферона, поскольку противовирусная активность индукторов интерферона, совпадает с активностью экзогенных интерферонов, с отсутствием и сведением к минимуму нежелательных реакций, присущих длительной интерферонотерапии, что является весьма привлекательным, поэтому индукторы интерферона, как реактиваторы системы интерферона, начинают постепенно вытеснять препараты рекомбинантного интерферона.
Таблица 1
Влияние циклоферона на инфекционную активность HCV культуре клеток МТ-4
|
Пробы культуральной жидкости из ВГС инфицированных культур клеток МТ-4, обработанных: |
Титры HCV (Lg ТЦД50 /20 мкл) на день |
|
|
4-й день |
7-й день |
|
|
Циклофероном |
1,5 |
6,0 |
|
Контроль, без обработки |
3,6 |
11,5 |
Антивирусное действие индукторов интерферона реализуется через механизм активации цитокинов, подавляемых при вирусном инфицировании, что подтверждено изучением влияния циклоферона, как наиболее безопасного, хорошо изученного и охарактеризованного препарата, на репродукцию вируса гепатита С и экспрессию м РНК цитокинов в клеточных культурах. В неинфицированных клетках присутствует мРНК всех исследованных цитокинов, за исключением ИЛ-8. В инфицированных HСV клетках ингибируется активность альфа/гамма-ИФН, ИЛ-2,-4,-6, также заметно (до 11.5 lg) нарастают титры вируса. Обработка инфицированных клеток циклофероном приводит к восстановлению активности мРНК цитокинов на фоне ингибиции вируса (табл. 1.).
Следовательно, антивирусное действие циклоферона реализуется через механизм активации цитокинов, подавляемых при вирусном инфицировании. Результаты исследования мРНК цитокинов в линии клеток выявили конститутивное присутствие мРНК ИФН-альфа, IL-2, -6, -8, -10, -12, -18 и ФНО-альфа. При обработке инфицированных HCV клеток выявились мРНК всех исследованных цитокинов, за исключением ИФН-альфа и ФНО.
Таблица 2
Исследование цитокинового спектра линии клеток человека SW-13
|
Цитокиновые мРНК |
Клетки+- Циклоферон |
Клетки+вирус +циклоферон |
Вирус |
|
|
Контроль клеток |
Контроль вируса |
|||
|
IFN-альфа |
+ |
- |
+ |
+ |
|
IFN-гамма |
+ |
+ |
- |
- |
|
IL-1β |
- |
+ |
- |
- |
|
IL-2 |
+ |
+ |
+ |
+ |
|
IL-4 |
+ |
+ |
- |
- |
|
IL-6 |
+ |
+ |
+ |
+ |
|
IL-8 |
+ |
+ |
+ |
- |
|
IL-10 |
+ |
+ |
+ |
+ |
|
IL-12 |
+ |
+ |
+ |
+ |
|
IL-18 |
+ |
+ |
+ |
+ |
|
ФНО |
+ |
- |
+ |
+ |
Полученные данные подтверждают положение, что при вирусных инфекциях цитокиновый ответ развивается по клеточному типу. Вместе с тем иммунный ответ при вирусных инфекциях строго не вписывается в двойственную природу Т-клеточного ответа. Определенную роль играет IL-4, ингибируемый HCV, но эта ингибиция преодолевается циклофероном, обеспечивая подавление инфекционной акти=вности. Циклоферон оказался перспективен для снижения инфекционной активности HCV, поскольку (в 1,9-2,4 раза) подавляет активность вируса, контролируя гены клеточного и гуморального иммунного ответа.
В связи с этим, целесообразно включение циклоферона в терапию хронического гепатита С, с целью ее совершенствования, уменьшения выраженности побочных эффектов и снижения экономических затрат, связанных с лечением. Целью включения циклоферона в комплексное лечение явилась оценка эффективности комплекса комбинированной противовирусной терапии больных, страдающих хроническим вирусным гепатитом С, раннее не ответивших на терапию интерфероном и/или рибавирином, а также изучение возможности нивелирования побочных эффектов, возникающих при применении химиотерапевтических средств и интерферонов.
Нами в ходе скрининга отобрано 78 больных, с верифицированным диагнозом «хронического вирусного гепатита С» (в фазе репликации) с 1b-й генотипом HCV. Перерыв от окончания ранее полученной стандартной терапии составлял от трех до шести месяцев. Пациенты были лицами мужского пола в возрасте от 18 до 50 лет, их средний возраст составил 32,6 ± 11,5 лет. Несмотря на то, что у 15 пациентов длительность инфицирования НСV превышала 5 лет, признаков цирроза печени не было выявлено ни у одного из обследованных.Включение пациентов в исследование производилось после тщательного клинико-инструментального обследования (с обязательным обследованием функции щитовидной железы), в сыворотке крови которых не обнаруживались маркеры других вирусных гепатитов. У всех наблюдаемых больных методом PCR определялась РНК HCV. Молекулярно-биологическое исследование подтвердило наличие у пациентов 1b генотипа вируса, а стартовый уровень цитолиза (АлАт) превышал уровень нормы не более чем в 2-5 раз.
Больные рандомизированно (с применением «метода конвертов») разделены на 2 группы (по 39 человек): однородные по полу, возрасту, наличию сопутствующих заболеваний и активности патологического процесса. Больные 1-й группы, получали реаферон (3 млн. МЕ в течение 48 недель, 3 раза в неделю), синтетический аналог нуклеозидов веро-рибавирин (600-1000 мг/ сутки в зависимости от массы тела) и дополнительно иммуномодулятор полиоксидоний (один раз в неделю в течение 48 недель).
Больным 2-ой группы назначался реаферон (3 млн. МЕ в течение 48 недель, 3 раза в неделю), синтетический аналог нуклеозидов - веро-рибавирин (600-1000 мг/ сутки в зависимости от массы тела) и дополнительно циклоферон (12,5 % раствор по 4 мл внутримышечно на 1, 2, 4, 6, 8 дни, а далее один раз в 3 дня в один день с введением реаферона) в течение 48 недель. Первичную оценку эффективности лечения с применением «тройных» схем у больных, ранее не ответивших на терапию, проводили через 12 недель лечения. При наличии у пациентов «биохимического» ответа на терапию (снижение АлАт в два и более раз) лечение продолжали до 48 недель. При отсутствии первичного биохимического ответа впервые три месяца терапии больного исключали из исследования.
Сравнительную эффективность терапии проводили спустя 72 недели (от начала лечения). Оценивался биохимический (цитолиз) и вирусологический ответ (отсутствие HCV, определяемое методом PCR). Клиническая симптоматика у наблюдаемых больных соответствовала течению заболевания. Большинство больных предъявляли жалобы на немотивированную слабость, снижение аппетита, периодически возникающую тошноту 56 и 36 % соответственно).
У части больных (7,6-21,0 %) наблюдалась головная боль и головокружение. Признаков геморрагического синдрома не было ни у одного больного. Вместе с тем, у 12-16 % больных выявлены внепеченочные проявления, в виде телеангиэктазий и сосудистых звездочек. У 15 % больных проявления плоского лишая, связывалось с манифестацией хронического гепатита. Стартовые значения АлАТ у пациентов обеих групп, превышали нормальные значения в 2-2,5 раза, и составляли от 90 до 103 ед/л. Уровень билирубина не отличался от значений здоровых лиц. Гематологические показатели пациентов также не выходили за пределы нормальных значений.
Проведение трехмесячного курса лечения показало удовлетворительную переносимость «тройной терапии» у пациентов. При мониторировании нежелательных реакций ни у одного из больных не выявлено серьезных осложнений, которые могли бы послужить основанием для прекращения терапии. Любопытные данные получены при изучении характера нежелательных явлений у больных. При стандартном наборе выявляемых побочных действий (табл. 3.) препаратов, заявленных в инструкции по их медицинскому применению, их выраженность и продолжительность были различны. Меньше всего нежелательных реакций на проводимую терапию (0,8, в пересчете на одного больного у пациентов, в схему лечения которых был включен циклоферон).Выраженность реакций была слабой (+), тогда как у больных второй группы их было 1,8 на одного больного, а выраженность реакций оценена как умеренная (++) и выраженная (+++). Лихорадка, отмечавшаяся практически у всех пациентов, в течение первых 2-3 дней, в последующем исчезала, больные хорошо переносили лечение, что не мешало пациентам вести привычный для них образ жизни. Часть пациентов жаловалось на нарушение сна, наличие кожного зуда, болей в суставах, немотивированной депрессии с элементами агрессивности. Все пациенты в начале терапии отмечали незначительное снижение массы тела, однако у лиц 1-ой группы чаще, чем у пациентов, получавших циклоферон, наблюдалось значительное снижение массы тела (2 пациента за период лечения похудели на 10,0 кг, а их вес не восстановился к концу терапии).
Вместе с тем нежелательные реакции - это лишь субъективные ощущения дискомфорта, тем более, что, применяя терапию в щадящем режиме, ни у одного пациента не выявили нарушений со стороны эндокринной системы, грубой неврологической симптоматики, а также существенных изменений в гемограмме.
Таблица 3
Характер нежелательных реакций у больных хроническим гепатитом С, получавших противовирусную терапию
|
Клинические симптомы |
Выявление побочных реакций (в %) в группах больных, получавших: |
|||
|
Реаферон+рибавирин+ |
Реаферон+рибавирин+ |
|||
|
Абс. xисло больных |
% |
Абс.число больных |
% |
|
|
1 |
2 |
3 |
4 |
5 |
|
Лихорадка |
22 |
56,4 |
15 |
38,5 |
|
Головная боль |
14 |
20,2 |
12 |
30,1 |
|
Боли в суставах |
14 |
20,2 |
5 |
12,8 |
|
Депрессия |
8 |
20,5 |
- |
- |
|
Бессонница |
6 |
125,4 |
- |
- |
|
Кожный зуд |
3 |
7,7 |
- |
- |
|
Сыпь |
- |
- |
- |
- |
|
Боли |
4 |
10,3 |
- |
- |
|
Снижение массы тела |
2 (-10кг) |
5,1 |
- |
- |
Существенным представлялась нам оценка биохимических и вирусологических показателей после окончания трехмесячной терапии: первичная биохимическая ремиссия, в группе больных получавших тройную терапию интерферон + рибавирин + полиоксидоний, получена у 11 (28,2 %) больных из 39, а в группе пациентов, получавших интерферон + рибавирин + циклоферон у 18 (46,2 %) больных из 39 (табл. 7).
Анализ содержания РНК HCV в сыворотке крови показал ее отстуствие, только у 1 пациента, получавшего дополнительно полиоксидоний и у 2 пациентов, получавших циклоферон.
Таблица 4
Первичный биохимический и вирусологический ответ на терапию
|
Клинические симптомы |
Эффективность терапии в группах больных получавших: |
|||
|
Реаферон+рибавирин+ |
Реаферон+рибавирин+ |
|||
|
Абс. число |
% |
Абс. число |
% |
|
|
Снижение АлАТ в 2 и более раз |
11 |
28,2 |
18 |
46,1 |
|
Отрицательная реакция в PCR |
1 |
2,3 |
2 |
4,6 |
Таким образом, после проведения больным ХГС с генотипом 1b трехмесячного курса «тройной» терапии пациентам, раннее «не ответившим» на стандартную терапию, дальнейшее лечение в течение 36 недель продолжили в первой группе 11 пациентов, а во второй группе 18 пациентов.
К 48-й неделе лечения вирусологический ответ (отрицательная реакция HCV) получен у 4 из 11 (36,4 %) человек, продолживших лечение [по схеме интерферон+рибавирин+ полиоксидоний], и у 16 (88,9 %) из 18 пациентов, получавших терапию [по схеме интерферон+рибавирин+циклоферон].
Диспансерное наблюдение в течение 6 месяцев за больными, получавшими «тройную терапию», показало, что рецидив инфекции (положительная реакция HCV) наблюдался у 2 пациентов в первой группе и у трех пациентов во второй группе, составив соответственно 25 и 20 %.
Оптимальный терапевтический эффект получен при применении циклоферона, что нашло подтверждение в биохимическом и вирусологическом ответах (через 72 недели наблюдения) у 66,6, против 27,2 % пациентов.
Получен клинический эффект, проявляющийся полным ответом (по PCR и АлАТ) у 38,4 % больных, с сохранением устойчивого вирусологического ответа (18 месяцев наблюдения) у 30,7 % больных, а биохимического ответа - у 41,0 % пациентов, тогда как, у больных группы сравнения, полный ответ выявлен у 10,3 % с сохранением устойчивого вирусологического ответа у 7,6 %, а биохимического - у 20,5 % больных.
Показано позитивное влияние проводимой терапии у больных 2-ой группы, на показатели качества жизни, большинство шкал опросника качества жизни «SF-36» пациентами оценено максимально (колебания от 90 до 100 баллов), что позволяет говорить об удовлетворенности результатами терапии.
Таблица 5
Эффективность «тройной» терапии больных, страдающих ХВГС
|
Срок (в нед) от начала терапии |
Показатели эффективности |
Эффективность терапии в группах больных, получавших: |
|||
|
Реаферон+ рибавирин+ |
Реаферон+рибавирин+ циклоферон (n=18) |
||||
|
Абс. число |
% |
Абс. число |
% |
||
|
24 |
Нормализация уровня АлАТ |
11 |
100 |
18 |
100 |
|
Отрицательная РНК HCV (в PCR) |
3 |
27,2 |
4 |
22,2 |
|
|
36 |
Нормализация уровня АлАТ |
10 |
90,9 |
15 |
83,3 |
|
Отрицательная РНК HCV (в PCR) |
3 |
27,2 |
15 |
83,3 |
|
|
48 |
Нормализация уровня АлАТ |
9 |
81,8 |
16 |
88,9 |
|
Отрицательная РНК HCV (в PCR) |
4 |
36,4 |
16 |
88,9 |
|
|
72 |
Нормализация уровня АлАТ |
8 |
36,3 |
16 |
28,2 |
|
Отрицательная РНК HCV (в PCR) |
3 |
27,2 |
12 |
66,6 |
|
Таблица 6
Ответ на противовирусную терапию больных с хроническим гепатитом С
|
Препараты |
Ответ на тройную терапию ХВГС, % |
|||
|
Ответ по АлАТ через |
Полный по ПЦР и АлАТ |
Ответ по PCR через |
Ответ по АлАТ через 18 месяцев |
|
|
Реаферон, рибавирин, |
28,2 |
10,3 |
7.6 |
20,5 |
|
Реаферон, Рибавирин, |
46,1 |
38,4 |
30,7 |
41,0 |
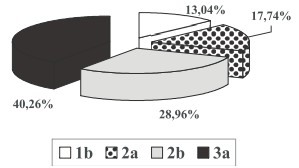
Рис. 1. Генетическая принадлежность HCV-RNA исследуемых больных
Эффективность комбинированных схем противовирусной терапии зависела от исходного состояния интерферонового ответа пациентов.
Таблица 7
Побочные эффекты терапии (частота прекращения лечения, необходимость снижения дозы, другие нежелательные проявления)
|
% больных, получивших терапию по схеме: |
|||
|
Последовательное применение препарата ИФН и циклоферона |
Сочетанное применение препарата ИФН и циклоферона |
Монотерапия препаратом ИФН- |
|
|
Необходимость отмены лечения |
- |
4 |
4 |
|
Необходимость снижения дозы |
- |
7 |
12 |
|
Нежелательные проявления терапии: |
|||
|
Анемия |
2 |
5 |
9 |
|
Лейкопения |
6 |
8 |
12 |
|
Снижение Массы тела |
6 |
16 |
22 |
|
Гриппоподобный синдром |
32 |
67 |
78 |
|
Артралгии |
5 |
11 |
10 |
|
Симптомы ЖКТ |
3 |
6 |
8 |
|
Психиатрические симптомы |
12 |
25 |
30 |
|
Кожные проявления |
5 |
8 |
12 |
|
Нарушение функции щитовидной железы |
4 |
4 |
6 |
Наибольшие успехи в терапии хронического гепатита В (ХГВ) получены при проведении интерферонотерапии, но частота стойкого ответа при использовании высоких доз альфа-интерферона не более 30-40 %, тогда как, при использовании пегилированных интерферонов выше. Другим из предложенных вариантов комбинированной терапии ХГВ является применение препаратов, модулирующих Т-клеточный иммунитет, показано успешное применение для терапии ХГВ комбинации альфа-интерферона с тимозином.
Нами в многоцентровом сравнительном исследовании изучена эффективность и переносимости комбинированной противовирусной терапии больных ХГВ, не ответивших на 24 недельный курс ламивудина. В единый протокол лечения включены 260 больных с верифицированным диагнозом ХГ B. Комбинированную терапию назначали при наличии минимальной или умеренной активности трансаминаз (уровень АлАТ, превышал норму не более чем в 1,5-2 раза) и фазы репликации (выявление ДНК HBV в сыворотке крови методом PCR), а также желания больного.
Полный курс лечения был завершен у 206 пациентов (93,6 %).
В соответствии с рандомизацией (использован «метод конвертов») больные хроническим гепатитом В разделены на три группы.
В 1-й группе больных (90 человек) применялся циклоферон [12,5 % 1 раз в сутки из расчета 5-8 мг/кг веса (у пациента с весом до 50 кг 2,0 мл на введение, более 60 кг 4,0 мл на введение) два дня подряд, а затем 3 раза в неделю (в понедельник, среду, пятницу)] и ламивудин (перорально из расчета 3 мг/кг веса, но не более 100 мг в сутки, ежедневно, длительность курса 24 недели).
2 группа больных (90 человек), получала альфа-интерферон [(реаферон) (3 млн. МЕ, но не более 6 млн. МЕ 1 раз в сутки 3 раза в неделю (в понедельник, среду и пятницу)] и ламивудин (3 мг/кг веса, но не более 100 мг в сутки, ежедневно), длительность курса 24 недели.
Больные 3 группы (80 человек) получали реаферон по 3 млн. МЕ [но не более 6 млн. МЕ] и циклоферон (12,5 % раствор) 5-8 мг/кг веса два дня подряд, а затем 3 раза в неделю (в понедельник, среду, пятницу)].
Среди наблюдаемых больных 140 мужчин и 120 женщин в возрасте от 20 до 40 лет (средний возраст 34,6±0,8 лет). Средняя масса тела составила 79,2±12,8 (от 53 до 127) кг. Давность инфицирования, которую определяли от момента появления хотя бы одного фактора риска или перенесенного острого гепатита В составила от 6 месяцев до 5 лет.
Ведущим синдромом был астеновегетативный, проявлялся нарушением сна, утомляемостью, потливостью, снижением аппетита, эмоциональной лабильностью, регистрируемый в 62-68 % случаев. Диспептический (тошнота, отрыжка, чувство распирания, боли в эпигастрии и правом подреберье, запор и/или понос), выявляемый в 44-50 % случаев.
Эти симптомы обусловлены не только поражением печени, но и желчевыводящих путей и гастродуоденальной зоны. Однако самым частым клиническим проявлением было увеличение печени в 85-87 % случаев. Печень выступала на 2-5 см из-под реберной дуги. Увеличение селезенки отмечалось не всегда. «Малые» печеночные знаки (телеангиэктазии, пальмарная эритема и др.) регистрировались лишь у части больных.
Гиперферментемия регистрировалась у 42 % больных и не превышала норму более чем в 1,5-2 раза, что соответствовало минимальной активности трансаминаз, у остальных больных, уровень АЛаТ и АСаТ не превышал норму. В ряде случаев отмечалась билирубинемия, ее уровень превышал норму не более чем в 2 раза, определялась репликация вируса [(ДНК HBV (+)], маркеры вирусного гепатита В [HBsAg (+), HBeAg (+), HBcorAB(+)]. Диспротеинемия с гипергаммаглобулинемией отмечалась у 15-18 % больных.
Эффективность лечения оценивалась у 84 человек 1-ой группы, у 78 - второй группы и у 68 человек третьей группы (не учитывались результаты лечения больных с длительностью терапии менее 3-х месяцев).
Стабильным ответом на противовирусное лечение больных ХГ В считали нормализацию АлАТ, в случае регистрации первоначально гиперферментемии, и элиминацию вируса (отрицательная реакция ДНК HBV) через 24 недели комбинированной терапии.
Таблица 8
Клиническая симптоматика у наблюдаемых больных
|
Симптомы/частота выявления, в % |
1-я группа больных |
2-я группа больных |
3-я группа больных |
|
Диспептический |
45,2 |
50,0 |
44,1 |
|
Астеновегетативный |
66,6 |
67.9 |
61,7 |
|
Гепатомегалия |
86,9 |
84,6 |
85,2 |
|
Спленомегалия |
28,5 |
29,4 |
29,4 |
|
Иктеричность кожи и склер |
25,0 |
20,5 |
23,5 |
Наблюдение за больными показало, что 57,7 % больных, получавших терапию циклофероном и ламивудином, а так же 76,4 % больных, лечившиеся интерфероном + циклофероном, обращали внимание на значительное субъективное улучшение самочувствия (повышение работоспособности и исчезновение слабости).
Пациенты, получавшие реаферон + ламивудин, субъективно оценивали терапию негативно (53,3 % больных предъявляли жалобы, отмечали ухудшение самочувствия и снижение работоспособности), а всего лишь 22,2 % больных, оценивали свое состояние здоровья как не изменившееся.
Показатели цитолиза улучшались вне зависимости от используемого препарата, указывая на уменьшение интенсивности синдрома цитолиза. Исключение составляли 1 больной из второй и 2 больных из третьей группы, у которых сохранялась гиперферментемия до конца терапии. Однако при обследовании больных через 6 месяцев после окончания терапии нами зарегистрированы биохимические рецидивы у 3-х человек 1-ой группы, у 2-х из второй группы и у 4-х из третьей группы.
Таким образом, любой вариант комбинированной противовирусной терапии приводил к обратному развитию синдрома цитолиза у пациентов, имеющих гиперферментемию, перед началом проведения курса лечения.
Таблица 9
Эффективность терапии (в %) больных ХГВ противовирусными препаратами
|
Фазы ремиссии |
1 группа больных, (n=84) |
2 группа больных (n=78) |
3 группа больных, (n=68) |
|
Стабильная |
47,6 |
50,0 |
58,8 |
|
Длительная |
35,7 |
39,7 |
44,1 |
У больных, получавших интерферон + циклоферон, стабильная ремиссия получена у 58,8 % больных с сохранением ее до конца курса терапии. Кроме того, у 4 пациентов (5,8 %) имела место неполная ремиссия, с отсутствием в сыворотке крови HBeAg при наличии высоких титров HВeAb, но сохранением ДНК HBV. В то же время, через 6 месяцев после окончания лечения, у 10 пациентов (14,7 %) возобновилась вирусологическая активность процесса с сохранением нормальных показателей АлАТ, при этом у 6 пациентов, отсутствовал в сыворотке крови HBeAg, сохранялись HВeAb, но выявлялась DNA HBV, а у 4-х оставшихся отмечалось появление и HBeAg и DNA HBV. Вирусологический ответ (снижение ДНК HBV до неопределяемых цифр), после курса терапии ламивудином с циклофероном был ниже, в сравнении с применением ламивудина и реаферона (составив 47,6 %, против 50,0 %), а ремиссия сохранялась длительно (соответственно у 35,7 и 39,7 % больных).
Используемые противовирусные препараты оказывали выраженное действие и на наступление сероконверсии.
Так, элиминация HBeAg с появлением анти-HВeАb выявлялась у 57,1 % больных, получавших циклоферон и ламивудин, у 64,1 % пациентов, лечившихся интерфероном с ламивудином и у 66,2 % больных, в терапию которых включен интерферон с циклофероном.
За время наблюдения (в течение 24 недель после окончания терапии) частота стойкого ответа, с сохранением нормального уровня трансаминаз, отсутствием HBeAg, DNA HBV и появлением HBeAb у наблюдаемых нами больных (1-й, 2-ой и 3-ей групп) составила, соответственно, 39,2, 41, и 45,5 %.
Таким образом, лечение закончило 84 человека в 1-ой группе, 78 пациентов 2-ой и 68 больных 3-й группы.
Больные ХГ В удовлетворительно переносили терапию. Нежелательные реакции оценивались у больных, включенных в исследование. По медицинским показаниям лечение было прекращено у 3-х человек 1-ой группы (из-за обострений сопутствующей патологии гастродуоденальной системы), у 8 человек 2-ой группы (у 2-х из-за выявленного аутоиммунного тиреоидита, у 3-х из-за цитопенического синдрома и у 3-х человек - из-за наступления депрессии). 4 больных второй группы самостоятельно прекратили лечение раньше срока (из-за снижения массы тела (1 человек), выпадения волос (3 человека).
В третьей группе больных, несмотря на хорошую переносимость интерферона в комбинации с циклофероном, 12 пациентов отказались продолжать курс лечения до ее окончания.
Таблица 10
Регистрация сероконверсии (HBeAg на анти-Hbe Ab) у больных, получавших противовирусную терапию
|
Установление ремиссии от начала лечения |
1 группа больных (n=84) |
2 группа больных (n=78) |
3 группа больных (n=68) |
|
Через 3 месяца |
36,9 |
43,5 |
50,0 |
|
После окончания курса |
57,1 |
64,1 |
66,2 |
|
Через 6 месяцев |
39,2 |
41,0 |
45,5 |
Больные 3 группы, получавшие интерферон с циклофероном, хорошо переносили терапию, нежелательные реакции на фоне лечения регистрировались в 13,75 % случаев (у 2 больных экзантема на второй неделе применения препарата, у 4-х пациентов обострение нейродермита и у одного больного обострение хронического эрозивного гастрита, а у 5 человек наблюдалось выпадение волос). Несмотря на незначительные побочные эффекты от терапии 68 больных провели курс лечения полностью, а 12 человек не закончили его.
Больные 2-ой и 3-ей групп наблюдения переносили лечение несколько хуже, побочные реакции регистрировались чаще, чем у больных третьей группы, но они были умеренно выражены и обратимы.
Гриппоподобные явления в виде слабости, усталости, повышения температуры, головокружения, головных и/или суставных болей отмечались, у 71,1 % больных 2-й группы, назначение симптоматических корригирующих препаратов позволило купировать эту симптоматику.
У 52 (57,7 %) больных 2-й группы, через 3 месяца применения противовирусной терапии, появлялись нарушения со стороны психо-эмоциональной сферы. Чаще встречалась аффективная возбудимость на минимальные раздражители у 47,1 % больных, плохой сон и снижение массы тела у 34,4 % больных, а так же чувство тревоги в 30,0 % случаев, не требующее назначения антидепрессантов. В то же время, у 35,0 % больных, лечившихся реафероном и ламивудином, выявлена депрессия, потребовавшая назначение антидепрессантов.
Таблица 11
Побочные эффекты противовирусной терапии
|
Выявленные побочные эффекты / частота выявления в % |
1-я группа больных |
2-я группа больных |
3-я группа больных |
|
Гриппоподобный синдром |
0 |
71,1 |
0 |
|
Артралгии |
0 |
60,0 |
0 |
|
Миалгии |
0 |
57,7 |
0 |
|
Обострение хронического панкреатита |
3,33 |
5,6 |
0 |
|
Депрессия |
0 |
34,4 |
0 |
|
Снижение либидо |
0 |
30,0 |
0 |
|
Выпадение волос |
0 |
34,4 |
6,25 |
|
Цитопенический синдром |
0 |
14,4 |
0 |
|
Снижение веса |
0 |
34,4 |
0 |
|
Кожные высыпания |
3,3 |
3,3 |
7,5 |
Нейтропения (менее 0,75 · 109/л) отмечалась у одного пациента 2-ой группы, назначение адекватной терапии с временным снижением доз интерферона до 3 млн. МЕ дало возможность избежать отмены препарата и нормализовать показатели крови. У пяти больных 2-ой группы имело место преходящее снижение числа нейтрофилов и тромбоцитов, у трех из них пришлось отменить терапию.
Снижение уровня гемоглобина (менее 100 г/л) наблюдалось у 5 больных из 2-ой группы, использование препаратов железа позволило контролировать это нежелательное явление.
Уровень тиреотропного гормона на фоне лечения, повышался у 9 больных 2-ой группы (10,0 %), у 2 пациентов выявлен аутоиммунный тиреоидит, потребовавший отмены терапии.
Среди других побочных эффектов следует остановиться на выпадении волос у 34,4 % больных, получавших реаферон с ламивудином. Это особо беспокоило женщин, часть из них отказались от терапии, несмотря на убеждение врачей продолжать лечение. Этот симптом частично купировался применением шампуней с цинком.
Таким образом, эффективность комбинированной терапии с применением интерферона и циклоферона у больных ХГВ, не ответивших ранее на монотерапию ламивудином, позволяет добиться ремиссии у 58,8 % больных, указывая на высокий фармакотерапевтический эффект, однако устойчивый биохимический и вирусологический ответ сохраняется лишь у 44,1 % больных. При применении же циклоферона и ламивудина полная стабильная ремиссия (биохимическая и вирусологическая) была достаточно высокой и наблюдалась в 47,6 % случаев, что сопоставимо с применением реаферона и ламивудина.
Проводимая противовирусная терапия оказывала выраженное действие и на частоту наступления сероконверсии. Элиминация HBeAg и появление анти-HВeАb регистрировалась в наблюдаемых нами группах больных в 57,1-66,2 % случаев, самая высокая у больных, получавших терапию циклофероном и интерфероном.
Необходимо обратить внимание, что у больных, не ответивших ранее на монотерапию ламивудином, и получавших позже различные препараты, мутантные штаммы не возникали, а эффективность терапии, за счет этого, возрастала до 35,7-44,1 %.
Таким образом, применение комбинированной терапии для лечения больных ХГ В, в частности, ламивудина не только с интерфероном-альфа, но и с циклофероном, перспективное направление в гепатологии.
Целью многоцентрового исследования, результаты которого приведены ниже, явилась оценка эффективности применения циклоферона (таблетированная форма) и ламивудина в виде монотерапии и комбинированной терапии (циклоферон+ламивудин) больных ХВГВ.
В исследовании принимало участие 300 человек. Пациенты разделены на три группы - 1-я группа (пациенты получали только таблетки циклоферона) - 100 человек; 2 группа (пациенты, получали только ламивудин) - 100 человек; 3 группа (комбинированная терапия циклофероном и ламивудином) - 100 человек.
Циклоферон применяли 1 раз в сутки, 3 раза в неделю (понедельник, среда, пятница) из расчета 10-15 мг/кг массы тела (4-6 таблеток на прием). Длительность курса 12 мес.
Ламивудин применяли 1 раз в сутки, ежедневно из расчета 3мг/кг массы тела, но не более 100 мг в сутки. Длительность курса 12 мес.
Основным критерием эффективности терапии являлся устойчивый ответ на отсутствие в сыворотке крови ДНК ВГВ через 6 месяцев после завершения лечения.
Среди лабораторных показателей часто регистрировалась гиперферментемия (уровень АЛаТ и АСаТ превышал норму в 4,5-8 раз).
У 36-42,0 % больных отмечалась билирубинемия, ее уровень не превышал норму более чем в 2 раза. У 11-13,0 % больных наблюдалось повышение уровня билирубина за счет неконъюгированной фракции, обусловленной нарушением процесса глюкуронирования.
Выраженность изменений уровней аминотрансфераз и билирубина зависела от степени активности печеночного процесса.
Улучшение состояния при проведении курсов противовирусной терапии отметили практически все пациенты. Так, 29 % больных, получавших ламивудин и 45 %, получавших циклоферон, сообщили о значительном улучшении самочувствия, но наиболее высоко субъективно оценили больные комбинированную терапию циклофероном и ламивудином 59 % больных оценили ее как значительное улучшение).
Таблица 12
Субъективная оценка эффективности терапии больными ХВГВ
|
Препарат |
Эффективность лечения (в%) |
||
|
Слабая |
Умеренная |
Значительная |
|
|
Циклоферон |
15 |
40* |
45* |
|
Ламивудин |
10 |
61* |
29* |
|
циклоферон+ ламивудин |
8.0 |
33* |
59* |
* - (р≤0,001) в сравниваемых группах
В целом эффективность применения различных схем терапии можно оценить как высокую. Среди обследованных пациентов не было человека, у которого лечение оказалось абсолютно неэффективным. Использование любой схемы терапии сопровождалось рядом положительных результатов: пациенты 1 и 3 групп отмечали более быстрое, чем у больных 2 группы повышение работоспособности и исчезновение слабости. У многих исследуемых сокращались размеры печени (у 22,4-58,3 % больных). В тоже время, более быстрое снижение уровня ферментов (АЛаТ и АСаТ) до нормы регистрировалось не только у больных получавших комбинированную терапию, но и монотерапию циклофероном.
Применение противовирусных препаратов приводит к снижению активности воспалительного процесса в печени. В то же время, более медленная нормализация трансаминаз у больных, получавших ламивудин, по-видимому, связана с отсутствием у противовоспалительного действия на ткань печени.
Таким образом, первичная биохимическая ремиссия регистрировалась в 12,9-24,5 % случаев, самый высокий ответ отмечался у больных, получавших комбинированную терапию (24,5 %).
Таблица 13
Эффективность терапии противовирусными препаратами больных хроническим гепатитом В
|
Виды ремиссии |
1 группа |
2 группа |
3 группа |
|||
|
N |
% |
N |
% |
N |
% |
|
|
Первичная биохимическая |
19 |
19,8* |
12 |
12,9 |
24 |
24,5* |
|
Отсутствие ремиссии |
8 |
8,3 |
10 |
10,8* |
3 |
3,06 |
|
Рецидив заболевания |
21 |
21,9 |
42 |
45,2* |
7 |
7,1 |
|
Стабильная |
32 |
33,3 |
41 |
44,1* |
53 |
54,08* |
* - значения (р≤0,005) отличающиеся от параметров групп сравнения
Стабильная ремиссия получена у 54,08 % больных, получавших комбинированную терапию. Вирусологический ответ (снижение ДНК ВГВ до неопределяемых цифр) после курса циклоферона был чуть ниже применения ламивудина (33,3 %, против 44,1 %). Кроме того, еще у 38 чел. (39,6 % больных), получавших циклоферон, отмечалась частичная биохимическая ремиссия с нормализацией трансаминаз во время лечения, лишь у 14,6 % больных она была длительной.
В группе больных, получавших ламивудин, частичная биохимическая ремиссия регистрировалась реже, чем вирусологическая (37,6 %, против 7,5 %), но у 25,8 % больных с вирусологической ремиссией возобновлялась репликация вируса через 3-6 месяцев после отмены препарата.
У больных, лечившихся комбинацией ламивудина и циклоферона, неполная ремиссия регистрировалась у 42 (42,8 %) человек: из них у 16 - биохимическая, а у 6 вирусологическая ремиссия, которая сохранялась в течение 6 месяцев после отмены препаратов.
Таблица 14
Частота неполной ремиссии у больных ХВГВ
|
Препараты |
Частота неполной ремиссии (в %) |
|||
|
Биохимическая |
Вирусологическая |
|||
|
После курса лечения |
Через 6 мес. |
После курса лечения |
Через 6 мес. |
|
|
Циклоферон |
38 (39,6)*** |
14 (14,6)* |
- |
- |
|
Ламивудин |
7 (7,5) |
5 (5,4) |
35 (37,6)*** |
11 (11,8) |
|
циклоферон+ |
30 (30,6)*** |
16 (16,3)* |
12 (12,2) |
6 (6,1) |
* - значения существенно (р≤0,005) отличающиеся в группе сравнения на данном этапе лечения
** - значения существенно (р≤0,005) отличающиеся от параметров до лечения в данной группе
В целом препараты хорошо переносились и давали минимальные побочные эффекты. В данном исследовании нежелательные реакции на фоне лечения противовирусными препаратами были зафиксированы у 2 пациентов, получавших циклоферон (2,08 %), у 4 человек принимавших ламивудин (4,3 %) и у 3 больных, лечившихся ламивудином и циклофероном (3,06 %).
Наиболее часто встречались обострения сопутствующей соматической патологии, особенно со стороны желудочно-кишечного тракта, исключение составил 1 пациент, у которого на поздних сроках применения ламивудина развилась тромбоцитопения с резким снижением тромбоцитов, потребовавшая отмены препарата и назначения специфической терапии. Других побочных эффектов со стороны периферической крови нами зарегистрировано не было.
Основной причиной низкой эффективности ламивудина, по-видимому, является отсутствие возможности у препарата убрать существовавшую до начала лечения ДНК или возникающую во время терапии вирусную резистентность путем селекции мутантов по YMDD-мутации в ВГВ-полимеразе. Следствием этих процессов является возобновление репликации вируса и повышение АЛаТ, несмотря на продолжающуюся терапию. В то же время, ведение пациентов с возникшей мутацией неоднозначно. Некоторые специалисты предпочитают продолжение терапии даже после формирования резистентности с целью поддержания более низкого уровня ДНК ВГВ, АЛаТ и гистологического улучшения, а также реактивации дикого штамма ВГВ.
Другие считают, что продолжение лечения пациентов с наступившей резистентностью к ламивудину не эффективно. Ведение этих больных остается спорным.
Таблица 15
Частота (в %) появления мутантных вирусов у больных ХВГ В
|
Препарат |
Нет мутаций |
Мутации в pre C-зоне HBV |
YMDD-мутант |
|
Циклоферон |
96 чел. (100.0) |
- |
-* |
|
Ламивудин |
41 чел. (44,1) |
8 чел. (8,6) |
44 чел. (47,3)* |
|
Циклоферон+ Ламивудин |
84 чел. (85,7) |
1 чел. (1,02) |
13 чел. (13,3)* |
* - значения существенно (р≤0,005) отличающиеся в группе сравнения на данном этапе лечения
Мутация в pre C-зоне HBV регистрировалась у 8 человек, YMDD-мутации в ВГВ-полимеразе у 44 больных, причем 6 больным пришлось отменить терапию. В то же время, необходимо обратить внимание, что у больных, получавших циклоферон, мутантные вирусы не возникали, а применение комбинированной терапии снижало их появление до 14 %, эффективность же терапии за счет этого возрастала до 54,08 %.
Таким образом, показана клиническая эффективность препаратов циклоферон и ламивудин при терапии больных ХВГВ.
Циклоферон (в дозе 15 мг/кг массы) при длительном применении (в течение 12 месяцев) не вызывал побочных и аллергических реакций как в виде монотерапии, так и в комбинации с ламивудином, обеспечивая стабильную ремиссию у 54,08 % больных с отсутствием формирования резистентности к ламивудину и появления мутантных вирусов.
В целом рациональная фармакотерапия вирусных гепатитов остается очень сложной задачей. Наиболее эффективными остаются препараты интерферона и его индукторы, особенно при комбинированной терапии с рибавирином при ХВГС и ламивудином при ХВГВ.
Список литературы
- Ершов Ф.И. Вирус гепатита С и система интерферона // Интерфероны и их индукторы (от молекул до лекарств). М., 2005. - С. 89-123.
- Ершов Ф.И. Вирусные гепатиты // Антивирусные препараты. - Справочник. Издание второе. - М., 2006. - С. 269-287.
- Ершов Ф.И., Романцов М.Г. Вирусные гепатиты //Лекарственные средства, применяемые при вирусных заболеваниях. - М., 2007. - С. 84-106.
- Прикладная фармакоэкономика / Под ред. академика РАМН, профессора В.И. Петрова: учебное пособие. - М., 2005.
- Сологуб Т.В., Романцов М.Г., Ершов Ф.И. Эффективность иммуномодуляторов в комплексной терапии хронических вирусных гепатитов // Лекарственные средства, применяемые при вирусных заболеваниях. - М., 2007. - С. 158-163.
- Сологуб Т.В., Романцов М.Г., Коваленко С.Н. Комбинированная терапия хронического вирусного гепатита В и ее влияние на качество жизни // Вестник Санкт-Петербургской государственной медицинской академии им. И.И. Мечникова. - 2006. - №1. - С. 3-12.
- Сологуб Т.В., Романцов М.Г., Баранова И.П. Комбинированная терапия больных хроническим вирусным гепатитом В, резистентных к лечению ламивудином // Вестник Санкт-Петербургской государственной медицинской академии им. И.И. Мечникова. - 2006. - №2. - С. 7-13.
- Романцов М.Г., Сологуб Т.В., Гуренкова Н.П. «Тройная терапия» хронического вирусного гепатита С у пациентов с генотипом 1b //ВРАЧ. - 2006. - №7. - С. 1-4.
- Романцов М.Г., Коваленко А.Л. Индуктор интерферона - Циклоферон. Итоги и перспективы клинического применения. - Санкт-Петербург. - 2007. - 24 с.
- Об утверждении стандарта медицинской помощи больным хроническим вирусным гепатитом // Приказ Минздравсоцразвития России №571 от 21 июля 2006 г.
- Буловская Л.Н., Борисенко Г.Н., Дробаченко О.А. и др. Определение фенотипа N-ацетилтрансферазной активности // Лаб. дело. - 1990. - №10. - С. 28-30.
- Гребенник Л.И. Об определении производных гидразида изоникотиновой кислоты и продуктов их превращения в организме // Пробл. туберкулеза. - 1961. - №4. - С. 69-74.
- Дюг Е.М., Прокопишин В.И., Подымов В.К. и др. Полиморфизм по N-ацетилтрансферазе в норме у группы населения Молдавской ССР // Здравоохранение. - 1979. - №6. - С. 29-32.
- Журавский С.Г. Сенсоневральная тугоухость: молекулярно-генетические, структурные и лечебно-профилактические аспекты: Автореф. дис.... д-ра мед. наук. - СПб., 2006. - 35 с.
- Катцунг Б.Г. Базисная и клиническая фармакология: Т. 1 / Пер. с англ. - М.: Бином; СПб.: Нев. диалект., 1998 - 660 с.
- Кукес В.Г. Метаболизм лекарственных средств: клинико-фармакологические аспекты. - М., 2004. - с. 81-83.
- Логинов А.С., Блок Ю.Е. Хронические гепатиты и циррозы печени. - М.: Медицина, 1987. - с. 76-82.
- Радченко В.Г., Шабров А.В., Зиновьева Е.Н. Основы клинической гепатологии. - СПб.: Диалект, 2005. - C. 306-318.
- Рациональная фармакотерапия заболеваний органов пищеварения. Под общ. ред. Ивашкина В.Т. - М.: Литтерра, 2003. - C. 250-251, 423-425.
- Тихонова В.А. Особенности течения, исходов и терапии НВ-вирусной инфекции у детей с различным фенотипом ацетилирования: Автореф. дис.... канд. мед. наук. - СПб., 1995. - 17 с.
- Саscorbi I., Brockmoller J., Mrozikiewicz P.M., Muller A. et al. Homozygous rapid arylamine NAT2 genotype as a susceptibility factor for lung cancer // Cancer Res. - 1996. - Vol.56, N 17. - P. 3961-3966.
- Саscorbi I., Brockmoller J., Mrozikiewicz P.M., Muller A. Arylamine N-acetyltransferase activity in man // Drug metab. rev. - 1999. - Vol.31, N 2. - P. 489-502.
Библиографическая ссылка
Сологуб Т.В., Романцов М.Г., Кетлинская О.С., Петров А.Ю., Комиссаров С.Н., Кремень Н.В., Александрова Л.Н., Суханов Д.С., Ледванов М.Ю., Стукова Н.Ю., Козько В.М., Бондарь А.Е., Бизенкова М.Н., Полякова Т.Д., Старчикова Н.Е. СОВРЕМЕННЫЕ МЕДИЦИНСКИЕ ТЕХНОЛОГИИ ТЕРАПИИ БОЛЬНЫХ ХРОНИЧЕСКИМ ВИРУСНЫМ ГЕПАТИТОМ // Современные проблемы науки и образования. 2010. № 6. ;URL: https://science-education.ru/en/article/view?id=4549 (дата обращения: 02.06.2026).



