Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
DIAGNOSIS OF HERPETIC EPITHELIAL KERATITIS BASED ON PHOTOS OF THE EYE SURFACE USING ARTIFICIAL INTELLIGENCE TOOLS
Введение
Среди причин воспалительной патологии органа зрения до 57 % приходится на долю герпесвирусов, а доминирующей клинической формой является кератит [1; 2]. Поражение глаз герпесвирусом может проявляться как первичная инфекция или рецидив латентного заболевания [3]. Рецидивирование является важным аспектом герпетического кератита (ГК) [4]. Повторяющиеся эпизоды ГК могут привести к образованию помутнений роговицы, снижению остроты зрения вплоть до слепоты и, как следствие, ухудшению качества жизни пациентов [5; 6]. ГК является основной причиной инфекционной слепоты во всем мире [7].
При эпителиальном древовидном кератите дефект зачастую распространяется глубже боуменовой мембраны, в результате чего могут формироваться помутнения роговицы, соответствующие области дефекта. Интенсивность помутнения сильно варьирует от его отсутствия до значительного в зависимости от индивидуальной иммунной реакции [8, с. 839–840]. При определенных условиях течение заболевания приобретает более тяжелый характер, воспалительный процесс начинает затрагивать все большую площадь поверхности и распространяется глубже, в роговичную строму, характер поражения становится картообразным [9, с. 120]. Считается, что у 25 % пациентов стромальный кератит развивается после эпителиального [10].
Раннее начало местного или системного противовирусного лечения снижает тяжесть и продолжительность заболевания [3]. Таким образом, ранняя диагностика и лечение ГК на этапе эпителиального кератита способны помочь добиться большей прозрачности роговицы и, следовательно, более высоких показателей остроты зрения.
Атипичная клиническая картина осложняет дифференциальную диагностику ГК, возможно воздействие и иных факторов, таких как вторичная инфекция, присоединение которой наблюдается при длительном течении патологии, в том числе на фоне терапии [11].
Для точной диагностики и выбора наиболее эффективной стратегии лечения офтальмологи сталкиваются с необходимостью тщательно анализировать и учитывать обширный массив данных, что зачастую является сложной задачей. Однако на помощь врачам приходят новые технологии и подходы, направленные на автоматизацию процессов диагностики. Одним из перспективных направлений является использование фотографий глазной поверхности, полученных с помощью цифровых фотощелевых ламп. Алгоритмы машинного обучения способны анализировать большие объемы данных, выявляя закономерности и отклонения, которые могут остаться незамеченными для человеческого глаза. Это позволяет не только сократить время, необходимое для диагностики, но и повысить вероятность выявления заболеваний на ранних стадиях, что, в свою очередь, увеличивает шансы на успешное лечение. Таким образом, сочетание традиционных методов диагностики с современными технологиями открывает новые горизонты в области офтальмологии, улучшая качество медицинской помощи.
Настоящее исследование уникально тем, что разработан ранее не существующий метод диагностики, основанный на бинарной классификации фотографий глазной поверхности, полученных посредством фотощелевой лампы, с клиническими признаками ГК и фотографий без клинических признаков ГК, решение данной задачи достигается благодаря использованию методов машинного обучения. Данная модель способна помочь автоматически распознавать ГК, то есть производить его диагностику. Разработанная система должна помочь офтальмологам в качестве мощного инструмента поддержки принятия врачебных решений.
Цель исследования – создание диагностического инструмента эпителиального герпетического кератита с применением искусственного интеллекта (ИИ) по фотографическим изображениям глазной поверхности.
Материалы и методы исследования
Исследование проводилось на базе отделения инфекционных и аллергических заболеваний глаз ФГБУ «НМИЦ ГБ им. Гельмгольца» Минздрава России. Разработанный сервис был получен в результате обучения модели нейросети Inception_v3 на языке программирования Python. Для построения сервиса был использован датасет из 216 фотографий глазной поверхности. В зависимости от наличия или отсутствия признаков ГК было выделено две группы.
Критерии включения для исследуемой группы: постпервичный поверхностный ГК, подтвержденный методом полимеразной цепной реакции. Критерии исключения: глубокие стромальные и эндотелиальные формы ГК, явления увеита. В исследуемую группу вошли 116 фото, из них 76 были взяты из общедоступных источников сети Интернет, а 40 представляли фото пациентов НМИЦ ГБ им. Гельмгольца. В качестве контрольной группы служили здоровые глаза без признаков ГК. В данную группу было включено 100 фотографий глазной поверхности парных (здоровых) глаз пациентов и глаз здоровых добровольцев. Фотографии глазной поверхности 40 пациентов из исследуемой группы, а также всех пациентов контрольной группы были получены за фотощелевой лампой NIDEK SL-1800 после проведения флюоресцеиновой пробы.
Результаты исследования и их обсуждение
Поскольку применяемый в исследовании набор данных включал фотографии глазной поверхности, в том числе взятые и из общедоступных источников сети Интернет, то условия получения снимков отличались и были сделаны за разными фотощелевыми лампами. Поэтому все снимки датасета оцифровывались и подвергались препроцессингу, а именно приводились к общему разрешению 150 на 150 пикселей. На рис. 1 и 2 изображены примеры элементов датасета.
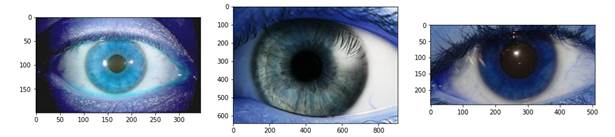
Рис. 1. Примеры фотографий глазной поверхности без признаков ГК.
Источник: составлено авторами
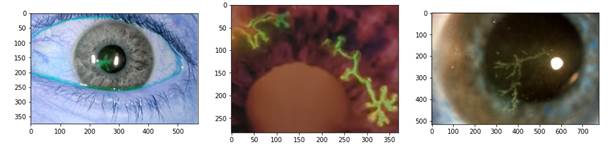
Рис. 2. Примеры фотографий глазной поверхности с признаками ГК.
Источник: составлено авторами
Рис. 3 изображает нейросеть Inception_v3, а точнее фрагмент ее предобученной модели, которая использовалась для диагностики эпителиального ГК.

Рис. 3. Фрагмент модели сверточной нейросети Inception_v3.
Источник: составлено авторами
Метрика (Dice) учитывает и чувствительность модели (долю правильно идентифицированных положительных результатов диагностики), и специфичность (долю правильно идентифицированных отрицательных результатов диагностики). Данная метрика применялась для оценки качества обучения. Использование этой метрики сделало возможным увеличение эффективности диагностики.
Составляющие датасета были отнесены к двум категориям: 1 – снимки глазной поверхности с ГК, 0 – снимки глазной поверхности без признаков ГК. Количество элементов в этих категориях отличалось, то есть датасет был разбалансирован, что обусловило предел показателя метрики в 80 %, другими словами, качество обучения нейросетевой модели было недостаточным [12]. Для устранения этой проблемы и повышения эффективности обучения данной модели была применена техника аугментации [13]. Набор данных был увеличен посредством искажения уже имеющихся составляющих датасета, таким образом датасет был сбалансирован.
В ходе дальнейшего обучения нейросетевой модели был использован оптимизатор Adam [14]. Его применение позволило стабилизировать и повысить результативность обучаемой модели. Благодаря увеличению числа эпох процесс обучения стал устойчивее как на тренировочном, так и на тестовом наборах данных.
Корректировка последних слоев, введение верхнего дополнительного слоя нейросети, использование оптимизатора Adam, балансировка датасета, подбор гиперпараметров модели и построение ансамбля моделей позволили добиться высокого качества дообучения предобученной модели нейросети Inception_v3.
Оценить качество предсказания классификации снимка и эффективность обучения модели возможно, проанализировав рис. 4. На рисунке демонстрируется график кривой ROC (ROC – receiver operating characteristic, рабочая характеристика приемника). Кривая ROC в данном исследовании является метрикой способности отличать фото с ГК от фото без данной патологии, показывает зависимость чувствительности нейросетевой модели (доли верно идентифицированных положительных результатов проведенной диагностики) от специфичности модели нейросети (доли верно идентифицированных отрицательных результатов проведенной диагностики). Кривая ROC изображена синим цветом на рис. 4, характеризует процесс обучения нейросетевой модели на несбалансированном наборе данных как без оптимизаторов, так и без подбора гиперпараметров модели. Качество модели характеризуется площадью под кривой ROC в соответствии с методом AUC-ROC (AUC – area under the curve, площадь под кривой) [15]. Чем больше площадь, а в идеале площадь под кривой ROC должна стремиться к 1 (когда предсказание патологий происходит без ошибок), тем выше эффективность механизма диагностики ГК. Как раз на графике (рис. 4) оранжевым цветом выделена кривая ROC, соответствующая процессу обучения. Высокое качество модели предсказания ГК и эффективность примененных подходов подтверждается столь высокой (0,95) площадью под кривой ROC.
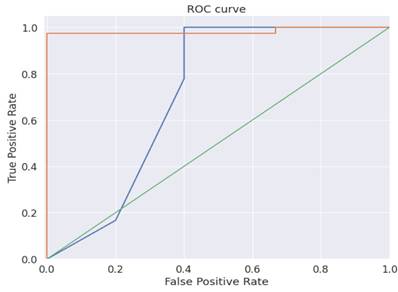
Рис. 4. График ROC-кривой.
Источник: составлено авторами
ИИ уже использовали для диагностики различных кератитов инфекционной этиологии [16–18]. Некоторые исследования были направлены на диагностику ГК [19–21]. Отсутствие клинических испытаний этих технологий, а также тот факт, что качество не оценено независимыми экспертами медицины, не дали распространиться технологиям ИИ в медицинской практике. Описываемая работа отличается от проведенных ранее тем, что создан диагностический инструмент эпителиального герпетического кератита с применением ИИ по фотографическим изображениям глазной поверхности. Данный инструмент способен добиться более высокой скорости и мобильности диагностики ГК, а также снизить бюджетные потери в будущем. Чувствительность и специфичность разработанной модели подтверждена ручной оценкой опытных врачей-офтальмологов.
Данная работа показала значительный потенциал инструментов машинного обучения в распознавании с высокой точностью за короткий промежуток времени признаков изучаемой патологии. Разработанный сервис применим еще на этапе доврачебной помощи в качестве скринингового метода распознавания признаков ГК, что возможно благодаря тому, что фиксировать состояние глаза за фотощелевой лампой может и человек без медицинского образования, ИИ автоматически проанализирует полученное изображение и при выявлении признаков заболевания поможет грамотно осуществить маршрутизацию пациента. То есть актуальность настоящей разработки не вызывает сомнений, учитывая, что в труднодосягаемых районах страны снижена доступность офтальмологической помощи и что, в дополнение к этому, здравоохранение делает акцент на профилактику. В случаях тяжелых форм ГК, а также при развитии токсико-аллергических реакций или иных осложнений при длительном применении местной терапии определенный интерес представляет возможность применения инструментов ИИ в дифференциальной диагностике ГК. Также сервис может быть полезен врачам в процессе ведения пациентов с данной патологией. В процессе последующего добора данных для поддержания и увеличения стабильности работы сервиса будет произведено его включение в современную систему помощи принятия врачебных решений.
Заключение
Таким образом, в результате исследования был создан и подготовлен специальный набор данных, содержащий изображения поверхности глаза с признаками и без признаков ГК. Также произведено дообучение нейросетевой модели Inception_v3, позволяющее классифицировать снимки глазной поверхности на две категории (снимки глазной поверхности с ГК, снимки глазной поверхности без признаков ГК), то есть нейросеть обучена проводить диагностику ГК. Полученная модель продемонстрировала точность 95 % на тестовой выборке. Это свидетельствует о высоком потенциале метода и возможности дальнейшего повышения его эффективности. Вероятность ложноположительных результатов составляет 5 %. В будущем планируется увеличение набора данных новыми фотографиями и обучение модели на более масштабной выборке.
Данная разработка является информативным диагностическим инструментом, способным выявить признаки заболевания на раннем этапе его проявлений, может служить надежным помощником в оценке эффективности проводимой терапии. Таким образом рабочая рутина офтальмологов по поиску патологий может быть разгружена с помощью разработанной модели, путем автоматизации процесса диагностики ГК.
Настоящее исследование подчеркивает значительный потенциал машинного обучения в офтальмологии, представляя собой значимый этап в создании автоматизированной системы поддержки принятия врачебных решений в НМИЦ ГБ им. Гельмгольца. Результаты исследования демонстрируют высокую эффективность предложенного метода диагностики и открывают новые перспективы для повышения качества медицинской помощи.
Conflict of interest
Библиографическая ссылка
Нероев В.В., Брагин А.А., Яни Е.В., Ступакова М.М. ДИАГНОСТИКА ГЕРПЕТИЧЕСКОГО ЭПИТЕЛИАЛЬНОГО КЕРАТИТА ПО ФОТОГРАФИЯМ ГЛАЗНОЙ ПОВЕРХНОСТИ С ПОМОЩЬЮ ИНСТРУМЕНТОВ ИСКУССТВЕННОГО ИНТЕЛЛЕКТА // Современные проблемы науки и образования. 2025. № 3. ;URL: https://science-education.ru/en/article/view?id=34106 (дата обращения: 29.04.2026).
DOI: https://doi.org/10.17513/spno.34106



