Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
COMBINED SURGICAL METHOD FOR CORRECTION OF HIGH REGULAR AND IRREGULAR POSTKERATOPLASTIC ASTIGMATISM IN PATIENTS WITH CATARACT
Введение
Развитие помутнения хрусталика у людей, которые перенесли ранее сквозную кератопластику (СКП), вызывает снижение зрения, требующее его восстановления [1]. Кроме катаракты, в подавляющем большинстве случаев у данной категории пациентов диагностируется роговичный астигматизм (РА) [2]. Увеличение величины РА и его высокая нерегулярность приводят к повышению аберраций, снижению качества зрения и, как следствие, к неудовлетворенности пациентов оптическим результатом СКП [3]. Метод удаления катаракты с помощью факоэмульсификации в сочетании с последующей установкой торической интраокулярной линзы (тИОЛ), несмотря на то, что устраняет помутнение хрусталика, включая посткератопластический РА, имеет следующие ограничения: величина торического компонента выпускаемых тИОЛ (до 12,0 дптр включительно), а также регулярная или иррегулярная форма РА по типу «галстук-бабочка» [4, 5]. В научной литературе отмечается высокая эффективность применения для коррекции посткератопластического РА интрастромальных роговичных сегментов (ИРС) [6, 7]. При низкой эффективности факоэмульсификации катаракты (ФК) с имплантацией тИОЛ для коррекции посткератопластической аметропии может быть применен комбинированный хирургический метод, который включает первоначальную имплантацию ИРС на I этапе операции с целью уменьшения РА и повышения симметричности роговицы. На II этапе проводится удаление катаракты, что делает данный комбинированный хирургический метод достаточно актуальным [8].
Цель исследования – провести клинико-функциональный анализ комбинированного метода хирургической коррекции высокого регулярного и иррегулярного посткератопластического астигматизма у пациентов с катарактой.
Материал и методы исследования
Была выполнена хирургическая коррекция посткератопластического РА у 20 пациентов (20 глаз) с катарактой. По данным кератотопографии, у всех больных были диагностированы регулярная форма посткератопластического РА более 12,0 дптр или иррегулярная форма РА типа «галстук-бабочка». Возрастные рамки составили от 36 до 72 лет, средний возраст около 59±15 лет. Среди пациентов было больше мужчин (12 человек) по сравнению с женщинами (8 человек). В истории болезни выявлены следующие причины предыдущих СКП: наследственная дистрофия роговицы у 6 глаз, пеллюцидная дегенерация роговицы – у 3, центральные рубцовые изменения роговицы после травм – у 4, помутнение вследствие язвы роговицы – также в 4 случаях. Кроме того, отмечались кератоконус IV стадии и вторичная кератэктазия (по одному глазу). Все донорские кератотрансплантаты имели хорошую прозрачность. По классификации L. Buratto, плотность ядра хрусталика I степени наблюдалась у 10 пациентов, II степени – у 6 и III степени – в 4 случаях [8, p. 196]. Хирургическое лечение данных пациентов проходило в 2 этапа.
В данном исследовании, направленном на улучшение коррекции рефракционных нарушений после СКП, использовался двухэтапный подход. На I этапе всем пациентам была проведена имплантация ИРС («Научно-экспериментальное производство Микрохирургия глаза», Россия) с применением фемтосекундного лазера (ФСЛ) «ФемтоВизум» (Троицк, Россия). Применение ФСЛ диктовалось необходимостью высокой точности и предсказуемости при создании интрастромального тоннеля внутри донорского трансплантата. При формировании тоннеля придерживались строго заданных параметров: внутренний диаметр – 5,0 мм, наружный – 6,2 мм, а глубина составила 80% от пахиметрии роговичного трансплантата в месте его формирования. Ключевым аспектом была точная центровка тоннеля относительно зрительной оси глаза пациента, что обеспечивало оптимальное положение ИРС и отсутствие индуцированного астигматизма. На II этапе через специально сделанный вертикальный разрез два ИРС имплантировались в уже подготовленный интрастромальный тоннель с использованием микрохирургического пинцета, а затем они позиционировались в соответствии с кератотопографическими данными относительно сильной оси кератометрии.
В течение 3–6 месяцев после имплантации ИРС, при достижении стабилизации рефракции, пациентам проводилась ФК с имплантацией тИОЛ модели RayOne Toric RAO610T (Rayner, United Kingdom). Расчет ИОЛ проводился по онлайн-калькулятору Barrett True – K Toric Calculator в связи с возможностью внесения в данном калькуляторе значения кератометрии одного из главных меридиана задней поверхности роговичного трансплантата более 7,5 дптр, которое встречалось в 8 глазах (8 пациентов). При проведении расчета тИОЛ длина глаза, а также толщина хрусталика, расстояние «от белого до белого» и глубина передней камеры были измерены с использованием оптической биометрии на аппарате IOL Master 500 (Carl Zeiss AG, Германия). Кератометрические данные и положение главных меридианов передней поверхности роговичного трансплантата определялись с помощью кератотопографа TMS-5 (Tomey, Япония). Задняя поверхность роговичного трансплантата анализировалась с использованием оптической когерентной томографии (ОКТ) роговицы на аппарате CASIA 2. При расчете тИОЛ в калькуляторы ИОЛ вносились также значение A константы ИОЛ, Lens Factor, индуцированный астигматизм, положение основного разреза, рефракция цели, центральная пахиметрия кератотрансплантата, измеренная при помощи ОКТ роговицы на аппарате CASIA 2.
До начала операции больному проводили маркировку горизонтальной оси кератотрансплантата при помощи щелевой лампы. ФК выполняли на аппарате Stellaris PC Vision Enhancement System (Bausch+Lomb, USA). В начале операции при помощи кольца Мендеса делали разметку сильного меридиана кератометрии роговичного трансплантата. Затем производили основной разрез и 2 парацентеза. После введения вискоэластика в переднюю камеру с помощью инсулиновой иглы проводили непрерывный круговой передний капсулорексис. Затем использовали факоэмульсификатор для удаления ядра хрусталика, после чего коаксиальным наконечником ирригации-аспирации убирали кортикальные массы и эпинуклиус. Имплантацию предустановленной тИОЛ осуществляли с помощью инжектора от производителя, при этом центровали метки тИОЛ по размеченной оси сильного меридиана кератометрии роговичного трансплантата. Завершая операцию, вымывали вискоэластик из передней камеры и герметизировали разрезы стерильным физиологическим раствором, после чего делали инъекцию антибиотика и кортикостероида.
В отдаленном послеоперационном периоде у всех пациентов была проанализирована динамика изменения плотности эндотелиальных клеток (ПЭК) с использованием эндотелиального микроскопа Tomey EM-3000 (Tomey, Япония). Срок наблюдения после ФК составил 12 месяцев.
Статистическую обработку данных проводили в программе IBM SPSS Statistics 20. Для проверки нормальности распределения исследуемых показателей использовали критерий Шапиро–Уилка. Достоверность различий оценивали по параметрическому t-критерию для зависимых переменных благодаря нормальному распределению значений. Все средние значения исследуемых параметров, измеренные в различные периоды после операций, сравнивали с дооперационными данными. Результаты были представлены в виде M±σ, где M – среднее арифметическое, а σ – стандартное отклонение. Различия считались статистически значимыми при p<0,05.
Результаты исследования и их обсуждение
Сквозной роговичный трансплантат был прозрачный у всех пациентов при биомикроскопии, что связано с расположением ИРС только в пределах кератотрансплантата, без затрагивания зоны посткератопластичекого рубца. ИРС находились в правильном положении и располагались симметрично относительно сильной оси кератометрии кератотрансплантата. Из-за помутнения хрусталика глубжележащие структуры было трудно рассмотреть. Правильная глубина расположения ИРС подтверждалась пахиметрическими данными ОКТ роговицы (рис. 1).

Рис. 1. ОКТ роговицы после имплантации ИРС в роговичный трансплантат с применением ФСЛ. Визуализируется профиль ИРС, расположенных на глубине 80% от пахиметрических данных сквозного роговичного трансплантата в месте их имплантации
Через 1 месяц после имплантации ИРС среднее значение некорригированной остроты зрения (НКОЗ) увеличилось на 0,14±0,12 (р=0,0315), а затем к 3 месяцам повысилось еще на 0,02±0,01 (р=0,0374) (табл. 1).
Таблица 1
Результаты коррекции посткератопластической аметропии до имплантации на I этапе ИРС в роговичный трансплантат и через 1 и 3 месяца после операции (M±σ), n=20
|
Показатели |
До операции |
Через 1 месяц |
p |
Через 3 месяца |
р |
|
НКОЗ |
0,03±0,01 |
0,17±0,13 |
0,0315 |
0,19±0,14 |
0,0336 |
|
КОЗ |
0,08±0,11 |
0,34±0,27 |
0,0386 |
0,37±0,28 |
0,0314 |
|
РА, дптр |
–11,4±5,5 |
–3,9±2,1 |
0,0126 |
–3,6±2,0 |
0,0144 |
|
SRI |
1,41±0,24 |
1,18±0,18 |
0,0146 |
1,15±0,17 |
0,0154 |
|
SAI |
2,12±0,28 |
1,33±0,20 |
0,0174 |
1,22±0,19 |
0,0166 |
Через 1 месяц после операции корригированная острота зрения (КОЗ) увеличилась на 0,26±0,16 (р=0,0386), а затем к 3 месяцам возросла еще на 0,03±0,01 (р=0,0316). Стабилизация НКОЗ и КОЗ наблюдалась через 3 месяца после операции. Коэффициент эффективности (Кэфф) составил 2,4±0,07.
По данным компьютерной кератотопографии на аппарате TMS-5, через 1 месяц после операции среднее значение РА снизилось на 7,5±3,4 дптр (р=0,0126), затем к 3 месяцам после операции понизилось еще на 0,3±0,1 дптр (р=0,0163) (рис. 2).
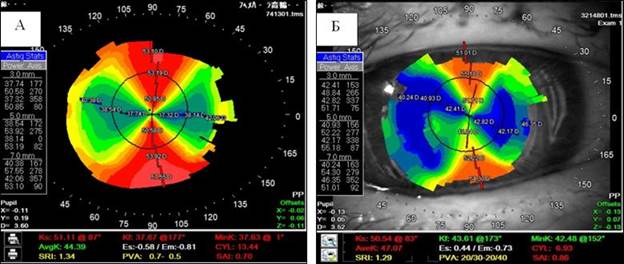
Рис. 2. Клинический пример кератотопограммы пациента К.: А – до операции визуализируется регулярный роговичный астигматизм высокой степени, Б – через 3 месяца после имплантации ИРС в роговичный трансплантат с применением ФСЛ отмечается снижение роговичного астигматизма на 6,51 дптр
Через 1 месяц после операции среднее значение индекса SRI (surface regularity index, индекс регулярности поверхности роговицы) снизилось на 0,23±0,06 (р=0,0146), индекса SAI (surface asymmetry index, индекс асимметрии поверхности роговицы) – на 0,79±0,08 (р=0,0174). Затем к 3 месяцам после операции индекс SRI понизился еще на 0,03±0,01 (р=0,0141), индекс SAI – на 0,11±0,01 (р=0,0172). Стабилизация РА и кератотопографических индексов наступила к 3 месяцам после операции.
Таким образом, после имплантации ИРС по данным кератотопографии значительно скорригировалось значение РА и снизились кератотопографические индексы, что привело к повышению сферичности и регулярности роговичного трансплантата. Невысокое остаточное значение посткератопластического РА может быть докорригировано тИОЛ во время ФК на II этапе хирургического лечения.
При проведении I этапа комбинированного хирургического лечения осложнений как во время операций, так и в послеоперационном периоде отмечено не было. Коэффициент безопасности (Кб) у пациентов составил 4,6±0,05. Значение ПЭК уменьшилось через 3 месяца после операции с 2086±225 до 2067±217 кл/мм2 (р=0,0222) и через 6 месяцев составило 2048±212 кл/мм2 (р=0,0253). По данным литературы, потеря ПЭК после имплантации ИРС в роговичный трансплантат на I этапе комбинированного хирургического лечения сопоставима с аналогичным периодом снижения ПЭК у пациентов после выполненной ранее СКП. Исследования, посвященные имплантации ИРС для коррекции посткератопластической аметропии, действительно подтверждают как эффективность, так и безопасность данной процедуры. Многие научные работы показывают положительные результаты как в улучшении зрительных функций, так и в снижении зависимости от очков или контактных линз у пациентов с аметропией после СКП. В клиническом ретроспективном исследовании S. Coscarelli на 59 глазах (54 пациентов) после имплантации ИРС (FerraraRing) в роговичный трансплантат среднее значение КОЗ увеличилось с 0,35±0,17 до 0,5±0,17, сфероэквивалент рефракции снизился с –6,34±3,40 до –2,66±2,52 дптр. Ни у одного из пациентов не было отмечено потери строк КОЗ. РА, по данным кератотопограмм, уменьшился с –3,37±1,51 до –1,69±1,04 дптр [9]. В клиническом исследовании P.F. Tzelikis по имплантации ИРС с длиной дуги 340° с помощью ФСЛ на 20 глазах (18 пациентов) с посткератопластической аметропией через 1 год после операции было отмечено увеличение НКОЗ в среднем с 0,08 до 0,29, КОЗ – с 0,57 до 0,8, среднее значение РА снизилось с –5,55±2,29 до –3,92±1,82 дптр [10].
Через 3–6 месяцев после I этапа лечения всем пациентам был выполнен II этап – ФК с имплантацией тИОЛ.
При биомикроскопии на следующий день после ФК у всех пациентов роговичный трансплантат был прозрачный, что связано с достаточным количеством ПЭК до операции и невысокой плотностью ядра хрусталика у всех пациентов. ИРС были расположены центрированно относительно сильного меридиана кератометрии (рис. 3).
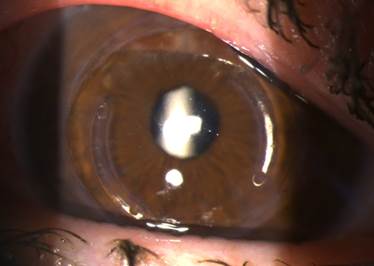
Рис. 3. Фото глаза на следующий день после ФК с имплантацией тИОЛ после ранее выполненной имплантации ИРС в роговичный трансплантат с применением ФСЛ
Визуализируются центрированно расположенные относительно сильного меридиана роговичного трансплантата ИРС, в проекции зрачка визуализируется оптическая часть тИОЛ
Метки торического компонента тИОЛ у всех пациентов совпадали с осью сильного меридиана роговичного трансплантата.
При осмотре пациентов на следующий день после операции среднее значение НКОЗ увеличилось на 0,19±0,03 (р=0,0136), затем через 1 месяц повысилось еще на 0,03±0,01 (р=0,0152) и к 3 месяцам возросло еще на 0,02±0,01 (р=0,0182) (табл. 2).
Таблица 2
Результаты коррекции посткератопластической аметропии до выполнения на II этапе ФК с имплантацией тИОЛ и в различные сроки после операции (M±σ), n=20
|
Показатели |
До операции |
1-й день |
р |
Через 1 месяц |
p |
Через 3 месяца |
р |
|
НКОЗ |
0,19±0,14 |
0,38±0,13 |
0,0125 |
0,41±0,14 |
0,0144 |
0,43±0,15 |
0,0148 |
|
КОЗ |
0,37±0,28 |
0,59±0,15 |
0,0131 |
0,64±0,12 |
0,0125 |
0,66±0,11 |
0,0121 |
|
Sph, дптр |
0,87±5,2 |
0,66±1,1 |
0,0322 |
0,18±1,2 |
0,0336 |
0,2±1,2 |
0,0224 |
|
Cyl, дптр |
–3,31±1,9 |
–1,41±0,6 |
0,0284 |
–1,17±0,5 |
0,0214 |
–1,15±0,4 |
0,0292 |
|
РА, дптр |
–3,6±2,0 |
–3,3±1,9 |
0,0264 |
–3,1±1,8 |
0,0221 |
–3,0±1,8 |
0,0262 |
|
Угол ротации тИОЛ, ° |
– |
2,41±0,95
|
0,0012 |
3,12±1,29
|
0,0049 |
3,36±1,38 |
0,0055 |
На следующий день после операции среднее значение КОЗ увеличилось на 0,22±0,13 (р=0,0165), затем через 1 месяц возросло еще на 0,05±0,03 (р=0,0134) и к 3-му месяцу повысилось еще на 0,02±0,01 (р=0,0161). НКОЗ и КОЗ больше не менялись в течение 12 месяцев наблюдения. Стабилизация остроты зрения наступила к 3-му месяцу после операции. Кэфф составил 1,2±0,07.
На следующий день после операции среднее значение сферического компонента рефракции (Sph) увеличилось на 0,21±4,1 дптр (р=0,0322), затем через 1 месяц повысилось на 0,48±0,01 дптр (р=0,0368) и через 3 месяца после операции возросло еще на 0,02±0,01 дптр (р=0,0136). На следующий день после операции среднее значение цилиндрического компонента рефракции (Cyl) уменьшилось на 1,9±1,3 дптр (р=0,0284), затем к 1 месяцу понизилось еще на 0,24±0,02 дптр (р=0,0224) и через 3 месяца после операции снизилось еще на 0,02±0,01 дптр (р=0,0244). Среднее значение РА понизилось на следующий день после операции на 0,3±0,1 дптр (р=0,0264), затем к 1 месяцу уменьшилось еще на 0,2±0,1 дптр (р=0,0285) и через 3 месяца после операции снизилось еще на 0,1±0,02 дптр (р=0,0211). Sph, Cyl и РА больше не менялись в течение 12 месяцев наблюдения. Стабилизация рефракции наступила к 3 месяцам после операции.
Таким образом, выполнение на I этапе имплантации ИРС в роговичный трансплантат создало оптимальные условия для эффективной докоррекции остаточного РА во время ФК с имплантацией тИОЛ и получение высокого рефракционного результата.
У всех пациентов была оценена ротационная стабильность тИОЛ после ФК. На следующий день после ФК среднее значение ротации тИОЛ составило 2,41±0,95°. Через 1 месяц было отмечено небольшое увеличение ротации тИОЛ на 0,71±0,34° (р=0,0249), которая к 3 месяцам исследования повысилась еще на 0,24±0,09° (р=0,0333) и дальше оставалась неизменной. У всех пациентов угол ротации тИОЛ в течение всего периода наблюдения после ФК не превышал 5°, т.е. не оказывал влияния на рефракционный результат выполненных операций.
Интра- и послеоперационные осложнения на II этапе хирургического лечения отсутствовали. Кб составил 1,8±0,06, что свидетельствовало об отсутствии потери строк КОЗ после операции. При оценке безопасности ФК большое значение имеет потеря ПЭК после операции. Через 3 месяца после операции было отмечено снижение ПЭК с 2048±212 до 1865±217 кл/мм2 (р=0,0285), что составило 8,9% по сравнению с дооперационным значением. Спустя 6 месяцев после ФК ПЭК составила 1848±205 кл/мм2 (р=0,0236) и затем к 12 месяцам снизилась еще до 1822±192 кл/мм2. По данным научной литературы, применение современных вискоэластиков при выполнении ФК у пациентов после СКП приводит к потере ПЭК примерно 6–9%, что сопоставимо с результатами, отмеченными авторами данного исследования [11]. Низкая потеря ПЭК также во многом объясняется дооперационной плотностью ядра хрусталика, которая в данном исследовании была ограничена III степенью по классификации L. Buratto. В литературных источниках описываются случаи снижения ПЭК до 26% и развития вторичной эндотелиальной декомпенсации роговичного трансплантата после ФК с плотностью ядра по классификации L. Buratto III–IV степени [12, 13].
Заключение. Комбинированный хирургический метод, состоящий из двух этапов и включающий в себя на I этапе имплантацию ИРС в роговичный трансплантат, а на II этапе – ФК с последующей имплантацией тИОЛ, продемонстрировал высокую эффективность и безопасность при коррекции регулярного и нерегулярного посткератопластического астигматизма у пациентов с помутнением хрусталика.
Библиографическая ссылка
Синицын М.В., Воскресенская А.А., Поздеева Н.А. КОМБИНИРОВАННЫЙ ХИРУРГИЧЕСКИЙ МЕТОД КОРРЕКЦИИ ВЫСОКОГО РЕГУЛЯРНОГО И ИРРЕГУЛЯРНОГО ПОСТКЕРАТОПЛАСТИЧЕСКОГО АСТИГМАТИЗМА У ПАЦИЕНТОВ С КАТАРАКТОЙ // Современные проблемы науки и образования. 2024. № 6. ;URL: https://science-education.ru/en/article/view?id=33786 (дата обращения: 10.05.2026).
DOI: https://doi.org/10.17513/spno.33786



