Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
THE EFFECT OF THE TIMING OF TRACHEOSTOMY ON THE NEED FOR MEDICAL SEDATION, VASO-INOTROPIC SUPPORT AND THE DURATION OF STAY IN THE INTENSIVE CARE UNIT DURING ARTIFICIAL LUNG VENTILATION IN PATIENTS WITH A NEW CORONAVIRUS INFECTION
Введение. Новая коронавирусная инфекция (НКИ) COVID-19 стала неотъемлемой частью медицинской жизни, приобретя сезонный характер. Доля госпитализаций в профильные инфекционные стационары снизилась по сравнению с прошедшими годами из-за перехода вируса в своей эволюции в менее агрессивную форму. Однако определенному контингенту все же требуется респираторная поддержка разной степени инвазивности [1]. Согласно многопрофильному руководству ВОЗ, 5-12% от общего числа госпитализированных в тяжелом и крайне тяжелом состоянии находилось в отделениях интенсивной терапии и реанимации [2]. В начале пандемии в 85% случаев у пациентов данной группы проводилась длительная аппаратная искусственная вентиляция легких (ИВЛ). Такое количество длительной ИВЛ было связано со специфичностью поражения легочной ткани – интерстициальной пневмонией с развитием острого респираторного дистресс- синдрома [2; 3].
Ввиду использования длительной респираторной поддержки 1% переболевших COVID-19 было произведено наложение трахеостомы. Известно, что трахеостомия позволяет уменьшить мертвое пространство, облегчает санацию трахеобронхиального древа (ТБД), потенциально снижает риск развития отсроченных постинтубационных осложнений, а также способствует снижению дозировок применяемых препаратов, снижению уровня седативной нагрузки и дает возможность ранней активизации пациента. Тем не менее у данного оперативного пособия есть риски развития кровотечений, послеоперационной инфекции, стенозов трахеи и других осложнений. С целью максимально эффективного использования данного оперативного вмешательства с минимизацией операционных и послеоперационных осложнений нашим коллективом авторов производится ретроспективная работа относительно показаний, сроков, а также влияния трахеостомии на течение заболевания у пациентов с COVID-19. Определенные вопросы у данной группы пациентов продолжают оставаться открытыми, в частности выбор времени проведения трахеостомии у пациента на ИВЛ. Данная проблема продолжает являться клинически важной в практике ОРИТ инфекционных стационаров.
В рамках данной работы был проведен анализ медицинской документации пациентов с НКИ, у которых использовали респираторную поддержку (ИВЛ) и по показаниям было проведено оперативное вмешательство на трахее (трахеостомия) в различные сроки от момента интубации трахеи: через 1 сутки, 3 суток и на 7-14-е сутки. Учитывались показатели – уровень глубины седации (Richmond Agitation-Sedation Scale, RASS) и показатель фармакологической сердечно-сосудистой поддержки (Vasoactive-Inotropic Score, VIS) [4], а также производилась оценка общего количества дней в отделении анестезиологии реанимации, количества дней на ИВЛ после оперативного вмешательства и количества суток медицинской седации после наложения трахеостомы.
Цель работы. Определить влияние сроков трахеостомии на длительность пребывания в отделении реанимации и интенсивной терапии, потребность в медицинской седации и вазоинотропной поддержки у пациентов с COVID-19, находящихся на ИВЛ.
Материалы и методы исследования. Проведен ретроспективный анализ медицинской документации пациентов, получавших стационарное лечение с 01.06.2021 г. по 31.03.2022 г. в ГБУЗ МО «Видновская районная клиническая больница». В данном исследовании приняло участие 90 человек (табл.).
Характеристика пациентов по группам
|
Показатели |
1-я группа, операция на 1-е сутки (n=30) |
2-я группа, операция на 3-и сутки (n=30) |
3-я группа, операция на 7-14-е сутки (n=30) |
Все пациенты (n=90) |
|
Возраст, лет |
60 (45;69) |
59 (48; 65) |
62 (53;71) |
62 (45;71) |
|
Мужчин, n (%) |
8 (27) |
12 (40) |
18 (60) |
38 (42) |
|
Женщин, n (%) |
22 (73) |
18 (60) |
12 (40) |
52 (58) |
|
Оперативное вмешательство проведено в ОРИТ, n (%) |
12 (40) |
19 (63) |
13 (43) |
44 (49) |
|
Оперативное вмешательство проведено в операционной, n (%) |
18 (60) |
11 (37) |
17 (57) |
46 (51) |
Всем пациентам был выставлен диагноз COVID-19 (подтвержденный клинико-лабораторными данными). Данная группа (n=90) получала продолжительную ИВЛ (степень поражения легких по рентгенологическим признакам - КТ 2-4), а также всем проводилось оперативное вмешательство – трахеостомия. Все оперативные вмешательства были выполнены после получения информированного письменного согласия пациентов (или их законных представителей) и/или проведения медицинского консилиума. Наложение трахеостомы проводилось открытым (классическим) способом по показаниям (невозможность санации ТБД, предполагаемая длительная ИВЛ и др.) [5]. Вскрытие трахеи производилось в области второго/третьего трахеального полукольца с установкой трахеостомической трубки размерами внутреннего диаметра от 6,5 до 8,0 мм. Давление в манжете поддерживали на уровне 25-30 см H2О (водного столба). Все операции были выполнены врачами-оториноларингологами, в условиях общей анестезии, как в операционной (51%), так и в палате ОРИТ (49%). В соответствии с установленным протоколом мер безопасности весь персонал использовал средства индивидуальной защиты (СИЗ), включая лицевую маску класса N95 [6]. Средний возраст составил 62 ± 12 лет. Исследуемые были разделены на группы по времени оперативного вмешательства от момента интубации: 1-е сутки (1-я группа, n=30), 3-и сутки (2-я группа, n=30) и 7-14-е сутки (3-я группа, n=30). Оценка дозировки вазоактивных препаратов производилась с учетом максимального объема кардиотонической поддержки каждый день в течение двух дооперационных и двух послеоперационных суток. Расчёт вазоактивного инотропного индекса проводился по Gaies с соавторами: VIS = допамин (мкг/кг/мин.) + добутамин (мкг/кг/мин.) + 100 × адреналин (мкг/кг/мин.) + 100 × норэпинефрин (мкг/кг/мин.) + 10 × милринон (мкг/кг/мин.) + 10,000 × вазопрессин (мкг/кг/мин.) + 50 × левосимендан (мкг/кг/мин.) [7]. При оценке уровня глубины седации была использована шкала RASS (шкала возбуждения-седации Ричмонда) – в баллах от +4 до -4, где 0 соответствует бодрствованию, +4 – агрессии, -4 – глубокой седации [8]. Всем пациентам в условиях ОРИТ выполнялась оценка RASS и VIS ежедневно. Для всех групп использовались динамические данные пациентов на протяжении 5 суток. Медиана – день проведения оперативного вмешательства – трахеостомии, а также 2 суток до операции и 2 суток после вмешательства. Для проведения сравнительного анализа групп в данном исследовании были выбраны 2 контрольные точки: 1 сутки до операции (Тдо1), обусловленная наличием группы, где операция производилась на 1 сутки от интубации, и 2 сутки после проведенного вмешательства (Т2). По данным из историй болезни был произведен подсчет общего количества дней в отделении анестезиологии реанимации, количества дней на ИВЛ после оперативного вмешательства и количества суток медицинской седации после проведения операции - наложения трахеостомы.
Статистическая обработка полученных результатов проводилась с использованием программ Graph Pad Prism v8.0 и Microsoft Exсel 2010. Характер распределения исследуемых показателей оценивали с учетом объема выборки по критерию Шапиро-Уилка. Категориальные переменные представлены в виде количества пациентов и процента от общего числа пациентов. Для оценки трех независимых выборок был выбран критерий Краскела-Уоллиса. С помощью критерия Вилкоксона оценивали статистическую значимость изменений показателей в динамике. Нулевая гипотеза отвергалась при р<0,05.
Результаты исследования и их обсуждение. При оценке уровня глубины седации использовали шкалу RASS (рис. 1). Оперативное вмешательство (трахеостомия, Т) производили на 1, 3, 7-14-е сутки от оротрахеальной интубации.
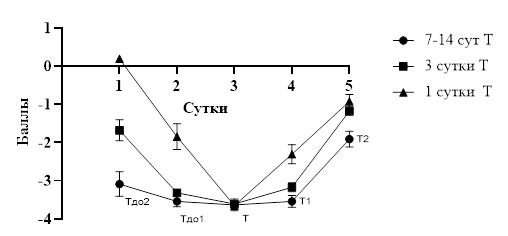
Рис. 1. Динамика RASS у пациентов 1, 2 и 3-й групп* *- здесь и далее данные представлены в виде Mean+SEM.
Динамически после наложения трахеостомы (1-е сутки Т) в 1-й группе пациентов (рис. 1) наблюдали увеличение количества баллов шкалы RASS у большинства больных (92,3%), что указывало на снижение необходимости в седации у пациентов данной группы. Получили статистически значимое различие в 2 контрольных точках при анализе показателей (Тдо1 vs Т2) (Wilcoxon Test, р=0,0354). На 2-е сутки после наложения трахеостомы (Т2) график стремился к 0 значению, что подтверждалось данными из историй болезни – у большинства пациентов отмечали снижение доз седативных препаратов с целью ранней активизации больного.
После наложения трахеостомы (3-и сутки Т) во 2-й группе пациентов (рис. 1) также происходило увеличение количества баллов шкалы RASS у 90,2% больных, что говорит о снижении уровня седации у пациентов данной группы. При анализе показателей выявлено статистически значимое различие в 2 контрольных точках (Тдо1 vs Т2) (Wilcoxon Test, р<0,0001).
Наложение трахеостомы (7-14-е сутки Т) в 3-й группе пациентов (рис. 1) увеличивало количество баллов шкалы RASS у 63,6% больных, что свидетельствовало о снижении уровня седации у пациентов данной группы. При анализе показателей было выявлено статистически значимое различие между двумя контрольными точками (Тдо1 vs Т2) (Wilcoxon Test, р<0,0001). Даже при наличии длительной ИВЛ у данной группы пациентов удавалось снизить дозировку седативных препаратов и предпринимать попытки к активизации больных (RASS на графике стремится к 0). Однако у 36,4% пациентов данной группы этого сделать не удалось, что указывает на снижение эффекта от оперативного вмешательства по сравнению с другими группами.
Параллельно оценивали показатель потребности в фармакологической сердечно-сосудистой поддержке (VIS) пациентам, которым проводилось оперативное вмешательство (трахеостомия, Т) на 1, 3, 7-14-е сутки от оротрахеальной интубации (рис. 2).
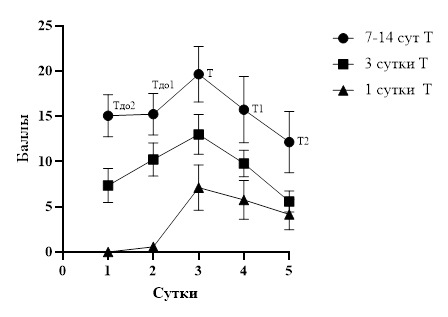
Рис. 2. Динамика VIS у пациентов 1, 2 и 3-й групп
В 1-й группе (трахеостомия на 1-е сутки после интубации) отметили наименьшее количество пациентов, которым потребовалась инотропная и/или вазотропная поддержка (рис. 2) – 57,7%. Динамически после наложения трахеостомы (1-е сутки Т) в этой группе произошло снижение количества баллов вазоактивного инотропного индекса (VIS) у 90% больных. При статистической обработке было выявлено статистически значимое различие в двух контрольных точках (Wilcoxon Test, р= 0,0234). Впрочем, в данном случае мы связываем достоверность различий в большей степени с отсутствием у пациентов фармакологической коррекции артериального давления и инотропной поддержки до момента перевода на ИВЛ. У пациентов 2-й группы (рис. 2) после наложения трахеостомы (3-и сутки Т) происходило снижение количества баллов вазоактивного инотропного индекса (VIS) у 82,7% больных. Отметим, что при этом фармакологическая сердечно-сосудистая поддержка потребовалась 70,7% пациентов.
При анализе показателей было выявлено статистически значимое различие между двумя контрольными точками (Тдо1 vs Т2) (Wilcoxon Test, р= 0,0002). На графике видно общее увеличение индекса VIS (площадь под графиком больше, чем в группе 1), что показывает достоверное увеличение потребности в использовании фармакологических препаратов.
У пациентов 3-й группы (рис. 2) после оперативного вмешательства (7-14-е сутки Т) произошло снижение количества баллов VIS в 72,7% наблюдений. Фармакологическая сердечно-сосудистая поддержка требовалась 86,3% пациентам. При анализе показателей было выявлено статистически значимое различие между двумя контрольными точками (Тдо1 vs Т2) (Wilcoxon Test, р= 0,0048). При этом на графике прослеживается еще большее увеличение индекса VIS (площадь под графиком больше, чем в группах 1 и 2), что говорит об общем увеличении фармакологической нагрузки в данной группе, связанной, по всей видимости, с продолжительностью искусственной вентиляции лёгких.
При определении длительности пребывания пациентов в отделении анестезиологии реанимации, количества дней на ИВЛ после оперативного вмешательства и количества суток медицинской седации после наложения трахеостомы у исследуемых пациентов были получены результаты, представленные на рисунке 3.
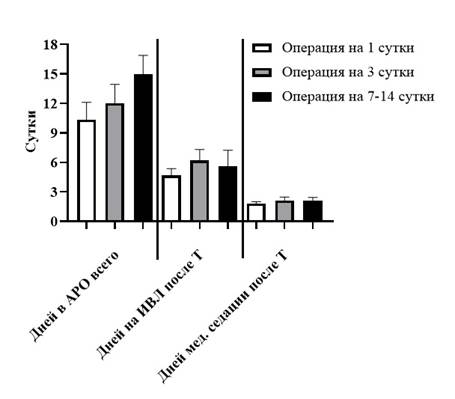
Рис. 3. Показатели дней в АРО, дней на ИВЛ после операции и дней медицинской седации у пациентов 1, 2 и 3-й групп
На рисунке 3 отчетливо прослеживается статистически значимая тенденция к увеличению количества дней в реанимационном отделении от группы 1 к группе 3 (рис. 3) (Kruskal-Wallis test p= 0,0112). Количество дней на ИВЛ после оперативного вмешательства во всех трех группах статистически не различалось (Kruskal-Wallis test p= 0,3732), что говорит об их однородности по данному показателю. Медицинская седация после наложения трахеостомы во всех трех группах продолжалась в среднем около 2 суток, при этом не было получено достоверных различий между группами (Kruskal-Wallis test p= 0,9986), что свидетельствовало о положительном эффекте от операции у исследуемых пациентов вне зависимости от времени проведения трахеотомии.
В связи с полученными данными, а также учитывая то, что трахеостомия, произведенная на 3-и сутки после интубации, динамически значимо снижала показатели парциального давления углекислого газа венозной крови у пациентов с COVID-19 инфекцией и динамически значимо вызывала увеличение соотношения P/F (PaO2/FiO2), описанные авторами данной статьи ранее, становится очевидной актуальность вопроса о переносе сроков наложения трахеостомии на более ранние, 1-е сутки, от момента оротрахеальной интубации у тяжелых пациентов с НКИ [9]. Новейший опыт мирового сообщества также показывает положительный эффект оперативного вмешательства (ранней трахеостомии <7 сут.), при этом в публикации Chen X.H. с соавторами и Alkoheji H. с соавторами приходят к выводу, что операция не влияет на показатели выживаемости [10; 11]. Проблема сроков наложения трахеостомы остается актуальной для дальнейших исследований.
Выводы
1. Трахеостомия, произведенная в ранние сроки от момента интубации пациента с COVID-19, статистически значимо уменьшает потребность в вазоинотропной поддержке.
2. Наибольшую фармакологическую нагрузку отмечали у пациентов, которым накладывали трахеостому на 7-14-е сутки.
3. При ранней трахеостомии (1-е сутки) статистически значимо уменьшалось количество дней, проведенных в АРО, на 14-30% (по сравнению с группами 2 и 3 соответственно).
4. При межгрупповом сравнении было установлено, что вне зависимости от срока наложения трахеостомы оперативное вмешательство снижает длительность ИВЛ и количество дней использования медицинской седации у пациентов с COVID-19.
Библиографическая ссылка
Егоров В.И., Овезов А.М., Салихов Д.А., Пряников П.Д., Таджикулова К.Н. ВЛИЯНИЕ СРОКОВ ТРАХЕОСТОМИИ НА ПОТРЕБНОСТЬ В МЕДИЦИНСКОЙ СЕДАЦИИ, ВАЗОИНОТРОПНОЙ ПОДДЕРЖКЕ И ДЛИТЕЛЬНОСТЬ ПРЕБЫВАНИЯ В ОТДЕЛЕНИИ РЕАНИМАЦИИ ПРИ ПРОВЕДЕНИИ ИСКУССТВЕННОЙ ВЕНТИЛЯЦИИ ЛЁГКИХ У ПАЦИЕНТОВ С НОВОЙ КОРОНАВИРУСНОЙ ИНФЕКЦИЕЙ // Современные проблемы науки и образования. 2024. № 5. ;URL: https://science-education.ru/en/article/view?id=33663 (дата обращения: 31.05.2026).
DOI: https://doi.org/10.17513/spno.33663



