Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
COMPARATIVE CHARACTERISTICS OF TREATMENT RESULTS IN PATIENTS WITH SCARRING POST-BURN ESOPHAGEAL STRICTURES
Введение
Доброкачественные рубцовые стриктуры составляют от 20 до 40% всех заболеваний пищевода, и большинство таких пациентов требуют стационарного лечения. Самая частая жалоба при госпитализации - наличие дисфагии [1].
Эндоскопические методы лечения являются основными при оказании медицинской помощи этой категории больных. Указанные вмешательства могут быть выполнены в большинстве наблюдений при доброкачественных рубцовых стенозах пищевода. По данным авторов, это удается сделать у 97,7% больных [2].
В последнее время чаще всего применяется баллонная дилатация, стентирование зоны стеноза, инъекция стероидов, использование ионизированной аргоновой плазмы. Эти методы отлично себя зарекомендовали как малотравматичные и высокоэффективные способы лечения рубцовых стриктур [3-5].
Рестеноз пищевода после завершенного лечения встречается в 30% случаев. Также зачастую клиницисты сталкиваются с рефрактерными стриктурами (не поддающимися расширению методами бужирования или баллонной дилатации за 5 сеансов в течение 2 недель) и рецидивными стриктурами (при невозможности сохранения удовлетворительного просвета в зоне стеноза в течение 4 недель после дилатации стриктуры до 14 мм) [6-8].
Основа патогенеза рецидива стеноза пищевода - возникновение микро- и макроразрывов в области проведения бужирования или дилатации и формирование хронического воспаления в толще рубцовой стриктуры [9].
Перспективным выглядит способ лечения рубцовых стриктур путем внутристеночного введения различных гормональных препаратов (в том числе бетаметазона) с проведением последующего бужирования пищевода [10].
В сравнении с открытыми хирургическими методами лечения эндоскопические имеют свои преимущества в виде малого травматизма и низкого процента осложнений. В группе открытой хирургии описаны 12-54,6% случаев несостоятельности швов анастомоза, развитие рубцовых стриктур пищеводно-кишечных анастомозов развивается в 9-19,6% случаев. Авторы приводят данные о количестве гнойных осложнений, которые в структуре ранних осложнений составили 34,9%. Всего количество послеоперационных осложнений оценено в 10,6% [1; 9].
Цель исследования. Сравнение результатов лечения пациентов с рубцовыми послеожоговыми стриктурами пищевода методом «классического» бужирования и методикой комбинированного лечения (внутристеночное введение бетаметазона с последующим бужированием пищевода).
Материалы и методы исследования
В период с 2007 по 2023 год в отделении торакальной хирургии ГОБУЗ «Новгородская областная клиническая больница» эндоскопически было пролечено 134 больных. Для исследования всего было отобрано 63 пациента (47 мужчин и 16 женщин) в возрасте от 22 до 78 лет, разделенных на две группы. В I группу вошло 30 человек, им выполнялись внутристеночные инъекции бетаметазона, с последующим интраоперационным бужированием пищевода. Во II группу вошло 33 больных, которым проводилось бужирование пищевода под эндоскопическим контролем по струне-направителю («классический» метод). Всем пациентам перед проведением хирургического вмешательства проводилась рентгеноскопия и/или рентгенография пищевода с использованием жидкой бариевой взвеси.
Различные варианты стриктур пищевода по рентгенологическим данным представлены на рисунке 1.
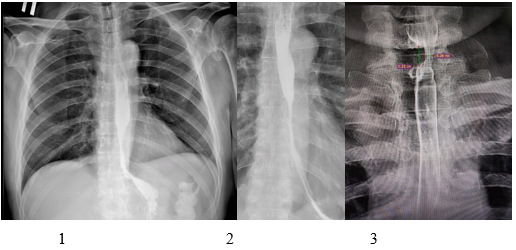
Рис. 1. Варианты стриктур пищевода: 1 - протяженная стриктура нижней трети пищевода; 2 - протяженная стриктура средней трети с переходом на нижнюю треть пищевода; 3 - локальная стриктура верхней трети пищевода
Исследование одобрено локальным этическим комитетом (протокол заседания локального этического комитета ФГБОУ ВО «НовГУ им. Ярослава Мудрого» №2 от 28.02.2023). Все пациенты перед проведением манипуляции подписывали добровольное медицинское согласие.
Из исследования исключены пациенты, у которых отсутствовали жалобы на дисфагию, больные со стенозом пищевода I степени, пациенты с подтвержденным пептическим рефлюкс-эзофагитом.
Эндоскопическое лечение рубцовых стриктур пищевода производилось с помощью видеогастроскопа Pentax-2990К (Pentax Medical, Япония). По ходу пищевода под контролем эндоскопа устанавливалась струна-проводник. Оценивалась зона стеноза, диаметр стеноза, тип стриктуры. Проводилось бужирование пищевода бужами типа Savary от № 12 до 40 Fr. В I группе пациентов перед проведением бужирования проводились подслизистые инъекции бетаметазона 1,0 мл в зоне максимального стеноза (за одну процедуру проводилось от 1 до 3 инъекций), осуществлялся визуальный контроль. Инъекции выполнялись иглой Clear-Jet Injection Catheter, 23G (Finemedix, Корея). В конце оперативного вмешательства под контролем эндоскопа проводился осмотр пищевода, исключались осложнения (разрывы, перфорации и значимые кровотечения), оценивался диаметр пищевода после бужирования.
Клиническая характеристика пациентов представлена в таблице 1.
Таблица 1
Клиническая характеристика пациентов
|
Показатель |
I группа, 30 чел. |
II группа, 33 чел. |
|
Мужчины |
22 (73,3%) |
25 (75,8%) |
|
Женщины |
8 (26,7%) |
8 (24,2%) |
|
Средний возраст (лет) |
51,9±13,1 |
53,4±12,7 |
|
Патология сердечно-сосудистой системы (ИБС, нарушения ритма, гипертоническая болезнь) |
14 (46,7%) |
15 (45,5%) |
|
Патология пищеварительного тракта (язвенная болезнь желудка и двенадцатиперстной кишки, цирроз печени, хронический панкреатит) |
18 (60,0%) |
20 (60,6%) |
|
Сахарный диабет, 2-й тип |
2 (6,7%) |
2 (6,1%) |
|
|
1 (3,3%) |
1 (3,0%) |
|
2 балла |
5 (16,7%) |
6 (18,2%) |
|
3 балла |
22 (73,3%) |
24 (72,7%) |
|
4 балла |
2 (6,7%) |
2 (6,1%) |
Оценка степени дисфагии при поступлении и выписке пациента проводилась в соответствии со шкалой Bown: отсутствие дисфагии - 0 баллов, периодические трудности при проглатывании твердой пищи - 1 балл, питание полужидкой пищей - 2 балла, питание жидкой пищей - 3 балла, полное отсутствие возможности проглотить пищу - 4 балла [11].
Степень стеноза пищевода оценивалась по классификации Ю.И. Галлингера и Э.А. Годжелло: I степень - 9-11 мм, II степень – 6-8 мм, III степень – 3-5 мм, IV степень – 0-2 мм [2].
Всем пациентам в I исследуемой группе ранее уже был выполнен минимум один сеанс бужирования пищевода, и они повторно обратились с клинической картиной рестеноза. Во II группе 7 (21,2%) больных госпитализированы первично, ранее хирургическое лечение не проводилось.
Статистический анализ полученных клинических данных выполнен с помощью программы IBM SPSS Statistics (версия 26). Тест Колмогорова-Смирнова показал, что значения в выборках не подчинялись нормальному закону распределения, использовались непараметрические критерии. Сравнение количественных параметров в анализируемых группах осуществлялось с использованием критерия Манна-Уитни. Частоту качественных показателей оценивали с помощью метода χ2. Различие считалось статистически значимыми при р < 0,05.
Результаты исследования и их обсуждение
Длительность госпитализации в I группе составила от 7 до 26 суток (9,2 ± 3,7), во II группе от 7 до 41 суток (13,1±8,2), разница была статистически значимой (р < 0,001).
Основные этапы проведения комбинированного лечения (внутристеночное введение бетаметазона с последующим бужированием пищевода) у пациента с рецидивирующей стриктурой средней трети пищевода представлены на рисунке 2.
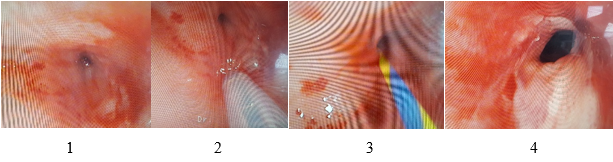
Рис. 2. Основные этапы лечения: 1 - стеноз средней трети пищевода IV степени; 2 - выполнение иглой Clear-Jet Injection Catheter, 23G (Finemedix, Корея) подслизистых инъекций бетаметазона; 3 - установка струны-проводника; 4 - просвет пищевода после проведенного бужирования (диаметр 13 мм)
Локализация уровня сужений пищевода (верхняя треть, средняя треть, нижняя треть), протяженность стриктур (одиночные, множественные) и степени стеноза пищевода (II, III и IV) для обеих групп указана в таблице 2.
Таблица 2
Характеристика поражения пищевода
|
Показатель |
I группа, 30 чел., n (%) |
II группа, 33 чел., n (%) |
p |
|
Стриктура пищевода в верхней трети |
14 (46,7) |
18 (54,6) |
>0,05 |
|
Стриктура пищевода в средней трети |
13 (43,3) |
14 (42,4) |
>0,05 |
|
Стриктура пищевода в нижней трети |
3 (10) |
1 (3) |
>0,05 |
|
Стеноз II степени |
1 (3,3) |
1 (3) |
>0,05 |
|
Стеноз III степени |
26 (86,7) |
27 (81,8) |
>0,05 |
|
Стеноз IV степени |
3 (10) |
5 (15,2) |
>0,05 |
|
Одиночные стриктуры |
26 (86,7) |
25 (75,7) |
>0,05 |
|
Множественные стриктуры |
4 (13,3) |
8 (24,3) |
>0,05 |
Положительных результатов в результате лечения пациентов методом бужирования удалось добиться у 30 (90,9%) пациентов и у 28 (93,3%) больных при лечении комбинированным методом (внутристеночные инъекции бетаметазона, с последующим интраоперационным бужированием) соответственно.
Положительными авторы считали результаты, когда за период одной госпитализации удалось добиться купирования или выраженного уменьшения явлений дисфагии (0-1 балл по шкале Bown) и восстановления диаметра пищевода 12 мм и более в сравнении с исходными данными.
У 60 из всех 63 исследуемых пациентов (95,2%) просвет пищевода в зоне стриктуры после вмешательства был стабилизирован на диаметре от 9 до 22 мм (в среднем - 13 мм). Самый ранний срок возобновления явлений дисфагии и необходимости повторной госпитализации в I группе составил 20 дней, во II группе - 28 дней.
Количество повторно госпитализированных пациентов для выполнения этапного бужирования составило 22 (73,3%) для I группы и 28 (84,8%) для II группы соответственно, разница оказалась статистически значимой (р < 0,05). Однако стоит учитывать, что подавляющее большинство пациентов (100% для I группы и 78,8% для II группы) имели рецидивируюшие и/или рефрактерные стенозы.
Длительность оперативного вмешательства в I группе составила 36±11,4 минуты, во II группе 31±9,6 минуты соответственно, разница оказалась статистически не значимой (р > 0,05).
Результаты лечения пациентов и осложнения (интраоперационные, послеоперационные) в обеих группах представлены в таблице 3.
Таблица 3
Результаты лечения больных обеих групп
|
Показатель |
I группа, 30 чел., n (%) |
II группа, 33 чел., n (%) |
p |
|
Диаметр пищевода 12 мм и более |
20 (66,7) |
21 (63,6) |
>0,05 |
|
Диаметр пищевода 10-11 мм |
9 (30,0) |
10 (30,3) |
>0,05 |
|
Диаметр пищевода 8-9 мм |
1 (3,3) |
2 (6,1) |
>0,05 |
|
Эрозивный эзофагит |
5 (16,7) |
6 (18,2) |
>0,05 |
|
Перфорация пищевода струной |
1 (3,3) |
1 (3,0) |
>0,05 |
|
Разрыв пищевода при бужировании |
0 |
1 (3,0) |
>0,05 |
|
|
28 (93,3) |
30 (90,9) |
>0,05 |
|
2 балла |
2 (6,7) |
3 (9,1) |
>0,05 |
Неудовлетворительный результат лечения характеризовался дилатацией пищевода менее 8 мм и сохраняющимися явлениями дисфагии (2 балла по шкале Bown), он был отмечен у двух пациентов в I группе и у трех - во II группе. Все указанные больные имели рецидивируюшие и/или рефрактерные стенозы и ранее подвергались сеансам бужирования от 3 до 8 раз (в среднем 5 раз).
Перфорация пищевода струной (n=2) в обеих группах не потребовала хирургического лечения, при контрольной фиброгастродуоденоскопии (ФГДС) через 3 суток выявлен формирующийся точечный рубец в месте перфорации, на повторной ФГДС через 7 суток дефекта в пищеводе не обнаружено.
Разрыв пищевода при проведении бужа во II группе (n=1) потребовал хирургического лечения. Разрыв локализовался в нижней трети пищевода, выполнен шов дефекта, лечение больного проводилось по авторскому зарегистрированному патенту №2637824 от 07.12.2017 - «Способ лечения повреждений нижней трети рубцово-суженного пищевода».
Послеоперационный период протекал без осложнений. На контрольной ФГДС через 14 суток дефект не выявлен, при выполнении рентгеноскопии пищевода с контрастированием затека контраста не выявлено. Пациент выписан в удовлетворительном состоянии на 24-е сутки.
Летальных исходов за время стационарного лечения в I группе не наблюдалось, во II группе зафиксирован 1 случай смерти, не связанный с течением основного заболевания. Причина смерти – острый трансмуральный инфаркт миокарда на 7-е сутки после оперативного лечения.
Сроки возникновения рестеноза после завершенного курса лечения для I группы составили от 20 дней до 6 лет (средний срок - 7 месяцев), для II группы – от 28 дней до 3 лет (средний срок – 4 месяца). Разница оказалась статистически значима (U= -3,460; р < 0,001). Частота повторных госпитализаций для I группы колебалась от 1 до 6 в год (в среднем 2,6 в год), для II группы от 1 до 7 в год (в среднем 4,1 в год) соответственно. Разница оказалась статистически значима (U= -3,355; р < 0,001).
В подавляющем большинстве случаев (93,3% для I группы и 90,9% для II группы) удалось добиться удовлетворительного диаметра просвета пищевода и купирования явлений дисфагии. Разница между группами оказалась статистически не значима (р>0,05).
При лечении пациентов с доброкачественными послеожоговыми рубцовыми стриктурами пищевода в стационарных условиях ГОБУЗ «Новгородская областная клиническая больница» (клиническая база кафедры госпитальной хирургии Новгородского государственного университета имени Ярослава Мудрого) авторами всегда используется метод бужирования, так как он является наиболее изученным и безопасным для больного. Введение бужа осуществляется исключительно по струне-направителю, не применяется бужирование «вслепую», врачом во время операции мануально оценивается степень ригидности стриктуры, обеспечивается строгий контроль прилагаемого усилия при проведении бужа. Рестеноз пищевода после завершенного лечения авторы встречали у 41,4% пациентов среди всех случаев оказания помощи.
Особую группу составляют больные с наличием протяженных и/или рефрактерных стенозов III и IV степени (диаметр просвета 5 мм и менее), которые склонны к рестенозированиям после проведения бужирования и требуют более частых госпитализаций. У указанной категории пациентов с целью профилактики рестеноза, а также для снижения плотности и ригидности рубцовой ткани применяются интрамуральные инъекции стероидов [4-6]. Зарубежными авторами данные методы лечения используются при неэффективности многократных бужирований, а именно: невозможность восстановить просвет пищевода до 14 мм за 5 сеансов лечения в течение 2 недель [7; 8].
Авторы в своей клинической практике считают стриктуры пищевода склонными к рецидивированию, когда в процессе этапного лечения наблюдается прогрессивное сужение просвета в течение 4 недель, а рефрактерными стенозами - не поддающиеся расширению в течение 5 сеансов бужирования за срок не более 14 суток.
Из всего многообразия инъекционных гормональных препаратов авторами был выбран бетаметазон (дипроспан), который успешно применяли в течение 15 лет у пациентов с послеожоговыми рубцовыми стриктурами пищевода. Для больных с рецидивирующими и рефрактерными стенозами всегда используется комбинированная методика (внутристеночное введение бетаметазона с последующим бужированием пищевода), что было представлено у 100% больных в анализируемой I группе [10].
После проведения инъекций дипроспана в зону стеноза мануально было отмечено снижение ригидности рубца за счет действия препарата (противовоспалительный, противоаллергический и антиэкссудативный эффекты), тем самым облегчался и ускорялся процесс последующих этапных бужирований при повторных госпитализациях пациента.
Оказание помощи больным с рецидивирующими и рефрактерными стенозами пищевода является достаточно сложным и трудоемким процессом, большинство пациентов имеют низкую приверженность к лечению, зачастую пренебрегая рекомендациями врача к проведению этапных бужирований. Однако, несмотря на это, авторы в своей клинической практике всегда используют комбинированный метод лечения как основной, не прибегая к открытым хирургическим методикам даже в случаях с частыми рецидивами (рестеноз через 1-2 недели), объясняя это высоким процентом осложнений (в том числе и фатальных) при проведении реконструктивных операций на пищеводе, всегда пытаемся сохранить собственный пищевод пациента [10; 12].
Заключение
В настоящее время одной из главных проблем лечения пациентов с рубцовыми послеожоговыми стриктурами пищевода остается формирование рестеноза в зоне ранее проведенного бужирования. Разработанная авторами методика интрамурального введения препарата бетаметазон в рубцовую ткань пищевода с последующим проведением бужирования активно применяется в условиях стационара ГОБУЗ «Новгородская областная клиническая больница» при лечении пациентов с рецидивирующими и/или рефрактерными стенозами. Данный вид оказания помощи позволяет добиться хороших результатов в виде снижения числа повторных госпитализаций и увеличения сроков формирования рестенозирования, является перспективным, требует дальнейшего изучения и накопления опыта.
Библиографическая ссылка
Суковаткин С.И., Сулиманов Р.А., Сулиманов Р.Р., Спасский Е.С., Коротков И.В., Воронкина В.В. СРАВНИТЕЛЬНАЯ ХАРАКТЕРИСТИКА РЕЗУЛЬТАТОВ ЛЕЧЕНИЯ ПАЦИЕНТОВ С РУБЦОВЫМИ ПОСЛЕОЖОГОВЫМИ СТРИКТУРАМИ ПИЩЕВОДА // Современные проблемы науки и образования. 2024. № 4. ;URL: https://science-education.ru/en/article/view?id=33572 (дата обращения: 23.05.2026).
DOI: https://doi.org/10.17513/spno.33572




 Оценка степени дисфагии по Bown: 1 балл
Оценка степени дисфагии по Bown: 1 балл Степень дисфагии по Bown 0-1 балл
Степень дисфагии по Bown 0-1 балл