Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
RESULTS OF OPTIMIZED COMPLEX TREATMENT OF PATIENT WITH FACIAL SKELETON TUMOR
Известно, что в ходе лечения пациентов со злокачественными новообразованиями челюстно-лицевой области, в частности распространенного рака верхней челюсти, применяется метод отсроченной многоэтапной терапии [1; 2, c. 50], включающий: на первом этапе проведение консервативной химиотерапии и лучевой терапии основного онкологического заболевания [2; 3], на втором этапе хирургическое вмешательство, направленное на наиболее радикальное иссечение пораженных тканей; на третьем этапе постановку дентальных имплантатов и снятие оттисков с целью создания опоры для будущей ортопедической конструкции, и на четвертом этапе постановку протеза в полости рта с целью компенсации образовавшегося послеоперационного дефекта [4]. Бисфосфонаты, используемые в химиотерапии, снижают функциональную активность и количество остеобластов и остеокластов, участвующих в процессах регенерации костной ткани после резекции кости и последующей дентальной имплантации [5]. Свой вклад в искаженный остеогенез костной ткани вносит несовершенный ангиогенез, являющийся следствием применения препаратов бисфосфонатного ряда. Отсроченная реконструкция послеоперационного дефекта сопряжена с потерей опоры мягких тканей средней трети лица, ведущей к рубцеванию и атрофии, безвозвратному сокращению объема тканей в этой области [6, c. 158] (рис. 1).
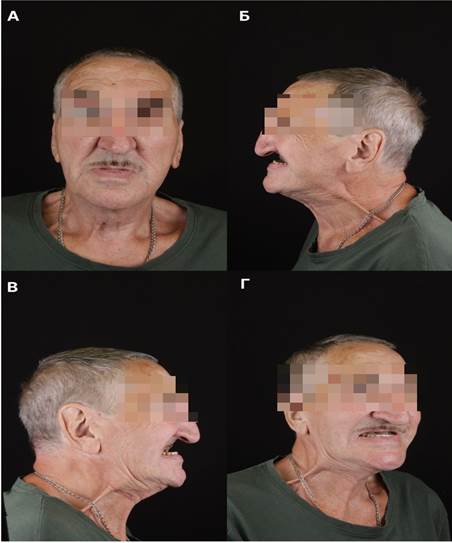
Рис. 1. Пациент после резекции верхней челюсти: А – фас, Б-В – профиль, Г – ¾
Отметим, что утрата жевательной нагрузки со временем приводит к изменению конфигурации суставной головки нижней челюсти, возникновению прогении, ведущей к изменению эстетических параметров лица, а также функциональной атрофии жевательных мышц [7]. Поступление пищи в организм становится возможным только посредством применения назогастрального зонда. Значительно затрудняется речеобразование. Вышеперечисленный ряд изменений твердых и мягких тканей лица в конечном итоге существенно затрудняет адекватное ортопедическое лечение пациентов [8, c. 511]. Отсутствие механической преграды между полостями носа и рта ведёт к нарушению нормального оттока слизи из воздухоносных пазух лицевого скелета, нарушению герметичности полости носа, что затрудняет адекватное носовое дыхание. Дефект нижней стенки полости носа подвергается заживлению первичным натяжением, что вызывает трудности в послеоперационном ведении, а зачастую и невозможность устранения такового [9]. Отсроченное многоэтапное лечение предполагает проведение двух или трех оперативных вмешательств с применением общего анестезиологического пособия, неблагоприятно сказывающегося на реабилитации пациентов. Заслуживает внимания вопрос психоэмоционального состояния пациента, перенесшего ряд длительных и комплексных этапов лечения, многократную госпитализацию, а также весь вышеперечисленный перечень осложнений лечения, значительно затрудняющих функциональную и эстетическую реабилитацию и снижающих качество жизни пациента [9, c. 147].
В литературе описаны методы реконструкции послеоперационного дефекта при помощи малоберцового, лопаточного, лучевого трансплантатов с применением микрохирургических технологий для восстановления костного каркаса скелета [10; 11], однако применение перемещенных трансплантатов невозможно ввиду анатомических особенностей организма пациента. Помимо этого, микрохирургическая реконструкция сопряжена с вероятностью отторжения трансплантата, дентальных имплантатов, невозможностью полноценного восполнения дефекта, с повреждением периферических нервов, сосудов, а также высокой степенью травматизации тканей донорского ложа.
Использование протеза-обтуратора [12, c. 19], выступающего ближайшей альтернативой съемному протезу, имеет недостатки в виде значительной травматизации оставшихся слизистой оболочки и мягких тканей, отсутствия ретенционных пунктов для фиксации, а также в значительно меньшей, в сравнении со съемным протезом, устойчивости к жевательной нагрузке.
Проблема реабилитации утраченных эстетических и функциональных параметров челюстно-лицевой области, адекватный индивидуализированный подход к ведению пациентов на всех этапах комплексного лечения, основывающийся на современных достижениях науки, является одной из главных в повышении качества жизни пациентов после перенесенного лечения онкологического заболевания [13, c. 801].
Цель исследования
Демонстрация клинического случая лечения пациента с опухолью костей лицевого скелета с последующим реконструктивным этапом.
Материалы и методы исследования
Была проанализирована история болезни пациента, включавшая анамнестические сведения, протокол ведения больного, фотопротокол, а также особенности лечения и реконструктивные этапы.
Результаты исследования и их обсуждение
Клинический пример.
Пациентка Н., 65 лет, госпитализирована в ГБУЗ «НИИ-ККБ № 1» им. профессора С.В. Очаповского в 2022 г. с диагнозом: аденокарцинома малой слюнной железы справа. Из анамнеза – страдает от заболевания с 2012 г., многократно проходила хирургическое лечение по поводу новообразования твердого неба. Жалобы при поступлении: на наличие новообразования твердого неба, заложенность носа, нарушение речи. 2012 г. – хирургическое лечение доброкачественного новообразования твердого неба. 2017 г. – резекция твердого неба с реконструкцией височным лоскутом. Аллергологический анамнез не отягощен, переливания компонентов крови, эпидемиологические заболевания, туберкулез, вирусные гепатиты, ВИЧ, заболевания, передающиеся половым путем, отрицает. Семейный анамнез не отягощен. Физикальная диагностика: при осмотре и пальпации структур твердого неба определяется новообразование мягко-эластической консистенции, располагается по обе стороны от небного шва, 6х5 см в максимальном размере, пальпация безболезненна, слизистая оболочка над образованием не изменена. Предварительный диагноз: С-r малой слюнной железы – аденокистозный рак. Рецидив после хирургического лечения от 2017 г. Диагностические процедуры - прижизненное гистологическое исследование операционного материала от 2022 г.: аденокистозная карцинома слюнной железы с инвазией в прилежащие мягкие ткани. Клинический диагноз: C08.8 – C-r малой слюнной железы (аденокистозный рак) TxNoMo после хирургического лечения от 2020 г. II кл. гр. Дифференциальная диагностика: аденома малой слюнной железы. Медицинские вмешательства: в 2022 г. -экстирпация верхней челюсти, постановка дентальных имплантатов, одномоментная постановка временного съемного протеза, снятие оттисков, курс послеоперационной дистанционной гамма-терапии: аппарат АГАТ-С статическим методом, ускоренное фракционирование, 5 раз в неделю с двух противолежащих полей - 7х8, РИК – 75 см, РОК – 4,5 см, РОД – 2,5 Гр, СОД – 40 Гр, установка постоянного зубного протеза, компьютерная томография лицевого скелета. Динамика и исходы: учитывая вероятность возникновения ряда неблагоприятных осложнений лечения, было принято решение о проведении оптимизированного комплексного лечения, включающего одномоментную резекцию костей лицевого скелета, дентальную имплантацию и установку временного съемного протеза, и снятии оттисков для изготовления постоянного съемного протеза. Спустя два месяца были запланированы консервативное лечение методами химио- и радиотерапии, через полгода – установка постоянного съемного протеза. На первом этапе в предоперационном периоде была выполнена конусно-лучевая компьютерная томография лицевого скелета, интраоральное сканирование зубов и слизистой оболочки полости рта, были совмещены данные обоих исследований при помощи программного обеспечения, созданы 3D-модели костной части, зубов и слизистой оболочки верхней челюсти, шаблоны для резекции верхней челюсти и направленной дентальной имплантации, протез верхней челюсти, а также определены границы резекции верхней челюсти. Запланирована установка дентальных имплантатов в области контрфорсов, определены длина и ширина имплантатов (рис. 2).
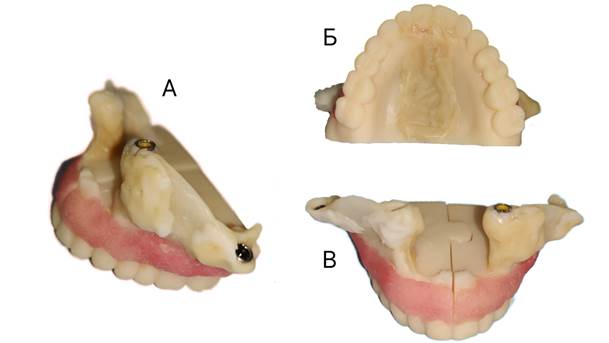
Рис. 2. Временный протез: А - вид сбоку, Б – вид снизу, В – вид сверху
На втором этапе после трёхкратной обработки операционного поля раствором йодсодержащего кожного антисептика и обработки полости рта раствором хлоргексидина биглюконата 0,05% был произведен разрез слизистой оболочки с вестибулярной стороны по ходу межзубных сосочков от области бугра верней челюсти одной стороны до другой стороны до надкостницы верхней челюсти, продолжающийся по границе твёрдого и мягкого нёба, окаймляя бугор верхней челюсти, соединяясь по срединной линии нёба. Произведены поднадкостничная, поднадхрящничная мобилизация мукопериостальных и мукоперихондральных лоскутов, включая слизистую оболочку полости носа; визуализирована опухоль. При помощи винтов была фиксирована 3D-модель шаблонов в области спланированных линий остеотомии, выполнена остеотомия верхней челюсти по шаблонам. Мобилизована верхняя челюсть с опухолью от удерживающих мягких тканей, удалены мобилизованные ткани, осуществлен гемостаз. Таким образом, была осуществлена тотальная максиллэктомия изолированно трансоральным доступом, что послужило фактором ранней реабилитации пациента в послеоперационном периоде. Было произведено частичное покрытие участков открытой костной ткани и раневой поверхности слизистой оболочкой преддверия полости рта. Слизистая оболочка полости носа на уровне средних носовых раковин мобилизована и впоследствии ушита, отграничивая полость носа. Дефект ушит узловыми швами рассасывающимся шовным материалом, произведена установка дентальных имплантатов по линиям остеотомии по 3D-моделям шаблонов, а затем - шариковых абатментов (рис. 3).
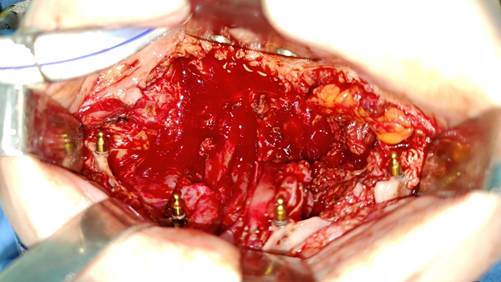
Рис. 3. Имплантаты, установленные в скуловые и носовые кости
Было произведено снятие двухфазного одноэтапного оттиска с корригирующей массой при помощи индивидуальной ортопедической ложки с уровня абатментов, антисептическая обработка полости рта. В зуботехнической лаборатории с использованием аналогов абатментов получена гипсовая модель, наложена лицевая дуга, определено центральное соотношение челюстей, выполнена аксиография, изготовлен функциональный протез с учетом лицевых признаков пациента. Выполнена проверка соответствия временного протеза размеру дефекта, произведена фиксация временного протеза в полости рта на абатментах, произведен контроль окклюзии. На третьем этапе, через 2 месяца после проведения компьютерной томографии и непосредственной визуализации начальных признаков интеграции имплантатов, произвели весь комплекс химиотерапевтических и радиотерапевтических вмешательств, причем через 6 месяцев после оперативного вмешательства выполнили замену временного протеза на постоянный (рис. 4).
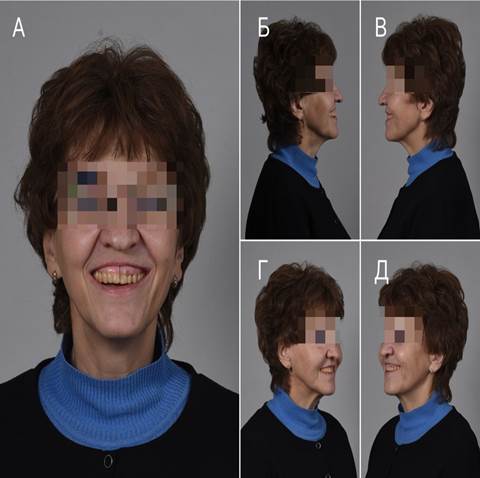
Рис. 4. Пациент c временным протезом в полости рта: А – фас, Б-В – профиль, Г-Д – ¾
Прогноз: благоприятный в отношении повышения качества жизни пациента. Мнение пациента: пациент был удовлетворен результатами лечения, выразил благодарность за удачно спланированный протокол лечения, высказывается о повышении качества жизни, нормальной социализации и оптимистичном настрое. Решение о проведении отсроченного консервативного лечения онкологического заболевания, основывающееся на современных представлениях о патогенезе воздействия препаратов бисфосфонатного ряда и лучевой терапии на костную ткань, привело к полноценной остеоинтеграции дентальных имплантатов и заживлению послеоперационной раны. Тотальная максиллэктомия через внутриротовой доступ – одна из причин оптимизированного эстетического и функционального результатов лечения. Одномоментная реконструкция привела к сохранению опоры мягких тканей, препятствующей рубцеванию и атрофии, сокращению объема тканей средней трети лица. Одномоментная жевательная нагрузка способствовала сохранению конфигурации суставной головки, воспрепятствовала прогении, ведущей к изменению эстетических параметров лица, и функциональной атрофии жевательных мышц. Отсутствие назогастрального зонда, полноценное речеобразование, нормальная дыхательная функция, адекватное дренирование околоносовых пазух послужили факторами благоприятного течения послеоперационного периода наряду с психоэмоциональной стабильностью пациента [14; 15]. Качество жизни пациента было значительно повышено (рис. 5).
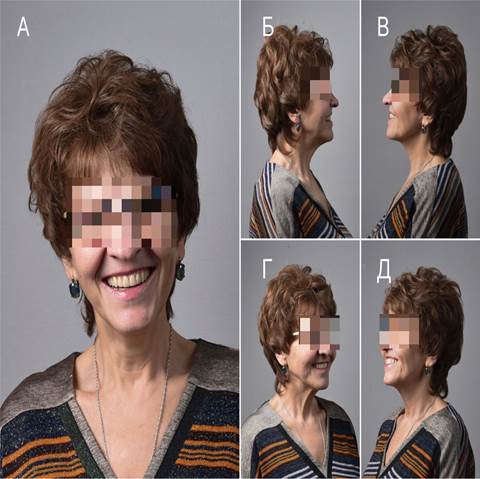
Рис. 5. Заключительный результат лечения: А – фас, Б-В – профиль, Г-Д – ¾
Заключение
Комплексный подход, ориентированный на повышение качества жизни пациентов с онкологическим заболеванием, необходим для получения наиболее успешных результатов в лечении и реабилитации. Многосторонняя проблема ведения таких пациентов требует междисциплинарного взаимодействия врачей разных специальностей. Эстетико-функциональный аспект лечения больных онкологического профиля в последние годы занимает главенствующую позицию в концепции организации комплексного лечения данной категории пациентов, что во многом диктуется возрастающими требованиями самих пациентов. Осваивая идеологию многопрофильного подхода в хирургии головы и шеи, специалист, берущий на себя ответственность за здоровье больного, обязан иметь опыт работы в таких областях, как онкология, челюстно-лицевая, пластическая, эстетическая, реконструктивная хирургия, а также ортопедическая стоматология.
Библиографическая ссылка
Кокаев К.Т., Забунян Г.А., Теремов А.В., Мартиросян А.А. РЕЗУЛЬТАТЫ ОПТИМИЗИРОВАННОГО КОМПЛЕКСНОГО ЛЕЧЕНИЯ ПАЦИЕНТА С ОПУХОЛЬЮ КОСТЕЙ ЛИЦЕВОГО СКЕЛЕТА // Современные проблемы науки и образования. 2024. № 3. ;URL: https://science-education.ru/en/article/view?id=33454 (дата обращения: 28.05.2026).
DOI: https://doi.org/10.17513/spno.33454



