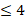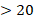Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
THE DYNAMICS OF SOME HEMOSTASIS PARAMETRES IN PATIENTS WITH ISHEMIC STROKE RECEIVING ANTICOAGULANTS
Инсульт – это одна из главных причин летального и долгосрочного инвалидизирующего воздействия на население. Ишемический инсульт (ИИ) встречается примерно в 75–80% случаев нарушения кровообращения в мозге [1]. У лиц, подвергшихся инсульту или транзиторной ишемической атаке, риск повторного инсульта увеличивается в десять раз, преимущественно в течение первого года после первого эпизода, согласно данным литературы [2]. Кардиоэмболический инсульт (КИ), развившийся в результате артериальной окклюзии эмболом, первоначально сформированным в сердце [3], чаще всего возникает на фоне фибрилляции предсердий (ФП), вследствие чего нередко наблюдаются острое развитие неврологического дефицита и его максимальная выраженность в разгаре заболевания [4, 5]. ФП является нарушением сердечного ритма, которым страдают 33 млн человек во всем мире [6]. ФП увеличивает вероятность развития инсульта в 3–5 раз [7].
Активация процессов свертывания крови и дисфункция эндотелиальных клеток играют ключевую роль в развитии ишемического инсульта, часто приводя этот процесс к образованию тромбов и эмболий. Более 60% случаев инсульта связано с атеротромбозом и тромбоэмболическими осложнениями [3]. В начальных периодах инсульта отмечаются изменения в системе сосудистых и тромбоцитарных реакций, указывающие на продолжительное воздействие свертывающих факторов, повышенную склонность к тромбообразованию и дисфункцию эндотелия, а также на увеличенную активность тромбоцитов. Для понимания биохимических процессов ИИ требуется глубокое изучение переплетенных процессов, включая метаболические пути и механизмы свертывания крови. Нарушения в системе гемостаза запускают сложную цепь биохимических реакций в ответ на повреждения мозговой ткани. Гемостаз постоянно модулируется, реагируя на повреждения мозга и изменения биомаркеров. В острой фазе инсульта наблюдаются усиление активности плазменных факторов свертывания (например, фибриногена, тромбина), уменьшение прочности сосудистой стенки к образованию тромбов, уменьшение активности системы антикоагуляции (например, снижение уровня протеина S) и снижение активности фибринолитической системы [8]. Аномалии в системе гемостаза у пациентов с ФП могут оказывать дополнительное влияние на процессы свертывания, воздействие которых требует более глубокого изучения. Однако понимание взаимосвязей между свертывающими и противосвертывающими механизмами открывает путь к целенаправленному воздействию на эти системы, что благоприятно сказывается на прогнозе заболевания.
Раннее введение антикоагулянтов при ИИ позволяет ограничить распространение тромба в мозговой артерии и снизить риск тромбоэмболических осложнений, тромбоза глубоких вен. Это, в свою очередь, может уменьшить объем инфаркта головного мозга, а также неврологический дефицит, инвалидность и смертность. Однако использование антикоагулянтов сопряжено с риском кровотечения, который необходимо тщательно взвесить по сравнению с потенциальными преимуществами. Для принятия решения о назначении антикоагулянтов при ИИ клиницисты должны учитывать индивидуальный профиль риска и пользу для пациента, стремясь к оптимальному балансу между предотвращением тромбоэмболических событий и минимизацией риска кровотечений [9].
Несмотря на наличие в настоящее время большого арсенала антикоагулянтных препаратов, наиболее часто применяемым по-прежнему остается гепарин. Открытие гепарина относится к 1916 году, но лишь в 1937 году благодаря усовершенствованию методов его очистки препарат был применен в клинической сфере выдающимся канадским хирургом Г. Морреем, что заложило основу для его широкого использования в медицинской практике [10]. Гепарин – это антикоагулянт, который широко используется для лечения и профилактики тромбоэмболических осложнений. Он действует путем связывания с антитромбином, который является естественным ингибитором тромбина и фактора свертывания Ха. Гепарин способствует разрушению тромбов за счет активации фибринолиза, что благоприятствует перераспределению тромботической массы и улучшению микроциркуляции в мозге. Он имеет способность снижать воспалительные процессы в сосудистой стенке, что помогает уменьшить местный воспалительный ответ в окружающих тканях при инсульте [11]. Также гепарин помогает защитить эндотелий сосудов от повреждений, уменьшая риск дальнейшего развития цереброваскулярных осложнений. Эти свойства гепарина обусловливают его эффективность в лечении инсульта и позволяют снизить риск осложнений, улучшить прогноз пациентов.
Однако в настоящее время требуется более глубокое изучение эффективности антикоагулянтной терапии с использованием гепарина у пациентов, страдающих ишемическим инсультом, который сопровождается фибрилляцией предсердий, ввиду ограниченного объема научных исследований, посвященных данной тематике. Исследования взаимосвязи изменений параметров гемостаза у пациентов с ишемическим инсультом на фоне приема антикоагулянтов являются ключевыми аспектами данного исследования.
Цель исследования: оценка изменений показателей гемостаза у больных в острый период ишемического инсульта на фоне приема антикоагулянтов.
Материал и методы исследования. Состояние системы гемостаза было исследовано у 48 пациентов в возрасте от 57 до 82 лет, проходивших лечение в отделении неврологии № 1 для лечения больных с острым нарушением мозгового кровообращения (ОНМК) ГБУЗ РМ «Мордовская республиканская центральная клиническая больница» в период со 2 декабря 2021 г. по 17 мая 2024 г. с диагнозом ОНМК. Все участники исследования получали полный стандартный курс лечения основного заболевания и сопутствующей патологии в соответствии с нозологическими стандартами, действовавшими на момент госпитализации.
Критерии включения в исследование: возраст старше 18 лет; установленный на основании данных компьютерной томографии головного мозга диагноз ишемического ОНМК (кардиоэмболический подтип по критериям TOAST); установленный в анамнезе или на момент госпитализации факт наличия любой формы ФП; риск кардиоэмболических осложнений по шкале CHA2DS2-VASc – 1 у мужчин и 2 – у женщин. Критериями исключения из исследования были: геморрагический инсульт, подтвержденный методами нейровизуализации; инфаркт головного мозга с геморрагическим пропитыванием; инфаркт миокарда в анамнезе давностью менее 1 года; эпилепсия; системные заболевания соединительной ткани.
Оценка тяжести неврологического дефицита осуществлялась по шкале National Institute of Health Scale (NIHSS) и имела следующие особенности: легкий неврологический дефицит (до 4 баллов по National Institute of Health Scale – NIHSS) – 8 пациентов, средней тяжести (5–20 баллов) – 32 пациента, тяжелый (более 20 баллов) – 8 пациентов (табл. 1). Все пациенты, включенные в исследование, получали антикоагулянтную терапию нефракционированным гепарином в дозе 5000 МЕ каждые 6 часов в течение 5–7 дней, антитромбоцитарную терапию препаратами ацетилсалициловой кислоты (АСК) в течение 10 дней.
Таблица 1
Тяжесть перенесенного инсульта
|
Тяжесть течения ОНМК |
Число баллов по NIHSS |
% |
n |
|
Легкая |
|
16,7 |
8 |
|
Средней тяжести |
5–20 |
66,7 |
32 |
|
Тяжелая – крайне тяжелая |
|
16,7 |
8 |
В данном исследовании проводилась оценка следующих показателей: тромбоцитов для оценки изменений в сосудисто-тромбоцитарном гемостазе, активированного частичного тромбопластинового времени для выявления изменений во внутреннем механизме плазменного гемостаза, протромбинового индекса и протромбинового времени для выявления изменений во внешнем механизме плазменного гемостаза, протромбинового отношения для оценки изменений плазменного гемостаза и активности протромбинового комплекса, фибриногена для оценки третьей фазы плазменного гемостаза (образование фибрина).
Помимо тщательного анализа параметров, ответственных за свертываемость крови, каждому пациенту был предоставлен целый комплекс лабораторных и инструментальных исследований, охватывающий разнообразные аспекты согласно приказу Минздрава РФ относительно оказания медицинской помощи пациентам, столкнувшимся с ОНМК. Набор исследований включал в себя биохимический анализ крови, отражающий уровень липидов в организме, рентгенографию органов грудной клетки, ЭКГ, электроэнцефалографию, а также ультразвуковую допплерографию брахиоцефальных артерий, КТ головного мозга, а также консультацию специалистов (кардиолога, терапевта и др.).
Статистическую обработку полученных данных проводили с применением программы StatTech v. 4.1.0. Количественные показатели оценивали на предмет соответствия нормальному распределению с помощью критерия Шапиро–Уилка. Различия считались статистически значимыми при p<0,05.
Результаты исследования и их обсуждение. Нами осуществлено изучение лабораторных показателей 48 пациентов с установленным диагнозом ОНМК. В состав группы исследуемых вошли пациенты в возрасте от 57 до 82 лет, из них мужчин 20 человек (42%), женщин 28 (58%). Превалирование среди пациентов женщин подтверждает общие статистические показатели по данному заболеванию.
Сопутствующая патология выявлена у 48 пациентов (100%): сахарный диабет – у 19 больных (40%), ИБС – у 19 больных (100%), ГБ – у 43 больных (90%). Таким образом, пациенты с ОНМК и ФП имели коморбидную патологию, ухудшающую прогноз. Установлено, что у больных сахарным диабетом отмечались угнетение противосвертывающей и активация свертывающей системы. У больных ГБ существенных изменений показателей системы гемостаза не выявлено. Необходимо отметить, что общеизвестным важным фактом, подтвержденным множеством клинических наблюдений и исследований, является высокий риск развития геморрагических осложнений при сочетании фибрилляции предсердий и инсульта. В остром периоде инсульта происходит комплексный каскад изменений функций систем гемостаза, обусловленных не только объемом пораженной ткани, но и предшествующим состоянием системы гемостаза, наличием сопутствующих заболеваний и различных механизмов патогенеза нарушения кровоснабжения мозга.
По данным КТ головного мозга была отмечена локализация инсульта в следующих сосудистых бассейнах: в бассейне левой средней мозговой артерии у 9 пациентов (19%), в бассейне правой средней мозговой артерии у 34 пациентов (71%), в вертебрально-базилярном бассейне у 5 пациентов (10%). Большой объем очага составил более 50 см3 и отмечался у 5 пациентов (10%), средний очаг объемом от 10 до 50 см3 – у 33 пациентов (69%), малый очаг объемом до 10 см3 – у 10 пациентов (21%). По данным дуплексного сканирования брахиоцефальных артерий у 30 пациентов (63%) установлен стеноз правой внутренней сонной артерии менее 50%, у 6 пациентов (13%) – стеноз левой внутренней сонной артерии менее 50%, у 3 пациентов (6%) – стеноз правой общей сонной артерии менее 50%, у 9 пациентов (19%) гемодинамически значимых стенозов не обнаружено. Зависимости изменений показателей гемостаза от локализации инсульта, размера ишемического очага, наличия или отсутствия стенозирования брахиоцефальных артерий не отмечалось. У пациентов с тяжелым неврологическим дефицитом (по шкале NIHS) в лабораторных анализах отмечался более высокий уровень фибриногена (6,88±1,98), чем у пациентов со средним и легким неврологическим дефицитом (p=0,001). Это свидетельствует о зависимости склонности к гиперкоагуляции от степени тяжести неврологического статуса.
Рассмотрим результаты проведенных гемостазиологических параметров наблюдаемых больных в 1-й и 10-й день заболевания, представленные в таблице 2. Проанализировав данные, представленные в таблице 2, можно сделать вывод, что тромбоциты находятся в пределах нормы в 1-й и 10-й день заболевания, и на 10-й день мы наблюдаем незначительное снижение показателя (p=0,001). Это свидетельствует о благоприятном течении острого периода, так как повышенный уровень тромбоцитов или изменение их функции могут привести к усилению тромбообразования и обострению ишемического повреждения. Гепаринотерапия может осложниться развитием гепарин-индуцированной тромбоцитопении, поэтому важно определять этот показатель до начала лечения и на 6–14-е сутки терапии [10].
Таблица 2
Показатели системы гемостаза в 1-е и 10-е сутки заболевания
|
Показатели |
M ± SD |
95% ДИ |
min |
max |
|
В 1-е сутки заболевания (n=48) |
||||
|
Фибриноген, г/л |
5,74±1,26 |
5,27–6,21 |
2,57 |
8,86 |
|
Протромбиновое время, сек. |
12,54±1,48 |
11,22–13,20 |
10,90 |
17,40 |
|
Протромбиновый индекс, % |
95,97±15,37 |
90,23–101,71 |
59,00 |
116,00 |
|
Протромбиновое отношение |
1,15±0,14 |
1,03–1,21 |
1,00 |
1,60 |
|
АЧТВ, сек. |
31,67±4,37 |
29,65–33,85 |
22,10 |
46,10 |
|
Тромбоциты, х109/л |
234,37±62,8 |
196,25–264,75 |
131,00 |
450,00 |
|
На 10-е сутки заболевания (n=48) |
||||
|
Фибриноген, г/л |
6,59±1,65 |
5,98–7,21 |
3,71 |
9,56 |
|
Протромбиновое время, сек. |
13,04±1,84 |
12,36–13,73 |
9,90 |
17,40 |
|
Протромбиновый индекс, % |
88,97±15,91 |
83,02–94,91 |
59,00 |
116,00 |
|
Протромбиновое отношение |
1,22±0,23 |
1,10–1,32 |
0,91 |
2,07 |
|
АЧТВ, сек. |
32,45±6,00 |
30,21–34,69 |
21,20 |
47,30 |
|
Тромбоциты, х109/л |
213,00±64,79 |
188,81–237,19 |
110,00 |
405,00 |
АЧТВ находится в диапазоне референсных значений как в 1-е, так и на 10-е сутки заболевания. Но на 10-е сутки можно отметить некоторое повышение показателя, однако различия признаны статистически недостоверными (p=0,281), следовательно, показатель оставался стабильным. Это свидетельствует об эффективности терапии гепарином, поскольку для острого периода инсульта, не сопровождающегося приемом антикоагулянтов, характерна тенденция к снижению данного показателя. Показатель ПТИ также не выходит за пределы нормы на 1-е и 10-е сутки заболевания, но на 10-е сутки значение приближается к нижней границе нормы и составляет 88,97±15,91 (p=0,001). Протромбиновое время в 1-е сутки заболевания находится на верхней границе нормы, а на 10-е сутки незначительно повышается (13,04±1,84) (p=0,001). Удлинение протромбинового времени является благоприятным признаком в отношении профилактики повторного ОНМК. Протромбиновое отношение в 1-е и 10-е сутки заболевания приближено к верхней границе нормы, и на 10-е сутки можно отметить незначительный рост показателя (p=0,004). В острейшем периоде ОНМК у пациентов определялось повышенное содержание маркера гиперкоагуляции – фибриногена. Тенденция к его увеличению (6,59±1,65) сохранялась и на 10-е сутки на фоне лечения гепарином и являлась статистически значимой (p=0,001), что говорит о сохранении гиперкоагуляционного потенциала. Это подтверждают литературные данные, согласно которым в остром периоде инсульта выявляется гемостатический дисбаланс с активизацией системы гемостаза [8]. Повышенный уровень фибриногена увеличивает вероятность образования тромбозов и усугубляет течение заболевания. Регулярный мониторинг показателей гемостаза позволяет выявлять любые потенциальные осложнения, такие как чрезмерное увеличение АЧТВ, что может указывать на повышенный риск кровотечения.
Заключение. Таким образом, при сопоставлении показателей гемостаза у больных в 1-е и 10-е сутки заболевания на фоне приема нефракционированного гепарина в дозе 15000 МЕ в сутки была отмечена склонность к гиперкоагуляции. Полученные данные могут быть рассмотрены при разработке дифференцированной антикоагулянтной терапии и возможности применения прямых оральных антикоагулянтов.
Мониторинг динамики показателей гемостаза у больных с ишемическим инсультом на фоне приема антикоагулянтов имеет решающее значение для оптимизации лечения и минимизации риска тромбоза и кровотечения. Проведение анализа реологических параметров в остром периоде инсульта открывает перспективу индивидуализированной коррекции с целью профилактики развития повторного ОНМК. Понимание влияния антикоагулянтов на гемостаз и клинического значения изменений показателей гемостаза является важным аспектом лечения пациентов с ИИ. Продолжающиеся исследования в этой области помогут достичь оптимальной стратегии мониторинга и лечения, направленной на улучшение исходов заболевания и качества жизни пациентов с ишемическим инсультом.
Конфликт интересов: авторы заявляют об отсутствии конфликта интересов.
Библиографическая ссылка
Роганова Н.А., Бойнова И.В., Токарева Н.Г. ДИНАМИКА НЕКОТОРЫХ ПОКАЗАТЕЛЕЙ ГЕМОСТАЗА У БОЛЬНЫХ С ИШЕМИЧЕСКИМ ИНСУЛЬТОМ НА ФОНЕ ПРИЕМА АНТИКОАГУЛЯНТОВ // Современные проблемы науки и образования. 2024. № 3. ;URL: https://science-education.ru/en/article/view?id=33430 (дата обращения: 28.05.2026).
DOI: https://doi.org/10.17513/spno.33430