Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
ONE-STAGE REVISION ANTERIOR CRUCIATE LIGAMENT RECONSTRUCTION WITH BONE TUNNEL MALPOSITION. A CLINICAL CASE
Разрыв передней крестообразной связки (ПКС) является одной из распространенных травм коленного сустава (КС). Выполнение первичной артроскопической реконструкции ПКС в большинстве случаев приводит к удовлетворительным результатам лечения [1]. Однако, по данным научной литературы, частота возникновения несостоятельности трансплантата ПКС при минимальном пятилетнем сроке наблюдения составляет 5,8% [2], а при десятилетнем сроке наблюдения – 7,9% [3].
На сегодняшний день у хирургического сообщества нет однозначной точки зрения на причины неудовлетворительных исходов первичной реконструкции ПКС. Тем не менее установлено, что одним из основных факторов риска является мальпозиция проведенных костных каналов [4].
В свою очередь, в отличие от первичной реконструкции ПКС, неудовлетворительные исходы ревизионного вмешательства встречаются в 3-4 раза чаще [5; 6]. Однако, несмотря на тенденцию к снижению процента неудачных повторных реконструкций ПКС [7], клинические и функциональные результаты после данного оперативного вмешательства являются не сопоставимыми с результатами первичной реконструкции ПКС. Одним из важных аспектов, позволяющих улучшить результаты ревизионной реконструкции ПКС, является адекватное предоперационное планирование, которое должно учитывать возможные причины первичной неудачи, технические особенности ревизионной операции, а также возможность выполнения повторного вмешательства в один этап, с целью снижения хирургической агрессии.
Таким образом, ревизионная реконструкция ПКС требует от хирурга понимания причин первичных неудач, а также грамотного подхода к планированию и определению оптимальной тактики оперативного вмешательства.
Цель исследования: предоставить описание клинического случая одноэтапной ревизионной реконструкции передней крестообразной связки при мальпозиции костных каналов.
Клинический случай
Пациентка К., 40 лет, обратилась в консультативно-диагностическое отделение ФГБУ «ННИИТО им. Я.Л. Цивьяна» Минздрава России. После осмотра, сбора жалоб, анамнеза и предоставленной документации, а также имеющихся результатов инструментальных методов исследования был выставлен диагноз: «Разрыв трансплантата передней крестообразной связки левого коленного сустава. Передняя нестабильность левого коленного сустава 3 степени. Левосторонний посттравматический гонартроз 1 ст. НФС 0-1 ст. (Реконструкция передней крестообразной связки аутотрансплантатом из сухожилий подколенных сгибателей голени c кросс-пин-фиксацией от 2012 г.)».
Пациентка предъявляла жалобы на боль, усиливающуюся при физической нагрузке, ограничение функции и чувство нестабильности левого коленного сустава.
Из анамнеза: получила травму в результате падения на левую нижнюю конечность в декабре 2011 г. Обратилась в травматологический пункт, где выполнено рентгенологическое исследование, в результате которого не было выявлено костных повреждений. Затем на амбулаторном этапе проводилась консервативная терапия со слабой положительной динамикой: болевой синдром купирован, однако нестабильность и ограничение функции в коленном суставе прогрессировали. Было рекомендовано выполнение МРТ-исследования, в результате которого диагностирован полный разрыв передней крестообразной связки. В 2012 году выполнено оперативное вмешательство – артроскопическая реконструкция передней крестообразной связки аутотрансплантатом из сухожилий полусухожильной и тонкой мышц с кросс-пин-фиксацией. Реабилитационный период протекал без особенностей. После завершения восстановительного периода, в промежутке с 2013 по 2020 год, пациентка отмечала эпизоды нестабильности в коленном суставе при ротационных движениях, частота возникновения которых увеличивалась с течением времени, однако по данному поводу за медицинской помощью не обращалась. В январе 2021 года также произошел эпизод нестабильности левого коленного сустава, при котором возникла резкая боль в суставе. После интерпретации результатов исследований было рекомендовано оперативное вмешательство – ревизионная реконструкция передней крестообразной связки.
1 мая 2022 года пациентка поступила для оперативного лечения в травматолого-ортопедическое отделение № 4 ФГБУ «ННИИТО им. Я.Л. Цивьяна» Минздрава России.
Травматолого-ортопедический статус. Ходит без дополнительных средств опоры, прихрамывая на левую нижнюю конечность. Положение левой нижней конечности – правильное. Область коленного сустава правильной формы, кожные покровы чистые, контуры сустава сглажены. При пальпации отмечается болезненность в проекции суставной щели. Менисковые симптомы слабоположительные. Симптом баллотирования надколенника отрицательный. Объем движений в коленном суставе полный. Связочный аппарат: симптом переднего выдвижного ящика, тест Лахмана и тест pivot-shift – «+++», симптом заднего выдвижного ящика, тест на повреждение боковых связок отрицательные. Нагрузка по оси голени безболезненна. Гипотрофии мышц нижней конечности не отмечается. Послеоперационные рубцы без особенностей. Сосудистых, двигательных, чувствительных нарушений в дистальных отделах нижних конечностей не выявлено. Контралатеральная нижняя конечность без особенностей – кожный покров не поврежден, движения в полном объеме, периферическая пульсация, чувствительность сохранены.
Показатели функции коленного сустава оценивались по шкалам Lisholm и IKDC и составили 58 и 56 баллов соответственно. Функциональное состояние левого голеностопного сустава оценивалось с применением шкалы AOFAS и составило 98 баллов.
Предоперационное планирование
Стандартная предоперационная оценка состояния коленного сустава. Была выполнена рентгенография коленных суставов в двух проекциях в опоре. Выявлен остеоартроз левого коленного сустава I стадии, другой костной патологии не обнаружено. Состояние после реконструктивной пластики передней крестообразной связки. Артифициальные каналы метафиза большеберцовой и бедренной кости.
Оценка трансплантата ПКС. Для определения целостности и сопутствующих повреждений коленного сустава анализировали данные магнитно-резонансной томографии коленного сустава. МРТ-исследование: состояние после реконструктивной пластики передней крестообразной связки левого коленного сустава. На момент исследования морфологически определяется нарушение целостности трансплантата. Дегенеративные изменения латерального мениска, заднего рога медиального мениска (II степень по Stoller). Гонартроз 1-2 степени.
Оценка положения костных каналов. Для определения положения костных каналов выполняли мультиспиральную компьютерную томографию (МСКТ) коленного сустава с последующей трехмерной реконструкцией.
Положение точки входа в большеберцовый канал рассчитывали по методу анатомических координатных осей в процентах (рис. 1).
При оценке положения большеберцового канала выявлено, что центр точки входа в большеберцовый канал располагался в 72,5% от переднего края плато большеберцовой кости (E/C%) и в 49,2% от медиального края плато большеберцовой кости (F/D%). Диаметр канала составлял 8 мм. В свою очередь, согласно исследованию Tsukada H. и соавт. [8], был отмечен «анатомичный» центр точки входа в большеберцовый канал (A/C (%) – 43,8%, B/D (%) – 48,9%) (рис. 1).
Также была проведена оценка процентной разницы между имеющимся положением большеберцового канала и предполагаемой планируемой точкой входа в канал. В результате оценки выявлено, что разница между центрами точек входа составляет 28,7%, что свидетельствует об отсутствии риска слияния имеющегося канала с планируемым.
Центральную точку входа в бедренный канал оценивали с помощью квадрантного метода, описанного M. Bernard и соавт. (при сгибании в коленном суставе под углом 90°) [9] (рис. 2).
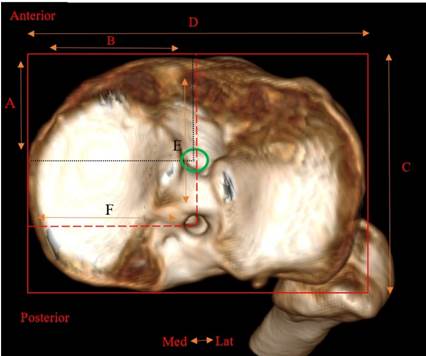
Рис. 1. Ось C – линия между передним и задним краем плато большеберцовой кости; ось D – линия между медиальным и латеральным краем плато большеберцовой кости
При оценке положения бедренного канала выявлено, что центр точки входа располагался в 60,1% от наиболее глубокой точки крыши межмыщелковой вырезки (B/t%) и в 14,0% от линии Blumensaat (A/h%). Диаметр канала составлял 8,3 мм. В свою очередь, согласно исследованию Tsukada H. и соавт. [8], был отмечен «анатомичный» центр точки входа в бедренный канал (D/t (%) – 30.4%, C/h (%) – 29,9%) (рис. 2).
Исходя из полученных данных, отсутствия каких-либо фиксаторов, не поддающихся удалению, а также учитывая диаметр и вектор направления имеющегося канала, было принято решение о проведении «нового» канала в другом векторе направления и с «анатомичной» точкой входа, при этом без риска пересечения и слияния с имеющимся каналом.
Ввиду отсутствия показаний не выполнялись восстановление переднелатерального комплекса и коррекция деформации плато большеберцовой кости в сагиттальной плоскости.
Дополнительные аспекты предоперационного планирования. В качестве трансплантата планировалось использование аутографта из сухожилия длинной малоберцовой мышцы (PLT). Фиксацию трансплантата планировалось осуществить комбинированным методом: большеберцовый конец трансплантата – интраканальным методом фиксации (биодеградируемый винт), а экстракортикальный метод применить для фиксации бедренного конца трансплантата.
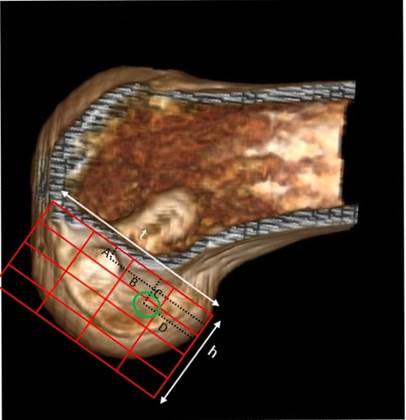
Рис. 2. Ось t – диаметр, измеренный по крайним точкам переднего и заднего края латерального мыщелка бедренной кости, проведенный по линии Blumensaat в сагиттальной плоскости; ось h – линия, проведенная перпендикулярно линии Blumensaat, которая является максимальной высотой межмыщелковой вырезки
Оперативное вмешательство. После проведения предоперационного планирования было выполнено оперативное вмешательство: артроскопия левого коленного сустава; одноэтапная ревизионная реконструкция передней крестообразной связки. Согласно полученным интраоперационным данным, было подтверждено повреждение трансплантата передней крестообразной связки и некорректное положение каналов. Бедренный канал от предшествующего оперативного вмешательства имел «неанатомичное» положение: вход в канал находился краниально и кпереди от планируемой, корректной точки входа (рис. 3). Вход в большеберцовый канал также имел «неанатомичное» положение - кзади от планируемой, корректной точки входа в канал. Сопутствующих повреждений гиалинового хряща, медиального и латерального менисков не выявлено. После обработки трансплантата его диаметр составил 9 мм. При проведении бедренного и большеберцового каналов не возникло пересечения или слияния с каналами от предшествующего оперативного вмешательства.
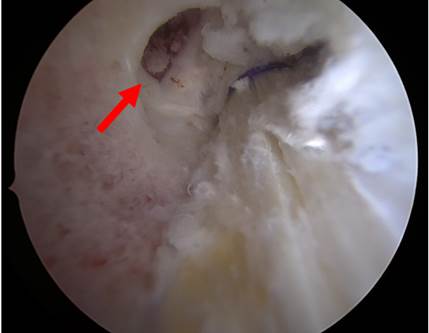
Рис. 3. Положение входа в бедренный канал от предшествующего вмешательства (красная стрелка) относительно канала, проведенного во время ревизионного вмешательства
Послеоперационный период. Послеоперационная оценка положения костных каналов проводилась по результатам МСКТ-исследования с последующей трехмерной реконструкцией (рис. 4, 5).
Положение точек входа вновь проведенных каналов соответствовало результатам предоперационного планирования, и полученные значения соотносились с общепринятыми нормами «анатомичного» места крепления трансплантата.
Ранний послеоперационный период протекал без особенностей, пациенткой был пройден курс физиотерапии и восстановительного лечения.
На контрольном осмотре через один месяц после оперативного вмешательства пациентка предъявляла жалобы на умеренную болезненность и возникновение отека области коленного сустава при физической нагрузке, а также ограничения сгибания, однако после прохождения курса реабилитационных мероприятий данные симптомы купировались. При осмотре: признаков синовита, инфекции области оперативного вмешательства, неврологических и сосудистых нарушений, а также нестабильности в коленном суставе не определялось.
На контрольном осмотре через 6 месяцев после оперативного вмешательства пациентка жалоб не предъявляла, передвигалась без средств дополнительной опоры. Область левого коленного сустава правильной формы, послеоперационные рубцы без признаков воспаления, отечность и болезненность отсутствовали. Симптомы Чаклина, Байкова, Брагарда, Штеймана отрицательные. Симптом баллотирования надколенника отрицательный. Движения в коленном суставе: 110/0/0. Связочный аппарат: симптом переднего выдвижного ящика, тест Лахмана и тест pivot-shift – отрицательные, симптом заднего выдвижного ящика, тест на повреждение боковых связок отрицательные. Нагрузка по оси голени безболезненна. Гипотрофии мышц нижней конечности не отмечается.

Рис. 4. Положение входа в бедренный канал. Зеленым цветом отмечен вновь проведенный канал, красным – предшествующий канал
Рис. 5. Положение входа в большеберцовый канал. Зеленым цветом отмечен вновь проведенный канал, красным – предшествующий канал
Пациентка удовлетворена результатом лечения, восстановлением функции и стабильности левого коленного сустава, а также возможностью вести активный образ жизни. Показатели функции коленного сустава существенно улучшились и в результате составили: по шкале Lisholm – 85 баллов, а по шкале IKDC – 80 баллов. При оценке функции стопы и голеностопного сустава по шкале AOFAS показатели не изменились и имели такие же значения, как и до операции – 98 баллов.
Обсуждение. Решение о проведении одноэтапной или двухэтапной ревизии ПКС зависит от множества факторов. Как правило, в современной литературе описывается выполнение одноэтапного вмешательства пациентам с корректно расположенными каналами, имеющими диаметр менее 14 мм, хороший костный запас, а также фиксаторы, поддающиеся удалению. Тем не менее в большинстве исследований диаметр канала не являлся основополагающим фактором в определении показаний к проведению одно- или двухэтапного оперативного вмешательства, в отличие от оценки разницы положений имеющихся и планируемых точек входа в каналы [7].
В свою очередь, имеются исследования, в которых рассматриваются методики, позволяющие выполнить одноэтапную ревизионную реконструкцию ПКС при корректно расположенных, но вторично расширенных каналах (диаметр которых более 14 мм). В частности, в работах B.C. Werner и соавт. [10] и J.L. Dragoo и соавт. [11] сообщалось о хороших послеоперационных клинических результатах одноэтапной повторной реконструкции ПКС с одновременной костной пластикой вторично расширенных каналов цилиндрическим аллокостным трансплантатом с press-fit-установкой и интраканальной фиксацией. Однако предложенные технологии обладают рядом недостатков: во-первых, те или иные виды костных аллотрансплантатов могут быть недоступны; во-вторых, относительная сложность данных одноэтапных методик может приводить к увеличению длительности операции и возникновению осложнений во время ее выполнения.
С другой стороны, полноценное предоперационное планирование позволяет определить возможность одноэтапного оперативного вмешательства, оценив взаиморасположение планируемых и имеющихся костных каналов. Авторы современных исследований сообщают, что анализ корректности проведенных первичных каналов может производиться с использованием различных методов, которые доказали свою эффективность [8; 12]. В частности, во многих работах оценка положения центральной точки входа в большеберцовый канал проводилась с использованием метода анатомических координатных осей [12-14], а анализ положения точки входа в бедренный канал осуществлялся с помощью квадрантного метода, описанного M. Bernard и соавт. [9]. Данные методики широко известны, длительное время используются хирургическим сообществом и хорошо себя зарекомендовали в качестве оценочных систем, несмотря на имеющиеся погрешности, возникающие при их использовании [8].
Учитывая отрицательные аспекты двухэтапного ревизионного оперативного вмешательства, J.-H. Ahn и соавт. в своем исследовании оценили возможности выполнения одноэтапных ревизионных реконструкций ПКС на основании предоперационного планирования, в результате которого пациентам с разницей между диаметром имеющегося входа в канал и планируемой точкой входа более 50% проводился «новый» канал, но в другом векторе направления от имеющегося и с «анатомичным» положением точки входа [12]. Для предоперационного анализа положений точек входа в каналы по результатам МСКТ-исследований, авторами использовался метод анатомических координатных осей для большеберцового и квадрантный метод для бедренного канала. Полученные в исследовании результаты одноэтапного хирургического лечения оказались сопоставимыми между группой, где проводились разнонаправленные имеющийся и «новый» каналы, и группой, где вновь проведенный канал совпадал с предшествующим, но имел больший диаметр.
Взяв во внимание отсутствие единого мнения в определении показаний к выполнению одно- или двухэтапного ревизионного вмешательства, S.A. Darren и соавт. разработали классификацию «REVISE ACL», которая, по их утверждению, позволяет стандартизировать подход к предоперационному планированию ревизий. Однако недостатком разработанной классификации является отсутствие конкретных критериев, на которые можно было бы опираться для принятия решения о выполнении одно- или двухэтапного оперативного вмешательства [15].
В свою очередь, ревизионная реконструкция ПКС при корректно расположенных каналах, которые имеют диаметр от 10 до 14 мм, может быть выполнена в один этап при условии использования подходящего сухожильного ауто- или аллотрансплантата с костным блоком. В данном случае необходимо учитывать геометрию вторично расширенного канала и дополнительное его увеличение после удаления склерозированного участка канала. Таким образом, наиболее оптимальным для одноэтапного вмешательства диаметром «анатомично» расположенного канала является размер до 10 мм, так как данное значение ширины канала позволяет без риска использовать различные виды наиболее часто используемых сухожильных трансплантатов и оптимальные методы фиксации [7].
Выбор трансплантата для ревизионной реконструкции ПКС является одним из важных аспектов данного вида вмешательств. Современные научные исследования сообщают о преимуществах применения собственных тканей пациента, в отличие от синтетических протезов и аллотрансплантатов [6; 16]. В частности, трансплантат, подготовленный из сухожилия длинной малоберцовой мышцы, является одним из наиболее оптимальных аутографтов, который с каждым годом становится все более популярным среди хирургов во время реконструкций ПКС. В то же время увеличение частоты использования данного вида трансплантата может быть объяснено наличием исследований, в которых были выявлены положительные стороны применения сухожилия длинной малоберцовой мышцы, а именно: высокая прочность полученного трансплантата, безопасность и относительно невысокие показатели длительности процедуры взятия сухожилия, а также отсутствие проблемы болезненности донорского места и негативного влияния на функцию стопы и голеностопного сустава в долгосрочной перспективе [17; 18].
Заключение. Одноэтапная ревизионная реконструкция передней крестообразной связки требует взвешенного и углубленного подхода к предоперационному планированию. Имеющиеся современные методы оценки положения костных каналов позволяют оптимизировать выявление показаний к одноэтапному лечению. Таким образом, в рамках предоперационного планирования ревизионной реконструкции передней крестообразной связки необходимо учитывать индивидуальные особенности пациентов и стремиться к определенным оценочным стандартам.
Библиографическая ссылка
Гофер А.С., Алекперов А.А., Гуражев М.Б., Авдеев А.К., Павлов В.В. ОДНОЭТАПНАЯ РЕВИЗИОННАЯ РЕКОНСТРУКЦИЯ ПЕРЕДНЕЙ КРЕСТООБРАЗНОЙ СВЯЗКИ ПРИ МАЛЬПОЗИЦИИ КОСТНЫХ КАНАЛОВ. КЛИНИЧЕСКИЙ СЛУЧАЙ // Современные проблемы науки и образования. 2023. № 5. ;URL: https://science-education.ru/en/article/view?id=32891 (дата обращения: 24.05.2026).
DOI: https://doi.org/10.17513/spno.32891



