Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
A COMPLEX APPROACH IN THE TREATMENT OF TUBERCULOSIS AGAINST THE BACKGROUND OF DRUG RESISTANCE OF THE PATHOGEN
Несмотря на то что по данным Всемирной организации здравоохранения туберкулез (ТБ) представляет угрозу для населения, в Российской Федерации отмечается улучшение эпидемических аспектов в борьбе с туберкулезом. Более того, ВОЗ в 2021 г. исключила нашу страну из списка стран с высокой распространенностью туберкулеза. Многие авторы считают, что это является результатом реализации поставленных национальных программ здравоохранения [1].
Согласно политической стратегии DOTS (лечение под непосредственным контролем коротким курсом) выявлено, что туберкулез остается одной из распространенных и смертоносных болезней в большинстве стран мира [2].
Данные литературы указывают, что лекарственная устойчивость (ЛУ) в мире составляет примерно 6,1% среди вновь выявленных случаев туберкулезной инфекции и около 20,4% среди пациентов, ранее получавших лечение [3]. Особое внимание также уделяется пациентам с туберкулезом с ЛУ и другими инфекциями, такими как ВИЧ и COVID. ВОЗ отмечает, что пандемия COVID-19 влечет тяжелые осложнения для человечества, которые будут расти в период с 2020 по 2025 гг., особенно при лекарственно-устойчивых формах заболевания [4].
Терапевтическая успешность лечения ЛУ, судя по данным современной литературы, равняется примерно 60% [5]. По данным современных исследований выявлено, что в основе эффективности применяемых в практике методов лечения ТБ лежат такие факторы, как устойчивость возбудителя, характер воспалительного процесса, объем поражения легочной ткани, приверженность больного к терапии. Поэтому многие исследователи придают важное значение течению и лечению ЛУ туберкулеза [6].
Новая программа лечения пациентов с устойчивой формой ТБ заключается в применении V режима химиотерапии с назначением наиболее эффективных противомикробных лекарств, таких как диарилхинолины, оксазолидиноны, фторхинолоны и др. Терапевтическая тактика лекарственно-устойчивого туберкулеза носит персональный характер, нередко требуется хирургическое вмешательство. В дополнение к применению современных противотуберкулезных препаратов большую значимость имеет рациональное комбинированное назначение химиопрепаратов [7].
При утяжелении патологии и развитии лекарственно-устойчивых штаммов возбудителя современные тактики лечения должны применяться с учетом роста лекарственной резистентности [8].
Итак, в данное время необходимо решить вопрос усиления воздействия препаратов, обладающих высокими противомикробными эффектами против микобактерии туберкулеза (МБТ) [9].
Цель исследования – усиление терапевтической эффектности лечения пациентов с туберкулезом легких с ЛУ.
Материалы и методы исследования
В клиническое обследование входили 90 пациентов с туберкулезом легких и лекарственной устойчивостью.
Критерии включения: собственное согласие на участие; клиническое подтверждение диагноза «туберкулез легких с ЛУ»; формы патологии – впервые выявленная и рецидивирующая; возраст – 25–65 лет; пол – женский и мужской; легкие сопутствующие патологии.
Критерии исключения: персональный отказ от исследования; туберкулез других органов, кроме легких; возраст моложе 25 и старше 65 лет; тяжелые сопутствующие болезни; ВИЧ-инфекция.
Верификация диагноза осуществлялась с применением молекулярно-генетических и лабораторных методов биологического материала мокроты с целью обнаружения ДНК, микроскопии, посева на плотные (ППС) и жидкие (ЖПС) питательные среды возбудителя.
Участники исследования распределены рандомным способом на 2 группы в зависимости от формы проявления патологии. Данные группы также были разделены на подгруппы в зависимости от базового вида химиотерапии.
Первая (основная, n=47) группа – больные с впервые выявленным ТБ и ЛУ, которая разделена на подгруппу 1 (n=16) – левофлоксацин (Lvf) + линезолид (Lzd), подгруппу 2 (n=17) – моксифлоксацин (Mfn) + Lzd + бедаквилин (Bq), подгруппу 3 (n=14) – Lzd + Bq.
Вторая (клинического сравнения, n=43) группа – с рецидивирующим ТБ и ЛУ, в которую входили подгруппа 4 (n=14) – левофлоксацин (Lvf) + линезолид (Lzd), подгруппа 5 (n=13) – моксифлоксацин (Mfn) + Lzd + бедаквилин (Bq), подгруппа 6 (n=16) – Lzd + Bq.
Гендерно-возрастной анализ показал, что средний возраст больных составил 45,2±2,87 года (в первой группе – 42,5±2,98 года, во второй – 48,3±2,71 года). При распределении изучаемых пациентов по полу выявлено, что мужчин было 50 (55,6%), а женщин – 40 (44,4%). В первой группе представители мужского пола составили 27 (57,4%), а женского – 20 (42,6%). Во второй группе этот показатель равнялся 25 (58,1%) и 18 (41,9%) соответственно.
При изучении анамнеза выявлено, что у пациентов группы наблюдения обнаружены сопутствующие заболевания, в том числе сердечно-сосудистые (у 22 (24,0%)), желудочно-кишечные (у 15 (16,7%)), эндокринные (13 (14,4%)), респираторные (17 (18,9%)), инфекционные (у 11 (12,2%)).
Обследование пациентов проводили клиническим методом: сбор анамнеза – жалобы, давность патологии, контакт с больными туберкулезом; бактериологическими методами: люминесцентная микроскопия (исследование мокроты на возбудителя туберкулеза) и ПЦР (молекулярно-генетическая идентификация МБТ), посевы ППС и ЖПС, анализ крови (лейкоциты, лимфоциты, гемоглобин и др.); инструментальными методами: рентгенографическое исследование и КТ органов грудной клетки, ЭКГ и др.
Для сравнения исследуемых параметров с референсным уровнем обследованы люди без признаков заболевания (n=10).
Период исследования – 3, 6 и 12 месяцев стационарного лечения.
Статистическая обработка полученного материала проведена с применением пакета прикладных программ Statistica 13.1. и программы IBM SPSS statistics 25, критерия χ2 Пирсона и Фишера.
Результаты исследования и их обсуждение
При клиническом обследовании выявлено, что у пациентов зарегистрированы интоксикационный и бронхопульмональный синдромы (рис. 1).
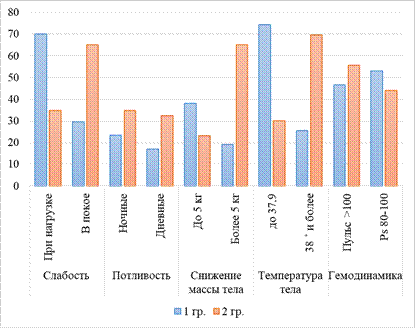
Рис. 1. Показатели синдрома интоксикации
По данным клинического обследования обнаружено, что умеренные признаки интоксикации (фебрильная температура, умеренная слабость, легкое потоотделение, умеренная неустойчивость) регистрировались среди пациентов с впервые возникшими формами (основная группа). У данных пациентов выраженность синдрома интоксикации соответствовала первой степени. У пациентов с рецидивными формами ТБ проявление интоксикации (температура 38˚С и более, снижение массы тела на 5 кг и более) соответствовало второй и третьей степеням тяжести (вторая группа) (рис. 1).
При изучении параметров бронхопульмонального синдрома продемонстрировано, что легкая респираторная депрессия (I степень) c такими признаками, как редкий кашель, мокрота 50–100 мл/сут, дыхательная недостаточность I степени, диагностирована у больных первой группы. Более тяжелые степени (II и III) бронхопульмонального синдрома, симптомы которых – выраженный кашель, мокрота >100 мл/сут, дыхательная недостаточность II и III степени, зарегистрированы у пациентов второй группы (рис. 2).
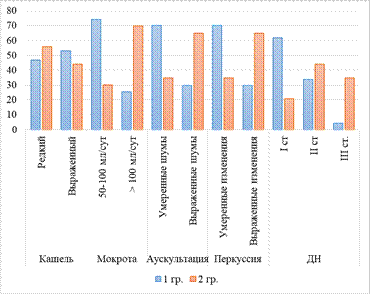
Рис. 2. Показатели бронхопульмонального синдрома
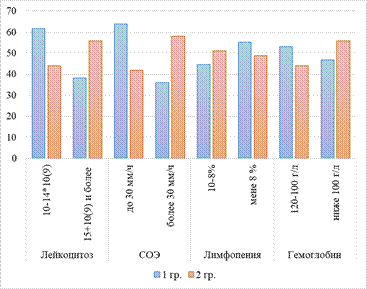
Рис. 3. Показатели общего анализа крови
Результаты исследования анализа крови показали, что у исследуемых больных с впервые выявленным ТБ отмечены лейкоцитоз (до 15х109) у, легкий палочкоядерный сдвиг – у 38 (38,0%), 8%-ная лимфопения – у 15 (15,0%) и повышение СОЭ (до 30 мм/ч). С-реактивный белок, АЛТ и АСТ превышали норму на 15,6, 21,1, 18,5 и 16,3% соответственно (р<0,05) (рис. 3).
У пациентов группы сравнения лабораторные сдвиги превышали аналогичные показатели пациентов первой группы в значительной степени. В данной группе уровень лейкоцитоза превышал 15х109, палочкоядерный сдвиг – тяжелый, 10%-ная лимфопения, рост СОЭ выше 30 мм/ч, увеличение С-реактивного белка, АЛТ и АСТ – на 26,4, 32,7 и 25,9% соответственно (р<0,05).
Результаты лучевой диагностики выявили, что среди клинических форм ТБ в основной группе чаще регистрировался инфильтративный (у 31 (66,0%)) и кавернозный (у 16 (34,0%)) туберкулез. В группе сравнения формы патологического процесса диагностированы в инфильтративной, фиброзно-кавернозной и диссеминированной формах – у 7 (16,2%), 26 (60,4%) и 10 (23,2%) человек соответственно.
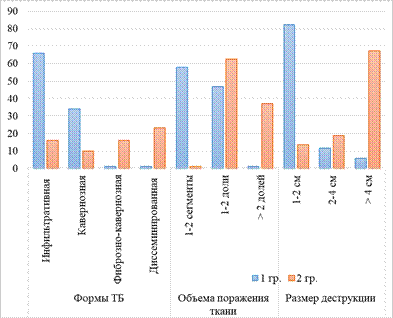
Рис. 4. Формы и объемы поражения легких при ТБ
Особый интерес уделяется сравнительным данным объема поражения ткани легких. По данным рентгенологического исследования выявлено, что у 25 (58,1%) больных основной группы патологические проявления обнаружены в 1–2-м сегментах, а у 22 (46,8%) поражены не более 2 долей легкого (р<0,05). В группе клинического сравнения зарегистрированы обширные поражения (более 2 долей легкого) среди 27 (62,7%) пациентов и ограниченные (в пределах одного сегмента) – у 16 (37,2%) пациентов (рис. 4).
Количество и размеры полостей распада у пациентов группы исследования различались. У 34 (72,3%) пациентов первой группы выявлены полостные образования, в том числе единичные выявлены у 22 (64,7%), а множественные – у 12 (35,2%). Во второй группе полости распада диагностированы у 37 (86,0%) человек, при этом единичные полости распада – у 28 (75,6%), а множественные – у 9 (24,3%) больных.
По размеру различали полости 1–2 см, 2–4 см и >4 см. В основной группе они составили 28 (82,3%), 4 (11,7%) и 2 (5,8%), в группе сравнения – 5 (13,5%), 7 (18,9%) и 25 (67,5%) соответственно.
По патогенетическим различиям полостные образования регистрировались в начинающей, пневмониогенной, ригидной, эластичной, фибрознозной формах. В первой группе обнаружены первые 4 вида, они соответственно отмечены у 8 (23,5%), 20 (58,8%), 4 (11,7%) и 2 (5,8%) больных. Во второй группе встречались пневмониогенный (у 3 (8,1%)), ригидный (5 (13,5%)), эластичный (7 (18,9%)), фибрознозный (22 (59,4%)) виды.
Анализ микробиологических особенностей течения туберкулеза с лекарственной устойчивостью (ТБ-ЛУ) показал, что результаты микроскопии и посева выявили скудное бактериовыделение у 36 (76,5%), р<0,05) и 33 (70,2%, р<0,05) пациентов первой группы соответственно. Во второй группе отмечено массивное бактериовыделение – у 31 больного (72,0%, р<0,05) по микроскопии и у 34 (79,0%, р<0,05) по посеву.
Спектр лекарственной устойчивости возбудителя у больных ТБ-ЛУ широкий. Спектры ЛУ+1 включили комбинацию HRAmKFq и HRAmCmFq, ЛУ+2 – HRAmEKFq + HRAmECmFq + HRAmKCmFq + HRAmKPtFq, ЛУ+3 – HRAmKEFqPAS + HRAmKFqPASCs + HRAmKPtCmFq + HRAmKPtPASFq, ЛУ+4 – HREKCmPtFq + HREKCsFqPASLzd + HRAmKECmFqPAS + HRKPtCmFqPAS, ЛУ+5 – HREKPtCmFqPASCs + HRKPtCmFqCsPAS. Итак, в первой группе ЛУ+1 диагностирована у 20 (42,5%), ЛУ+2 – у 12 (25,5%), ЛУ+3 – у 10 (21,2%), ЛУ+4 – у 4 (8,5%), а ЛУ+5 – у 1 (2,1%) больного. В группе сравнении показатели составили соответственно 8 (18,6%), 10 (23,2%), 13 (30,2%), 7 (16,2%) и 4 (9,3%) (рис. 5).
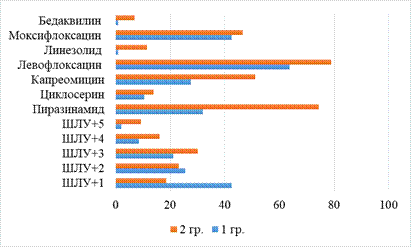
Рис. 5. Спектр лекарственной устойчивости возбудителя
Лекарственная устойчивость к химиопрепаратам у пациентов группы исследования регистрирована в разнообразных формах. В основной группе установлена устойчивость к левофлоксацину (30 (63,8%)), моксифлоксацину (у 20 (42,5%)), пиразинамиду (у 15 (31,9%)), капреомицину (у 13 (27,6%)), циклосерину (у 5 (10,6%)).
У пациентов второй группы лекарственная устойчивость регистрировалась к левофлоксацину (у 34 (79,0%)), пиразинамиду (у 32 (74,4%)), капреомицину (у 22 (51,1%)), моксифлоксацину (у 20 (46,5%)), циклосерину (у 6 (13,9%)), и линезолиду (у 5 (11,6%)) и бедаквилину (у 3 (6,9%)).
При изучении терапевтической эффективности применяемых методов лечения ТБ по сроку исследования выявлено, что применение разных схем терапии привело к разному исходу (табл. 1).
Таблица 1
Эффективность лечения по сроку наблюдения
|
Показатель |
Срок, месяцев |
Подгруппа, n (%) |
|||||
|
1 |
2 |
3 |
4 |
5 |
6 |
||
|
ПБВ |
3 |
5 (10,6) |
15 (31,9) |
9 (19,1) |
4 (9,3) |
10 (23,2) |
7 (13,9) |
|
Заживление деструктивных полостей |
4 (8,5) |
17 (34,0) |
7 (14,8) |
2 (4,6) |
8 (18,6) |
5 (11,6) |
|
|
ПБВ |
6 |
13 (27,6) |
27 (57,4) |
19 (40,4) |
9 (20,9) |
22 (51,1) |
13 (30,2) |
|
Заживление деструктивных полостей |
10 (21,2) |
24 (51,0) |
17 (36,1) |
7 (16,2) |
20 (46,5) |
10 (23,2) |
|
|
ПБВ |
12 |
22 (46,8) |
38 (80,8) |
30 (63,8) |
18 (41,8) |
33 (74,7) |
20 (46,5) |
|
Заживление деструктивных полостей |
19 (40,4) |
35 (74,4) |
27 (57,4) |
14 (32,5) |
30 (69,8) |
16 (37,2) |
|
ПБВ – прекращение бактериовыделения.
Установлено, что самой лучшей комбинацией в лечении как впервые выявленного ТБ, так и рецидивирующего являлась Mfn + Lzd + Bq. В подгруппе 2 бактериовыделение прекратилось у 15 человек (31,9%) спустя 3 месяца, у 27 (57,4%) – спустя 6 месяцев и у 38 (80,8%) – через12 месяцев. У больных подгруппы 5, которым назначена данная комбинация, эти параметры составили 10 (23,2%), 22 (51,1%) и 33 (74,7%) соответственно. В подгруппах 3 и 6, где принимались Lzd + Bq, эффект лечения был ниже, чем в вышеуказанных подгруппах. Критерий прекращения бактериовыделения в подгруппе 3 равнялся 9 (19,1%), 19 (40,4%) и 30 (63,8%) согласно периоду наблюдения, а в подгруппе 6 – 7 (13,9%), 13 (30,2%), и 20 (46,5%) соответственно. Минимальная терапевтическая эффективность выявлена при комбинации Lvf + Lzd. Признаки прекращения бактериовыделения у пациентов подгруппы 1 составили 5 (10,6%), 13 (27,6%) и 22 (46,8%), а в подгруппе 4 – у 4 (9,3%), 9 (20,9%) и 18 (41,8%) соответственно.
Об успешности химиотерапии свидетельствует процесс заживления деструктивных полостей, который в подгруппе 2 отмечался у 17 человек (34,0%) через 3 месяца лечения, у 24 человек (51,0%) – через 6 месяцев и у 35 (74,4%) – спустя 12 месяцев. В подгруппе 5 эти параметры составляли 8 (18,6%), 20 (46,5%) и 30 (69,8%) соответственно. Меньшая эффективность терапии отмечена в подгруппах 3 и 6, где симптомы заживления деструкций отмечались у 7 (14,8%), 17 (36,1%) и 27 (57,4%) человек и у 5 (11,6%), 10 (23,2%) и 16 (37,2%) соответственно на аналогичных сроках исследования. Успешность терапии при заживлении деструктивных поражений легочной ткани в подгруппах 1 и 4 была минимальной. В подгруппе 1 заживление полости наблюдалось у 4 (8,5%), 10 (21,2%) и 19 (40,4%), а в подгруппе 4 – у 4 (9,3%), 7 (16,2%) и 14 (32,5%) человек через 3, 6, 12 месяцев соответственно.
Выводы
1. Клинические и инструментальные признаки туберкулеза легких в условиях лекарственной устойчивости возбудителя сопровождаются проявлением инфильтративной формы, скудным бактериовыделением и наличием деструктивных полостей не более 2 см в основном у впервые выявленных пациентов; и признаками фиброзно-кавернозной формы, массивного бактериовыделения и деструктивных изменений легочной такни более 2 см – у рецидивирующих больных.
2. Спектры лекарственной устойчивости микобактерий у впервые выявленных больных ЛУ ТБ регистрируются в пределах 1–3 противотуберкулезных препаратов, а среди рецидивирующих пациентов – 3 препаратов и более.
3. Комплексное лечение пациентов со впервые выявленным ТБ-ЛУ, в которое включены линезолид, бедаквилин и моксифлоксацин, способствует быстрому снижению симптоматики (прекращению бактериовыделения и ускорению заживления деструктивных процессов). Терапия уже с 3-го месяца применения была выше других химиотерапий без бедаквилина.
Библиографическая ссылка
Басиева О.З., Джагаева З.К., Дзагоев В.В. КОМПЛЕКСНЫЙ ПОДХОД В ЛЕЧЕНИИ ТУБЕРКУЛЕЗА НА ФОНЕ ЛЕКАРСТВЕННОЙ УСТОЙЧИВОСТИ ВОЗБУДИТЕЛЯ // Современные проблемы науки и образования. 2022. № 6-1. ;URL: https://science-education.ru/en/article/view?id=32215 (дата обращения: 01.06.2026).
DOI: https://doi.org/10.17513/spno.32215



