Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
THE ROLE OF ADIPONECTIN IN THE FORMATION OF OVARIAN DYSFUNCTION IN OBESE ADOLESCENT GIRLS
В настоящее время около 60% населения экономически развитых стран имеет избыточную массу тела, 25-30% - ожирение. Нарушения репродуктивной сферы отмечаются у 30-50% случаев россиян детородного возраста, страдающих избыточной массой тела. Действительно, распространенность клинических проявлений гиперандрогении и нарушений менструального цикла у тучных женщин выше, чем в общей женской популяции, а у девочек с ожирением частота нарушений менструального цикла достигает 70% [1].
Как показали исследования последних лет, жировая ткань не только служит для накопления и хранения энергетических субстратов, но и весьма активна в метаболическом аспекте, продуцирует множество гормоноподобных веществ, медиаторов, цитокинов, которые действуют на местном и системном уровне и оказывают влияние на обменные процессы, чувствительность к инсулину, репродуктивную и иммунную систему. Среди активных веществ, секретируемых жировой тканью, особый интерес вызывает адипонектин. Известно, что его концентрация у женщин в 2 раза больше, чем у мужчин, что обусловлено особенностями продукции некоторых стероидных гормонов [2]. Адипонектин повышает чувствительность тканей к инсулину, толерантность к глюкозе, оказывает противовоспалительное и антиатерогенное действие, однако роль его в регуляции метаболизма еще недостаточно изучена. В то же время избыточная конверсия андрогенов на фоне увеличения количества клеток жировой ткани, участвующих в стероидогенезе, является триггером, вовлекающим в процесс все уровни регуляции эндокринной системы, диктуя необходимость углубленного изучения дополнительных механизмов формирования овариальной дисфункции на фоне гиперандрогении.
Цель исследования - исследовать роль адипонектина в формировании дисфункции яичников на фоне ожирения у девочек пубертатного возраста с учетом клинико-лабораторных проявлений гиперандрогении.
Материалы и методы исследования
Обследовано 105 девочек-подростков 14-17 лет с конституционально-экзогенным ожирением 1-2 степени и 40 девочек соответствующего возраста с нормальным индексом массы тела (ИМТ). Пациентки основной группы были разделены на 2 группы. В 1-ю группу вошли 55 пациенток с нарушением ритма менструаций. 2-ю группу составили 50 девочек-подростков без нарушений менструального цикла (МЦ). ИМТ рассчитывали по весу (кг) и росту (м) каждой девочки, а затем оценивали согласно центильным таблицам. Период от начала менархе составил не менее 2 лет. У всех пациенток определялось гирсутное число с использованием классической 4-балльной шкалы D. Ferriman и J. Gallwеy [1967].
Гормональное исследование включало определение 17-оксипрогестерона (17-OH), тестостерона (Т), дегидроэпиандростерона (ДГЭА), дегироэпиандростерон-сульфата (ДГЭА-С), андростендиона (∆А4), дигидротестостерона (ДГТ), инсулина, а также уровня адипонектина (нг/мл) методом иммуноферментного анализа (ИФА). Биохимические исследования включали определение показателей глюкозы, липидограммы. Для оценки инсулинорезистентности (ИР) применялся индекс НОМА-IR (Homeostasis Model Assessment of Insulin Resistance), который рассчитывался по формуле: НОМА = (уровень глюкозы (ммоль/л) х уровень инсулина (мкМЕ/мл)) / 22,5. Считают, что если у детей индекс НОМА более 3,2, то следует подозревать ИР.
Статистическая обработка полученных результатов проводилась с использованием прикладной программы MedCalc 11.4.2., непараметрического корреляционного анализа по Спирмену. Достоверность показателей определена по коэффициенту Стьюдента (t). За критический уровень значимости принято значение p<0,05.
Результаты исследований и их обсуждение
Ведущим клиническим симптомом, наиболее значимым в диагностике синдрома гиперандрогении СГА, считается гирсутизм. В группе девочек с нормальным весом гирсутизм не выявлялся ни в одном случае, тогда как гирсутное число более 12 баллов по шкале Ферримана-Голлвея было выявлено у 24,7% пациенток с ожирением, а в 27,6% случаев гирсутное число находилось в пределах пограничной зоны от 8 до 11 баллов. Следовательно, дерматологические проявления синдрома гиперандрогении были зафиксированы у 52,3% пациенток с ожирением. При этом в 1-й группе частота дерматологических проявлений СГА была несколько выше, чем во второй, не достигая, однако, достоверности различий (p>0,05).
Тяжесть гирсутизма не обязательно соответствует степени лабораторной гиперандрогении, поскольку зависит от множества других факторов, опосредующих влияние андрогенов на кожу (этнических, рецепторных, транспортных). Поэтому сравнительный анализ секреции андрогенов у обследуемых пациенток показал более значимое повышение частоты продукции всех исследуемых андрогенов у пациенток с ожирением, чем это можно было ожидать, основываясь на данных клинического осмотра (рис. 1). Наиболее часто у пациенток с ожирением встречался повышенный уровень ДГТ – 61,9%, тогда как в контрольной группе случаев содержания данного гормона в крови выше референсных значений зафиксировано не было (p=0,008). Стероидогенез у женщин устроен таким образом, что основная часть продукции андрогенов происходит в корковой зоне надпочечников, но отчасти также и в яичниках.
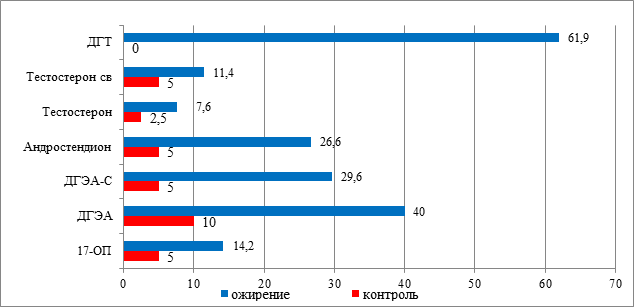
Рис. 1. Частота повышенных значений изучаемых андрогенов (выше верхних пределов референсных значений) у подростков с ожирением и с нормальным ИМТ
Повышенная частота ДГТ у пациенток с ожирением объяснима не только возможным вовлечением в дефектный стероидогенез надпочечников и яичников, как это происходит у пациенток с СГА, имеющих нормальную массу тела, но и дополнительным вкладом избыточной конверсии женских половых стероидов в андрогены на фоне увеличения количества клеток жировой ткани [3]. Дело в том, что адипоциты сами по себе являются местом метаболизма и взаимопревращения стероидных гормонов. Функцией фермента 17β-гидроксистероиддегидрогеназы в адипоцитах является превращение андростендиона в активный андроген тестостерон, а функцией фермента 5α-редуктазы – превращение тестостерона в более активный андроген 5α-дигидротестостерон, что также предрасполагает к развитию гиперандрогении при ожирении. Уровень ДГТ в 1-й группе превышал таковые показатели во 2-й группе [590,0 (360,0; 725,0) и 455,0 (285,0; 540,0) (пг/мл) (р=0,03)]. Данный факт представляется логичным, так как в предыдущих наших исследованиях была показана прямая корреляция между более высокими показателями андрогенов и формированием овариальной дисфункции [4].
Подобные же тенденции были выявлены и в отношении других исследуемых показателей андрогенов. Так, уровень ДГЭА был выше нормативных пределов в 40% случаев, тогда как в контрольной группе – в 10,0% случаев (p=0,003). Сульфатированная форма ДГЭА была повышена также в 29,5% случаев, в контрольной группе – в 5,0% случаев (p=0,002). Отмечено, что повышение уровня ДГЭА и его сульфатной конъюгаты не всегда сочеталось у одной и той же пациентки, поэтому общее число девочек, имеющих повышение уровня какого-либо из этих показателей, составило 49,5%. Отмечалось повышение значений ДГЭА в 1-й группе по сравнению со 2-й [14,7 (9,7;16,1) и 9,80 (6,14;11,4) (p=0,03)]. Повышение уровня андростендиона выше референсных значений было отмечено у 26,6% девочек с проявлениями ожирения, в то время как в контрольной группе – только в 5,0% случаев (p=0,001). При этом уровень андростендиона в 1-й группе был недостоверно выше, чем во 2-й (р>0,05). Повышенный уровень общего и свободного тестостерона определялся среди подростков с ожирением значительно реже (в 7,6% и в 11,4% случаев соответственно), в контрольной группе – в 2,5% и 5,0% случаев, p=0,008 и p=0,007 соответственно), при недостоверных отличиях между 1-й и 2-й группами (р>0,05).
Достоверное увеличение показателей ИРИ, а также индекса HOMA-IR (табл. 1) доказывало наличие гиперинсулинемии и инсулинорезистентности в группе девочек-подростков с ожирением (табл. 1). При этом медиана индекса HOMA–IR почти в 2,5 раза превышала значения этого показателя у девочек-подростков 2-й группы (p<0,05) и в 3 раза показатели группы контроля (p<0,05).
Таблица 1
Показатели углеводного обмена у пациенток 1-й, 2-й и контрольной групп (медианы, квартили)
|
Показатели Группы
|
ИРИ (мкЕд/мл) |
HOMA-IR |
|
1 группа
|
27,3*/** (12,7; 46,1) |
5,96*/** (4,67; 7,82) |
|
2 группа
|
19,7 (12,8; 28,2) |
3,65 (2,2; 4,9) |
|
Контрольная группа
|
13,0 (6,5; 19,4)
|
1,92 (1,6; 2,3) |
Примечание: * – статистические различия по сравнению с контрольной группой; ** - статистические различия между группами с ожирением
Сочетание инсулинорезистентности с гиперинсулинемией ведет к гиперсекреции андрогенов на уровне периферического звена – яичников. Это происходит как напрямую, так и опосредованно: путем стероидогенеза в клетках тека и гранулезы, и за счет усиления чувствительности гипофиза к гонадотропин-рилизинг-гормону [5; 6]. Кроме этого, повышение уровня инсулина инициирует подавление синтеза глобулина, связывающего половые стероиды, что приводит к увеличению продукции свободных андрогенов и, как следствие, к активации адреналовых андрогенов [7]. Конечным исходом данных процессов являются негативные влияния избытка андрогенов на процессы фолликулогенеза в яичниках. Частота и степень вовлеченности обусловлена как различным распределением ферментов в зонах желез, так и, возможно, их специфической чувствительностью к воздействиям со стороны гипоталамуса-гипофиза. В результате проведенного исследования установлено, что в группе подростков с ожирением уровень адипонектина был достоверно ниже, чем у девочек с нормальным ИМТ [15,7 (3,6; 25,0) и 28,9 (18,5;45,0) (нг/мл) (p=0,003)].
При этом уровень адипонектина (рис. 2) в 1-й клинической группе был в 1,46 раза ниже по сравнению с показателями 2-й группы ([11,4 (3,1; 22,0) и 16,7 (8,5;28,0) (нг/мл), p=0,04). Ген, ответственный за продукцию адипонектина, локализован в локусе, ассоциированном с метаболическим синдромом и ожирением, что подтверждает корреляцию адипонектина с повышенным индексом массы тела у обследуемых пациенток с ожирением (R=-0,73, p=0,001). При этом достоверной корреляции адипонектина с уровнем HOMA-IR выявлено не было (R=-0,23, p=0,15).
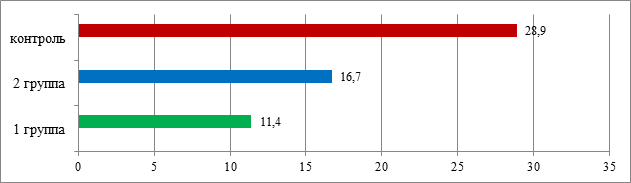
Рис. 2. Показатели адипонектина (нг/мл) у пациенток исследуемых групп
Существует множество исследований, свидетельствующих о связи половых гормонов с продукцией адипонектина. Так, по данным литературы, адипокины участвуют в нарушениях функции оси гипоталамус-гипофиз-яичники [8]. Данный факт подтверждается выраженным снижением уровня адипонектина у пациенток с СПКЯ и метаболическими нарушениями по сравнению с пациентками, имеющими нормальный индекс массы тела, а также прямой корреляцией адипонектина с уровнем ФСГ и обратной - с индексом свободных андрогенов [9]. Изучение коррелятивных взаимосвязей уровня адипонектина в нашем исследовании позволило выявить достоверную отрицательную связь данного показателя с содержанием некоторых андрогенов в крови (табл. 2).
Таблица 2
Результаты корреляционной связи адипонектина с показателями андрогенов у девочек-подростков 1-й и 2-й групп
|
Адипонектин |
17-ОП |
ДГЭА |
ДГЭА-С |
Т |
∆А4 |
ДГТ |
||||||
|
R |
p |
R |
p |
R |
p |
R |
p |
R |
p |
R |
p |
|
|
1 группа
|
-0,60 |
0,05 |
-0,77 |
0,04 |
-0,56 |
0,04 |
-0,75 |
0,02 |
-0,67 |
0,03 |
-0,74 |
0,02 |
|
2 группа
|
0,01 |
0,5 |
-0,87 |
0,05 |
-0,09 |
0,3 |
-0,95 |
0,04 |
0,09 |
0,7 |
0,15 |
0,3 |
Примечание: R – коэффициент корреляции по Спирмену: знак (-) свидетельствует об обратной корреляционной связи; отсутствие знака – о прямой корреляционной связи; p – значимость корреляционной связи по Спирмену.
Наши результаты показали различия в уровне адипонектина в сыворотке крови между пациентками с ожирением в зависимости от наличия овариальной дисфункции и группой контроля. Учитывая, что пациенты основной группы и контрольные субъекты различались по степени клинико-лабораторных проявлений гиперандрогении, распределению жира в организме и резистентности к инсулину, снижение уровня адипонектина в сыворотке крови, наблюдаемое у пациенток с ожирением, может быть связано с любой из этих переменных. Мы обнаружили, что в основном дигидротестостерон и, в меньшей степени, уровни инсулина и глюкозы коррелировали с концентраций адипонектина в сыворотке крови. На корреляции между концентрациями андрогенов и адипонектина в сыворотке крови указывали результаты и других авторов. Так, исследования на животных (мышах) и человеческих моделях (мужчины с гипогонадизмом после терапии тестостероном) показали ингибирующее действие тестостерона на секрецию адипонектина [10]. Поскольку было продемонстрировано, что сывороточный адипонектин играет важную роль в патогенезе и усилении резистентности к инсулину, было высказано предположение, что гипоадипонектинемия может способствовать развитию резистентности к инсулину у женщин с СПКЯ. После строгой статистической оценки авторы продемонстрировали, что уровни свободного тестостерона, возраст и абдоминальное ожирение, независимо от степени ожирения, являются основными факторами, определяющими гипоадипонектинемию. Концентрация адипонектина в сыворотке крови лучше всего коррелировала с соотношением талии/бедер, индексом свободных андрогенов и наличием нарушенной толерантности к глюкозе [11]. Эти результаты подтверждают гипотезу о том, что гиперандрогения может напрямую способствовать резистентности к инсулину у женщин, вызывая абдоминальное ожирение и, возможно, снижая адипонектин у пациентов с СПКЯ. С другой стороны, абдоминальное ожирение, резистентность к инсулину и компенсаторная гиперинсулинемия, приводящая к гиперандрогении, являются хорошо установленными патогенетическими механизмами при СПКЯ.
Снижение уровня адипонектина в периоде полового созревания ассоциируется с повышенным уровнем ДГЭА и его сульфатной конъюгаты, как основными триггерами, участвующими в процессе адренархе. Идиопатическое адренархе долго считалось вариантом нормы. Но открытие моногенных причин раннего избытка андрогенов, очевидного дефицита кортизон-редуктазы и сульфотрансферазы ДГЭА подтверждает мнение, что преждевременное адренархе может быть предшественником инсулинорезистентности и СПКЯ [12]. Кроме этого, при проведении исследования у мальчиков с нормальным индексом массы тела было выявлено выраженное снижение уровня адипонектина на фоне повышенного содержания тестостерона, что обусловлено подавляющим эффектом тестостерона на синтез гормона жировой ткани [13]. Данные факты подтверждают результаты нашего исследования, достоверную обратную корреляцию адипонектина с андрогенами ДГЭА, ДГЭА-С, Т, ∆А4 , ДГТ, особенно в группе с нарушеннием цикла.
В предыдущих публикациях нами было показано, что при ожирении у девочек-подростков гиперандрогенемия и инсулинорезистентность взаимно потенцируют свои негативные эффекты, формируя своеобразный «порочный» круг гормонально-метаболических расстройств [14]. Суммирование этих неблагоприятных влияний приводит в ряде случаев к овариальной функции различной степени выраженности: от учащения ановуляторных циклов при сохраненной регулярности менструаций до выраженных проявлений олигоменореи, вплоть до вторичной аменореи. Полученные нами данные о достоверно более низких показателях адипонектина и статистически значимой отрицательной его корреляции с повышением секреции андрогенов в группе подростков с нарушением МЦ могут доказывать патогенетическую значимость снижения его секреции в формировании овариальной дисфункции у девочек с ожирением, особенно при наличии гиперандрогении. Эти результаты показывают, что адипонектин может быть использован в качестве биохимического маркера для идентификации метаболических фенотипов девочек-подростков с ожирением, имеющих повышенный риск развития дисфункции репродуктивной системы. Однако прежде, чем рекомендовать измерение адипонектина в сыворотке крови в клинической практике, необходимы дальнейшие когортные исследования.
Библиографическая ссылка
Пузикова О.З., Московкина А.В., Попова В.А., Чурюкина Э.В., Кожин А.А., Созаева Д.И., Бережанская С.Б., Кравченко Л.В., Селютина С.Н., Друккер Н.А., Каушанская Л.В., Петров Ю.А. РОЛЬ АДИПОНЕКТИНА В ФОРМИРОВАНИИ ОВАРИАЛЬНОЙ ДИСФУНКЦИИ У ДЕВОЧЕК С ОЖИРЕНИЕМ // Современные проблемы науки и образования. 2022. № 2. ;URL: https://science-education.ru/en/article/view?id=31607 (дата обращения: 18.05.2026).
DOI: https://doi.org/10.17513/spno.31607



