Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
MATHEMATICAL MODEL FOR ASSESSMENT OF RISK OF THE DEVELOPMENT OF LIFE - THREATENING COMPLICATIONS IN ACUTE PHASE OF MYOCARDIAL INFARCTION
Острый период инфаркта миокарда (ИМ) характеризуется развитием жизнеугрожающих осложнений. Одним из наиболее тяжелых и прогностически неблагоприятных осложнений ИМ является острая левожелудочковая недостаточность, клинически проявляющаяся отеком легких и кардиогенным шоком (КШ) [1].
При этом важным направлением для улучшения прогноза в остром периоде ИМ является изучение биомаркеров с наибольшей прогностической значимостью [2]. В аспекте этиопатогенеза ИМ немаловажное значение имеет изучение биомаркеров воспаления и эндотелиальной дисфункции (ЭД) [3].
Биомаркеры воспаления, представителем которых является трансферрин (TFN), отражают степень некроза миокарда и коррелируют с тяжестью течения коронарной патологии, а изменение их имеет прогностическое значение у пациентов с ИМ, в том числе и в остром периоде [4]. Знания о роли TFN в патогенезе ИМ и возможность использования его в прогностических целях к настоящему времени находятся еще на стадии накопления [5]. По данным ряда исследований, TFN является косвенным маркером ЭД [6; 7].
Асимметричный диметиларгинин (ADMA) является эндогенным ингибитором синтазы оксида азота (NO), маркером ЭД. Повышение его уровня связано с риском острых коронарных событий, нарушениями перфузии миокарда и неблагоприятным прогнозом у пациентов с ИМ [8].
Еще одним перспективным биомаркером воспаления и ЭД является цитокин - фракталкин/CX3CL1 [9]. В доступной литературе представлены единичные исследования по изучению его уровня у пациентов с ИМ. К настоящему времени уже выявлено наличие корреляционных связей между уровнем фракталкина/CX3CL1 и уровнями NT-proBNP, кардиальных тропонинов, значением фракции выброса левого желудочка у пациентов с ИМ, а также установлена роль фракталкина/CX3CL1 в дестабилизации и разрыве атеросклеротической бляшки [10].
В современной литературе предложено достаточно широкое количество алгоритмов/математических моделей прогнозирования развития, течения и исхода ИМ [11]. В качестве предикторов авторами исследований рассматриваются клинико-анамнестические, лабораторные, инструментальные данные. Разработка персонализированных прогностических алгоритмов/математических моделей и внедрение их в клиническую практику вносит существенный вклад в улучшение прогноза у пациентов с ИМ.
Цель исследования: разработать математическую модель для оценки риска развития жизнеугрожающих осложнений - КШ и отека легких в остром периоде ИМ на основе анализа уровней фракталкина/CX3CL1, ADMA и TFN.

Рис. 1. Дизайн исследования с характеристикой обследуемых
Материал и методы исследования. В исследование «случай-контроль» были включены 63 пациента, обследованных в остром периоде ИМ (основная группа) и 20 соматически здоровых добровольцев (контрольная группа). Дизайн исследования с характеристикой обследуемых представлен на рисунке 1.
Клиническое исследование получило одобрение этического комитета (протокол № 12 от 2016 г.).
Критерии исключения: пороки сердца и наличие в анамнезе перенесенного в прошлом ИМ, аортокоронарного шунтирования и чрескожного коронарного вмешательства.
Методом иммуноферментного анализа в плазме крови были изучены уровни:
●фракталкина/CX3CL1, коммерческая тест-система «Ray Bio@Human Fractalkine»;
●ADMA, коммерческая тест-система «ADMA Xpress ELISA Kit»;
●TFN, коммерческая тест-система «Human Transferrin Assay Max ELISA Kit».
Уровни изучаемых биомаркеров у пациентов в остром периоде ИМ статистически значимо отличались от уровней соматически здоровых добровольцев (табл. 1).
Таблица 1
Уровни биомаркеров у пациентов в остром периоде ИМ (Me [5;95], U-критерий Манна - Уитни)
|
Биомаркер |
Контрольная группа |
Пациенты с ИМ |
p-value |
|
Фракталкин/CX3CL1, пг/мл |
335,7[284,4; 445,2] |
850,4[417,5; 1005,2] |
р<0,001 |
|
ADMA, мкмоль/л |
0,52[0,35; 1,2] |
1,22[0,97; 1,55] |
р<0,001 |
|
TFN, г/л |
3[1,68; 3,8] |
0,7[0,2; 2] |
р<0,001 |
Данные обрабатывались в программе Statistica версия 12.0. и SPSS-16. Данные представлены в виде медианы и процентилей (Ме [5;95]). Для каждого предиктора множественной логистической регрессионной модели были рассчитаны: β – коэффициент; стандартная ошибка; статистика критерия Вальда; p – значения вероятности статистической значимости связи предикторов с переменной отклика; отношение шансов и 95%-ный доверительный интервал (ДИ) для оценки отношений шансов. Порог отсечения был принят равным 0,5. Для оценки качества разработанной математической модели оценивали ее диагностическую чувствительность, специфичность и точность, прогностическую ценность положительного и отрицательного результата, а также оценивался показатель AUC (площадь под ROC-кривой) и значение 95%-ного ДИ соответствующей площади под кривой. Для оценки качества созданной модели использовали меру определенности R-квадрат Нэйджелкерка.
Результаты исследования и их обсуждение. Для разработки математической модели оценивались следующие клинико-анамнестические и лабораторные показатели (в качестве факторов-предикторов): ●возраст, ●пол, ●длительность симптомов ИБС, ●наличие стенокардии, ●ФК хронической сердечной недостаточности (по NYHA), ●длительность АГ в анамнезе, ●систолическое артериальное давление, ●диастолическое артериальное давление, ●уровень фракталкина/CX3CL1, ●уровень TFN и ●уровень ADMA.
В качестве исхода в математической модели рассматривались следующие варианты событий: 1 – жизнеугрожающие осложнения развивались, 0 – жизнеугрожающие осложнения не развивались.
В итоге полученная математическая модель имела следующий вид:
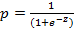 , где
, где
●р – вероятность наступления исхода развития жизнеугрожающих осложнений (КШ и отек легких) в остром периоде ИМ;
●e – число Эйлера (константа), равное 2,71828;
●z = 3,057 + 0,006 × фракталкин/CX3CL1 - 3,207 × ADMA- 6,465 × ТFN
●3,057 – константа.
●0,006 – коэффициент первой переменной,
●фракталкин/CX3CL1 – уровень фракталкина, пг/мл,
●-3,207 – коэффициент второй переменной,
●ADMA – уровень асимметричного диметиларгинина, мкмоль/л,
●-6,465 – коэффициент третьей переменной,
●ТFN – уровень трансферрина, г/л
Расчет универсального критерия коэффициентов модели указывает на статистическую значимость разработанной модели - χ2=38,155, df=3; р<0,001.
По данным классификационной таблицы, из общего числа пациентов у 8 человек (что составило 12,7%) было спрогнозировано развитие жизнеугрожающих осложнений, и они действительно у них развились, у 2 человек (что составило 3,2%) было спрогнозировано развитие жизнеугрожающих осложнений, но в итоге жизнеугрожающие осложнения у них не развились. У еще 2 человек (3,2%) из общего числа обследованных было спрогнозировано отсутствие развития жизнеугрожающих осложнений, но по результатам наблюдения у них было зарегистрировано развитие жизнеугрожающих осложнений. У 51 человека было спрогнозировано отсутствие развития жизнеугрожающих осложнений, что подтвердилось результатами наблюдений.
Таким образом, из 52 человек, у которых не наблюдалось развитие жизнеугрожающих осложнений, процент правильных прогнозов составил 96,2.
Среди пациентов, у которых в результате наблюдения было зарегистрировано развитие жизнеугрожающих осложнений, из 10 человек процент правильных прогнозов составил 80,0.
Суммарный процентный показатель правильных прогнозов составил 93,7%, или 59 случаев среди 63 обследуемых.
Значения показателей оценки качества разработанной математической модели представлены в таблице 2.
Таблица 2
Показатели оценки качества разработанной математической модели
|
Показатели |
% |
|
Диагностическая чувствительность |
96,2 |
|
Диагностическая специфичность |
80 |
|
Диагностическая точность |
93,7 |
|
Прогностическая ценность положительного результата |
86,4 |
|
Прогностическая ценность отрицательного результата |
80 |
Прогностическая критериальная валидность для математической модели составила r=0,76.
Значение статистического критерия Вальда (Wald) для ADMA = 0,260; для фракталкина/CX3CL1 = 0,800; для TFN = 8,718; constant = 0,133; значение p для всех критериев <0,05.
При пошаговом введении предикторов в математическую модель точность прогноза с одним предиктором (фракталкин/CX3CL1) достигала уровня 81%. С двумя предикторами (фракталкин/CX3CL1 и ADMA) – 88,9%, с тремя (фракталкин/CX3CL1, ADMA,TFN) – 93,7%.
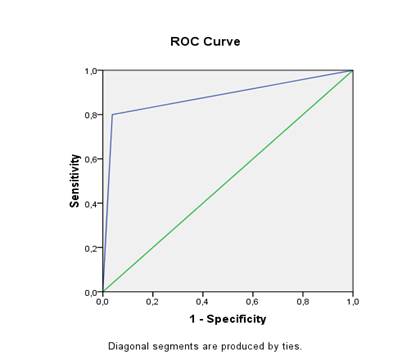
Рис. 2. ROC-кривая разработанной математической модели
Для оценки качества созданной модели использовали меру определенности Нэйджелкерка. R-квадрат Нэйджелкерка (псевдокоэффициент детерминации) составил 77,9%.
Площадь под ROC-кривой, соответствующей взаимосвязи прогноза жизнеугрожающих осложнений острого периода ИМ и значения регрессионной функции, составила 0,881±0,077 с 95% ДИ 0,731-1,032, что указывает на очень хорошее качество разработанного алгоритма (рис. 2).
Также были рассчитаны пороговые значения для прогноза развития жизнеугрожающих осложнений (КШ, отек легких) в острый период ИМ. Пороговый уровень фракталкина/CX3CL1 составил 753,5 мкмоль/л (площадь под кривой ROC составила 0,87 ± 0,052 с 95% ДИ 0,756 – 0,971 (р<0,001)). Чувствительность и специфичность метода составили 82,1% и 54,7% соответственно. Пороговый уровень ADMA, составил 1,4 мкмоль/л (площадь под кривой ROC составила 0,82 ± 0,102 с 95% ДИ 0,619 – 0,98 (р<0,001)). При этом чувствительность составила 80%, специфичность 88,7%. Уровни фракталкина/CX3CL1 и ADMA, равные или превышающие данные значения, соответствовали прогнозу наличия жизнеугрожающих осложнений (КШ, отек легких) в остром периоде ИМ.
Несмотря на то что включение уровня TFN в математическую модель в качестве маркера развития жизнеугрожающих осложнений увеличивало ее прогностическую ценность на 7,9%, площадь под кривой ROC составила 0,620 ± 0,095 с 95% ДИ 0,542 – 0,691 (р<0,001), что сделало диагностически нецелесообразным расчет его порогового уровня.
Заключение. Предложенная математическая модель позволяет осуществлять 7-дневный персонализированный прогноз развития жизнеугрожающих осложнений (КШ, отек легких) у пациентов в остром периоде ИМ. Данная математическая модель обладает высокой чувствительностью (89%) и прогностической значимостью (94%). Это позволяет рекомендовать её для использования в клинической практике, что, в свою очередь, будет способствовать эффективному прогнозированию риска развития жизнеугрожающих осложнений - КШ и отека легких - у пациентов в остром периоде ИМ.
Библиографическая ссылка
Прокофьева Т.В., Кузьмичев К.Ю., Полунина О.С., Липницкая Е.А., Полунина Е.А. МАТЕМАТИЧЕСКАЯ МОДЕЛЬ ДЛЯ ОЦЕНКИ РИСКА РАЗВИТИЯ ЖИЗНЕУГРОЖАЮЩИХ ОСЛОЖНЕНИЙ В ОСТРОМ ПЕРИОДЕ ИНФАРКТА МИОКАРДА // Современные проблемы науки и образования. 2021. № 4. ;URL: https://science-education.ru/en/article/view?id=31046 (дата обращения: 22.05.2026).
DOI: https://doi.org/10.17513/spno.31046



