Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
EXCIMER LASER TOPOGRAPHICALLY ORIENTED CORNEAL CROSSLINKING
Арсенал новых технологий роговичного кросслинкинга расширяется с каждым годом [1–3]. Это касается, прежде всего, применения кросслинкинга при патологии роговицы, включая первичные и вторичные кератоэктазии [4–5]. Накоплен клинический материал, доказывающий целесообразность применения профилактического кросслинкинга при истончении роговицы после различных лазерных, хирургических, фоторефракционных, фототерапевтических и комбинированных операций на роговой оболочке. Это связано не только с профилактикой возможности развития эктазии, но и с необходимостью компенсации ослабленной фотопротекторной функции истонченной роговой оболочки. Именно роговая оболочка и хрусталик являются не только главными преломляющими структурами, но и важнейшими защитными структурами глаза по блокированию внешнего УФ-излучения. Об этом необходимо помнить при оптико-реконструктивных операциях на глазах. Любое истончение роговицы неизбежно увеличивает внешнюю ультрафиолетовую (УФ) нагрузку на хрусталик и может явиться одним из факторов более раннего развития катаракты, а также нарушений в системе антиоксидантной защиты всех внутриглазных структур [6].
Целью настоящей работы явилось рассмотрение особенностей инновационной технологии эксимерлазерного топографически ориентированного кросслинкинга роговицы.
Материал и методы исследования
В основу работы положены клинические исследования по применению рибофлавина для фотопротекции и лазер-индуцированного кросслинкинга в фоторефракционной (510 операций) и фототерапевтической (72 операции) хирургии роговицы. Для профилактического кросслинкинга в фоторефракционной и фототерапевтической хирургии роговицы достаточной была активация рибофлавина вторичным излучением, индуцируемым при проведении абляции. При лечебном кросслинкинге применяли только плотности энергии излучения эксимерного лазера на аргон-фторе ниже порога абляции. Специальная технология использования субабляционных плотностей энергии была применена для формирования на абляционной поверхности боуменоподобной мембранной структуры. Насыщение стромы 0,1%-ным или 0,25%-ным изотоническим раствором рибофлавина проводилось капельным или аэрозольным способом с использованием портативного ультразвукового небулайзера с меш-технологией диспергирования раствора. При проведении профилактического кросслинкинга в фоторефракционной хирургии эпителий удаляли в режиме ФТК с учетом его толщины по данным ОКТ роговицы. Для лечебного кросслинкинга при кератоконусе, вторичных кератоэктазиях, инфекционных кератитах и другой патологии роговицы были применены плотности энергии эксимерлазерного излучения ниже порога абляции. Все исследования проводились с соблюдением принципов Хельсинкской декларации и с разрешения этического комитета ФГБУ «Национальный медико-хирургический центр им. Н.И. Пирогова» Минздрава России. Фоторефракционные и фототерапевтические операции с применением эксимерного лазерного излучения ниже порога абляции выполнялись на российском эксимерном лазере «Микроскан Визум-500». В данной лазерной установке была реализована возможность быстрого перехода от абляционного к субабляционным режимам без каких-либо дополнительных контрольных калибровок. Диаметр сканирующего пятна был равен 0,9 мм с Гауссовым профилем распределения энергии. Частота сканирования по роговице составляла 37 Гц. В клинике при оценке состояния роговицы после эксимерлазерного кросслинкинга особый акцент был сделан на высокоразрешающей спектральной оптической когерентной томографии (ОКТ) и денситометрии роговицы. Исследования проводили на приборах RTVue 100 и RTVue XR100 (Optovue, США). Кератотопографические и денситометрические исследования выполняли на приборе TMS-5 (Topcon, Япония). Кроме того, для оценки состояния роговицы после эксимерлазерного кросслинкинга была применена методика оценки динамических изменений гидратации и рефракционного индекса по данным двухволнового оптического сканирования роговицы в видимом (TMS-5) и инфракрасном (RTVue XR100) диапазонах.
Результаты исследования и их обсуждение
Клинические наблюдения выявили преимущество фоторефракционной абляции с предварительным насыщением стромы рибофлавином. Это проявлялось снижением асептической воспалительной реакции в раннем послеоперационном периоде, сокращением сроков стабилизации визуальных и оптико-рефракционных показателей. Использование портативного ультразвукового небулайзера с меш-технологией диспергирования раствора рибофлавина позволяло получить аэрозольные частицы размером в диапазоне от 1 до 5 мкм. Это улучшало проникновение аэрозольных частиц с деэпителизированной поверхности в строму роговицы и насыщение стромы рибофлавином. Анализ результатов различных фоторефракционных и фототерапевтических операций на роговице показал отсутствие влияния насыщения стромы 0,1%-ным или 0,25%-ным изотоническим раствором рибофлавина на точность абляции. При этом насыщенные рибофлавином слои стромы роговицы срабатывали как спектральные фильтры, защищая кератоциты и нервы в глубже расположенных слоях стромы от негативного влияния на них индуцированного абляцией вторичного УФ-излучения.
Клинические исследования по фотоабляции с рибофлавином легли в основу разработки в клинике профилактического и лечебного лазер-индуцированного роговичного кросслинкинга. Технология такого кросслинкинга заключалась в применении для активации рибофлавина вторичного излучения, которое формировалось при воздействии на строму излучения эксимерного лазера на аргон-фторе. При этом сканирование стромы роговицы, насыщенной рибофлавином, осуществлялось пятном не более 1,0 мм в диаметре. Это было связано с тем, что при большем диаметре пятна нельзя реализовать проведение персонализированной абляции по данным кератотопографии или аберрометрии.
Вторичное излучение имело место как при абляционных, так и при субабляционных плотностях энергии в импульсе. Широкий спектр индуцированного вторичного излучения включал ультрафиолетовый диапазон, который перекрывал все четыре пика максимального поглощения рибофлавином. Это указывало на преимущества применения вторичного излучения эксимерного лазера на аргон-фторе для инициирования эффекта кросслинкинга в строме роговицы. Такой лазер-индуцированный кросслинкинг позволил предложить ряд инновационных технологий эксимерной лазерной хирургии роговицы с фотопротекцией, профилактическим и лечебным роговичным кросслинкингом. Клинические наблюдения показали, что в большинстве случаев при фоторефракционной хирургии роговицы для профилактики кератоэктазий достаточным является проведение абляции после насыщения стромы роговицы 0,1%-ным или 0,25%-ным изотоническим раствором рибофлавина. В зависимости от степени аметропии и объема удаляемой ткани время насыщения колебалось от 2 до 10 мин. В то же время по завершении абляции в прилежащих слоях стромы инициировался эффект кросслинкинга. При этом на абляционной поверхности формировалась тонкая мембранная структура. При ОКТ роговицы мембрана выявлялась только в тех случаях, когда ее толщина превышала 5 мкм. Это было связано с разрешающей способностью применяемого оптического томографа. При денситометрии роговицы наблюдалось повышение оптической плотности в слоях стромы, прилежащих к зоне абляции. Такой лазер-индуцированный кросслинкинг в фоторефракционной хирургии роговицы имел профилактическую направленность и был более физиологичным. Прежде всего, это было связано с тем, что для активации рибофлавина использовалось только вторичное излучение, индуцированное в ходе рефракционной эксимерной лазерной кератоэктомии.
Основу технологии лечебного лазер-индуцированного кросслинкинга составило насыщение стромы роговицы рибофлавином и использование для его активации импульсного излучения эксимерного лазера на аргон-фторе при плотностях энергии в импульсе ниже порога абляции. Применение сканирующего пятна малого диаметра позволило провести персонализированный топографически ориентированный роговичный кросслинкинг. При сканирующей технологии кросслинкинга оксигенация стромы роговицы летающим пятном нарушалась в меньшей степени. Кроме того, широкий спектр индуцированного вторичного УФ-излучения увеличивал активацию рибофлавина, суммарный коэффициент экстинкции и эффект роговичного кросслинкинга. При этом запускался целый каскад реакций образования активных радикалов. Формирование таких радикалов обусловлено послеоперационной асептической воспалительной реакцией. Характер и степень выраженности этой реакции во многом предопределяли время появления, обратного развития и степень выраженности демаркационной линии в строме роговицы. Так, при ОКТ роговицы было отмечено углубление зоны кросслинкинга в строме на 6-й день по сравнению с первичной зоной спустя 1 сутки после лазер-индуцированного кросслинкинга (рис. 1).
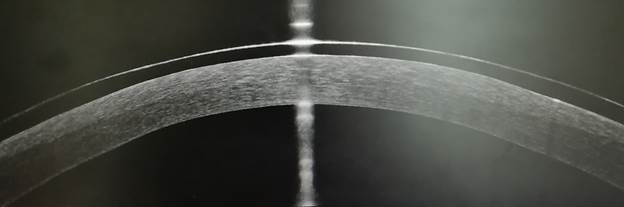
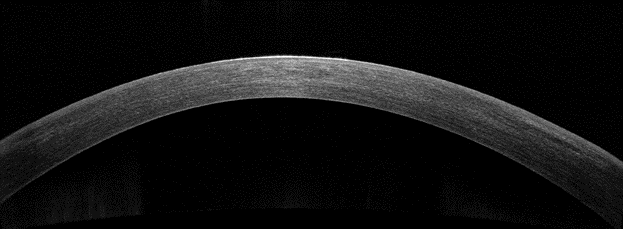
Рис.1. ОКТ роговицы через 1 (в контактной линзе) и 6 суток после топографически ориентированного лазер-индуцированного кросслинкинга излучением эксимерного лазера на аргон-фторе по поводу прогрессирующего кератоконуса II стадии
Во всех случаях форма и глубина залегания демаркационной линии в строме служили маркером конкретных зон роговицы, в которых произошел кросслинкинг. Следует отметить, что при профилактическом щадящем варианте кросслинкинга появление демаркационной линии было редким. О стабилизации процесса и достигнутом лечебном эффекте судили по данным дифференциальной кератотопографии и динамике скринингового индекса эктазии. По данным ОКТ и денситометрии роговицы лечебный лазер-индуцированный кросслинкинг роговицы проявлял все признаки традиционного роговичного кросслинкинга (рис. 2). Более подробно результаты ОКТ и денситометрии после лазер-индуцированного кросслинкинга были изложены в ранее опубликованной работе [7].
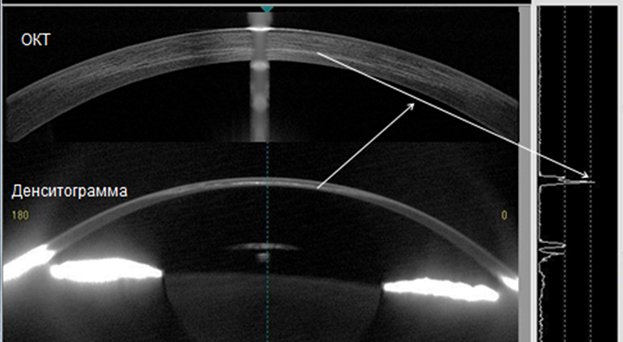
Рис. 2. ОКТ и денситограмма роговицы через 1 месяц после лечебного лазер-индуцированного кросслинкинга излучением эксимерного лазера на аргон-фторе по поводу прогрессирующего кератоконуса II стадии
В ряде случаев эффект лазер-индуцированного кросслинкинга был усилен за счет использования специальной технологии применения субабляционных плотностей энергии для формирования на абляционной поверхности боуменоподобной мембранной структуры.
Лечебный лазер-индуцированный кросслинкинг роговицы показал свою эффективность при эндотелиально-эпителиальной форме дистрофии роговицы с выраженным болевым синдромом, инфекционных язвенных кератитах и рецидивирующих эпителиальных эрозиях роговицы. При патологии роговицы лечебный роговичный кросслинкинг сочетался с фототерапевтической кератоэктомией помутневших или некротически измененных слоев роговичной стромы.
Применение офтальмологических эксимерных лазерных установок и субабляционных режимов облучения позволило впервые реализовать проведение персонализированного кросслинкинга роговицы по данным кератотопографии.
По данным двухволнового оптического сканирования в видимом (TMS-5) и инфракрасном диапазонах (RTVue XR100) были отмечены изменения степени гидратации и рефракционного индекса роговицы в различные сроки после эксимерлазерного кросслинкинга. Это позволило получить новую информацию о влиянии кросслинкинга на состояние роговицы. Кроме того, двухволновое оптическое сканирование роговицы позволило объяснить случаи повышения остроты зрения без и с коррекцией, которые входили в противоречие с данными компьютерной кератотопографии и рефрактометрии.
Преимущества инновационной технологии лазер-индуцированного кросслинкинга при применении эксимерного офтальмологического лазера с длиной волны 193 нм заключалось в следующем:
– впервые реализовать проведение персонализированного локального кросслинкинга по данным компьютерной кератотопографии путем ее сканирования пятном малого диаметра излучения эксимерного лазера на аргон-фторе;
– впервые осуществить активацию рибофлавина индуцированным вторичным лазерным УФ-излучением дальнего спектрального, широкий спектр которого перекрывает все 4 пика максимального поглощения рибофлавином;
– обеспечить лучшую оксигенацию стромы роговицы при ее сканировании летающим пятном малого диаметра импульсного излучения эксимерного лазера;
– значительно сократить время облучения роговицы;
– уменьшить ответную асептическую воспалительную реакцию и ускорить эпителизацию роговицы за счет лучшего эффекта поглощения УФ спектрального диапазона вторичного индуцированного излучения в слоях стромы, насыщенных рибофлавином.
Заключение
Кросслинкинг роговицы по данным компьютерной топографии может быть реализован путем сканирования насыщенной рибофлавином стромы излучением эксимерного лазера на аргон-фторе при абляционных и субабляционных плотностях энергии в импульсе и пятном не более 1,0 мм в диаметре.
Библиографическая ссылка
Корниловский И.М., Гиля А.П., Хататаев Р.Р. ЭКСИМЕРЛАЗЕРНЫЙ ТОПОГРАФИЧЕСКИ ОРИЕНТИРОВАННЫЙ КРОССЛИНКИНГ РОГОВИЦЫ // Современные проблемы науки и образования. 2021. № 2. ;URL: https://science-education.ru/en/article/view?id=30613 (дата обращения: 29.04.2026).
DOI: https://doi.org/10.17513/spno.30613



