Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
ACUTE RESPIRATORY VIRAL INFECTIONS COMPLICATED BY SEVERE OBSTRUCTIVE SYNDROME: CLINICAL AND LABORATORY CHARACTERISTICS
Бронхообструктивный синдром (БОС) в настоящее время привлекает большое внимание врачей-педиатров по двум основным причинам. Во-первых, быстрота и тяжесть возникновения клинических симптомов, требующих оказания неотложной помощи, диктуют необходимость постоянного совершенствования алгоритмов оказания неотложной помощи [1]. Во-вторых, возможна трансформация БОС в бронхиальную астму, поиску предикторов посвящены многочисленные исследования [2, 3].
Согласно литературным данным, около 5% детей младшего возраста хотя бы один раз в течение жизни переносили эпизод острой бронхиальной обструкции [4]. Дети с бронхообструктивным синдромом, осложняющим течение острых респираторных вирусных инфекций, составляют значительную часть пациентов, госпитализированных в детский инфекционный стационар [5]. Так, по данным ГБУЗ «Волгоградская областная детская клиническая инфекционная больница», количество детей с острой бронхиальной обструкцией, пролеченных в респираторных отделениях больницы в течение года, составляет в среднем 30–35% в общей структуре пациентов, поступивших на лечение с болезнями органов дыхания.
Цель исследования: дать клинико-лабораторную характеристику тяжелому бронхообструктивному синдрому у детей; выявить наиболее значимые диагностические и прогностические критерии, характеризующие тяжесть течения БОС.
Материал и методы исследования. Когортное исследование было проведено в ГБУЗ«Волгоградская областная детская клиническая инфекционная больница» в период 2017–2019 гг. До его начала было получено положительное разрешение от Этического комитета Волгоградского государственного медицинского университета. До начала работы был определен размер минимальной выборки, который, с учетом 95%-ного доверительного интервала 5%-ной возможной погрешности, составил 100 человек.
Всего в исследование были включены 268 детей с острыми респираторными вирусными инфекциями, осложненными БОС, проходивших лечение в инфекционной клинике. Первую (основную) группу (I) составили 94 ребенка с тяжелым течением БОС, получавших терапию в отделении интенсивной терапии и реанимации больницы. Группу сравнения (II) составили 174 пациента аналогичного возраста, имевшие легкое и среднетяжелое течение синдрома и проходившие лечение в общем респираторном отделении.
Критерии включения в исследования: возраст ребенка от 1 месяца до 5 лет; наличие патогномоничных признаков острой респираторной вирусной инфекции с бронхиальной обструкцией; отсутствие хронических заболеваний бронхолегочной системы; информированное согласие на участие в исследовании.
Критерии исключения: возраст детей младше 1 месяца и старше 5 лет; наличие в анамнезе врожденных и приобретенных хронических заболеваний бронхолегочной системы; отказ от участия в исследовании.
Для оценки течения БОС анализировали как клинико-лабораторные, так и анамнестические данные пациентов. Диагноз «бронхообструктивный синдром» устанавливали на основании наличия характерного клинического синдромокомплекса, включающего в себя экспираторную одышку с удлиненным выдохом, приступообразный кашель, свистящие хрипы, выслушиваемые при аускультации. Всем больным проводили комплексное исследование клинических лабораторных параметров, пульсоксиметрию, измерение частоты дыхания, измерение АД, пульса, КЩР, электролитов, по показаниям проводили ЭКГ, рентгенографию грудной клетки. Этиологическую верификацию ОРВИ осуществляли при исследовании смывов с носоглотки на респираторные вирусы методом мультиплексной ПЦР (единая диагностическая лаборатория Волгоградской области). Из анамнестических данных учитывали возраст, эндогенные факторы риска (преморбидный фон и аллергологический статус, возраст матери и наличие атопии в семье, особенности течения данной беременности и родов, тип вскармливания, частоту ОРВИ в течение последнего года); экзогенные факторы (курение родителей, количество детей в семье).
Статистический анализ полученных данных проводился с использованием программы STATISTICA-10. Для оценки количественных показателей применяли вычисление средних значений, стандартных отклонений, медианы, 95%-ного доверительного интервала (ДИ); для оценки категориальных различий независимых выборок использовали критерий χ2. За статистически значимый уровень вероятности принимали р<0,05.
Результаты исследования и их обсуждение. Всего бронхообструктивный синдром был диагностирован у 268 детей, при этом у 94 детей тяжесть БОС была определена как тяжелая. Эти дети составили основную (I) группу наблюдения. Среди них преобладали мальчики (58 человек, 61,7%), девочек было 36 (38,3%). Медиана среднего возраста детей составляла 9,0 месяцев с 95%-ным доверительным интервалом от 14,15 до 21,48 месяца.
В контрольную группу вошли 174 ребенка в возрасте от 1 месяца до 5 лет, переносящих БОС в легкой и среднетяжелой степени тяжести. Гендерный состав пациентов этой группы был 70,7% (123) мальчиков и 29,3% (51 ребенок) девочек, медиана возраста 8,0 месяца, ДИ 95% от 12,65 до 17,04 месяца.
Анализ основных анамнестических данных пациентов групп сравнения представлен в таблице.
Характеристика течения перинатального периода у детей с БОС
|
Анализируемые параметры |
I группа |
II группа |
||
|
абс. |
% |
абс. |
% |
|
|
Гестационный возраст при рождении* |
||||
|
Менее 38 недель |
27 |
28,7 |
21 |
12,1 |
|
Более 38 недель |
67 |
71,3 |
153 |
87,9 |
|
Значения критерия χ2 между группами 11,514, p<0,001 |
||||
|
Вес при рождении* |
||||
|
Менее 3000 г |
34 |
36,2 |
37 |
21,3 |
|
От 3000 до 4000 г |
49 |
52,1 |
119 |
68,4 |
|
Более 4000 г |
11 |
11,7 |
18 |
10,3 |
|
Значения критерия χ2 между группами 7,797, р=0,021 |
||||
|
Гестоз во время беременности* |
||||
|
Да |
46 |
48,9 |
31 |
17,8 |
|
Нет |
48 |
51,1 |
143 |
82,2 |
|
Значения критерия χ2 между группами 28,865, p<0,001 |
||||
|
Угроза прерывания беременности в анамнезе* |
||||
|
Да |
45 |
47,9 |
37 |
21,3 |
|
Нет |
49 |
52,1 |
137 |
78,7 |
|
Значения критерия χ2 между группами 20,347, p<0,001 |
||||
|
Диагностированная гипоксия плода* |
||||
|
Да |
28 |
29,8 |
32 |
18,4 |
|
Нет |
66 |
70,2 |
142 |
81,6 |
|
Значения критерия χ2 между группами 4,562, р=0,033 |
||||
|
Слабость родовой деятельности* |
||||
|
Да |
13 |
13,8 |
5 |
2,9 |
|
Нет |
81 |
86,2 |
169 |
97,1 |
|
Значения критерия χ2 между группами 11,693, p<0,001 |
||||
|
Заболевания сердечно-сосудистой системы у матери* |
||||
|
Да |
16 |
17,0 |
7 |
4,0 |
|
Нет |
78 |
83,0 |
167 |
96,0 |
|
Значение критерия χ2 между группами 13,143, p<0,001 |
||||
|
Отягощенный аллергический фон у матери* |
||||
|
Да |
13 |
13,8 |
9 |
5,2 |
|
Нет |
81 |
86,2 |
165 |
94,8 |
|
Значения критерия χ2 между группами 6,071, р=0,014 |
||||
|
Вид вскармливания в первом полугодии жизни* |
||||
|
Грудное |
53 |
56,4 |
149 |
85,6 |
|
Искусственное |
41 |
43,6 |
25 |
14,4 |
|
Значения критерия χ2 между группами 28,128, p<0,001 |
||||
|
Наличие 2 и более детей в семье |
||||
|
Да |
63 |
67,0 |
122 |
70,1 |
|
Нет |
31 |
33,0 |
52 |
29,9 |
|
Значения критерия χ2 между группами 0,273, р=0,602 |
||||
* – достоверность установленных различий по группам сравнения.
Было установлено, что среди детей I группы 27 (28,7%) родились недоношенными, при этом у 34 из них (36,2%) при рождении устанавливали низкую массу тела. Избыточный вес (более 4000 г) был у 11 детей (11,7%), медианный показатель веса пациентов данной группы при рождении составил 3200 г (ДИ 95% 2500–3500 г). В группе сравнения 21 ребенок (12,1%) родился недоношенным, при этом 37 детей (21,3%) имели низкую массу тела при рождении, тогда как у 10,3% детей (18 пациентов) определялся избыточный вес. Медианный показатель веса пациентов II группы при рождении составил 3252 г (ДИ 95% 3140–3365 г). Изучение достоверности различий изучаемых параметров показало, что дети, переносящие тяжелый БОС, достоверно чаще имели низкую массу тела при рождении (χ2 =7,797, р=0,021).
Была установлена взаимосвязь течения беременности матери и тяжести БОС у детей. Так, достоверно чаще развивался тяжелый БОС у пациентов от матерей с отягощенным акушерским анамнезом: гестоз беременных (χ2=28,865, p<0,001); диагностированная гипоксия плода (χ2=4,562, р=0,033); угроза прерывания беременности (χ2=20,347, p<0,001) и слабость родовой деятельности (значение критерия χ2 между группами 11,693, p<0,001).
Также на тяжесть течения БОС оказывали влияние отягощенный преморбидный фон матери: заболевания сердечно-сосудистой системы (пороки сердца, гипертоническая болезнь и др.) (значение критерия χ2 между группами 13,143, p<0,001), а также аллергические заболевания (бронхиальная астма, аллергический ринит и др.) (значение критерия χ2 между группами 6,071, р=0,014). В постнатальном периоде достоверно чаще тяжелый БОС развивался у детей, находящихся на искусственном вскармливании готовыми молочными смесями.
Соответственно, доношенные дети, рожденные от нормально протекающей беременности, с массой тела более 3 кг от матерей без аллергических заболеваний и заболеваний сердечно-сосудистой системы, достоверно реже разворачивали клинику тяжелой бронхообструкции.
Средний возраст матерей в I группе составил 29,05±5,66 года [Me 29; ДИ 95% 27,89–30,21 года], при этом большинство детей были рождены от 2-х родов (в среднем 2,13±1,26; Ме – 2-е роды). В соответствии с этим 63 ребенка (67,0%) имели сибсов в семье, а третьим и более ребенком по счету были 24 из них – 25,5%. В группе сравнения возраст матерей составил 30,66±5,59 года [Me 30; ДИ 95% 29,82–31,5 года]. Также 122 ребенка (70,1%) имели сибсов в семье, а третьим и более ребенком по счету был 41 из них – 23,6%. Полученные данные не выявили значимых различий по группам (р>0,05).
Анализ этиологической структуры БОС показан на рисунке.
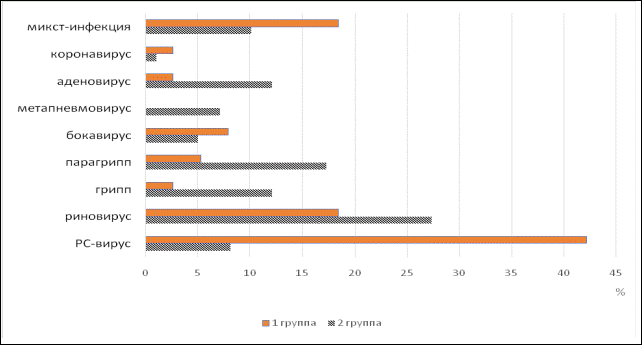
Этиология бронхообструктивного синдрома у детей с тяжелой (I группа) и среднетяжелой (II группа) формой течения заболевания (%)
Из данных рисунка следует, что основным этиологическим фактором тяжелого течения БОС являлись респираторно-синцитиальные вирусы (42,2%), несколько реже выделяли риновирусы (18,4%), бокавирусы – 7,9%, вирусы парагриппа – 5,3%, адено- и коронавирусы – в 2,6% случаев равнозначно. В группе сравнения наиболее частым патогеном был риновирус (27,3%), далее шли вирусы парагриппа (17,2%) и аденовирусы (12,1%). Вклад всех оставшихся вирусов был крайне незначительным и не превышал 10%.
При оценке течения заболевания было установлено, что у всех пациентов I группы диагностирована третья степень тяжести БОС, что требовало их госпитализации в отделение интенсивной терапии. Одним из ведущих критериев тяжести течения инфекционного процесса является интоксикация, при этом ее выраженность, как правило, коррелировала с уровнем температуры.
Установлено, что у пациентов с БОС температура не была связана с тяжестью дыхательной недостаточности и бронхообструкции, а ее выраженность была минимальной. Средние показатели температуры при поступлении у всех пациентов I группы варьировали от 35,9 до 39,50С со средними значениями в диапазоне 36,98±0,630С [Ме – 37,00С, ДИ 95% 37,11–37,420С], что характеризует собой субфебрильную температуру. В группе сравнения средние значения температуры тела при поступлении достоверно не отличались и составили 36,98±0,640С [Me – 36,90С; ДИ 95% 36,88–37,070С, с диапазоном показателей от 35,60С до 39,00С] (р>0,05).
У всех пациентов при поступлении отмечали выраженное тахипноэ, при этом среднее значение у пациентов I группы было определено как 47,22±9,23 дыханий в минуту [Ме – 47,0; ДИ 95% 45,33–49,11], тогда как во II группе эти показатели были достоверно ниже – 34,33±6,02 дыханий в минуту [Ме 34,0; ДИ 95% 33,43–35,23] (р<0,05).
Одним их главных признаков дыхательной недостаточности у детей является снижение уровня кислорода в крови. Было установлено, что у пациентов I группы средний показатель оксигенации крови при поступлении составлял 84,94±2,16 [Me – 85,0, ДИ 95% 84,49–85,38], при этом во II группе он был значительно выше – 95,19±1,65 [Me – 96,0, ДИ 95% 94,94–95,44] (р<0,05). Одновременно с этим отмечали компенсаторное увеличение частоты сердечных сокращений – 151,88±20,09 ударов в минуту [Ме – 155,00 ударов], в группе сравнения – 128,52±10,29 ударов в минуту [Ме – 128,00 ударов] (р<0,05).
При исследовании стандартных лабораторных показателей было установлено, что у детей I группы был выявлен нейтрофильный лейкоцитоз со средним уровнем лейкоцитов 11,97±5,83•109 г/л [Me 10,8•109 г/л, ДИ 95% 10,78–13,17•109 г/л], в лейкоцитарной формуле крови отмечался нейтрофильный сдвиг (60,47±22,52%, Ме – 66,5%, ДИ 95% 55,9–65,1%). В группе сравнения число лейкоцитов оставалось в пределах возрастной нормы либо отмечался незначительный лейкоцитоз со средним уровнем лейкоцитов 8,87±3,66•109 г/л [Ме 8,03•109 г/л, ДИ 95% 8,33–9,42•109 г/л]. В лейкоцитарной формуле крови данной категории детей выявлен относительный лимфоцитоз 45,29±20,39% [Me 46,0%, ДИ 95% 42,24–48,34%] (р<0,05).
При изучении течения БОС было установлено, что при тяжелом течении достоверно чаще регистрировали развитие осложнений (84,0% против 17,8%, р<0,05). Чаще всего они носили характер присоединения вторичной бактериальной инфекции: пневмонии – 45,7%, отиты – 20,2%, риниты – 14,9%, тонзиллофарингиты – 10,6%. В группе сравнения показатели выглядели как 2,3%, 8,6%, 6,3% и 1,7% соответственно.
Заключение
1. Наличие отягощающих преморбидных факторов влияет на тяжесть течения БОС при острых респираторных инфекциях у детей. Так, дети, реализующие тяжелый БОС, достоверно чаще рождались недоношенными, маловесными, от матерей, имевших неблагоприятно протекающую беременность (гестоз, угрозу прерывания, гипоксию плода), что в целом отражало их неблагоприятный преморбидный фон. Напротив, у доношенных детей, рожденных с массой тела более 3 кг, от физиологически протекающей беременности, БОС протекал достоверно легче.
2. Этиологическим фактором развития тяжелого БОС наиболее часто являлись респираторно-синцитиальные вирусы (42,2%), тогда как при риновирусной инфекции, парагриппе и аденовирусной инфекции данный синдром характеризовался более легким течением.
3. У большинства пациентов в лейкоцитарной формуле отсутствовали значимые изменения, однако в случае тяжелого течения в лабораторных показателях отмечался нейтрофильный лейкоцитоз, тогда как при нетяжелом течении регистрировался относительный лимфоцитоз.
4. Оценка преморбидного фона пациентов с БОС при поступлении позволяет выделить группу высокого риска и интенсифицировать лечение и наблюдение за такими пациентами, начиная с приемного покоя.
Библиографическая ссылка
Крамарь Л.В., Ларина Т.Ю. ОСТРЫЕ РЕСПИРАТОРНЫЕ ВИРУСНЫЕ ИНФЕКЦИИ, ОСЛОЖНЕННЫЕ ТЯЖЕЛЫМ ОБСТРУКТИВНЫМ СИНДРОМОМ: КЛИНИКО-ЛАБОРАТОРНАЯ ХАРАКТЕРИСТИКА // Современные проблемы науки и образования. 2021. № 1. ;URL: https://science-education.ru/en/article/view?id=30540 (дата обращения: 02.06.2026).
DOI: https://doi.org/10.17513/spno.30540



