Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
ESTIMATION OF THE DIAGNOSTIC SIGNIFICANCE OF CIRCULATING MICRORNAS IN BLOOD PLASMA OF PATIENTS WITH HIGH GRADE GLIOMAS
Глиальные опухоли представляют собой наиболее агрессивные первичные новообразования центральной нервной системы. В соответствии с классификацией Всемирной организации здравоохранения (ВОЗ) выделяют глиомы низкой (Grade I–II) и высокой степени злокачественности (Grade III–IV). К опухолям Grade I–II относят диффузную астроцитому, диффузную олигодендроглиому, диффузную олигоастроцитому, плеоморфную ксантоастроцитому, субэпиндимарную гигантоклеточную астроцитому и пилоидную астроцитому. Опухоли Grade III–IV включают анапластическую астроцитому, анапластическую олигоастроцитому, анапластическую олигодендроглиому и глиобластому [1]. Опухоли G IV являются наиболее злокачественными. Средний возраст пациентов с глиобластомой на момент постановки диагноза составляет 60–65 лет. Медиана выживаемости пациентов с глиомами высокой степени злокачественности равна 14,6 месяца, а пятилетняя выживаемость составляет не более 9,8% [2].
Современная диагностика опухолей головного мозга основана на методах нейровизуализации – магнитно-резонансной томографии (МРТ), компьютерной томографии (КТ) и позитронно-эмиссионной томографии (ПЭТ). Вышеуказанные методы позволяют осуществить диагностику, определить локализацию, метаболическую активность опухоли, но не способны в полной мере идентифицировать гистологический тип опухоли. Кроме того, МРТ-диагностика может иметь ряд препятствий для выполнения. К ним относятся избыточный вес пациента, клаустрофобия, беременность, наличие металлических или электрических имплантатов. Золотым стандартом в диагностике глиом является гистологическое исследование опухолевой ткани после проведения микрохирургической резекции или стереотаксической биопсии. Однако морфологический полиморфизм, опухолевая гетерогенность, множественные некрозы опухоли, компетенция нейроморфолога являются дополнительными факторами, осложняющими диагностику глиальных опухолей [3]. Эти ограничения подчеркивают актуальность поиска малоинвазивных и надежных биомаркеров для осуществления точной и своевременной диагностики глиом высокой степени злокачественности.
МикроРНК представляют собой короткие эндогенные некодирующие РНК, которые участвуют в посттранскрипционной регуляции экспрессии генов. МикроРНК участвуют в регуляции пролиферации клеток опухоли, миграции, инвазии и метастазировании. Поиск и идентификация микроРНК с аберрантной экспрессией в опухолевой ткани имеют большое значение для прогноза течения заболевания [4, 5]. Ярким примером является микроРНК hsa-miR-21, экспрессия которой повышена у пациентов с глиомами G IV. Эта микроРНК играет ключевую роль в опухолевой прогрессии, регуляции ангиогенеза и апоптоза. Однако ее экспрессия также значительно повышена при раке молочной железы, гепатоцеллюлярной карциноме, колоректальном раке, раке яичников и других онкологических заболеваниях, что в конечном итоге делает ее не лучшим кандидатом для применения в качестве биологического маркера при диагностике глиальных опухолей [6].
Известно, что при патологических состояниях микроРНК могут переходить из ткани мозга в кровоток, мигрируя через гематоэнцефалический барьер, что делает их потенциальными биомаркерами заболеваний центральной нервной системы [7]. Циркулирующие микроРНК плазмы или сыворотки могут быть использованы в качестве потенциальных биомаркеров для обнаружения, идентификации и мониторинга новообразований, поскольку профиль их экспрессии специфично изменяется при возникновении онкологической патологии [8]. Оценка содержания циркулирующих микроРНК в настоящее время является одним из наиболее перспективных направлений молекулярной диагностики. Это объясняется устойчивостью микроРНК к деградации, локализацией в биологических жидкостях и многообразием патологических процессов, при которых изменяется их экспрессия [9].
В связи с этим целью настоящей работы стало исследование дифференциальной экспрессии циркулирующих микроРНК и возможности их применения в качестве маркеров для диагностики глиом высокой степени злокачественности.
Материалы и методы исследования
Исследование было одобрено этическим комитетом ФГБУ «Национальный медицинский исследовательский центр онкологии» Минздрава России (Ростов-на-Дону). Основную группу составили 20 пациентов с первично диагностированной злокачественной глиальной опухолью головного мозга. Средний возраст равен 59,2±9,1 года. Группу контроля составили 10 потенциально здоровых волонтеров (средний возраст 51,2±9,2 года) и 10 пациентов, страдающих метастатическими опухолями головного мозга (средний возраст 56,2±9,8 года). В каждом случае было получено добровольное информированное согласие пациента на включение в исследование. Диагноз был подтвержден гистологически в соответствии с классификацией ВОЗ опухолей ЦНС (2016).
Цельную кровь собирали в пробирки с этилендиаминтетрауксусной кислотой в качестве антикоагулянта. Центрифугировали 10 мин при 1500 g (не позже чем через 2 ч после сбора крови), надосадочную жидкость перемещали в пробирки без РНКазы и центрифугировали 10 мин при 16000 g и 4°C для удаления клеток и их фрагментов. Далее плазму переносили в криопробирки и хранили при температуре –80°C. Образцы плазмы с гемолизом были исключены из исследования.
Выделение РНК. Нуклеиновые кислоты выделяли согласно рекомендациям производителя QIAzol (Qiagen, Германия). Очистку микроРНК проводили с использованием набора miRNeasy Serum/Plasma Kit (Qiagen, Германия) и экзогенного контроля микроРНК cel-miR-39-5p, микроРНК с последовательностью, не характерной для человека, которая вносится перед проведением анализа в стандартном количестве (1,6x108 копий/мкл) во все образцы для нормализации эффективности процедур выделения и обратной транскрипции микроРНК. Синтез кДНК осуществляли с использованием MMLV Reverta («Синтол», Россия).
Исследование экспрессии микроРНК hsa-miR-22-3p, hsa-miR-122-5p, hsa-miR-107, hsa-miR-324-5p, hsa-miR-34a-5p, hsa-miR-155-5p, hsa-miR-21-5p, hsa-miR-330-3p, hsa-miR-146a-5p, hsa-miR-92a-1-5p проводили методом RT-qPCR. В качестве референсной использовали последовательность экзогенной микроРНК cel-miR-39-5p Caenorhabditis elegans. Дизайн праймеров для исследуемых микроРНК осуществляли с применением miRBase v.22. ПЦР в реальном времени проводили в трех технических проворностях на термоциклере Bio-Rad CFX96 (Bio-Rad, США). Анализ данных количественной ПЦР осуществляли методом 2-ΔΔСt.
Анализ данных. Статистическую обработку данных проводили с помощью пакета программ STATISTICA 10 (Statsoft inc., США). Для оценки диагностической ценности исследуемых микроРНК был проведен анализ ROC-кривых в программной среде вычислений R 3.6.2. Различия экспрессии рассчитывали с помощью ANOVA. Значение p<0,05 указывает на статистическую значимость.
Результаты исследования и их обсуждение
Глиомагенез может быть вызван рядом генетических и эпигенетических нарушений. Молекулы, которые могут специфически отражать эти нарушения, способны служить потенциальными маркерами злокачественных глиом. Значительная роль в инициации и прогрессии злокачественных процессов отводится микроРНК. Ранее нами была произведена оценка экспрессии пула онкоассоциированных микроРНК в тканях глиом высокой степени злокачественности и выявлена зависимость выживаемости пациентов со злокачественными глиомами от уровня экспрессии микроРНК в опухоли hsa-miR-330-3p, hsa-miR-107, hsa-miR-22-3p [5]. В настоящем исследовании был определен профиль экспрессии циркулирующих микроРНК hsa-miR-22-3p, hsa-miR-122-5p, hsa-miR-107, hsa-miR-324-5p, hsa-miR-34a-5p, hsa-miR-155-5p, hsa-miR-21-5p, hsa-miR-330-3p, hsa-miR-146a-5p и hsa-miR-92a-1-5p в плазме крови 20 пациентов с первично диагностированной глиальной опухолью головного мозга, 10 потенциально здоровых волонтеров и 10 пациентов, страдающих метастатическими опухолями головного мозга. У пациентов с глиальными опухолями было выявлено статистически значимое (p<0,05) увеличение экспрессии hsa-miR-22-3p (p=0,000001), hsa-miR-122-5p (p=0,02156), hsa-miR-107 (p=0,000001), hsa-miR-324-5p (p=0,000001), hsa-miR-155-5p (p=0,000001), hsa-miR-21-5p (p=0,000001), hsa-miR-330-3p (p=0,00026) и hsa-miR-146a-5p (p=0,00026) относительно группы условно здоровых волонтеров. Для двух микроРНК (hsa-miR-92a-1-5p и hsa-miR-34a-5p) статистически значимых изменений их содержания в плазме крови обнаружено не было (рис. 1).
Для определения специфичности изменения экспрессии циркулирующих микроРНК у пациентов с глиальными опухолями высокой степени злокачественности относительно других нозологий было проведено исследование содержания исследуемых микроРНК в плазме крови пациентов, страдающих метастатическими опухолями головного мозга. В данном случае статистически значимое изменение содержания в плазме демонстрируют микроРНК hsa-miR-22-3p (p=0,00001), hsa-miR-122-5p (p=0,021557), hsa-miR-107 (p=0,000001), hsa-miR-324-5p (p=0,000001), hsa-miR-155-5p (p=0,00164) , hsa-miR-21-5p (p=0,04144), hsa-miR-330-3p (p=,00002) и hsa-miR-146a-5p (p=0,00001). Для микроРНК hsa-miR-92a-1-5p и hsa-miR-34a-5p статистически значимых изменений обнаружено не было (рис. 1).
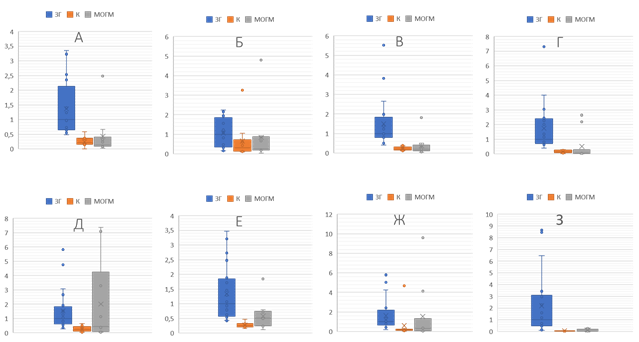
Рис. 1. Изменение относительной экспрессии микроРНК hsa-miR-22-3p (А),
hsa-miR-122-5p (Б), hsa-miR-107 (В), hsa-miR-324-5p (Г), hsa-miR-155-5p (Д),
hsa-miR-21-5p (Е), hsa-miR-330-3p (Ж) и hsa-miR-146a-5p (З) в исследуемых образцах плазмы крови пациентов со злокачественными глиомами (ЗГ), К – контрольной группы и группы пациентов с метастатическими опухолями головного мозга (МОГМ)
В представленной работе мы предприняли попытку определить диагностическую ценность исследуемых циркулирующих микроРНК. Проведенный ROC-анализ выявил сигнатуру, представляющую собой комбинацию микроРНК hsa-miR-107 и hsa-miR-122-5p (AUC=0,885), позволяющую идентифицировать у пациента наличие глиальной опухоли высокой степени злокачественности. Диагностическая чувствительность составила 100%, специфичность – 71,2% (рис. 2А).
Среди всех проанализированных микроРНК и их комбинаций ROC-кривая, позволяющая отделить пациентов со злокачественными глиомами от пациентов с метастатическими опухолями головного мозга, принадлежала сигнатуре hsa-miR-107, hsa-miR-155-5p и hsa-miR-122-5p (AUC=0,82). Диагностическая чувствительность и специфичность сигнатуры микроРНК hsa-miR-107, hsa-miR-155-5p и hsa-miR-122-5p составили 100% и 61,1% соответственно (рис. 2Б).
При наличии у пациента опухолей головного мозга циркулирующие биологические маркеры, в том числе и микроРНК, можно использовать в диагностических целях в качестве информативных биомаркеров заболевания, особенно в ситуации, когда операция противопоказана или результаты биопсии неоднозначны. Это исследование демонстрирует перспективность подхода использования комбинации микроРНК hsa-miR-107 и hsa-miR-122-5p в качестве биомаркера глиом высокой степени злокачественности.
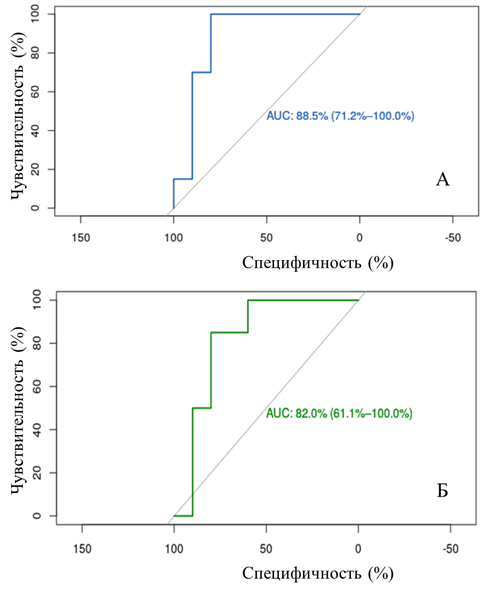
Рис. 2. Roc-кривые сигнатур микроРНК hsa-miR-107 и hsa-miR-122-5p, позволяющих дифференцировать пациентов с глиомами высокой степени злокачественности от здоровых волонтеров (А), и hsa-miR-107, hsa-miR-155-5p и hsa-miR-122-5p, позволяющих дифференцировать пациентов с глиомами высокой степени злокачественности от пациентов с метастатическими опухолями головного мозга (Б)
МикроРНК hsa-miR-107 участвует в регуляции процессов клеточного деления, миграции и ангиогенеза. Аберрантная экспрессия hsa-miR-107 способствует злокачественной трансформации клеток. МикроРНК hsa-miR-107 является отрицательным регулятором экспрессии фактора роста эндотелия сосудов (VEGF), тем самым ограничивая васкуляризацию опухоли [10]. Однако микроРНК hsa-miR-107 может выступать в качестве онкогена, способствующего клеточной миграции, инвазии и метастазированию при раке груди и желудка [11].
МикроРНК hsa-miR-122-5p участвует в пролиферации клеток глиомы за счет регуляции WNT-сигнального пути. Снижение транскрипционной активности hsa-miR-122-5p может привести к более интенсивной пролиферации клеток глиальной опухоли [12]. В качестве маркера глиальных опухолей в плазме крови больных со злокачественными глиомами данная микроРНК ранее не рассматривалась. Однако изменения содержания hsa-miR-122-5p в плазме связаны с негативным прогнозом течения заболевания для пациентов с раком поджелудочной железы [13].
Заключение
Разработка малоинвазивных диагностических методов для обнаружения опухолей головного мозга может способствовать улучшению результатов лечения пациентов с глиомами высокой степени злокачественности. МикроРНК обладают значительным потенциалом для создания чувствительных и специфичных панелей биомаркеров в целях диагностики злокачественных глиом. Сигнатура микроРНК hsa-miR-107 и hsa-miR-122-5p может быть использована в качестве маркера для диагностики глиом высокой степени злокачественности. Возможность применения данного подхода может быть уточнена в дальнейших масштабных исследованиях.
Исследование выполнено в рамках госзадания «Молекулярно-генетические маркеры глиом».
Библиографическая ссылка
Аллилуев И.А., Пушкин А.А., Кузнецова Н.С., Кавицкий С.Э., Росторгуев Э.Е. ОЦЕНКА ДИАГНОСТИЧЕСКОЙ ЗНАЧИМОСТИ ЦИРКУЛИРУЮЩИХ МИКРОРНК В ПЛАЗМЕ КРОВИ ПАЦИЕНТОВ С ГЛИОМАМИ ВЫСОКОЙ СТЕПЕНИ ЗЛОКАЧЕСТВЕННОСТИ // Современные проблемы науки и образования. 2020. № 6. ;URL: https://science-education.ru/en/article/view?id=30309 (дата обращения: 18.05.2026).
DOI: https://doi.org/10.17513/spno.30309



