Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
MODERN APPROACHES TO THE ASSESSMENT OF BIOLOGICAL MARKERS OF AUTOPHAGY AND APOPTOSIS IN ACUTE ISCHEMIC STROKE
Заболеваемость инсультом в мире постоянно растет. Европейская ассоциация по борьбе с инсультом (ESO) совместно с Национальной ассоциацией по борьбе с инсультом (НАБИ) указывают на необходимость формирования единой противоинсультной программы, главной задачей которой является разработка новых алгоритмов профилактики и ранней диагностики заболевания с целью сокращения смертности и инвалидизации [1].
В настоящее время особый интерес исследователей вызывает гибель нейронов по механизму апоптоза и аутофагии – программированной клеточной гибели I и II типа, усиление которой отмечается после острой ишемической атаки и приводит к увеличению объема очага поражения паренхимы головного мозга [2, 3]. В экспериментах установлено, что аутофагия, как и апоптоз, активируется в пенумбре [4]. По мнению ряда авторов, выяснение путей, которые лежат в основе патогенетических механизмов, действующих в пенумбре и, как было показано, влияющих на распространение аутоиммунного постишемического воспаления, имеет большой клинический интерес для разработки новых терапевтических стратегий [5]. Считается, что поврежденные апоптозом и аутофагией нейроны в зоне пенумбры можно восстановить, в отличие от нейронов, погибших по механизму некроза, локализующихся в зоне ишемического ядра и не подлежащих регенерации [6, 7]. Кроме того, эффекторные молекулы, участвующие в сигнальных каскадах апоптоза и аутофагии при остром ишемическом инсульте (ОИИ), представляют интерес не только в качестве мишеней для разработки новых методов лечения ОИИ, но и как новые биологические маркеры в диагностике данного заболевания [8, 9].
Большинство результатов по изучению механизмов апоптоза и аутофагии в патогенезе ОИИ получено в экспериментальных моделях церебральной ишемии. Не вызывает сомнений тот факт, что патологические изменения в организме человека носят более глубокий характер и экстраполяция эффектов, выявленных в системе in vitro или в экспериментальных моделях ОИИ с использованием животных, на организм человека не всегда правомочна. В связи с актуальностью проблемы и малой освещенностью вопроса, касающегося взаимодействия ключевых медиаторов апоптоза и аутофагии в патогенезе ОИИ, представляется перспективным изучение маркеров апоптоза и аутофагии в периферической крови у больных ОИИ в динамике острого периода заболевания [10].
Цель исследования – провести анализ данных литературы за последние 10 лет, посвященных современным лабораторным методам оценки биологических маркеров аутофагии и апоптоза, представляющим интерес для углубленного понимания патогенеза ОИИ и создания новых методов диагностики ОИИ.
Материал и методы исследования
При подготовке обзора были проанализированы 350 источников литературы, полученных из международных и отечественных баз данных: Scopus, Web of Science, Springer, Pubmed и РИНЦ. 45 публикаций были отобраны и включены настоящий обзор.
Результаты исследования и их обсуждение
Актуальность исследуемой задачи
По данным Всемирной организации здравоохранения ежегодно от цереброваскулярных заболеваний (ЦВЗ) умирают около 5 млн человек. При этом удельный вес острого ишемического инсульта (ОИИ) среди форм острого нарушения мозгового кровообращения достигает 80 –85% [1, 11].
В обновленных клинических рекомендациях по ведению пациентов с ОИИ, разработанных совместно с Национальной ассоциацией по борьбе с инсультом, Всероссийским обществом неврологов, Ассоциацией нейрохирургов России, а также Союзом реабилитологов России, особое внимание уделяется нейропротекции. В текущей редакции выделено важнейшее направление нейропротекции – уменьшение выраженности «отдаленных последствий» ишемии: окислительного стресса, избыточного синтеза NO, дисбаланса цитокинов, а также снижение активности процессов апоптоза, лежащих в основе отсроченной смерти клеток нервной ткани [11].
В РФ в качестве нейропротективной терапии наиболее часто назначаются препараты мексидол (этилметилгидроксипиридина сукцинат, ООО «НПК Фармасофт», РФ) и церебролизин (МНН: нет, РУ: «ЭВЕР Нейро Фарма ГмбХ», Австрия) [11, 12]. В рандомизированном двойном слепом мультицентровом плацебо-контролируемом исследовании, проведенном в Российской Федерации в 2017 г., в параллельных группах оценивались эффективность и безопасность длительной последовательной терапии мексидолом у пациентов с полушарным ОИИ в остром и раннем восстановительном периодах. В исследование были включены 150 человек (62 мужчины и 88 женщин). В группе пациентов, получавших мексидол, были выявлены статистически достоверное снижение тяжести неврологического дефицита, оцениваемого по шкале NIHSS (National Institutes of Health Stroke Scale), достоверное улучшение жизнедеятельности, измеренное по модифицированной шкале Рэнкина, и улучшение качества жизни по сравнению с группой пациентов, получавших плацебо [12]. Следует подчеркнуть, что важнейшим фармакологическим свойством мексидола является ингибирование апоптоза, лежащего в основе отсроченной гибели нейронов [11].
В систематическом обзоре, включающем 221 публикацию, проиндексированную в базах данных Scopus и Pubmed в период с октября 1993 г. по август 2019 г., А. Steliga и соавторы [13] проводят сравнительный анализ известных на сегодняшний день биомаркеров, используемых для диагностики ОИИ. Обсуждая перспективы дальнейшего улучшения диагностики заболевания, авторы обращают внимание на необходимость разработки лабораторных предикторов отсроченной гибели нейронов, влияющей на исход заболевания. Данное утверждение подчеркивает диагностическую значимость биомаркеров апоптоза и аутофагии – процессов, принимающих непосредственное участие в отсроченной гибели клеток головного мозга.
Таким образом, апоптоз и аутофагия представляют собой перспективные задачи для исследования с целью разработки принципиально новых методов нейропротекции, диагностики и прогноза исхода ОИИ.
Ключевые маркеры аутофагии, имеющие патогенетическое значение при ОИИ
Результаты анализа, полученные в ходе структурированного исследования библиографических баз данных последних 10 лет, посвященных роли аутофагии в патогенезе ОИИ, позволили сделать вывод, что в настоящее время наиболее надежными молекулярными биомаркерами аутофагии, определяемыми с помощью методов лабораторной диагностики, являются белки LC3, Beclin-1 и р62. В нескольких новейших литературных источниках, суммирующих результаты последних экспериментальных данных, полученных на клеточных культурах, а также с использованием лабораторных животных, делается вывод, что для получения более достоверных результатов рекомендована одновременная оценка всех трех показателей аутофагии в исследуемом биологическом материале [14, 15].
Белок LC3, являющийся убиквитин-подобным белком (кодируется геном Atg8), представляет собой надежный маркер аутофагии, так как его содержание в исследуемом биологическом материале положительно коррелирует с количеством активных аутофагосом – важнейших компонентов процесса аутофагии [16]. Показано, что синтез LC3 усиливается в процессе аутофагии [17]. Следует подчеркнуть, что белок LC3 существует в растворимой форме (LC3-I) и липидированной форме (LC3-II) [18]. Они также называются «цитоплазматическая и аутофагосомальная формы», так как в процессе аутофагии происходит транслокация цитоплазматического LC3-I в аутофагосому, где он липидируется с переходом в LC3-II форму и изолируется в аутофагосомальной мембране. Для оценки активности процесса аутофагии определяют липидированную форму LC3-II [19]. Установлено, что повышенные концентрации белков LC3-II и Beclin-1 в сыворотке и в спинномозговой жидкости пациентов с острым ИИ связаны с хорошим исходом заболевания [10]. Эти данные свидетельствуют в пользу защитной роли аутофагии при остром ИИ.
Другим маркером аутофагии является белок Beclin-1 (кодируется геном Atg6), играющий ключевую роль в инициации аутофагии [20]. В составе белкового комплекса, включающего серин-треониновую киназу р150, фосфатидилинозитол-3-киназу класса III (PI3КIII), протеин Atg14L и белки семейства Bcl-2, Beclin-1 участвует в инициации аутофагии [21]. При стимуляции аутофагии Beclin-1 и протеинкиназа PIK3III образуют агрегаты в области комплекса Гольджи, которые можно верифицировать с помощью метода флуоресцентной микроскопии или вестерн-блоттинга (Western blotting) и рассматривать в качестве маркера ранней аутофагии (фаза инициации) [22]. Beclin-1 необходим для нормального протекания митофагии (митохондриальной аутофагии). В эксперименте установлено, что ингибирование Beclin-1 в нейронах мышей с ОИИ приводит к митохондриальной дисфункции и прогрессированию постишемического нейровоспаления [23, 24].
Белок р62 (nucleoporin) является убиквитин-связывающим каркасным белком, участвующим в регуляции аутофагии и в формировании аутофагосомы [25]. Этот протеин непосредственно взаимодействует с белком LC3 и служит связующим звеном между LC3 и убиквитинированными субстратами [26]. Протеин р62 активно диссоциирует в процессе аутофагии. Таким образом, количественное определение уровня p62 может быть использовано для мониторинга аутофагического процесса [14, 27]. Установлено, что в отличие от белка LC3 содержание р62 в исследуемом биологическом материале обратно коррелирует с интенсивностью аутофагии, поэтому активность процесса аутофагии оценивают по отношению LC3-II/p62 [15, 28]. Скопление p62-позитивных включений, выявляемое иммуноцитохимическим методом, или повышенный уровень p62, детектируемый с помощью вестерн-блоттинга, расцениваются как признак снижения активности аутофагии [18, 29]. В литературе имеются указания на то, что при поверхностной экспрессии белка р62 может происходить его самоагрегация, занижающая показатели активности процесса аутофагии, поэтому рекомендуется определять концентрацию растворимого p62 совместно с оценкой его поверхностной экспрессии [15, 29]. В экспериментальной модели ОИИ показано, что в нейронах мышей содержание р62 повышено [30]. По мнению авторов, повышение р62 носит компенсаторный характер, так как этот белок осуществляет элиминацию поврежденных митохондрий посредством p62-опосредованной митофагии, основными целями которой являются осуществление «контроля качества» митохондрий и поддержание митохондриального гомеостаза [4, 30].
Ключевые маркеры апоптоза, имеющие патогенетическое значение при остром ИИ
Критический анализ 250 литературных источников последних 10 лет, посвященных роли ключевых апоптотических белков в патогенезе ОИИ, позволил выделить 56 наиболее релевантных исследований, 47 из которых свидетельствовали о двойственной роли белков р53 и Bcl-2 в гибели клеток головного мозга при ОИИ, в то время как 9 публикаций указывали на прямое участие этих белков в апоптотической гибели нейронов. Эти 9 работ были отобраны и включены в настоящий обзор.
В большинстве исследований последних 8 лет белок р53 рассматривается как один из основных проапоптотических факторов, участвующих в индукции программированной смерти клеток головного мозга при ОИИ [31, 32]. Это объясняется тем, что р53 способен индуцировать не только апоптоз, но и аутофагию [33, 34]. Показано, что ядерный р53 индуцирует аутофагию [3, 32]. Однако цитоплазматический р53 может выступать в качестве основного супрессора аутофагии в случае своей транслокации в митохондрии и связывания с антиапоптотическими членами семейства Bcl-2 (или при инактивации проапоптотических белков семейства Bcl-2). Таким образом, р53 регулирует баланс между апоптозом и аутофагией, а также контролирует выживание и гибель клеток в ответ на стресс [34].
Новейшие исследования выявили статистически достоверное повышение концентрации р53 в сыворотке пациентов с ОИИ на 1-е, 2-е и 3-и сутки после ишемической атаки по сравнению с пациентами с хронической ишемией головного мозга (группа сравнения) [31].
Семейство Вcl-2 включает как противоапоптотические белки Вcl-2 и Bcl-xL, так и проапоптотические белки Bax, Bim, Bik и Bak [33, 34]. Эти белки являются регуляторами митохондриального пути запуска апоптоза [35], играющего ключевую роль в гибели нейронов при церебральной ишемии [16, 31]. Установлено, что избыток противоапоптотических белков семейства Bcl-2 защищает ткань мозга от ишемии [30].
Экспериментальные исследования на лабораторных животных показали, что объем ишемического поражения головного мозга может быть уменьшен при введении таурина, способствующего активации противоапоптотических белков семейства Bcl-2, которые ингибируют митохондриально-опосредованный апоптоз нейронов за счет подавления цитозольного цитохрома C и поддержания активности противоапоптотического белка Bcl-xL [4, 30]. Отношение Bax/Вcl-2 регулирует баланс между процессами индукции и ингибирования апоптоза, предотвращая падение мембранного потенциала митохондрий через блокирование экспрессии кальпаина и активной каспазы-3 [3].
Современные подходы к верификации биологических маркеров аутофагии с помощью методов лабораторной диагностики
В систематическом обзоре, включающем 86 литературных источников, опубликованных в период с 1997 по 2010 гг., посвященном анализу лабораторных методов оценки аутофагии в клеточных культурах, тканевых биоптатах и периферической крови экспериментальных животных, N. Mizushima и соавторы [14] приходят к выводу, что среди современных лабораторных методов единого «золотого стандарта» для мониторинга активности процесса аутофагии не существует. Считается необходимым параллельное использование нескольких различных методов для точной оценки аутофагической активности в любом биологическом материале [15, 18, 23].
Оценка аутофагии с помощью лабораторных методов включает определение количества активных аутофагосом, мониторинг всех стадий аутофагии, а также измерение активности аутофагического процесса, осуществляемое с использованием индукторов и ингибиторов аутофагии [14, 15].
Для определения количества аутофагосом в клетке оценивают содержание липидированной формы белка LC3 (LC3-II), так как LC3-II является маркером активных аутофагосом [28]. Для определения LC3-II применяют моноклональные антитела, тандемные флуорохромы и используют следующие методы лабораторной диагностики: электронную микроскопию, флуоресцентную микроскопию, вестерн-блоттинг, проточную цитометрию [14].
Электронная микроскопия дает возможность визуализировать аутофагосомы и аутофаголизосомы, образующиеся на этапе слияния аутофагосом с лизосомами. На ультраструктурном уровне аутофаголизосома определяется в виде двухчленной структуры, содержащей непереваренные фрагменты цитоплазмы, которые не слились с лизосомой [18, 36]. Аутофагосомы также могут содержать включения в виде внутриклеточных органелл, например поврежденные митохондрии или фрагменты эндоплазматического ретикулума, выявляемые при электронной микроскопии [14, 22].
Флуоресцентная микроскопия позволяет визуализировать LC3-I, конъюгированный с флуоресцентным красителем GFP (green fluorescent protein), выявляемый по характерному диффузному зеленому свечению в цитоплазме или в виде пунктатных структур, которые в основном представляют собой активные аутофагосомы [22].
Метод вестерн-блоттинга (Western blotting) позволяет осуществлять мониторинг преобразования растворимой формы белка LC3-I, конъюгированного с GFP, в липидированную форму LC3-II [36, 37]. С помощью моноклональных антител (МКАТ) к LC3-I, к LC3-II и флурохрома GFP можно выявить превращение комплекса GFP-LC3-I в комплекс GFP-LC3-II [37]. Данный метод позволяет оценивать уровень экспрессии и других маркеров аутофагии: Beclin-1 и р62 [16, 19]. Проспективное исследование, включавшее 72 пациента с ревматоидным артритом и 20 доноров (контрольная группа), проведенное в 2018 г. Y. Chen и соавторами [28], выявило статистически достоверное повышение экспрессии LC3-I и LC3-II (р<0,05 и р<0,01 соответственно) и статически значимое снижение экспрессии p62 (р<0,001) в мононуклеарах периферической крови (ПК) больных ревматоидным артритом по сравнению с группой контроля (рис. 1).
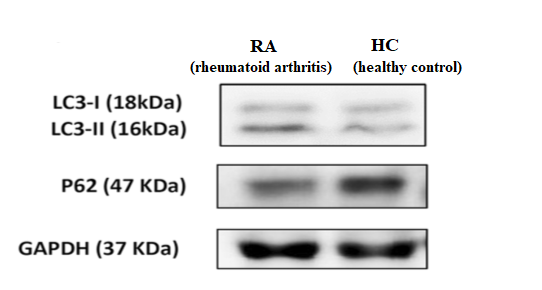
Рис. 1. Пример экспрессии белков LC3-I, LC3-II и p62 в мононуклеарах периферической крови у пациента с ревматоидным артритом (RA – rheumatoid arthritis) и донора (HC – healthy control), определяемой методом вестерн-блоттинга. Уровень экспрессии LC3-I, LC3-II и p62 оценивался относительно уровня экспрессии GAPDН – глицеральдегид-3-фосфатдегидрогеназы, используемой в качестве положительного контроля (Chen Y. et al., 2018 [28])
Мониторинг процесса аутофагии включает анализ конверсии LC3-I в липидированную форму (LC3-II), оценку диссоциации липидированного LC3-II с помощью тандемных красителей (анализ расщепления комплекса GFP-LC3-II) и мониторинг доставки белкового комплекса mRFP-GFP-LC3-II (LC3, конъюгированный с GFP и красным флуорохромом RFP – red fluorescent protein) в лизосому [14, 22].
Измерение активности аутофагического процесса проводится только с использованием тщательно подобранных концентраций индукторов и ингибиторов аутофагии, определяемых в результате серии предварительных экспериментов для установления оптимальных доз используемых препаратов [15]. Результаты регистрируют с помощью метода проточной цитометрии [38, 39].
Для оценки биологических маркеров аутофагии в различных популяциях клеток ПК проводится тщательная подготовка образцов крови, используются реагенты для фиксации и пермеабилизации мембраны клеток, специальные катионные амфифильные индикаторные красители, конъюгированные с флуорохромами, которые специфически распознают аутофагосомы и делают возможной их визуализацию с помощью проточной цитометрии [40]. Например, для количественного определения аутофагосом в циркулирующих клетках ПК применяют индикаторный краситель с коммерческим названием «Cyto-ID» [28, 38]. Исследуемую популяцию клеток окрашивают МКАТ, конъюгированными с флуорохромами, к основным маркерам аутофагии (LC3, Beclin-1, р62) и визуализируют с помощью проточной цитометрии [40, 41]. Полученные данные оценивают по средней интенсивности флуоресценции (MFI – mean fluorescence intensity) красителя «Cyto-ID» или флуорохрома, конъюгированного с МКАТ [38, 40]. В проспективном исследовании, проведенном Y. Chen и соавторами [28], было выявлено статистически достоверное снижение экспрессии p62 (р<0,05) в клетках ПК больных ревматоидным артритом по сравнению с группой контроля (рис. 2).
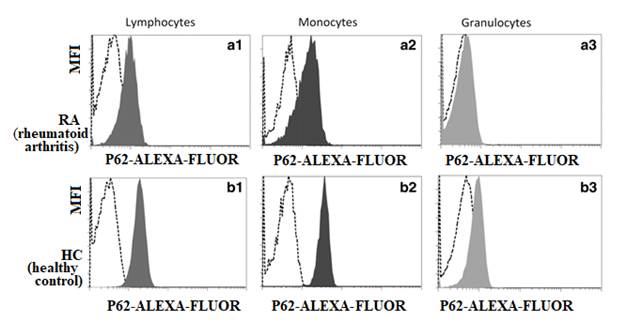
Рис. 2. Цитометрические гистограммы уровня экспрессии белка p62 в популяции лимфоцитов (a1 и b1), моноцитов (a2 и b2) и гранулоцитов (a3 и b3) периферической крови пациента с ревматоидным артритом (RA – rheumatoid arthritis) и донора (HC – healthy control). MFI – средняя интенсивность флуоресценции. На гистограмме клетки, экспрессирующие p62, представлены в виде окрашенных пиков серого и темно-серого цвета, демонстрирующих интенсивную флуоресценцию красителя Alexa-Fluor по сравнению с p62-«негативными» клетками, представленными неокрашенными пиками на гистограммах (Chen Y. et al., 2018 [28])
Согласно проанализированным данным литературы в настоящий момент не существует единого унифицированного метода для исследования биомаркеров аутофагии в клетках ПК с помощью конкретных методов лабораторной диагностики [15]. Новейшие литературные источники содержат рекомендации по усовершенствованию методов исследования аутофагии в ПК [15, 22]. В соответствии с этими рекомендациями при проведении пермеабилизации мембраны клеток для предотвращения преждевременной лизосомальной деградации необходимо использовать унифицированные ингибиторы аутофагии (Бафиломицин А1, хлорохин дифосфат, фолимицин). Для блокирования конечной точки лизосомальной деградации применяется ингибитор аутофагии 3-метиладенин [14]. Для оценки активности процесса аутофагии рекомендовано исследовать экспрессию маркеров аутофагии в клетках ПК методом проточной цитометрии с использованием тандемных флуорохромных красителей. В дополнение к измерению экспрессии белка LC3 рекомендуется определять уровень экспрессии белков p62 или Beclin-1 [15, 25].
Современные подходы к верификации биологических маркеров апоптоза с помощью методов лабораторной диагностики
В критическом обзоре, посвященном анализу современных методов изучения показателей апоптоза в различном биологическом материале, G. Banfalvi [42] приходит к выводу, что «золотым стандартом» среди лабораторных методов по-прежнему остаются исследования раннего и позднего спонтанного и индуцированного апоптоза с помощью определения количества аннексинV+–клеток (аннексин-«позитивные» клетки) и оценки поверхностной экспрессии активной формы эффекторной каспазы-3, осуществляемой методом проточной цитометрии. Однако Z. Xu и соавторы [43] в своем систематическом обзоре, включающем 93 источника литературы, суммируют результаты исследований оптической визуализации апоптоза последних 20 лет и приходят к выводу, что визуализационная проточная цитометрия имеет ряд преимуществ по сравнению с другими методами оценки апоптоза. Недостатком метода является высокая стоимость прибора и реагентов.
Установлено, что снижение мембранного потенциала митохондрий (ΔΨm) служит одним из самых ранних признаков апоптоза, так как оно предшествует транслокации фосфатидилсерина на наружную поверхность мембраны клеток и фрагментации ДНК [34], в связи с чем оценка данного показателя не менее востребована, чем определение количества аннексин-V+-клеток. Среди методов, позволяющих определять изменение ΔΨm, используются флуоресцентная микроскопия или проточная цитометрия с применением таких флуорохромов, как JC-1, CM-x-ROS, DiOC6(3), нонилакридин оранжевый (NAO), сафранин О, родамин-123 (Rh123) [44]. Приведенные выше флуорохромы представляют собой мембранопроницаемые липофильные катионы, обладающие способностью накапливаться в живых клетках и органеллах, обнаруживающих отрицательный мембранный заряд с внутренней стороны мембраны. После накопления в клетках катионные красители проявляют оптическую и флуоресцентную активность, что способствует их широкому применению для оценки состояния ΔΨm [42]. При снижении ΔΨ наблюдается уменьшение интенсивности флуоресценции этих красителей, что позволяет отличить живые неповрежденные клетки от клеток, в которых произошел запуск апоптоза [44].
Новейшие источники литературы свидетельствуют о том, что растворимые маркеры апоптоза, наиболее востребованными из которых в диагностике ОИИ являются белки-антагонисты Bcl-2 и р53, определяются методом иммуноферментного анализа ELISA (enzyme-linked immunosorbent assay) [31, 45] или вестерн-блоттинга [16].
Заключение
Таким образом, проведенный анализ литературы показывает, что биологические маркеры апоптоза и аутофагии, представляющие диагностическую ценность при ОИИ, могут быть определены в периферической крови пациентов с помощью современных высокотехнологичных методов лабораторной диагностики. Согласно результатам последних научных исследований перспективным направлением в современной инсультологии является сравнительная оценка динамики концентрации показателей апоптоза и аутофагии в периферической крови пациентов в остром периоде ишемического инсульта в сопоставлении с динамикой тяжести неврологического дефицита по шкале NIHSS (National Institutes of Health Stroke Scale – шкала инсульта Национального института здоровья) и объемом очага поражения головного мозга по результатам магнитно-резонансной томографии. Возможно, одновременная оценка показателей апоптоза и аутофагии сразу после начала заболевания и в динамике острого периода инсульта поможет созданию новых алгоритмов диагностики, прогноза течения и исхода заболевания.
Библиографическая ссылка
Луговая А.В., Эмануэль В.С., Артемова А.В., Митрейкин В.Ф. СОВРЕМЕННЫЕ ПОДХОДЫ К ОЦЕНКЕ БИОЛОГИЧЕСКИХ МАРКЕРОВ АУТОФАГИИ И АПОПТОЗА ПРИ ОСТРОМ ИШЕМИЧЕСКОМ ИНСУЛЬТЕ // Современные проблемы науки и образования. 2020. № 4. ;URL: https://science-education.ru/en/article/view?id=30017 (дата обращения: 16.05.2026).
DOI: https://doi.org/10.17513/spno.30017



