Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
EFFICACY OF DECOMPRESSION AND STABILIZATION OF TRAUMATIC DEFORMITIES OF THE SPINE USING DORSAL APPROACH IN CHILDREN
Позвоночно-спинномозговая травма (ПСМТ) продолжает оставаться одним из наиболее серьезных повреждений. Тяжесть данного вида травмы обусловлена выраженностью нарушения функции позвоночного столба вследствие возникновения механической нестабильности, а также значимыми неврологическими нарушениями, развивающимися как непосредственно в момент получения травмы, так и в отдаленном периоде. Несмотря на то что в структуре детского травматизма данный вид повреждений наблюдают сравнительно редко (2–3%), частота нестабильных и неврологически осложненных переломов в грудном и поясничном отделах варьирует от 11% до 23% в общей структуре тяжелых повреждений позвоночного столба [1]. Развитие неврологических нарушений в результате ПСМТ обусловлено возникновением вертебро-медуллярного конфликта: сдавлением спинного мозга вентрально расположенными костными отломками тела, дисковым компонентом травмированного позвонка или вследствие дислокации позвонков [2]. Исходя из этого первоочередными задачами хирургического лечения являются ликвидация стеноза позвоночного канала и декомпрессия невральных структур [3]. Тяжелая ПСМТ часто является одним из компонентов сочетанной травмы, что ставит под угрозу жизнь пациента и диктует необходимость выполнения минимального и достаточного объема хирургического вмешательства. В такой ситуации выбор доступа для выполнения декомпрессии и стабилизации является нерешенным вопросом [4]. У пациентов с политравмой выполнение декомпрессии с применением переднего доступа потенциально опасно усугублением их состояния ввиду травматичности доступа, увеличения времени вмешательства и объема кровопотери, а поэтому не всегда осуществимо. Вмешательство, выполняемое из одного дорсального доступа, заключает в себе преимущества в виде возможности достижения декомпрессии и одновременной коррекции и стабилизации травматической деформации [5]. Также, по мнению некоторых авторов, применение дорсального подхода сопровождается меньшей кровопотерей и снижением продолжительности оперативного вмешательства [6]. Стоит отметить, что в ряде работ авторы не продемонстрировали никаких значимых преимуществ одного доступа перед другим [7, 8] и рекомендуют делать выбор, основываясь на персональных предпочтениях и опыте оперирующего хирурга, так как и вентральные доступы, и выполнение декомпрессии из дорсального подхода требуют от оператора навыка и подготовленности. Также необходимо заметить, что вопросы лечения тяжелой позвоночно-спинномозговой травмы у детей освещены сравнительно не полно, вероятно, ввиду редкости данных повреждений в общей структуре детского травматизма.
Таким образом, проблема выбора объема планируемого вмешательства для ликвидации травматического стеноза позвоночного канала у пациентов детского возраста с позвоночно-спинномозговой травмой является актуальной ввиду малочисленности публикаций и разнонаправленности представленных мнений.
Цель исследования: оценка эффективности и безопасности ликвидации стеноза позвоночного канала у пациентов детского возраста с нестабильными повреждениями грудного и поясничного отделов позвоночника с применением дорсального доступа.
Материалы и методы исследования
Настоящая работа является моноцентровым проспективно-ретроспективным когортным исследованием, выполненным в отделении патологии позвоночника и нейрохирургии ФГБУ «НМИЦ детской травматологии и ортопедии им. Г.И. Турнера» Минздрава РФ.
Проспективная часть работы заключалась в отборе 13 пациентов (7 девочек и 6 мальчиков) в возрасте от 13 до 17 лет (средний возраст 16 лет) с позвоночно-спинномозговой травмой за период 2017–2019 гг. с целью проведения оценки результатов обследования и хирургического лечения.
Критериями включения являлись:
– детский возраст (до 18 лет);
– наличие механически нестабильного повреждения грудного и/или поясничного отделов позвоночника;
– отсутствие патологического перелома (на фоне инфекционного/опухолевого процесса);
– наличие стеноза позвоночного канала и компрессии его содержимого фрагментами сломанного позвонка;
– выполнение всего объема вмешательства в одну хирургическую сессию только из дорсального доступа;
– наличие полноценного архива инструментальных исследований;
– срок наблюдения за пациентом не менее 1 года.
Ретроспективно на основании данных проведенных исследований и истории болезни выбранных пациентов оценивали:
– механизм травмы и наличие повреждений других органов и систем;
– уровень неврологического дефицита по шкале ASIA;
– тип повреждения позвоночного столба согласно AOSpine Thoracolumbar Classification System;
– объем кровопотери и длительность выполнения вмешательства;
– необходимость в трансфузии препаратов крови, их вид и объем, а также объем интраоперационной реинфузии крови.
Для ретроспективной характеристики тяжести состояния пациентов исследуемой группы применяли шкалу оценки тяжести повреждений (Injury Severity Score – ISS) и оценивали уровень гемоглобина при поступлении, так как эти параметры имеют важное прогностическое значение [9, 10].
Всем пациентам при поступлении проводили клиническое обследование, включавшее, помимо совместного осмотра травматологом и реаниматологом, неврологический осмотр [11].
Повреждения позвоночного столба классифицировали согласно AOSpine Thoracolumbar Classification System на основании данных рентгенографии позвоночника в двух проекциях в положении лежа, а также данных мультиспиральной компьютерной томографии (МСКТ). Магнитно-резонансную томографию (МРТ) выполняли пациентам с полными взрывными переломами тел позвонков, а также при наличии неврологических нарушений с целью визуализации спинного мозга и оценки его состояния, уточнения характера и степени компрессии.
У всех пациентов, вошедших в данное исследование, были выявлены показания к проведению хирургического лечения в связи с наличием механически и неврологически нестабильной ПСМТ. После проведения предоперационной подготовки приступали к проведению хирургического вмешательства.
Весь объем (декомпрессию, коррекцию и стабилизацию деформации) выполняли в одну хирургическую сессию из дорсального доступа. Проводили скелетирование задних костных структур на уровне поврежденного сегмента и выполняли установку опорных элементов в количестве, достаточном для достижения полноценной репозиции и стабилизации, а также с учетом необходимости перекрытия металлоконструкцией переходных зон с целью профилактики контактного кифозирования. Затем с целью ревизии позвоночного канала выполняли гемиляминэктомию на стороне более выраженной компрессии, а в некоторых случаях фактически завершали ляминэктомию по существующей линии перелома дуги. Доступом через корень дуги позвонка осуществляли подход к позвоночному каналу и ликвидировали стеноз: удаляли фрагменты тела позвонка и/или диска, компримирующие дуральный мешок, выполняли кюретаж смежных дисков в пределах замыкательных пластин выше- и нижележащих позвонков. Переднюю половину тела травмированного позвонка не удаляли, ограничиваясь, по сути, резекцией средней колонны. Целью выполнения данного элемента операции являлась не только ликвидация стеноза, но и достижение необходимой для последующей репозиции мобильности. В ряде случаев на фоне увеличивающейся механической нестабильности укладывали стержень для провизорной фиксации с противоположной стороны (рис. 1А). Критериями достижения адекватной декомпрессии служили расправление дурального мешка и наличие его отчетливой пульсации, а также отсутствие с вентральной стороны позвоночного канала фрагментов поврежденного позвонка и диска. После достижения декомпрессии укладывали стержни в опорные элементы и осуществляли коррекцию и стабилизацию деформации. При наличии разрывов дурального мешка с эвентрацией корешков проводили ушивание твердой мозговой оболочки с погружением корешков внутрь дурального мешка. Завершали вмешательство выполнением спондилодеза аутокостью (рис. 1Б). Мы считаем выполнение данного элемента операции одним из ключевых, обеспечивающих высокие шансы сохранения достигнутой коррекции, выживаемости металлоконструкции и профилактики постляминэктомического кифозирования. В течение проведения вмешательства использовали аппарат для реинфузии крови – благодаря его наличию было возможно довольно точно установить объем интраоперационной кровопотери.
В раннем послеоперационном периоде выполняли контрольные лучевые исследования (рентгенографию в 2 проекциях и МСКТ) для оценки объема выполненной декомпрессии, степени коррекции деформации и корректности положения металлоконструкции.
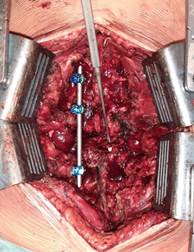
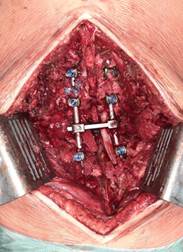
Рис. 1. А – установка провизорного стержня во время выполнения декомпрессии;
Б – завершающий этап дорсального спондилодеза аутотрансплантатом из ребра
В отдаленном периоде (минимум 1 год от проведения вмешательства) оценивали степень неврологического дефицита по шкале ASIA для определения эффективности проведенного лечения (переход из одного класса в другой). Также ретроспективно на основании данных истории болезни оценивали объем кровопотери и длительность выполнения вмешательства, необходимость в трансфузии препаратов крови, их вид и объем, а также объем интраоперационной реинфузии крови.
Результаты исследования и их обсуждение. По механизму полученных повреждений среди пациентов превалировала кататравма (n=10; 77%), у двух (15%) пациентов наблюдали автотравму, один пациент был травмирован проходящим поездом. У 10 пациентов (77%) имели место сочетанные повреждения, такие как: ЗЧМТ (n=7) и закрытые повреждения органов грудной клетки (n=3), живота (n=2) и конечностей (n=4). Полученные данные согласуются с данными литературы о превалировании по механизму получения травмы падений с высоты и ДТП, а также демонстрируют часто наблюдаемые у пациентов с ПСМТ повреждения других органов и систем [12].
Медиана значений по шкале ISS составила 31,5 (min=16, max=57), что характеризует группу пострадавших как тяжело травмированных, угрожаемых пациентов, нуждавшихся в минимизации хирургической агрессии. Уровень гемоглобина при поступлении составил в среднем 116,5 г/л (min=58 г/л, max=160 г/л), при этом 5 (38%) пациентам до поступления в стационар проводили заместительные гемо- и плазмотрансфузии в объеме нескольких доз. Таким образом, на момент выполнения вмешательств на позвоночнике основные угрожающие жизни состояния были ликвидированы, пациенты были частично компенсированы и стабильны, однако выполнение полного объема вмешательства с использованием переднего доступа было рискованным. Вышеуказанные характеристики группы объясняют выбор тактики хирургического лечения, направленной на достижение основной цели вмешательства (ранняя декомпрессия и стабилизация), с использованием минимальной по агрессивности хирургической техники.
По данным проведенного неврологического обследования на момент поступления у 5 (38,5%) пациентов уровень неврологического дефицита соответствовал типу А – в отдаленном периоде только у одного ребенка наблюдали регресс симптоматики до типа С; у трех (23%) пациентов – типу В: у одного пациента наблюдали полное восстановление (тип Е); у 3 (23%) – типу С (полное восстановление в двух случаях), двое детей (15,5%) не имели неврологических нарушений. К сожалению, лишь у малой части пациентов отмечалось улучшение неврологического статуса после проведения хирургического вмешательства. Мы предполагаем, что это может быть связано как с исходно тяжелым повреждением спинного мозга в результате прямого удара костными фрагментами, так и со временем, прошедшим с момента получения травмы: все пациенты до проведения вмешательства на позвоночнике нуждались в ликвидации иных угрожающих жизни состояний, что и объясняет длительность поступления в наше специализированное отделение.
По виду повреждения позвоночного столба пациенты распределились следующим образом: у 6 (46%) наблюдали повреждения типа С, у 7 (53%) – перелом типа А4, при этом у одного пациента имело место сгибательно-дистракционное повреждение типа В2 в сочетании с полным взрывным переломом тела типа А4. До проведения вмешательства у всех пациентов стеноз позвоночного канала составлял не менее 50% его диаметра (табл. 1).
Таблица 1
Характеристика пациентов исследуемой группы
|
№ |
Возраст |
Тип по АО |
Вид травмы |
ASIA до |
ASIA после |
Объем кровопотери |
Время операции |
Hb |
ISS |
|
1 |
15 |
С |
ката |
E |
E |
700 |
150 |
76 |
57 |
|
2 |
16 |
С |
ката |
A |
A |
1200 |
145 |
116 |
21 |
|
3 |
14 |
В2 (А4) |
ката |
E |
E |
1200 |
165 |
123 |
16 |
|
4 |
15 |
А4 |
ката |
B |
E |
600 |
250 |
138 |
57 |
|
5 |
16 |
С |
авто |
A |
A |
1300 |
235 |
117 |
34 |
|
6* |
17 |
С |
ката |
A |
A |
||||
|
7 |
17 |
А4 |
ката |
B |
В |
2500 |
300 |
143 |
29 |
|
8 |
14 |
С |
ката |
B |
В |
500 |
170 |
111 |
16 |
|
9 |
17 |
А4 |
авто |
C |
E |
2500 |
220 |
160 |
18 |
|
10 |
17 |
С |
ж/д |
A |
A |
500 |
230 |
78 |
34 |
|
11 |
13 |
А4 |
ката |
A |
C |
1300 |
330 |
104 |
50 |
|
12 |
16 |
А4 |
ката |
C |
С |
700 |
180 |
58 |
57 |
|
13 |
15 |
А4 |
ката |
C |
E |
2100 |
280 |
141 |
19 |
|
Med |
16 |
1200 |
225 |
116,5 |
31,5 |
* Пациент № 6 оперирован в ином лечебном учреждении выездной бригадой – некоторые данные недоступны
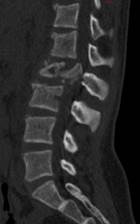
По результатам выполненной в раннем послеоперационном периоде МСКТ у всех пациентов достигнута полная декомпрессия позвоночного канала с восстановлением его формы и размеров, а также стабилизацией травмированного сегмента (рис. 2). Таким образом, все задачи оперативного вмешательства: ликвидация стеноза, коррекция деформации и фиксация позвоночного столба у пациентов с абсолютно нестабильными повреждениями – достижимы при использовании дорсального доступа.
 А
А 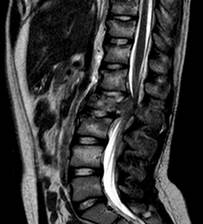 Б
Б 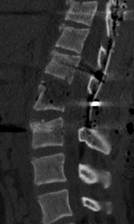 В
В
Рис. 2. Пациент К., 14 лет. Кататравма. А, Б – повреждение типа В2(А4) с тотальным стенозом позвоночного канала. Тип А по ASIA. В – достигнута полная декомпрессия в зоне повреждения. В дальнейшем наблюдали восстановление до типа С по ASIA
В течение всего периода наблюдения за пациентами мы не отметили случаев дестабилизации металлоконструкции, несмотря на то, что вентральная поддержка на уровне резецированной средней колонны не была воссоздана во время операции. Мы связываем это с тем, что передняя колонна позвоночника оставалась частично сохранной, а также с тем, что у всех пациентов выполняли этап дорсального спондилодеза, являвшийся наряду со стабильной металлофиксацией одним из условий восстановления заднего опорного комплекса.
Средняя длительность проведения оперативного вмешательства составила 225 минут (min=45 минут, max=330 минут), а объем интраоперационной кровопотери варьировал от 500 мл до 2500 мл, составив в среднем 1200 мл. Аппаратную реинфузию крови проводили 8 (62%) пациентам – ее объем составил 590 мл (min=10 мл, max=2000 мл). Объем периоперационной трансфузии эритроцитарной массы, в которой нуждались 6 (46%) пациентов, составил в среднем 950 мл (min=300 мл, max=2900 мл). Трансфузию свежезамороженной плазмы получили 10 (77%) пациентов: в среднем 600 мл (min=300 мл, max=1500 мл). Одному ребенку потребовалась трансфузия тромбовзвеси в объеме 600 мл – данный пациент поступил в стационар с уровнем гемоглобина 58 г/л и оценкой по шкале ISS 57 баллов. Эти данные характеризуют проведенные вмешательства как сравнительно травматичные и длительные, требующие присутствия подготовленного персонала, специальных технических средств (аппарата для реинфузии) и запаса компонентов крови. Ни у одного пациента не было отмечено влияние кровопотери на декомпенсацию витальных функций в ходе выполнения вмешательства или в раннем послеоперационном периоде.
Из осложнений стоит отметить эпизод ТЭЛА у пациента 16 лет с переломовывихом в Th7-Th8 и полной нижней параплегией, развившийся, несмотря на проведение всего комплекса тромбопрофилактики, в раннем послеоперационном периоде. Пациент получал консервативное лечение с хорошим исходом. Технически данная ситуация не связана с фактом выполнения оперативного вмешательства, но она характеризует тяжесть состояния пациентов данной группы и сложность их лечения. У одного ребенка в течение 3 месяцев развилась раневая инфекция, потребовавшая проведения хирургической санации и применения VAC-терапии, в результате чего процесс был купирован, металлоконструкция сохранена.
Мы осознаем, что существенным недостатком данного исследования является отсутствие контрольной группы пациентов, на примере которой было бы возможно сравнить аналогичные параметры (время вмешательства, объем кровопотери), но, как было сказано ранее, данные повреждения сравнительно редки, а состояние пациентов, как правило, тяжелое, что исключает возможность рандомизации по этическим соображениям.
Заключение
Результаты проведенной работы демонстрируют эффективность ликвидации травматического стеноза позвоночного канала только из дорсального доступа у пациентов с ПСМТ в структуре сочетанных повреждений. Выбранный метод декомпрессии и стабилизации позволил не только добиться адекватного восстановления размеров и формы позвоночного канала согласно данным контрольных лучевых исследований, но и создать условия для улучшения неврологического статуса у части пациентов.
К сожалению, подобным вмешательствам присуща сравнительно большая кровопотеря в связи с тем, что источниками кровотечения служат губчатая кость тела позвонка и сосуды эпидуральной клетчатки, которые с трудом поддаются контролю до завершения всех этапов операции. Поэтому необходимо располагать значительным запасом компонентов крови, а также владеть технологиями кровесбережения.
Таким образом, применение дорсального доступа для ликвидации стеноза позвоночного канала в условиях специализированного отделения у пациентов детского возраста с ПСМТ эффективно и целесообразно с позиций уменьшения хирургической агрессии и предотвращения усугубления состояния пострадавшего.
Библиографическая ссылка
Хусаинов Н.О., Виссарионов С.В., Белянчиков С.М., Кокушин Д.Н. ЭФФЕКТИВНОСТЬ ВЫПОЛНЕНИЯ ДЕКОМПРЕССИИ И СТАБИЛИЗАЦИИ ТРАВМАТИЧЕСКИХ ДЕФОРМАЦИЙ ПОЗВОНОЧНИКА У ДЕТЕЙ ИЗ ДОРСАЛЬНОГО ДОСТУПА // Современные проблемы науки и образования. 2020. № 3. ;URL: https://science-education.ru/en/article/view?id=29802 (дата обращения: 01.05.2026).
DOI: https://doi.org/10.17513/spno.29802



