Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
EFFICACY OF SWITCHING ANTI VASCULAR ENDOTHELIAL GROWTH (A-VEGF) TO AFLIBERCEPT IN WET AGE-RELATED MACULAR DEGENERATION (AMD) TREATMENT WITH RANIBIZUMAB RESISTANCE
Согласно исследованиям ВОЗ возрастная макулярная дистрофия сетчатки (ВМД) – наиболее часто встречающаяся причина потери центрального зрения у пациентов в возрасте от 55 лет. Более 45 млн человек в мире на сегодняшний день имеют возрастную макулодистрофию. Среди причин потери центрального зрения и инвалидности по зрению первое место принадлежит ВМД – как в РФ, так и в США, странах Европы и Юго-Восточной Азии [1, 2]. В этиологии ВМД ключевая роль отводится генетическому фактору и экологии. Тяжесть заболевания обусловлена тем, что процесс локализуется в центральной зоне сетчатки и чаще всего поражает оба глаза [1]. Различают три стадии развития ВМД – сухую, влажную и рубцовую. Возрастная макулодистрофия начинает развиваться с формирования сухой стадии, которая со временем превращается в наиболее активную и быстротечную влажную (экссудативную) стадию с формированием субретинальной неоваскуляризации. Итогом прогрессирования заболевания становится формирование хориоретинального рубца с необратимой потерей центрального зрения. Доступные источники литературы утверждают: 10–20% пациентов с сухой стадией ВМД со временем заболевают влажной [1–3]. Фактор роста эндотелия сосудов – VEGF (Vascular endothelial growth factor) – главный регулятор физиологического ангиогенеза, это пусковая молекула в патогенезе формирования хориоидальных новообразованных сосудов (ХНВ) [4–6]. При развитии ишемии макулярной зоны увеличение концентрации VEGF в стекловидном теле вызывает аномальный рост новых неполноценных сосудов в слое хориокапилляров центральной зоны сетчатки, что приводит к разрушению пигментного эпителия, скоплению жидкости под нейроэпителием и отеку макулярной сетчатки. В исходе «влажного» процесса формируются хориоретинальные рубцы с потерей центрального зрения [1, 7, 8]. В клинической практике наиболее положительный терапевтический эффект дает воздействие на пусковой фактор развития ХНВ, а именно ингибирование VEGF [9–11]. Современная научная литература утверждает, что в терапии глазных болезней, протекающих с хориоидальной неоваскуляризацией, на сегодняшний день лидирует антиангиогенная фармакотерапия. Она представляет собой введение анти-VEGF препаратов в стекловидное тело [10–12]. В РФ зарегистрированы для интравитреального введения 2 фармпрепарата, блокирующих рецепторы VEGF: ранибизумаб [Ranibizumab] (Луцентис) и афлиберцепт [Afibercept] (Эйлеа). Действие препаратов сопровождается регрессией неоваскулярных сосудов. Ранибизумаб является антигенсвязывающим фрагментом мышиного антитела к VEGF. Молекула ранибизумаба – высокоспецифичная часть антитела к VEGF. Низкий молекулярный вес препарата (48 кД) обеспечивает лучшее проникновение через ретинальные слои для взаимодействия с рецепторами VEGF новообразованных сосудов. Афлиберцепт зарегистрирован в РФ в 2016 г. Препарат является рекомбинантным белком, состоящим из частей человеческих рецепторов VEGF1 и F2 – внеклеточных доменов, связанных с Fc-фрагментом человеческого IgG1. Афлиберцепт приготовлен в виде изоосмотического раствора для интравитреального введения (ИВВ), он действует как растворимый рецептор-приманка, который связывает VEGF и плацентарный фактор роста – PIGF (Placenta Growth Factor) [11]. Препарат блокирует связывание ангиогенных молекул с нативными рецепторами, подавляя активность последних. Молекула ранибизумаба имеет только один домен, но, несмотря на единственный связывающий участок, обладает высоким сродством к VEGF. Период полураспада ранибизумаба составляет 28–30 дней. На основании этого срока формируются интервалы между ИВВ препарата. Ежемесячные ИВВ ранибизумаба останавливают рост сосудов в 90% случаев ВМД. У 30–40% пациентов при этом улучшается зрение.
Афлиберцепт – это димерный гликопротеин с белком молекулярной массой 97 кД. Период полувыведения из стекловидного тела ранибизумаба и афлиберцепта составляет 3,2 и 4,8 дня соответственно. Прогнозируемая интравитреальная биологическая активность 0,5 мг ранибизумаба через 30 дней схожа с прогнозируемой активностью 1,15 мг афлиберцепта через 79 дней после интравитреального ведения. Учитывая хронический характер заболевания, ВМД требует регулярного лечения в виде применения систематических ИВВ A-VEGF препаратов, что накладывает существенное материальное бремя на пациента и фонды бюджетного финансирования. В связи с этим особую актуальность приобретают способы удлинения периодов ремиссии влажной ВМД, приводящие к сокращению количества ИВВ. Известно, что после многократных, более 15, инъекций ранибизумаба в терапии влажной формы ВМД у части пациентов отмечается снижение чувствительности к вводимому препарату, вплоть до полного отсутствия клинической реакции на проводимое ИВВ [13–15]. В доступной научной литературе есть сообщения об эффективности лечения пациентов с влажной ВМД переключением антиангиогенной терапии на афлиберцепт [15–17].
Цель: анализ анатомических и функциональных результатов переключения A-VEGF терапии на афлиберцепт у пациентов, больных влажной ВМД с макулярными отеками, устойчивыми к ранибизумабу, после многократных ИВВ. Сравнение продолжительности временного интервала с отсутствием экссудативной активности хориоидальной неоваскуляризации после применения ранибизумаба и афлиберцепта у данной группы пациентов.
Материалы и методы исследования. Выполнен ретроспективный анализ результатов лечения пациентов с влажной формой ВМД, получивших в качестве антиангиогенной терапии более 15 ИВВ ранибизумаба. Две исследуемые группы составили 18 пациентов (глаз) в возрасте от 52 до 84 лет – 11 женщин и 7 мужчин. Средний возраст 65±5 лет. Все пациенты исследуемых групп на фоне лечения ранибизумабом показывали выраженную положительную динамику как в фазе загрузочных инъекций, так и в период дальнейшего лечения. У всех пролеченных пациентов регистрировались рецидивы влажной формы заболевания в виде снижения остроты зрения и скопления интра- и субретинальной жидкости. В последний год наблюдалось отсутствие прилегания отслойки нейроэпителия в макулярной зоне даже при ежемесячных введениях ранибизумаба, визометрия регистрировала снижение остроты зрения. У 10 пациентов первой группы были выполнены ежемесячные загрузочные ИВВ афлиберцепта [6], у 8 пациентов второй – контрольной – группы продолжалась терапия ранибизумабом. Для оценки динамики патологического процесса и эффективности проводимого лечения все пациенты были обследованы с применением следующих методов офтальмологической диагностики: ежемесячная визометрия с коррекцией, офтальмоскопия, фоторегистрация глазного дна, спектральная ОКТ макулярной зоны обоих глаз и периметрия центральной зоны сетчатки. Для ОКТ сканирования использовался аппарат SOCT CIRRUS HD (Carl Zeiss) с разрешающей способностью 5 мкм3. ОКТ-ангиография макулярной зоны пациентов в процессе A-VEGF терапии позволяет оценить динамику площади неоваскулярного комплекса, плотность и толщину новообразованных сосудов, разветвленность и перфузируемость субретинальной неоваскулярной мембраны. Эти параметры дают возможность дифференцировать типы ХНВ при ВМД [18]. Пациентам проводилась периметрия центральной зоны сетчатки по программе macula10 и macula30 на периметре OCULUS-TWINFIELD (OKULUS). При диагностике различных форм ВМД возможна не только регистрация морфологических структурных повреждений макулы, но и исследование функционального состояния центральной зоны сетчатки с помощью микропериметрии. Начальные стадии ВМД сопровождаются умеренными изменениями данных микропериметрии. При влажной форме ВМД отмечаются значительные нарушения светочувствительности макулярной зоны [19, 20]. Интервалы между обследованиями у пациентов исследуемых групп составляли 1 месяц после каждого ИВВ, также проводился комплекс исследований перед началом лечения. ИВВ осуществлялись стандартным методом в стерильной операционной, в соответствии с инструкцией по медицинскому применению лекарственного средства. В клинической практике ОКТ-ангиография (ОКТА) и микропериметрия не являются решающими для оценки эффективности лечения и дальнейшего планирования повторных ИВВ [18–20]. Ввиду этого в комплекс методов обследования пациентов с влажной ВМД, получающих переключение A-VEGF терапии, ОКТА и микропериметрия не были нами включены.
Статистическая обработка данных проводилась в программе Excel (описательная статистика, критерий Стьюдента).
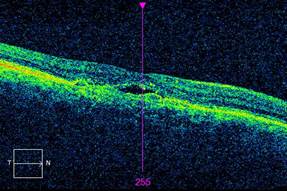
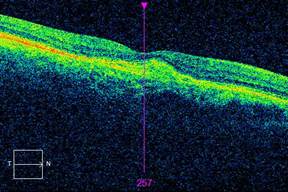
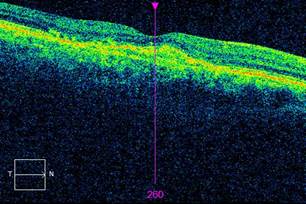
Результаты исследования и обсуждение. Исследуемые группы были сопоставимы по полу, возрасту и сопутствующей патологии. Все пациенты при первом обращении предъявляли жалобы на снижение зрения. Регистрировались наличие интра- и субретинальной жидкости, а также элевация пигментного эпителия по данным ОКТ (рис. 1). В соответствии с инструкцией по применению препарата ранибизумаб всем пациентам в исследуемых группах проводились загрузочные ИВВ с интервалом в 1 месяц. После загрузочных 3 ежемесячных ИВВ ранибизумаба у всех 18 пациентов ретроспективно регистрировалась положительная динамика по данным ОКТ (рис. 2) и остроте зрения. До лечения офтальмоскопировались диффузный ретинальный отек, локальные дефекты и элевации пигментного эпителия в макуле. СОКТ определяла интраретинальный отек, отслойку нейроэпителия, элевацию и дезагрегацию пигментного эпителия. После 3 ИВВ ранибизумаба офтальмоскопически визуализировались полное прилегание пигментного эпителия и отсутствие субретинальной жидкости (СРЖ). На сканах ОКТ регистрировались восстановление фовеального профиля макулярной зоны, резорбция интраретинальной и субретинальной жидкости.
|
|
|
|
Рис. 1. ОКТ при первичном обращении |
Рис. 2. ОКТ после 3-й ИВВ ранибизумаба |
Динамика толщины сетчатки в макулярной зоне представлена в таблице 1. При первичном обращении пациенты предъявляли жалобы на снижение остроты зрения и центральное «пятно» перед глазом. Особенный дискомфорт доставляли пациентам искажения в центральном зрении – метаморфопсии, сопровождающие все наблюдаемые случаи. В ходе лечения после каждой ИВВ ранибизумаба субъективно пациенты отмечали улучшение зрения, вплоть до полного восстановления после 3 загрузочных ежемесячных ИВВ.
Таблица 1
ОКТ динамика изменений толщины сетчатки макулярной зоны в ходе A-VEGF терапии
|
Период обследования |
Толщина сетчатки в макулярной зоне (мкм) |
|
|
Группа 1 (10 глаз), M±σ |
Группа 2 (8 глаз), M±σ |
|
|
До начала лечения |
339,8 ± 40,7 |
316,2±31,7 |
|
После 3-й ИВВ ранибизумаба |
241,5±12,0 |
249,7±13,0 |
|
После 15-й ИВВ ранибизумаба |
342,9±44,6 |
309,0±18,7 |
|
По окончании лечения |
После загрузочных ИВВ афлиберцепта 238,8±18,0** |
После 20-й ИВВ ранибизумаба 301,3±19,0* |
Примечание: статистическая значимость различий: * – р<0,05 (с группой 1); ** – р<0,05 (с данными до терапии)
Изменения максимальной корригируемой остроты зрения (МКОЗ) представлены в таблице 2.
Таблица 2
Динамика изменений максимально корригируемой остроты зрения (МКОЗ) у больных в течение A-VEGF терапии
|
Период обследования |
МКОЗ |
|
|
Группа 1 (10 глаз), M±σ |
Группа 2 (8 глаз), M±σ |
|
|
До лечения |
0,45±0,06 |
0,44±0,1 |
|
После загрузочных ИВВ ранибизумаба |
0,75±0,1 |
0,72±0,1 |
|
После 15-й ИВВ ранибизумаба |
0.44±0,1 |
0,41±0,09 |
|
По окончании лечения |
После загрузочных ИВВ афлиберцепта 0,71±0,01** |
После 20-й ИВВ ранибизумаба 0,38±0,07* |
Примечание: статистическая значимость различий: * – р<0,05 (с группой 1); ** – р<0,05 (с данными до лечения)
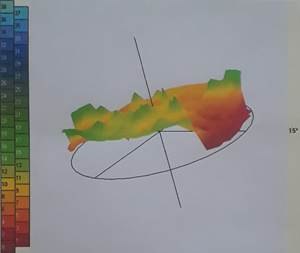
Компьютерная микропериметрии макулярной зоны у всех пациентов регистрировала снижение световой чувствительности в среднем на 10 dB (рис. 3.а,б).
|
|
|
|
Рис. 3а. Данные центральной микропериметрии пациента Н. |
Рис. 3б. 3D график центральной микропериметрии пациента Н. |
Изменения световой чувствительности на фоне А-VEGF терапии колебались в среднем на 2 dB, что не являлось статистически значимым критерием для оценки результатов лечения и планирования дальнейшей тактики.
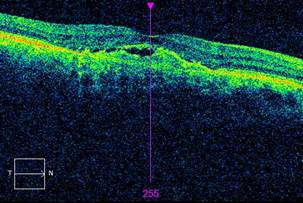
Анализ показателей клинического течения заболевания в части ретроспективного исследования выявил среднюю продолжительность подавления активности ХНВ 98±10 дней. Планирование последующих ИВВ ранибизумаба у каждого пациента проводилось индивидуально. ИВВ повторялись в сроки 3–4 месяца по результатам контрольных ОКТ при появлении СРЖ. Поддерживающий режим у пациентов исследуемых групп составил 3–5 инъекций ранибизумаба в год. За 3 года A-VEGF терапии ранибизумабом пациенты исследуемой группы получили в среднем 21(±3) ИВВ. Результаты динамического ОКТ и визометрического наблюдения регистрировали значительное снижение анатомического и функционального ответа сетчатки на ИВВ ранибизумаба. Даже при ежемесячных инъекциях отмечалась незначительная резорбция СРЖ (табл. 1, рис. 4), отсутствовало улучшение остроты зрения субъективно и по данным визометрии (табл. 2) у всех пациентов в исследуемых группах.
Терапия афлиберцептом согласно инструкции предписывает проведение ИВВ 1 раз в 2 месяца после выполнения трех ежемесячных загрузочных инъекций на первом году терапии. В проспективной части исследования всем пациентам 1-й исследуемой группы выполнено ИВВ афлиберцепта 2 мг. У 7 из 10 пациентов через 1 месяц после первой инъекции регистрировалась полная резорбция СРЖ с прилеганием нейро- и пигментного эпителия (рис. 5). Двум пациентам первой группы для достижения полной анатомической стабилизации проводилось повторное ИВВ афлиберцепта. Одному пациенту были выполнены три ежемесячных ИВВ афлиберцепта, после которых СРЖ не регистрировалась. Толщина сетчатки в макуле составила в среднем 238,3±18 мкм. Максимальная корригируемая острота зрения у всех пациентов (10 глаз) после загрузочных введений афлиберцепта достоверно улучшилась по данным визометрии с 0,45±0,06 до 0,71±0,01, р<0,05 (табл. 2). Субъективно все пациенты отмечали улучшение качества и контрастности центрального зрения.
Пациентам 2-й контрольной группы продолжали выполнять ежемесячные ИВВ ранибизумаба. У всех пациентов отсутствовала полная резорбция СРЖ, сохранялась отслойка нейро- и пигментного эпителия. Толщина сетчатки в макуле составила в среднем 301,3±19 мкм по сравнению с 238,8±18,0 в 1-й группе, р<0,05, где произошло купирование макулярного отека. Корригируемая острота зрения у всех 8 пациентов в ходе терапии по данным визометрии несколько снизилась. Субъективно пациенты контрольной группы не отмечали улучшения остроты и контрастности центрального зрения.
При оценке продолжительности подавления экссудативной активности в макуле отслеживались сроки возобновления отека и отслойки нейроэпителия на ежемесячных ОКТ. Длительность ремиссии при применении афлиберцепта составила в среднем 2,1±0,2 месяца. Терапия ранибизумабом пациентов 2-й группы сопровождалась 4-недельными периодами снижения экссудативной активности с последующим усилением макулярного отека.
Установленная нами продолжительность подавления «влажного» процесса в макуле на срок более 2 месяцев указывает на возможность увеличения временных промежутков между введениями афлиберцепта, сопоставимого с результатами Queguiner F (2020) [17], показавшим, что «переключение с ранибизумаба на афлиберцепт у “неоптимальных” пациентов значительно снижается количество последующих визитов и ИВВ, при сопоставимой эффективности».
|
|
|
|
Рис. 4. ОКТ после 20-й ИВВ ранибизумаба |
Рис. 5. ОКТ после 3-й ИВВ афлиберцепта |
Анализ полученных в ходе ретроспективного исследования результатов подтверждает эффективность резорбции экссудативного содержимого в макуле при первичном применении в качестве средства лечения ранибизумаба. Однако далее нами установлено, что после многократных (более 15) ИВВ ранибизумаба у пациентов с влажной формой ВМД развивается резистентность ретинального отека к ранибизумабу, вплоть до полной устойчивости терапии, что согласуется с данными других исследователей [13, 14, 17]. При переключении A-VEGF фармакотерапии таким пациентам на афлиберцепт уже после загрузочных инъекций отмечается выраженная положительная динамика, сопровождающаяся купированием отека в макулярной зоне, что подтверждается данными СОКТ и визометрии.
Заключение. ИВВ афлиберцепта эффективно купируют экссудативный процесс в макулярной зоне пациентам с влажной формой ВМД в случае развития резистентности к действию ранибизумаба после предшествующих многократных ИВВ. Переключение ранибизумаба на афлиберцепт оптимально в клинической работе.
Результаты динамического наблюдения после загрузочных инъекций афлиберцепта подтвердили увеличение (2,1±0,2 месяца) периодов подавления активности ХНВ, что позволяет облегчить бремя лечения пациента. Продолжение терапии ранибизумабом сопровождалось 4-недельными периодами снижения экссудативной активности с последующим усилением макулярного отека.
Библиографическая ссылка
Козина Е.В., Сахнов С.Н., Заболотний А.Г., Мясникова В.В., Быкова Е.В. ЭФФЕКТИВНОСТЬ ПЕРЕКЛЮЧЕНИЯ ANTI VASCULAR ENDOTHELIAL GROWTH FACTOR (A-VEGF) ТЕРАПИИ ВЛАЖНОЙ ВОЗРАСТНОЙ МАКУЛОДИСТРОФИИ (ВМД) НА АФЛИБЕРЦЕПТ ПРИ РЕЗИСТЕНТНОСТИ К РАНИБИЗУМАБУ // Современные проблемы науки и образования. 2020. № 2. ;URL: https://science-education.ru/en/article/view?id=29671 (дата обращения: 11.06.2026).
DOI: https://doi.org/10.17513/spno.29671