Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
RESEARCH OF THE INDICATORS OF BIOSOCOMPATIBILITY OF A NEW SAMPLE OF HERNIOENDOPROTHESIS WHEN TOGETHER USE WITH DEPROTEINIZED DIALYSIS FROM BLOOD OF DAIRY CALVES
Вопрос послеоперационных вентральных грыж традиционно актуален для современной хирургической практики: проблема их эффективного лечения все еще актуальна. Также не разрешена проблема подбора экономически целесообразной методики лечения вентральных грыж [1; 2]. Существует более чем 150 способов пластики грыжевых дефектов, но даже такое количество методов не гарантирует отсутствие рецидивов, возникающих в 13-35% случаев [3].
Послеоперационные вентральные грыжи в структуре грыж передней брюшной стенки находятся на втором месте после паховых грыж. Возникновение их наблюдается примерно в 8-16% случаев после осуществления лапаротомных операций, проводимых по поводу иных патологий в брюшной полости. Большое количество клинических исследований, осуществленных за последние пятнадцать лет, обозначают количество послеоперационных вентральных грыж в пределах от 53 до 79% от общего количества вентральных грыж. Причиной этого является не только увеличение общего количества хирургических вмешательств на органах брюшной полости, но и увеличение количества работ, посвященных системному анализу всех имеющихся сведений [4; 5].
Так как материал, из которого изготавливаются герниоэндопротезы, является чужеродным для организма, то в зоне имплантации возникает локальное асептическое воспаление, препятствующее процессу нормального заживления послеоперационной раны и надежной фиксации импланта [6].
Несмотря на использование материалов, применение которых раньше в хирургии не представлялось возможным, исходы лечения грыж передней брюшной стенки сложно назвать удовлетворительными. Значительность воспалительных явлений в области грыжевых ворот выражается в результатах, которые не дают нам право называть аутопластику эффективным методом лечения данной патологии [4; 7; 8].
Первоначально введенные в хирургическую практику искусственные материалы вызывали чрезмерный иммунный ответ, что, по всей видимости, можно объяснить неудовлетворительными характеристиками самого материала, служившего основой эндопротеза, и одновременно отсутствием технической и теоретической баз выполнения операций с использованием имплантов [2; 5]. Хотя отрицательные результаты способствовали некоторому затиханию интереса научного сообщества к такого рода способу решения проблемы, исследования не были прекращены, и с момента первого применения герниоэндопротезы претерпели значительные изменения. Производители имплантов с учетом клинической практики совершенствуют имеющиеся эндопротезы, улучшая их характеристики и свойства [2; 8]. Имплант нового поколения представлен разработкой компании Covidien – эндопротез Parietene ProGrip. Он представляет собой полурассасывающийся, самофиксирующийся герниоэндопротез с размером пор, обеспечивающим оптимальное прорастание его соединительной тканью [7; 9; 10].
Концепция нарушения синтеза коллагена является базовой в современном представлении научного сообщества о грыжеобразовании. Диспропорция между коллагеном I и III типов является причиной ухудшения прочностных характеристик брюшной стенки, что негативно сказывается на ее механической функции [5; 6; 8].
Таким образом, конечного результата, удовлетворяющего потребностям современной абдоминальной хирургии, до сих пор не получено. Поиск способов превентивного лечения грыж передней брюшной стенки, а также разработка эффективного герниоэндопротеза для этих целей остаются актуальными целями [2]. Параллельно с этим существует задача поиска лекарственного препарата, имеющего способность к уменьшению экссудативных проявлений и ускорению наступления пролиферативной фазы воспалительной реакции в месте имплантации герниоэндопротеза для ускорения регенерации и улучшения качества прочности соединительной ткани; изучения и внедрения способа коррекции коллагенообразования, необходимого для стимуляции образования зрелого соединительного волокна [11; 12]. Решение перечисленных вопросов даст возможность снизить количество рецидивов и улучшить прогноз лечения вентральных грыж.
Целью данного исследования являлась оценка гистологических изменений в зоне имплантации герниоэндопротеза «Эсфил» с обработкой препаратом «Солкосерил».
Материал и методы исследования. Экспериментальная часть исследования выполнялась на 80 мышах мужского пола линии Vistar (по 40 мышей в каждой группе) средним весом 30 граммов. Исключение самок было необходимо для предотвращения беременности и исключения возможной разницы в гормональном фоне.
В эксперименте проводилась имплантация герниоэндопротеза «Эсфил», разработанного совместно с фирмой ООО «Линтекс» (г. Санкт-Петербург), при этом производилось деление на группы:
группа № 1 – без использования препарата «Солкосерил» (контрольная группа);
группа № 2 – с использованием препарата «Солкосерил».
«Эсфил» – сетка-эндопротез, предназначенная для укрепления мягких тканей, испытывающих максимальную нагрузку, при оперативном лечении грыж различных локализаций, после удаления опухолей, при повреждениях грудной стенки и в других областях пластической хирургии. Имплантированные эндопротезы-сетки служат каркасом для прорастания тканей и придают им дополнительную прочность во время и после заживления.
«Солкосерил» – препарат, представляющий собой депротеинизированный гемодиализат, содержащий широкий спектр низкомолекулярных компонентов клеточной массы и сыворотки крови молочных телят с молекулярной массой 5000 D, изготовленный компанией MEDA Pharmaceuticals Switzerland GmbH (Швейцария).
Эксперимент осуществлялся на базе НИИ экологической медицины ФГБОУ ВО «Курский государственный медицинский университет» в операционной лабораторного блока. Экспериментальное исследование на лабораторных животных проводилось в полном соответствии с Конвенцией Совета Европы от 1986 г. (Страсбург). Помимо этого выполнялись все Директивы Совета 86/609/ЕЕС от 24.11.86. по согласованию законов, правил и административных распоряжений стран–участниц в отношении защиты животных, применяемых в экспериментальных исследованиях.
Крысам по переднебоковой поверхности производился разрез кожи длиной 15 мм, после чего при помощи сосудистого зажима производилось разделение кожи и подкожно-жировой клетчатки от нижележащих мышц передней брюшной стенки. В образовавшемся пространстве размещали имплант размерами 10*5 мм, без его фиксации, таким образом, чтобы его края не попадали в рану. Это условие было необходимо для предупреждения повреждения импланта животными. Имплантация осуществлялась исследователями таким образом с целью моделирования пластики по методике on-lay. После имплантации рана ушивалась тремя или четырьмя узловыми швами (шовный материал – крученая капроновая нить). Животным интраоперационно 50%-ным раствором депротеинизированного гемодиализата обрабатывался имплант, а также область вокруг протеза. После этого раствор вводился интраперитонеально по 0.1 мл с помощью инсулинового шприца. Введение препарата производилось в течение 90 дней один раз в двое суток. Животные выводились из эксперимента на 10, 30, 60 и 90-е сутки. На указанных сроках после передозировки эфирного наркоза выполнялось иссечение тканей передней брюшной стенки, вместе с мышцами и имплантом. Полученный фрагмент размерами 15*15 мм помещали в емкость с 10%-ным раствором формалина. Данный материал заключали в парафиновые блоки, из которых получали срезы толщиной 4-5 мкм. Для определения характера и количества клеточных элементов применялась окраска гематоксилин-эозином.
Для выяснения микроструктурных характеристик нами был использован микроскоп «Альтами ПОЛАР 2» (ООО «Альтами», Российская Федерация, г. Санкт-Петербург), увеличение объективов которого составляло х25 и х40; увеличение окуляра х10. Окуляр имел вставку размерами 1*1 мм, ограничивающую поле зрения. Микрофотографии были получены с помощью цифровой окулярной камеры Altami USB 3150R6 1/2CMOS (CMOS матрица 3 Мпикс). При исследовании гистологических срезов в каждом изучали 10 «стандартных полей зрения». На каждом этапе выводили от 6 до 7 экспериментальных животных. Это было необходимо для получения статистически достоверных (p<0,05) результатов исследования. Для установления точного клеточного состава ткани в околопротезной капсуле подсчитывали следующие клетки: макрофагов, фибробластов, нейтрофилов и лимфоцитов. Изучение данных клеточных элементов и выражение их количества в относительных единицах давали возможность определить тип и фазу воспалительного процесса, его интенсивность, что позволяет судить о биосовместимости конкретного импланта, а также влиянии на этот процесс добавляемого лекарственного вещества. В качестве программной среды для обработки статистических данных использовали программы Statistica (версия 6.0) и Biostatistics (версия 4.03), с помощью которых производился подсчет среднего арифметического числа и среднеквадратичного отклонения.
Результаты исследования и их обсуждение. Характеристика клеточного состава в области расположения импланта из группы № 1 представлена в таблице 1.
Таблица 1
Клеточный состав области расположения герниоэндопротеза из группы № 1
|
Клетки (%) Сутки |
Фибробласты |
Макрофаги |
Лимфоциты |
Нейтрофилы |
|
10 |
63,1±1,15 |
6,0±0,59 |
18,0±1,08 |
20,4±0,61 |
|
30 |
66,2±1,08* |
6,1±0,75* |
16,3±0,65* |
15,2±0,74* |
|
60 |
70,2±1,34* |
5,8±0,44 |
16,0±0,73 |
8,0±0,42* |
|
90 |
71,8±1,53 |
5,5±0,57 |
16,6±0,52 |
6,1±0,59* |
Примечание: * – критерий достоверности р<0,05 при сравнении c предыдущим сроком эксперимента между одним и тем же типом клеток.
На 10-е сутки качественное соотношение клеточного состава отражает процесс перехода экссудативной стадии воспаления в пролиферативную. Фибробласты составляют основное вещество соединительной ткани, образуются тонкие соединительнотканные волокна в стенках пор и около них. Новые соединительнотканные структуры врастают в толщу протеза между его нитями, формируя ячейки.
На 30-е сутки происходит дальнейшее снижение количества лимфоцитов (16,3±0,65 против 18,0±1,08) и нейтрофилов (15,2±0,74 против 20,4±0,61). Такое отношение элементов морфологической картины свидетельствует о продолжающемся окончании экссудативной фазы воспаления в области расположения импланта. Отмечается возрастание количества фибробластов (66,2±1,08 против 63,1±1,15), что говорит о дальнейшем развитии пролиферации в месте имплантации герниоэндопротеза. При гистологическом исследовании определяются новообразовывающиеся соединительнотканные волокна и зрелые фибробласты в стенках пор, имеются единичные воспалительные клеточные инфильтраты, скопления гигантских многоядерных клеток инородных тел (рис. 1). Был отмечен значительный отек, имеющий тенденцию к уменьшению, а также рыхлое сращение молодой соединительной ткани с окружающими гистологическими структурами, ведущие к их разделению.
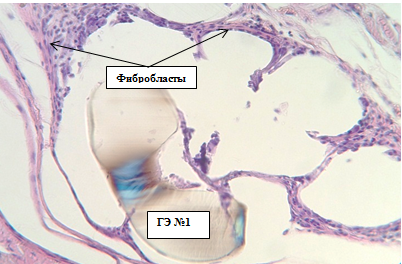
Рис. 1. Световая микроскопия места размещения герниоэндопротеза группы № 1 на 30-е сутки: соединительнотканные волокна и фибробласты в стенках ячеек, очаговые скопления воспалительных клеток. Окр. Г+Э. Световая микроскопия. Ув. х250
К 60-м суткам в морфологической картине тканей около герниоэндопротеза преобладают зрелые фибробласты (70,2±1,34), количество которых достоверно растет в сравнении с предыдущими сроками, достоверно уменьшается относительное количество нейтрофилов (8,0±0,42). Обнаруживаются гигантские клетки инородных тел.
Морфологическая картина капсул, состоящих из соединительной ткани, около нитей герниоэндопротеза представлена внутренним слоем немногочисленных фибробластов и различной толщины и зрелости изоморфными соединительнотканными тяжами, многослойно лежащими вокруг. Внешний слой капсул состоит из самых крупных и сформированных волокон. Межъячеечное пространство занято слабоструктурированной соединительной тканью с весомым количеством разной степени зрелости фибробластов, что может говорить о развитом процессе организации в месте имплантации протеза.
К 90-м суткам морфологическая картина продолжает меняться в сторону уменьшения количества экссудативно-воспалительных и увеличения количества соединительнотканных клеточных и межклеточных структур (рис. 2). «Клетки воспаления» представлены малочисленными нейтрофилами (6,1±0,59); тем не менее удельное количество лимфоцитов достоверно не уменьшается (16,6±0,52), что наряду с наличием гигантских клеток инородных тел свидетельствует о продолжающейся иммунной реакции на импланты группы № 1. Гистологическая картина свидетельствует о развитии соединительнотканной капсулы вокруг места имплантации – организации ткани внутреннего и внешнего слоев, наличии единичных зрелых фибробластов.
Таким образом, к 90-м суткам не достигнуты удовлетворительные показатели иммунного ответа организма подопытного животного на герниоэндопротез.
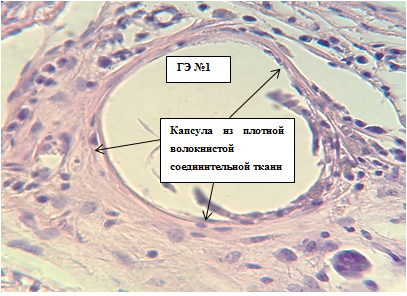
Рис. 2. Световая микроскопия места размещения герниоэндопротеза № 1 на 90-е сутки: плотная волокнистая соединительная ткань формирует капсулы вокруг нитей герниоэндопротеза, единичные гигантские клетки инородных тел. Окр. Г+Э.
Световая микроскопия. Ув. х400
Характеристика клеточного состава в области расположения импланта из группы № 2 представлена в таблице 2.
Таблица 2
Клеточный состав области расположения герниоэндопротеза из группы № 2
|
Клетки (%) Сутки |
Фибробласты |
Макрофаги |
Лимфоциты |
Нейтрофилы |
|
10 |
65,83±1,12* |
4,63±0,64* |
18,39±1,11* |
11,15±0,43* |
|
30 |
68,24±1,17* |
2,85±0,72* |
22,46±1,21* |
6,45±0,31* |
|
60 |
73,5±1,09* |
2,8±0,51 |
18,77±0,93* |
4,93±0,48* |
|
90 |
76,15±1,46* |
2,1±0,47 |
17,7±0,59 |
3,7±0,33* |
Примечание: * – критерий достоверности р<0,05 при сравнении c предыдущим сроком эксперимента между одним и тем же типом клеток.
К 10-м суткам ячейки имеют полностью оформленную, круглую форму. Контуры ячеек вокруг волокон импланта без интервалов (рис. 3), ячейки сформированы из тонких стенок, состоящих из внутреннего (фибробласты) и наружного (молодые волокна соединительной ткани) слоев.

Рис. 3. Световая микроскопия места размещения герниоэндопротеза № 2 при применении депротеинизированного гемодиализата на 10-е сутки: непрерывные контуры ячеек, фибробласты во внутреннем слое стенок ячейки, большое скопление фибробластов в окружающей ячейки ткани. Окр. Г+Э. Световая микроскопия. Ув. х250
Пространство между ячейками заполнено свежей грануляционной тканью, в морфологический состав которой входят лимфоциты, макрофаги и фибробласты (табл. 2). Имеются волокнистые соединительнотканные структуры в границах ячеек и тонкие волокна вокруг них, встречаются немногочисленные гигантские клетки инородных тел.
На 30-й день после имплантации наблюдается процесс стихания отечной фазы воспаления. Структурные волокна протеза располагаются в закругленных обособленных секциях.
Наблюдается процесс постепенного созревания соединительной ткани капсулы вокруг импланта, который можно описать как структурирование ранее разрозненных пучков. Увеличивается количество фибробластов в капсуле.
Зафиксировано уменьшение количества воспалительноклеточных элементов. Относительное количество нейтрофилов ниже примерно в два раза, нежели в группе № 1 (6,45% и 15,2% соответственно), что свидетельствует об эффективном подавлении воспалительной реакции с помощью депротеинизированного диализата. Преобладают зрелые фибробласты и фиброциты (68,24%), в меньшей степени представлены лимфоциты и макрофаги (табл. 1), имеются небольшие скопления гигантских клеток инородных тел.
К 60-м суткам основными морфологическими структурами являются фиброциты и фибробласты (73,5%).
В стенках ячеек по-прежнему встречаются отдельные гигантские клетки инородных тел. Соединительнотканные волокна соединены в плотные, толстые пучки.
Процентное соотношение лимфоцитов несколько больше, чем на аналогичных сроках в группе № 1, что, вместе с наличием гигантских клеток инородных тел, говорит о том, что в месте имплантации проходит пролиферативная фаза воспаления с выраженной гранулематозной реакцией на ксеноматериал.
В дальнейшем количество клеточных элементов, характерных для экссудативной фазы воспаления, продолжает неуклонно снижаться, и к 90-м суткам относительное количество нейтрофилов составляет 3,7%, что приблизительно в два раза меньше, чем при использовании герниоэндопротеза из группы № 1. Наблюдаются лишь единичные гигантские клетки инородных тел.
Капсулы ячеек вокруг нитей импланта объединены плотными толстыми изоморфными пучками соединительнотканных волокон в виде цепочек (рис. 4).
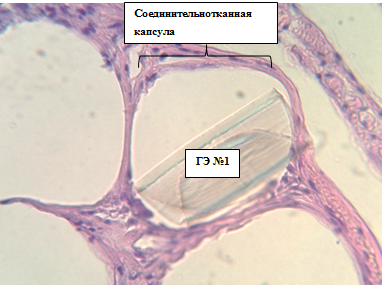
Рис. 4. Световая микроскопия места размещения герниоэндопротеза № 2 при применении депротеинизированного гемодиализата на 90-е сутки: прочная сетчатая соединительнотканная структура создает каркас для нитей эндопротеза. Окр. Г+Э. Световая микроскопия. Ув. х400
Относительное количество фибробластов и фиброцитов увеличивается (76,15%) в сравнении как с предыдущими сроками в пределах данной серии, так и с аналогичными сроками группы исследования при использовании герниоэндопротезов группы № 1 без применения депротеинизированного диализата. Данная морфологическая картина демонстрирует окончание процессов организации (заживления).
Выводы. На основании полученных данных можно с уверенностью сказать, что в группе животных № 2 (с применением депротеинизированного диализата из крови молочных телят) степень выраженности и продолжительность экссудативной фазы воспалительной реакции достоверно меньше, что выражается в количестве клеток на различных этапах процесса заживления (поэтапное уменьшение количества макрофагов и нейтрофилов более чем в 2 раза на каждом из исследуемых сроков). Одновременно с этим пролиферативная и синтетическая активность фибробластов значительно выше, что обусловливает более раннее формирование прочных соединительнотканных капсул вокруг волокон герниоэндопротеза. Такие результаты говорят нам о том, что использование препаратов, стимулирующих коллагеногенез, оправдывается лучшим результатом лечения и снижением вероятности развития постоперационных осложнений. Одновременно с этим необходим дальнейший поиск лекарственных средств, способных продемонстрировать еще лучший результат при их применении.
Библиографическая ссылка
Объедков Е.Г., Иванов С.В., Иванов И.С., Жабин С.Н., Ушанов А.А. ОЦЕНКА ТКАНЕВОЙ РЕАКЦИИ НА ПОЛИПРОПИЛЕНОВЫЙ ГЕРНИОЭНДОПРОТЕЗ ПРИ ИСПОЛЬЗОВАНИИ ДЕПРОТЕИНИЗИРОВАННОГО ДИАЛИЗАТА ИЗ КРОВИ ТЕЛЯТ (ЭКСПЕРИМЕНТАЛЬНОЕ ИССЛЕДОВАНИЕ) // Современные проблемы науки и образования. 2019. № 6. ;URL: https://science-education.ru/en/article/view?id=29387 (дата обращения: 19.05.2026).



