Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
THE COATING INFLUENCE ON THE EFFECTS OF GOLD NANORODS AT INTRAVENOUS ADMINISTRATION IN RATS WITH ALLOXAN DIABETES
Несмотря на значительные усилия, направленные на профилактику и борьбу с диабетом и его осложнениями, согласно данным Международной диабетической ассоциации в настоящее время этим заболеванием страдают более 463 миллионов человек в мире, диабет является седьмой по значимости причиной смертности [1]. Длительное воздействие хронической гипергликемии без надлежащей терапии может приводить к различным сосудистым осложнениям и является основной причиной заболеваемости и смертности у больных диабетом. По оценкам Всемирной организации здравоохранения, в 2040 г. заболеваемость диабетом может составить около 642 миллионов человек [2]. Это обусловливает необходимость поиска новых терапевтических стратегий для лечения диабета, одним из перспективных направлений является применение нанотехнологий. Золотые наночастицы в связи с их низкой токсичностью и наличием антиоксидантных свойств [3] являются перспективными агентами для направленной доставки гипогликемических препаратов в диабетологии [4, 5]. Значительное влияние на эффекты наночастиц in vivo может оказывать характер покрытия наночастиц [6, 7], особенно в условиях развития в организме патологических процессов.
Цель исследования: оценить влияние покрытия золотых наностержней на морфологические изменения во внутренних органах при внутривенном введении у крыс с аллоксановым диабетом.
Материалы и методы исследования
Экспериментальное исследование на лабораторных животных было выполнено на базе ЦКП СГМУ им. В.И. Разумовского. Белым беспородным крысам-самцам внутривенно вводили золотые наностержни (ЗНС) (концентрация золота 400 мкг/мл), покрытые полиэтиленгликолем (PEG) и полистиролсульфонатом (PSS). Синтез и вычисление параметров ЗНС проводили в лаборатории нанобиотехнологии и в ЦКП «Симбиоз» ИБФРМ РАН (г. Саратов). Определение длины и диаметра ЗНС осуществляли по трансмиссионным электронно-микроскопическим (ТЭМ) изображениям микроскопа Libra-120 (Carl Zeiss, Germany). Средние размеры ЗНС составили: длина 41±8 нм и диаметр 10±2 нм.
При исследовании на лабораторных животных учитывали требования положений Европейской конвенции защиты позвоночных животных для экспериментальных и других научных целей (Страсбург, 1986), рекомендации комитета по этике ФГБОУ ВО Саратовский ГМУ им. В.И. Разумовского Минздрава РФ (протокол № 6 от 06.02.2018 г.).
Крысы случайным образом были распределены на 6 групп – 1 контрольная и 5 опытных. Контрольная группа была представлена интактными животными. Животным первой и второй опытных групп внутривенно вводили по 1 мл ЗНС с покрытием PEG и PSS соответственно. Крысам остальных опытных групп моделировали диабет посредством внутрибрюшинного введения аллоксана моногидрата (Sigma, США) из расчета дозы 100 мг/кг. Глюкометром Accu-Chek Performa Roche (Швейцария) измеряли концентрацию уровня глюкозы в крови. Крысам четвертой и пятой опытных групп на 15-е сутки после формирования аллоксанового диабета внутривенно вводили ЗНС, покрытые PEG и PSS соответственно. Через сутки после внутривенного введения животные всех групп выводились из опыта методом декапитации, у них забирали сыворотку крови и образцы внутренних органов для морфологического исследования.
Перекисное окисление липидов оценивали на спектрофлуориметре RF-5301 PC (Shimadzu Corporation, Япония) по изменению показателей концентрации в сыворотке крови промежуточных продуктов – малонового диальдегида (МДА) и гидроперекисей липидов (ГПЛ).
При морфологическом исследовании использовали стандартный протокол приготовления материала. Фрагменты печени, почек и селезенки фиксировали в растворе забуференного 10%-ного формалина, помещали в спиртовую проводку и после заливки в парафин окрашивали гематоксилином и эозином. Наличие в тканях гликогена определяли с помощью окрашивания препаратов реактивом Шиффа (ШИК-реакция). Морфометрические исследования проводили с использованием системы анализа цифровых изображений Микровизора медицинского (µVizo-103 ЛОМО).
Статистическую обработку данных проводили с использованием пакета статистических программ SSPS-13.0. Проверку нормальности распределения значений в выборке осуществляли с помощью теста Колмогорова–Смирнова. В случае нормального распределения определяли среднее арифметическое и стандартную ошибку, различия между группами вычисляли с использованием критерия Крамера–Уэлча. Если распределение отличалось от нормального, рассчитывали медиану, квартили и достоверность различий (р) с применением непараметрического критерия Манна–Уитни.
Результаты исследования и их обсуждение
Проведенные исследования показали, что при однократном внутривенном введении ЗНС с различным покрытием в органах у здоровых крыс развиваются дистрофические изменения паренхиматозных элементов и нарушения кровообращения в строме (отек и полнокровие), более выраженные в группе с внутривенным введением PSS-покрытых ЗНС. При морфологическом исследовании почек в корковом веществе на фоне полнокровия капилляров было обнаружено незначительное расширение клубочков. Канальцы имели округлую или овальную форму, при внутривенном введении PSS-покрытых ЗНС в эпителиальных клетках развивалась белковая дистрофия. Просвет большинства канальцев имел суженный вид вследствие увеличения высоты эпителия до 17,4±0,8 мкм (при значениях в контрольной группе 15,3±1,3 мкм). В печени гистоархитектоника органа была сохранена, отмечались умеренно выраженное венозное полнокровие органа и при введении PSS-покрытых ЗНС – дистрофия гепатоцитов незначительной степени выраженности. В селезенке красная пульпа преобладала над белой пульпой, граница различалась отчетливо, лимфоидные фолликулы не имели светлых центров.
При биохимическом исследовании продуктов перекисного окисления в сыворотке крови липидов изменения были обнаружены только в группе введения ЗНС, покрытых PSS: концентрация малонового диальдегида превысила показатели контрольной группы в 3 раза и составила 1,6 [1,27; 1,82].
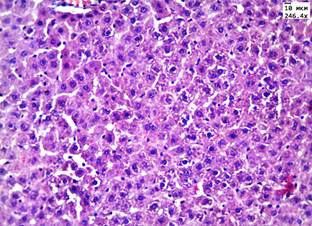
Введение аллоксана сопровождалось появлением у животных полидипсии, полиурии, в сыворотке крови на 15-е сутки после введения аллоксана отмечалось повышение уровня глюкозы в 3 раза по сравнению с группой контроля – до 18,5 ммоль/л. Летальность животных в данных группах на 5-е сутки составила 8,3%. При морфологическом исследовании в группах с аллоксановым диабетом в почках и печени обнаружены признаки, характерные для повреждения паренхимы органа при гипергликемии (рис. 1, А, В).
|
А) |
Б) |
|
В) |
Г) |
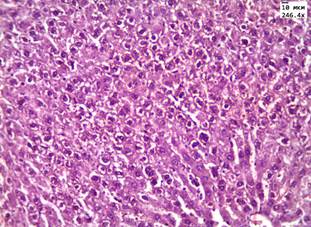
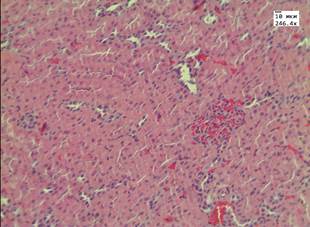
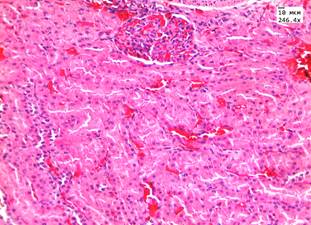
Рис. 1. Печень в группе животных с диабетом: А) при введении ЗНС, покрытых PEG; Б) при введении ЗНС, покрытых PSS. Почки в группе животных с диабетом: В) при введении ЗНС, покрытых PEG; Г) при введении ЗНС, покрытых PSS. Гематоксилин-эозин. Ув. х246,4
В почках наблюдались признаки нарушения кровообращения в виде отека стромы, умеренного полнокровия сосудов и наличия плазматического пропитывания в стенках мелких артериол. В корковом веществе в клубочках отмечалось увеличение капсулы Шумлянского–Боумена за счет отека. При морфометрическом исследовании обнаружено увеличение площади клубочков на 25% по сравнению с показателями в контрольной группе до 9,3±0,4 мм2 за счет умеренного полнокровия капилляров. Просвет извитых канальцев был сужен, эпителий находился в состоянии умеренно выраженной дистрофии. При морфометрическом исследовании обнаружено увеличение высоты эпителия извитых канальцев до 19,5±0,8 мкм (в контроле 15,3±1,3 мкм). При окрашивании реактивом Шиффа в цитоплазме эпителия и в просвете канальцев отмечались ШИК-положительные включения – гранулы гликогена. При морфологическом исследовании печени балочное строение было сохранено, наблюдалось умеренно выраженное полнокровие центральных вен и синусоидов. В пятой опытной группе с введением ЗНС, покрытых PSS, в половине наблюдений в корковом веществе почек были обнаружены очаговые лимфоидные инфильтраты. В чашечно-лоханочной системе во всех случаях обнаружены атрофические изменения уротелия. В гепатоцитах отмечалась дистрофия различной степени выраженности, имелись участки фокального некроза (рис. 1, Б).
При окрашивании реактивом Шиффа в цитоплазме гепатоцитов регистрировалось снижение уровня гликогена, что вероятнее всего связано со снижением его концентрации в тканях на фоне моделированного аллоксанового диабета. При морфометрическом исследовании печени определяли количество гепатоцитов с дистрофическими изменениями в цитоплазме и в состоянии некроза, подсчитывали число непаренхиматозных элементов печени (НПЭ) и двуядерных гепатоцитов. В качестве НПЭ печени учитывали лимфоциты, клетки Купфера и клетки Ито. Результаты морфометрического исследования представлены в таблице 1.
Во всех опытных группах с моделированным аллоксановым диабетом обнаружены признаки повреждения паренхимы печени, проявляющиеся в виде значительного повышения числа гепатоцитов, находящихся в состоянии некроза, – до 49 [31;57], что в 3 раза превышает значение показателя в контрольной группе. Степень выраженности некробиотических процессов в паренхиме печени оценивали с использованием коэффициента нормализации паренхимы (КНП). КНП определяли как отношение числа гепатоцитов с дистрофическими изменениями к гепатоцитам в состоянии некроза на поле зрения (х774).
Во всех опытных группах с моделированным аллоксановым диабетом установлено достоверное снижение КНП по сравнению с группой контроля. Минимальные значения КНП – 0,7 – были получены в группе моделированного аллоксанового диабета с введением ЗНС, покрытых PSS.
Таблица 1
Результаты морфометрических исследований в печени
|
Группы наблюдения |
Морфометрические показатели в поле зрения |
||||
|
Количество гепатоцитов с дистрофи-ческими изменениями |
Количество гепатоцитов в состоянии некроза |
КНП |
Количество НПЭ печени |
Количество двуядерных гепатоцитов |
|
|
Контрольная |
39 [33;43] |
15 [13;19] |
2,6 |
7[5;8] |
|
|
ЗНС (PEG) |
43 [37;47] |
17 [13;19] |
2,5 |
4[3;5] |
5 [3;7] |
|
ЗНС (PSS) |
45 [39;48] |
19 [14;21] |
2,3 |
5[3;7] |
4 [3;6] |
|
Диабет |
41 [40;59] |
49 [31;57]* |
0,83* |
13[10;17]* |
1 [1;2]* |
|
Диабет + ЗНС (PEG) |
32 [25;35] |
37 [33;39]* |
0,86* |
21[18;24]* |
1 [0;2]* |
|
Диабет + ЗНС (PSS) |
35 [27;42]* |
50 [36;59]* |
0,7* |
22[13;25]* |
2 [1;3]* |
*– p<0,05 достоверность отличия с контрольной группой
Воздействие на макрофагальную систему печени оценивали по результатам подсчета числа НПЭ – лимфоцитов, резидентных макрофагов (клеток Купфера и Ито) в поле зрения (х774). У животных с моделированным аллоксановым диабетом введение ЗНС, покрытых PEG и PSS, сопровождалось увеличением числа НПЭ печени до 21 [18;24] и 22 [13;25] соответственно, что в 3 раза превышало показатели в контрольной группе.
Для оценки выраженности пролиферативных процессов подсчитывали количество двуядерных гепатоцитов в поле зрения (х774). Во всех опытных группах с моделированным диабетом было установлено уменьшение в 5 раз количества двуядерных гепатоцитов по сравнению с группой контроля.
В группах с моделированным диабетом в селезенке строма органа имела нормальное строение, красная пульпа преобладала над белой, граница между ними различалась отчетливо. Лимфоидные фолликулы имели обычные размеры, округлую или овальную форму и были представлены скоплениями Т- и В-лимфоцитов, плазмоцитами и макрофагами, без светлых центров размножения.
В сыворотке крови крыс с моделированным аллоксановым диабетом во всех опытных группах происходило увеличение количества МДА и ГПЛ по сравнению с группой контроля (табл. 2). В опытной группе с моделированным аллоксановым диабетом без введения ЗНС наблюдалось увеличение концентрации МДА до 0,97 [0,64; 1,24] и ГПЛ до 3,1 [1,89; 3,3].
Таблица 2
Содержание МДА и ГПЛ в сыворотке крови
|
Группы наблюдения |
МДА, мкмоль/л |
ГПЛ, ед/мл |
|
Контрольная |
0,53 [0,48; 0,71] |
0,93 [0,78; 1,25] |
|
ЗНС (PEG) |
0,52 [0,48; 0,58] |
0,82 [0,68; 0,98] |
|
ЗНС (PSS) |
1,6 [1,27; 1,82]* |
1,5 [1,15; 1,82] |
|
Диабет |
0,97 [0,64; 1,24]* |
3,1 [1,89; 3,3]* |
|
Диабет + ЗНС (PEG) |
1,39 [0,79; 2,07]* |
3,65 [3,48; 4,2]* |
|
Диабет + ЗНС (PSS) |
2,5 [2,3; 2,75]*,** |
3,77 [3,46; 4,12]*,** |
*– достоверность отличия от контрольной группы (p<0,05), ** – от группы с диабетом (p<0,05)
Внутривенное введение ЗНС сопровождалось еще более значимым накоплением продуктов перекисного окисления липидов в сыворотке крови. Максимальное повышение уровня МДА до 2,5 [2,3; 2,75] и ГПЛ до 3,77 [3,46; 4,12] наблюдалось в опытной группе крыс с введением ЗНС, покрытых PSS. Следует отметить, что внутривенное введение ЗНС, покрытых PEG, крысам с моделированным аллоксановым диабетом, несмотря на повышение титра МДА и ГПЛ, не сопровождалось развитием достоверных изменений по сравнению с группой животных с аллоксановым диабетом.
Таким образом, внутривенное введение ЗНС с покрытием PEG и PSS лабораторных крысам с моделированным аллоксановым диабетом сопровождалось появлением морфологических изменений в органах (повреждением паренхимы вплоть до развития участков некроза, отеком, полнокровием стромы, пролиферацией лимфоидных клеток и макрофагов) и накоплением в крови продуктов перекисного окисления липидов (МДА и ГПЛ). Наиболее выраженные изменения были обнаружены нами в опытной группе введения ЗНС, покрытых PSS. Полученные данные о влиянии покрытия при воздействии ЗНЧ на морфологию внутренних органов согласуются с результатами работ ряда авторов [6, 7] и ранее выполненных нами исследований [8, 9].
Заключение
Проведенные исследования показали, что в печени и почках крыс всех опытных групп с моделированным аллоксановым диабетом развивались дистрофические и некротические изменения в паренхиме, отек и полнокровие стромы, пролиферация лимфоидных клеток и макрофагов. Наиболее выраженные морфологические изменения и наибольшее накопление продуктов липопероксидации были обнаружены в опытной группе с введением ЗНС, покрытых PSS. Полученные результаты вероятнее всего связаны с наличием отрицательного заряда у полистиролсульфонатной оболочки ЗНС. Внутривенное введение ЗНС, покрытых полиэтиленгликолем, не вызывало значительных морфологических изменений во внутренних органах у животных с аллоксановым диабетом, что позволяет рекомендовать их использование в исследованиях на животных с моделированными патологическими процессами.
Конфликт интересов. Авторы заявляют об отсутствии явных и потенциальных конфликтов интересов, связанных с настоящей статьей.
Исследование проведено в рамках реализации государственного задания Минздрава России.
Библиографическая ссылка
Дихт Н.И., Пахомий С.С., Бучарская А.Б., Годаге П.П., Наволокин Н.А., Терентюк Г.С., Маслякова Г.Н., Хлебцов Б.Н., Хлебцов Н.Г. ВЛИЯНИЕ ПОКРЫТИЯ НА ЭФФЕКТЫ ЗОЛОТЫХ НАНОСТЕРЖНЕЙ ПРИ ВНУТРИВЕННОМ ВВЕДЕНИИ У КРЫС С АЛЛОКСАНОВЫМ ДИАБЕТОМ // Современные проблемы науки и образования. 2019. № 6. ;URL: https://science-education.ru/en/article/view?id=29384 (дата обращения: 19.05.2026).
DOI: https://doi.org/10.17513/spno.29384