Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
THE DYNAMICS ANALYSIS OF MYCOBACTERIUM TUBERCULOSIS CULTURES DRUG RESISTANCE FORMATION, ALLOCATED IN FIRST IDENTIFIED PATIENTS IN THE REPUBLIC OF MORDOVIA
Туберкулез является одним из наиболее часто встречающихся инфекционных заболеваний в мире. Российская Федерация входит в 30 стран с наибольшим бременем туберкулеза. Включение России в данный список обусловлено существенным возросшим абсолютным числом новых зарегистрированных случаев и рецидивов туберкулеза в течение 2015 года – 115 тысяч [1, с. 7-16]. В настоящее время в Российской Федерации наблюдается улучшение эпидемической обстановки по туберкулезу, о чем свидетельствует положительная динамика основных показателей. Так, по данным Федеральной службы государственной статистики, с 2005 по 2017 год отмечается тенденция к снижению заболеваемости туберкулезом – с 84,7 до 48,3 человека на 100 тыс. населения (на 42,9%), к снижению показателя смертности от туберкулеза – с 22,5 до 12,1 человека на 100 тыс. населения (на 46,2%) [2, с. 22, 35]. Наряду с этим происходит увеличение доли пациентов с множественной (МЛУ) и широкой лекарственной устойчивостью (ШЛУ) возбудителя к противотуберкулезным препаратам (ПТП) с 23,4% в 2008 г. до 54,0% в 2017 г. [3, с. 15-24]. Следует отметить, что проблема устойчивости микобактерии туберкулёза (МБТ) к ПТП является глобальной проблемой, однако наибольшим бременем проблема МЛУ ложится на три страны: Индию, Китай и Российскую Федерацию, на долю которых в совокупности приходится почти половина всех случаев в мире [4].
Приобретение МБТ устойчивости к антибиотикам, как и других бактерий, может развиваться посредством случайных мутаций и/или благодаря воздействию антибактериальных препаратов. В связи с этим первоначально был рекомендован комбинированный прием препаратов для снижения риска развития лекарственной устойчивости сразу к нескольким из них. Однако лечение туберкулеза осуществлялось без предшествующего определения лекарственной чувствительности МБТ к ПТП. Незавершенное или неадекватное предыдущее лечение (например, лечение недостаточными дозами препаратов первого ряда), а также использование некачественных ПТП явилось одной из причин формирования лекарственной устойчивости возбудителя. Основой резистентности МБТ к ПТП являются спонтанные точечные мутации в специфических независимых генах. В свою очередь, неадекватное воздействие ПТП на популяцию МБТ обеспечивает селективный отбор резистентных штаммов [5, с. 7].
Помимо возникновения точечных мутаций в генах существуют и других механизмы формирования резистентности, такие как модификация молекул антибиотиков ферментными системами бактерий, гиперэкспрессия эффлюксных систем и белков, участвующих в нейтрализации действия препарата, изменения белков-поринов в клеточной стенке, изменение проницаемости клеточной стенки и другие [6, с. 1229-1238].
Исследователями были получены данные о гиперэкспрессии белков Rv0148 (редуктаза короткоцепочечного типа), Rv1876 (бактериоферритин) и Rv3841 (ферритин) у МБТ, устойчивых к аминогликозидам. В частности, белок Rv0148 имеет домен SDR, который способен связывать аминогликозиды, приводя к их нейтрализации. Амикацин и канамицин также способны связываться с бактериоферритиновым доменом Rv1876 и ферритиновым доменом Rv3841. Следовательно, избыточная экспрессия этих белков может нейтрализовать эффект аминогликозидов и играть роль в возникновении лекарственной устойчивости [7, с. 1-9].
Эффлюксные системы играют важную роль в устойчивости бактерий к лекарственным препаратам. Одним из видов эффлюксных насосов являются ABC-транспортеры, которые состоят из белков-экспортеров и белков-импортеров. Экспортеры ответственны за транспортировку различных субстратов, таких как антибиотики, белки и липиды, в то время как импортеры транспортируют широкий спектр субстратов, включая аминокислоты, пептиды, сахара, металлы и другие метаболиты. МБТ с МЛУ экспрессируют большое количество АBC-транспортеров, что приводит к снижению концентрации препарата внутри клетки и в совокупности с другими механизмами позволяет бактериям достигать значительной устойчивости к лекарственным средствам [8, с. 248-261].
Цель исследования: проанализировать динамику формирования лекарственной устойчивости (ЛУ) МБТ, выделенных из мокроты больных впервые выявленным туберкулезом легких в Республике Мордовия в период за 2014-2018 годы.
Материалы и методы исследования. Объектом исследования явились 534 штамма M. tuberculosis, выделенные от впервые выявленных, ранее не леченных больных туберкулезом (n=534). Все пациенты проходили обследование с января 2014 г. по декабрь 2018 г. в ГКУЗ Республики Мордовия «Республиканский противотуберкулезный диспансер» г. Саранска. Определение лекарственной устойчивости штаммов МБТ, выделенных из мокроты впервые выявленных больных туберкулезом, к ПТП проводилось методом пропорций на жидкой среде в автоматизированном анализаторе с флуоресцентной детекцией результата - Bactec MGIT 960 и методом абсолютных концентраций на среде Левенштейна-Йенсена. Показатели рассчитывались от количества культур, исследованных на лекарственную чувствительность. Обработку результатов проводили с помощью программы Microsoft Office Excel.
Результаты исследования и их обсуждение. Всего за 2014-2018 гг. в Республике Мордовия выявлено 1342 случая туберкулеза легких, при этом минимальное количество случаев зарегистрировано в 2018 г. (239 случаев), а максимальное - в 2017 г. (299 случаев). Выделение МБТ за весь период наблюдения составило 534 случая (39,8%). Было установлено, что более половины культур МБТ (53,6%) были чувствительны к ПТП.
ЛУ хотя бы к одному ПТП за пять лет составила 45,9%, имела тенденцию к снижению и колебалась по годам от 42,0% (2017 г.) до 48,2% (2016 г.). Аналогичные результаты по Республике Мордовия были получены и в предыдущие годы. Это позволяет выразить надежду по стабилизации ситуации с ЛУ МБТ. Такие же данные опубликованы и по другим субъектам РФ [9; 10].
Монорезистентность обнаружена у 7,7% культур МБТ, обследованных на лекарственную чувствительность, полирезистентность (ЛУ к 2 и более ПТП, но не к сочетанию изониазида и рифампицина) в 11,5% культур. При анализе динамики ЛУ за анализируемый период установлено, что монорезистентность изменялась от 4,5% (2016 г.) до 13,3% (2018 г.). По структуре ЛУ МБТ среди монорезистентных культур в 58,5% случаев определялась к изониазиду, в 34,2% - к стрептомицину, к этамбутолу – 7,3% (выделено три указанные культуры МБТ в 2014, 2017, 2018 гг.). Анализируя полирезистентность МБТ, была отмечена тенденция к снижению от 33,3% в 2015 г. до 4,8% в 2018 г.
ЛУ к двум ПТП, включая изониазид и другие (без рифампицина), за весь период составила 8,9%, имела тенденцию к снижению от 11,5% в 2014 г. до 2,2% в 2018 г. ЛУ к сочетанию изониазида и стрептомицина составила 8,3% и снижалась от 11,5% в 2014 г. до 0% в 2018 г. ЛУ к сочетанию изониазида и этамбутола составила за весь период 0,4% и регистрировалась только в 2016 и 2018 гг. ЛУ к трем ПТП, включая изониазид и другие (без рифампицина), установлена в 1,9% выделенных за пять лет культур, данный показатель был наибольшим в 2016 г. – 9,4%, в 2018 г. – не выявлялся. ЛУ к сочетанию изониазида, стрептомицина и этамбутола выявлена в 1,3% выделенных МБТ, изониазида, стрептомицина и пиразинамида - 0,6%, данные показатели регистрировались ежегодно и не превышали 2,7% выделенных МБТ. ЛУ к четырем ПТП, включая изониазид и другие (без рифампицина), выявлена в двух культурах МБТ (0,4%), выделенных в 2016 г. (изониазид, капреомицин, этамбутол, пиразинамид – 0,9%) и в 2017 г. (изониазид, капреомицин, этамбутол, пиразинамид - 1,0%). ЛУ к пяти ПТП, включая изониазид и другие (без рифампицина), зарегистрирована у 1 культуры МБТ (0,2%), выделенной в 2015 г., сочетание ПТП – изониазида, стрептомицина, этамбутола, циклосерина, аминосалициловой кислоты – 0,8%. ЛУ к шести ПТП, включая изониазид и другие (без рифампицина), установлена у 1 культуры МБТ (0,2%) при сочетании изониазида, стрептомицина, этамбутола, канамицина, этионамида, пиразинамида в 2014 г. – 0,9%. ЛУ к сочетанию рифампицина и других ПТП (без изониазида) составила за анализируемый период 0,2% и была выявлена в 1 случае в 2014 г. ЛУ к двум ПТП, включая рифампицин и другие ПТП (без изониазида), составила за анализируемый период 0,2% и была выявлена в 1 случае в 2014 г. при сочетании рифампицина и стрептомицина. Культуры МБТ, устойчивые к сочетаниям 3, 4, 5, 6 ПТП, включая рифампицин и другие ПТП (без изониазида), за анализируемый период не выделялись.
Согласно современным клиническим рекомендациям МЛУ МБТ определяется как устойчивость возбудителя как к изониазиду, так и рифампицину, вне зависимости от устойчивости к другим ПТП. Культуры МЛУ (устойчивые к изониазиду, рифампицину и другим ПТП) составили за 2014-2018 гг. 17,9% от выделенных МБТ по годам имели незначительную тенденцию к росту и изменялись от 16,7% в 2018 г. до 20% в 2017 г. (рисунок).
Так, МЛУ к трем ПТП (изониазид, рифампицин и другие ПТП) выявлена у 9,6% культур МБТ, данный показатель колебался от 6,4% в 2016 г. до 13,3% в 2018 г. Чаще всего МЛУ определяли как сочетание изониазида, рифампицина и стрептомицина у 7,3% культур МБТ, по годам изменялась от 3,3% в 2018 г. до 11,9% в 2015 г. МЛУ к сочетанию изониазида, рифампицина, этамбутола составила за пять лет 2,3% и регистрировалась в 2017 г. (3%) и в 2018 г. (10%).
МЛУ к четырем ПТП (изониазид, рифампицин и другие ПТП) регистрировалась в 4,3% культур МБТ, по годам увеличивалась от 0% в 2018 г. до 7,0% в 2017 г. МЛУ к изониазиду, рифампицину, стрептомицину, этамбутолу составила за пять лет 3,6%, по годам увеличивалась от 0% (2018 г.) до 5,9% (2015 г.). Наблюдалась МЛУ к сочетанию изониазида, рифампицина, стрептомицина, пиразинамида по 0,6% случаев (2014, 2016, 2017 гг.) и 0,2% культур в 2017 г.; сочетанию изониазида, рифампицина, стрептомицина, этамбутола - 0,4% в 2017 г.; сочетанию изониазида, рифампицина, стрептомицина, этамбутола, пиразидамида – 1,7% культур МБТ, выявленных в 2014, 2016 и 2017 гг.; сочетанию изониазида, рифампицина, стрептомицина, циклосерина, пиразинамида – 0,2% в 2017 г.
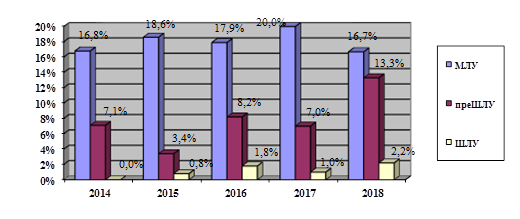
Динамика выявления МЛУ, преШЛУ, ШЛУ, за 2014-2018 гг.
Предширокая лекарственная устойчивость микобактерий туберкулеза (преШЛУ) представляет собой такой вид лекарственной устойчивости, при которой определяется устойчивость МБТ не только к изониазиду и рифампицину, но и к фторхинолону или аминогликозиду/полипептиду (канамицин и/или амикацин и/или капреомицин) вне зависимости от наличия устойчивости к другим ПТП [5; 11]. ПреШЛУ, устойчивые к изониазиду, рифампицину, офлоксацину, канамицину и/или амикацину и/или капреомицину, регистрировались за пять лет в 7,5% выделенных культур МБТ, при тенденции к увеличению доли этих штаммов, наибольший показатель был отмечен в 2018 г. – 13,3%, наименьший – 3,4% - в 2015 г. (рисунок). ПреШЛУ к трем ПТП выявлена в 0,4% выделенных культур и только в 2018 г., когда отмечена преШЛУ к сочетанию изониазида, рифампицина, канамицина (2,2% выделенных в этот год культур). ПреШЛУ к четырем ПТП выявлена в 1,5% выделенных культур, по годам этот показатель изменялся от 0% (2017 г.) до 3,3% (2018 г.). ПреШЛУ к сочетанию изониазида, рифампицина, стрептомицина, канамицина отмечена только в 2016 г. (0,9%), к сочетанию изониазида, рифампицина, этамбутола, канамицина отмечена в 2018 г. – 3,3%, к сочетанию изониазида, рифампицина, стрептомицина, этамбутола, канамицина отмечена в 2015 г. – 2,5%, к сочетанию изониазида, рифампицина, канамицина, пиразинамида выявлена в 2014 г. – 0,9% культур. ПреШЛУ к пяти ПТП выявлена за анализируемый период в 2,8% выделенных культур МБТ, изменения по годам от 0% (2015 г.) до 4,4% (2018 г.). ПреШЛУ к сочетанию изониазида, рифампицина, стрептомицина, этамбутола, офлоксацина зарегистрирована за пять лет в 0,2% случаев и отмечена только в 2016 г. (1,0%); к сочетанию изониазида, рифампицина, стрептомицина, этамбутола, канамицина - 1,7% (в 2014 г. - 2,7%, 2016 г. - 3,6%, 2017 и 2018 гг. - по 1,0%); к сочетанию изониазида, рифампицина, этамбутола, офлоксацина, канамицина – 0,4%, только в 2018 г. (2,2%); к сочетанию изониазида, рифампицина, стрептомицина, канамицина, пиразинамида – 0,4%, в 2016 г. – 09%, 2017 г. – 1,0%; к сочетанию изониазида, этамбутола, канамицина, капреомицина – 0,2%, только в 2018 г. (1,1%). ПреШЛУ к шести ПТП выявлена за анализируемый период в 2,6% выделенных культур МБТ, изменения по годам от 0,8% (2015 г.) до 5,7% (2016 г.). ПреШЛУ к сочетанию изониазида, рифампицина, стрептомицина, этамбутола, канамицина, капреомицина зарегистрирована за пять лет в 0,2%, отмечена только в 2017 г. (1,0%); к сочетанию изониазида, рифампицина, стрептомицина, этамбутола, канамицина, пиразинамида выявлена в 0,4%, в 2014 г. (1,8%); к сочетанию изониазида, рифампицина, стрептомицина, этамбутола, канамицина, амикацина выявлена в 0,2% в 2015 г. (0,8%); к сочетанию изониазида, рифампицина, стрептомицина, этамбутола, канамицина, этионамида зарегистрирована в 0,6% культур в 2014 г. (1,8%) и 2017 г. (1,0%).
В случае ШЛУ МБТ определяется устойчивость к изониазиду, рифампицину, фторхинолону и аминогликозиду/полипептиду (канамицину и/или амикацину и/или капреомицину) одновременно, независимо от наличия устойчивости к другим ПТП [7; 10]. ШЛУ, устойчивые к изониазиду, рифампицину, офлоксацину, канамицину и/или капреомицину, регистрировались за пять лет в 1,1% (6 культур), указанные МБТ выявлялись в 2015 г. (1 штамм, 0,8%), 2016 г. (2 штамма, 1,8%), 2017 г. (1 штамм – 1,0%), 2018 г. (2 штамм – 2,2%) (рисунок). ШЛУ к четырем ПТП выявлена в 1 случае (0,2%) к сочетанию изониазида, рифампицина, офлоксацина, канамицина в 2018 г. (1,1%). ШЛУ к пяти ПТП выявлена также в 1 случае (0,2%) к сочетанию изониазида, рифампицина, стрептомицина, канамицина в 2017 г. (1,0%). ШЛУ к шести и более ПТП выявлена в 4 случаях (0,8%): к сочетанию изониазида, рифампицина, стрептомицина, канамицина, офлоксацина, амикацина в 2015 г. (0,8%); к сочетанию изониазида, рифампицина, стрептомицина, этамбутола, канамицина, офлоксацина, пиразинамида в 2016 г. (0,9%), к сочетанию изониазида, рифампицина, стрептомицина, этамбутола, канамицина, офлоксацина, этионамида, циклосерина, пиразинамида в 2016 г. (0,9%); к сочетанию изониазида, рифампицина, офлоксацина, капреомицина, аминосалициловой кислоты, пиразинамида в 2018 г. (1,1%).
Другие варианты ЛУ за 2014-2018 годы наблюдались в 2 культурах (0,4%): в 2016 г. к стрептомицину, этамбутолу – в 0,9% культур и в 2017 г. к стрептомицину, пиразинамиду - в 1,1% случаев.
Выводы
1. В настоящее время в Республике Мордовия, как и в целом по Российской Федерации, продолжает оставаться актуальной проблема роста устойчивости МБТ к ПТП, в том числе формирование МЛУ и ШЛУ. Учитывая важность микробиологического мониторинга устойчивости МБТ к ПТП, в Республике Мордовия постоянно проводятся микробиологические исследования биологических субстратов от больных различными формами туберкулеза со статистическим анализом полученных данных.
2. Доля МЛУ МБТ за пятилетний период составила 17,9% без значительной динамики, но увеличивается доля преШЛУ с 7,1% до 13,3% и ШЛУ с 0% до 2,2%.
3. В случае МЛУ чаще всего встречается комбинация таких противотуберкулезных препаратов, как изониазид, рифампицин, стрептомицин, преШЛУ - изониазид, рифампицин, офлоксацин, канамицин и/или амикацин и/или капремицин, а при ШЛУ – сочетание лекарственной устойчивости к изониазиду, рифампицину, офлоксацину, канамицину и/или капремицину.
4. Спектр МЛУ расширяется к четырем препаратам.
5. Отмечено, что устойчивость к резервным ПТП с доминированием резистентности к инъекционным антибиотикам, протионамиду и к этамбутолу наблюдается практически у половины культур МЛУ МБТ.
6. В настоящее время ввиду распространения возбудителя туберкулеза с МЛУ является очевидным проведение дополнительных противоэпидемических мероприятий, а также подбор оптимальных схем химиопрофилактического лечения лиц из групп риска.
Авторы выражают благодарность сотрудникам централизованной бактериологической лаборатории ГКУЗ Республики Мордовия «РПТД» за предоставленную информацию.
Библиографическая ссылка
Костина Ю.А., Лапштаева А.В., Гуляева Л.Р., Шишканова Т.И., Дзюба А.И. АНАЛИЗ ДИНАМИКИ ФОРМИРОВАНИЯ ЛЕКАРСТВЕННОЙ УСТОЙЧИВОСТИ КУЛЬТУР MYCOBACTERIUM TUBERCULOSIS, ВЫДЕЛЕННЫХ У ВПЕРВЫЕ ВЫЯВЛЕННЫХ БОЛЬНЫХ В РЕСПУБЛИКЕ МОРДОВИЯ // Современные проблемы науки и образования. 2019. № 5. ;URL: https://science-education.ru/en/article/view?id=29212 (дата обращения: 16.05.2026).
DOI: https://doi.org/10.17513/spno.29212



