Цель исследования: анализ патофизиологических и биохимических процессов осложнений, происходящих при острой скелетной травме, и оценка возможности их коррекции с помощью магнитотерапии.
Травматизм является одной из наиболее острых медико-социальных проблем современности. Травмы и несчастные случаи занимают 15% в структуре первичной заболеваемости у взрослых и 28,8% среди причин временной нетрудоспособности. При этом его уровень продолжает оставаться высоким, составляя 82,7 на 1000 взрослого населения. В то же время в последние 10 лет намечается тенденция к его незначительному снижению [1].
В общей структуре переломов преобладают переломы костей верхней конечности (46,3%). Обращаемость среди них наибольшая при переломах костей предплечья (19,5%). Второе место занимают переломы костей голени и голеностопного сустава – 17,1%. Среди переломов костей нижних конечностей доминируют переломы лодыжек (40-60% случаев).
У трудоспособного населения преобладают переломы костей запястья и кисти, затем следуют переломы области голеностопного сустава и стопы. У лиц старших возрастных групп чаще встречаются переломы костей предплечья, реже - области голеностопного и плечевого суставов. В целом наиболее высокие показатели инвалидности и длительной нетрудоспособности наблюдаются при травмах нижней конечности [2].
Материалы и методы исследования: при подготовке статьи использовали аналитический метод.
Результаты исследования и их обсуждение
Повреждения опорно-двигательного аппарата сопровождаются широким спектром патологических изменений в тканях, в ряде случаев имеющих необратимый характер. Коррекция данных изменений продолжает оставаться трудной задачей ввиду сложности их патогенеза.
Патогенез нарушений при переломах довольно многообразен. В первые сутки после травмы наблюдается изменение тонуса артерий крупного и среднего калибров и микроциркуляторного русла, которое приводит к снижению кровенаполнения мышц и затруднению венозного оттока. Ухудшается снабжение тканей кислородом и питательными веществами, затрудняется удаление недоокисленных продуктов обмена, развивается тканевая гипоксия, гиперкапния и метаболический ацидоз. Резко увеличивается проницаемость сосудистой стенки капиллярного русла, развивается травматический отёк.
Истинный травматический отёк периартикулярных тканей развивается через 6-10 часов после травмы, распространяясь как в проксимальном, так и в дистальном направлении конечности, и имеет плотную консистенцию [3]. Отёчные ткани находятся в состоянии гипоксии и ацидоза, в результате развивается дисфункция клеточных мембран. Отмечено, что при переломах костей предплечья 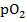 в первые 12 часов после травмы снижается почти на 40%, в течение суток – на 70%, продолжая затем падать. В ряде случаев на фоне отёка возможно развитие компартмент-синдрома, при котором мягкие ткани увеличиваются в размерах в пределах одного или нескольких фасциальных футляров. Внутрифасциальное давление повышается (в норме его референсные значения не превышают 10 мм рт. ст.), компенсаторно повышается и венозное давление. Когда оно превышает капиллярное давление перфузии, наступает коллапс капилляров, увеличивается их проницаемость, усугубляется интерстициальный отёк, внутрифасциальное давление увеличивается ещё больше. В конечном итоге развивается некроз мышц, продукты распада которых блокируют почечные канальцы. Развивается острая почечная недостаточность, которая может привести к гибели пациента. Считается, что к летальному исходу может привести компартмент-синдром в объёме мягких тканей, равном объёму предплечья [4].
в первые 12 часов после травмы снижается почти на 40%, в течение суток – на 70%, продолжая затем падать. В ряде случаев на фоне отёка возможно развитие компартмент-синдрома, при котором мягкие ткани увеличиваются в размерах в пределах одного или нескольких фасциальных футляров. Внутрифасциальное давление повышается (в норме его референсные значения не превышают 10 мм рт. ст.), компенсаторно повышается и венозное давление. Когда оно превышает капиллярное давление перфузии, наступает коллапс капилляров, увеличивается их проницаемость, усугубляется интерстициальный отёк, внутрифасциальное давление увеличивается ещё больше. В конечном итоге развивается некроз мышц, продукты распада которых блокируют почечные канальцы. Развивается острая почечная недостаточность, которая может привести к гибели пациента. Считается, что к летальному исходу может привести компартмент-синдром в объёме мягких тканей, равном объёму предплечья [4].
Гемодинамические нарушения обусловлены в том числе формированием стойкого очага афферентной импульсации с последующим выходом в кровеносное русло медиаторов воспаления и продуктов распада тканей. Это приводит к выбросу в кровеносное русло биологически активных веществ с вазоконстрикторным эффектом и может способствовать развитию апоптоза как эндотелиальных, так и гладкомышечных клеток артерий. Отмечено, что у пациентов с осложнёнными переломами дистального отдела предплечья в 96% случаев отмечаются отклонения интегрального показателя активности регуляторных систем от нормальных показателей. Данные компьютерной кардиоинтервалографии у таких пациентов свидетельствуют о функциональном напряжении систем регуляции и вегетативных сдвигах с выраженной симпатикотонией. Изменения в микроциркуляторном русле при капилляроскопии в стадии субкомпенсации проявляются уменьшением общего количества капилляров, замедлением движения эритроцитов. В стадии декомпенсации – значительным уменьшением общего количества капилляров, сужением или парезом части из них, слабой контурированностью и извитостью [5].
Среди гемодинамических типов микроциркуляции в остром периоде травмы в подавляющем большинстве случаев преобладает застои?но-стазическии? тип, составляющий 77,14% случаев при переломах костей нижней конечности. Указанный тип характеризуется снижением скорости кровотока и стазом тока крови на уровне капиллярного звена. Реже выявляются нормоциркуляторный и гиперемический типы [6].
Значительную роль в нарушениях микроциркуляции играет возникающее при переломах усиление способности эритроцитов к агрегации. Формирующиеся при этом эритроцитарные агломераты вызывают окклюзию капилляров, ухудшая тканевую перфузию и приводя к развитию капиллярной недостаточности. Увеличивается количество необратимо измененных форм эритроцитов, нарушается их проходимость через капилляры, что способствует формированию стаза и дальнейшему усугублению агрегации форменных элементов. Отмечено, что силы сцепления между изменёнными формами эритроцитов выше по сравнению с нормальными формами вследствие уменьшения сил электрического отталкивания. К указанным изменениям присоединяется микротромбообразование и активация свертывающей системы крови, приводящая к усилению синтеза крупнодисперсных белковых фракций, способствующих агрегации эритроцитов [7].
На фоне гипоксии ухудшается репаративная способность тканей и их сопротивляемость инфекции. Длительно существующий отёк приводит к формированию фиброза мягких тканей, что ведёт к их неполному функциональному восстановлению [8; 9].
Помимо описанных нарушений, травматический отёк может опосредованно влиять и на тактику лечения пациентов. На фоне травматического отёка в коже возникают сдвигающие силы, действующие на неё изнутри, что приводит к формированию эпидермальных пузырей (фликтен), наполненных прозрачным или геморрагическим содержимым. Первые располагаются в пределах эпидермиса, вторые распространяются в дерму, способствуя нарушениям микроциркуляции. Отмечено, что фликтены при переломах костей нижних конечностей встречаются в 7,2% случаев, при этом почти половина из них (47%) имеют геморрагическое содержимое, 43% – серозное, а 10% - смешанное. Появление фликтен вынуждает откладывать хирургическое вмешательство и требует активной тактики лечения [10].
Одним из наиболее тяжело поддающихся лечению осложнений при травмах является синдром Зудека, или комплексный регионарный болевой синдром (КРБС). К основным факторам риска развития данного осложнения относятся непосредственно сама травма (в 80-85% случаев – переломы, в 10% случаев – незначительные травмы) и неправильная иммобилизация конечности. Частота КРБС составляет порядка 25 случаев на 100 тыс. населения в возрасте от 40 до 60 лет, в 3-4 раза чаще у женщин. Среди всех переломов наиболее частой причиной КРБС являются переломы дистального отдела предплечья, особенно разгибательные переломы лучевой кости в типичном месте. В основе патофизиологии КРБС лежат периферическая сенсибилизация, вегетативные нарушения, увеличение концентрации противовоспалительных цитокинов, приводящие к нарушениям микроциркуляции. В клинической картине преобладают выраженный болевой синдром, отёк конечности и трофические нарушения [11].
В связи с этим своевременная коррекция возникших нарушений уменьшает риск развития осложнений, позволяет сократить продолжительность лечения, а также улучшить функциональные исходы. Многие публикации свидетельствуют о необходимости проведения физиопроцедур в самые ранние сроки после переломов. Однако значительная часть таких пациентов немобильна вследствие пребывания на скелетном вытяжении либо вследствие тяжести состояния. Среди физиопроцедур максимально выраженным противоотёчным эффектом обладает магнитотерапия. Достаточная проникающая способность магнитного поля позволяет проводить процедуры через повязки (в том числе и гипсовые).
Спектр физико-химических и биологических эффектов магнитотерапии весьма разнообразен. В их основе лежит воздействие силы Лоренца и эффект Холла. Сила Лоренца - сила, с которой электромагнитное поле действует на точечную заряженную частицу. В организме человека этими частицами являются активные центры (часть молекулы, определяющая её специфичность и каталитическую активность) рецепторов или ферментов. В результате воздействия силы Лоренца происходит изменение заряда активного центра, приводящее к изменению активности ферментов и изменению чувствительности рецепторов клеточных мембран. Например, увеличивается активность калий-натриевой АТФазы (усиливается транспорт ионов через клеточные мембраны), снижается чувствительность ряда адренорецепторов к катехоламинам.
Эффект Холла – появление разности потенциалов в проводниках и электролитах под действием силы Лоренца. В организме человека электролитами являются кровь, лимфа, тканевая жидкость, цитоплазма. В результате эффекта Холла происходит изменение объёмных электрических зарядов в клеточных мембранах и примембранных областях, и их упорядочивание; в жидкостях организма возникают вихревые электрические токи. Описанные эффекты максимально выражены в тканях, богатых водой: кровеносных сосудах, нервных и мышечных волокнах. В большей степени энергия магнитного поля поглощается нервной тканью.
В движущейся крови указанные изменения более выражены при воздействии постоянным магнитным полем, особенно когда силовые линии поля перпендикулярны направлению движения крови. В покоящихся биологических жидкостях вихревые токи возникают в большей степени при воздействии переменных и импульсных магнитных полей. Ввиду незначительной напряжённости магнитного поля, применяемого в физиотерапии, величина вызываемого им электрического тока незначительна, поэтому тепловой эффект не возникает [12].
Противоотёчный эффект магнитотерапии является наиболее выраженным. Он обусловлен усилением капиллярного кровотока вследствие снижения чувствительности α-адренорецепторов эндотелия к норадреналину. Это способствует раскрытию прекапиллярных сфинктеров, увеличению площади функционирующего капиллярного эндотелия, активизации транскапиллярного обмена между плазмой крови и тканевыми жидкостями. При этом отмечается снижение секреции лимфы. Активация Na-KАТФазы способствует трансмембранному транспорту ионов натрия из цитоплазмы в кровяное русло, вместе с ионами натрия из клеток выходит и вода [13].
Имеются данные о центральном механизме противоотёчного действия магнитотерапии за счёт увеличения секреции альдостерона и стимуляции активности антидиуретической и натрийуретической систем. Имеются также данные о стимулирующем влиянии низкочастотного магнитного поля на синтез эндогенного эритропоэтина, это проявляется увеличением среднего объема эритроцитов и их общего количества, а также среднего содержания гемоглобина в эритроцитах. Также отмечается повышение индекса деформируемости эритроцитов. Предполагают, что в основе этого механизма лежит изменение скорости диссоциации оксигемоглобина и конформационные изменения вторичной структуры белков крови [14].
Иммуномодулирующий эффект заключается в способности магнитного поля оказывать влияние на иммунокомпетентные клетки крови. Это проявляется усилением бластотрансформации лимфоцитов, активизацией клеточной перестройки лимфоидной ткани, повышением Т-хелперной активности и завершённости фагоцитоза. Благоприятное влияние на антиокислительные и свободнорадикальные процессы обусловлено повышением концентрации каталазы и супероксиддисмутазы в фагоцитах, а также SH-соединений во внутренней среде, что обусловливает усиление неспецифической резистентности организма [14].
Обезболивающий эффект реализуется за счёт снятия отёка и улучшения микроциркуляции, особенно при травматических повреждениях и воспалительных процессах. На фоне дегидратации нервных окончаний происходит снижение болевой импульсации. Усиление активности калий-натриевой АТФазы приводит к увеличению трансмембранного потенциала покоя нейронов и торможению проведения импульсов по восходящим путям ретикулярной формации. Центральное анальгетическое действие в большей степени выражено при транскраниальной магнитной стимуляции, при этом происходит увеличение секреции серотонина и дофамина (обладающего сильным антицептивным действием) в синапсах спинного мозга и увеличение концентрации эндорфинов в крови и ликворе [15].
Десенсибилизирующий эффект базируется на уменьшении дегрануляции тучных клеток за счёт стабилизации их мембран. Под действием магнитного поля происходит снижение экскреции медиаторов воспаления - гистамина, брадикинина и т.д., что также тормозит развитие отёка тканей и воспалительного процесса [16].
Трофический эффект обусловлен усилением капиллярного кровотока и транскапиллярного транспорта, улучшением утилизации глюкозы и липидов с помощью окислительного фосфорилирования, усилением синтеза белка и активацией внутриклеточных свободнорадикальных реакций за счёт потенциирования активности ферментов. Отмечен положительный эффект от применения магнитотерапии при вялотекущих раневых процессах (трофических язвах). В некоторых публикациях имеются данные об ускорении формирования костной мозоли при переломах, однако авторы данной статьи подвергают это утверждение сомнениям [17].
Противоопухолевый эффект, по мнению ряда исследователей, основан на способности оказывать тормозящее влияние на рост некоторых перевиваемых опухолей и усиливать эффект лучевой терапии [18].
Следовательно, магнитное поле обладает широким и многообразным действием на организм человека в норме и патологии [19]. Оно является более слабым раздражителем, чем большинство применяемых в физиотерапии факторов, поэтому действие его очень мягкое и физиологичное. Наиболее выражены ответные реакции при воздействии импульсным магнитным полем, особенно при частоте его до 20 Гц [20-22]. Слабее переменное магнитное поле, и самое мягкое действие оказывает постоянное магнитное поле. Физиологические и лечебные эффекты магнитного поля наблюдаются после многократных воздействий, но зато достигнутый эффект сохраняется в течение нескольких месяцев. Магнитотерапия является одним из наиболее щадящих методов воздействия, она легко переносится, не сопровождается какими-либо явными субъективными ощущениями и общими реакциями, хорошо сочетается с воздействием ряда других физических факторов [23]. Несмотря на значительное количество публикаций, посвящённых данному методу, некоторые механизмы действия магнитотерапии остаются мало изученными либо подвергаются сомнению [24]. По мнению авторов данной статьи, необходимо исследовать влияние магнитотерапии на созревание и дифференцировку костной мозоли и на динамику венозного давления при дегенеративно-дистрофических заболеваниях суставов.
Заключение
Таким образом, магнитотерапия является высокоэффективным методом для профилактики и комплексного лечения ряда осложнений при скелетной травме, среди которых особое место занимает истинный травматический отёк. Использование магнитотерапии возможно в ранние сроки после травмы в составе комплекса лечебных мероприятий. Особенно актуально использование портативных аппаратов для магнитотерапии у маломобильных пациентов. Целесообразно оснащать травматологические отделения портативными магнитотерапевтическими аппаратами.
Библиографическая ссылка
Кузьманин С.А., Назаров Е.А., Рябова М.Н. ВОЗМОЖНОСТИ МАГНИТОТЕРАПИИ ПРИ ЛЕЧЕНИИ ОСТРОЙ СКЕЛЕТНОЙ ТРАВМЫ // Современные проблемы науки и образования. 2019. № 4. ;URL: https://science-education.ru/en/article/view?id=29093 (дата обращения: 25.04.2026).



