Согласно современным представлениям, распространённый гнойный перитонит (РГП) является одним из тяжёлых проявлений абдоминальной хирургической инфекции, лечение которой должно соответствовать принципам комплексного лечения абдоминального сепсиса [1-3]. Одной из актуальных проблем комплексного лечения РГП, на наш взгляд, является недооценка возможностей диагностики состояния иммунной системы с целью оптимизации хирургической тактики [4-6]. Концептуально исход заболевания при РГП зависит от варианта взаимовлияния воспалительного и противовоспалительного ответов. Благоприятный исход возникает при перекрывании синдрома системного воспалительного ответа (ССВО) и компенсаторного противовоспалительного синдрома с развитием синдрома смешанного антагонистического ответа. Если преобладает ССВО, развиваются полиорганная недостаточность (ПОН) и сепсис с неблагоприятным исходом. Если на первый план выходит компенсаторный противовоспалительный синдром, возникает синдром вторичного иммунодефицита с развитием вторичных очагов инфекции и сепсиса, что также становится причиной смерти больных. В повседневной клинической практике эти процессы можно обнаружить в рутинном общем клиническом анализе крови (ОАК), интерпретируя который, можно выявить различные типы реакции иммунной системы и их характеристики как исходно, так и в динамике заболевания [7-9].
Цель исследования: оценить клиническое значение состояния иммунной системы по данным гемограммы у больных РГП.
Задачи исследования
1. Определить по данным гемограммы показатели «Тип реакции иммунной системы» и «Характеристика типа реакции иммунной системы» у больных РГП исходно и в динамике заболевания.
2. Провести анализ связи исходного показателя «Тип реакции иммунной системы» с полом, возрастом, методом ведения брюшной полости, фазой течения патологического процесса, тяжестью перитонита и общего состояния больного, исходом заболевания.
3. Оценить возможности использования показателей «Тип реакции иммунной системы» и «Характеристика типа реакции иммунной системы» для оптимизации лечебной тактики при РГП.
Материал и методы исследования
Для решения поставленных задач был проведён ретроспективный анализ лечения 152 больных РГП, находившихся на лечении в Красноярской межрайонной клинической больнице скорой медицинской помощи им Н.С. Карповича. Данное исследование было одобрено этическим комитетом ФГБОУ ВО «КрасГМУ им. проф. В.Ф. Войно-Ясенецкого» Минздрава России (выписка из протокола № 89/2019 от 17.04.2019). Больные были в возрасте от 15 до 84 лет, средний возраст составил 52,1±17,9 года. При этом 80 (52,6±4,1%) больных были старше 50 лет. Соотношение мужчин и женщин было, соответственно, 80 (52,6±4,1%) и 72 (47,4±4,1%).
Основными причинами РГП были перфоративные гастродуоденальные язвы [31 (20,4±3,3%) больной], перфорации кишечника [27 (17,8±3,1%) больных], послеоперационный перитонит [27 (17,8±3,1%) больных] и острый аппендицит [22 (14,5±2,9%) больных]. На эти четыре причины пришлось 70,4±3,7% (107 из 152 больных) от всех случаев. Общая летальность составила 36,8±3,9% (56 больных). У 31 (20,4±3,3%) больного было выполнено по одной операции (полузакрытый метод ведения брюшной полости), летальность среди которых составила 9,7±5,3% (3 больных). У 121 (79,6±3,3%) больного выполнялись релапаротомии (РП) как по программе, так и по требованию (полуоткрытый метод ведения брюшной полости; среднее количество операций – 3,5), летальность в данной подгруппе составила 43,8±4,5% (53 больных).
Для определения показателей «Тип реакции иммунной системы» (ТР) и «Характеристика типа реакции иммунной системы» (ХТР) использовали программу для ЭВМ «ПРОТИСТ» (Программа оценки типа реакции иммунной системы; свидетельство о государственной регистрации программы для ЭВМ № 2017619658 от 01.09.2017) [8]. Данная программа позволяет на основании интерпретации ОАК дать предварительную оценку состоянию иммунной системы больного (с выделением уровня реактивности врождённого и адаптивного иммунитета) с определением следующих показателей:
§ ТР: активация адаптивного иммунитета (АА), активация врождённого иммунитета (АВ), инертность адаптивного иммунитета (ИА), ареактивность иммунной системы (Т), угнетение иммунной системы (ИД);
§ ХТР: активация лимфопоэза (АЛ), асимметричная стимуляция гранулопоэза (НЛ), нормореакция (Н), недостаточная активация лимфопоэза (АГ), декомпенсированный лейкопоэз (Д).
ТР рассчитывается из соотношения абсолютного количества гранулоцитов и лимфоцитов и характеризует состояние врождённого и адаптивного иммунитета (пониженное, норма, повышенное). ХТР рассчитывается из соотношения процентного и абсолютного количества лимфоцитов и характеризует механизм реакции костного мозга, формирующий соответствующее состояние иммунной системы.
ТР и ХТР иммунной системы оценивались исходно, до первичной операции по поводу перитонита, а также в динамике заболевания на 1, 3, 5, 7, 10, 15, 20 и 28-е сутки.
Тяжесть РГП оценивали по Мангеймскому индексу перитонита (МИП) и индексу брюшной полости (ИБП; В.С. Савельев с соавт., 1998), тяжесть общего состояния – по шкале SAPS-II, ПОН – по шкале SOFA.
Статистическую обработку данных проводили методами вариационной статистики. Параметрические данные представлены в виде M±σ, непараметрические – Ме (25%; 75%). Относительные частоты представлены со стандартной ошибкой доли (%±S%). Для сравнения несвязанных групп по количественным признакам использован U-критерий Манна-Уитни. Сравнение групп по качественному признаку выполняли с использованием критерия χ² или (при необходимости) двустороннего критерия Фишера. Для исследования взаимосвязи признаков использован метод корреляционного анализа Спирмена. Критический уровень значимости (p) при проверке статистических гипотез в данном исследовании принимался равным 0,05.
Результаты исследования и их обсуждение
Из пяти возможных ТР иммунной системы у исследуемых нами 152 больных РГП исходно были выявлены четыре ТР (таблица 1).
Таблица 1
Исходные типы реакции и характеристики типа реакции иммунной системы у 152 больных РГП
|
ТР |
ХТР |
Количество сочетаний |
Летальность |
Возраст ≥51 года |
Женский пол |
Релапаро- томии |
|
Абс. (%±S%) |
||||||
|
АВ 86 (56,6±4,0) |
Д |
63 (41,4±4,0) |
19/63 (30,2±5,8) |
32/63 (50,8±6,3) |
34/63 (54,0±6,3) |
45/63 (71,4±5,7) |
|
НЛ |
23 (15,1±2,9) |
8/23 (34,8±9,9) |
10/23 (43,5±10,3) |
8/23 (34,8±9,9) |
18/23 (78,3±8,6) |
|
|
ИД 40 (26,3±3,6) |
Д |
36 (23,7±3,4) |
12/36 (33,3±7,9) |
20/36 (55,6±8,3) |
15/36 (41,7±8,2) |
31/36 (86,1±5,8) |
|
АГ |
4 (2,6±1,3) |
1/4 |
3/4 |
1/4 |
4/4 |
|
|
АА 24 (15,8±3,0) |
НЛ |
19 (12,5±2,7) |
10/19 |
9/19 |
10/19 |
17/19 |
|
АЛ |
5 (3,3±1,4) |
4/5 |
4/5 |
3/5 |
4/5 |
|
|
Т 2 (1,3±0,9) |
НЛ |
1 (0,7±0,7) |
1/1 |
1/1 |
1/1 |
1/1 |
|
Н |
1 (0,7±0,7) |
1/1 |
1/1 |
0/1 |
1/1 |
|
|
Все 152 (100,0) |
152 (100,0) |
56/152 (36,8±3,9) |
80/152 (52,6±4,1) |
72/152 (47,4±4,1) |
121/152 (79,6±3,3) |
|
У 86 (56,6±4,0%) больных наблюдался наиболее физиологический ТР «Активация врождённого иммунитета» (АВ). У 40 (26,3±3,6%) больных обнаружен ТР «Угнетение иммунной системы» (ИД). На эти два ТР исходно пришлось 82,9±3,1% всех случав. Другие два ТР: «Активация адаптивного иммунитета» (АА) и «Ареактивность иммунной системы» (Т), исходно выявлены у 24 (15,8±3,0%) и 2 (1,3±0,9%) больных, соответственно.
Анализ распределения больных РГП по показателям ТР/ХТР иммунной системы, исходно и в динамике заболевания, в различных подгруппах позволил выявить ряд закономерностей.
Исходное сочетание ТР «Активация врождённого иммунитета» (АВ) с ХТР «Асимметричная стимуляция гранулопоэза» (НЛ) чаще наблюдалось у мужчин (p=0,039).
При сравнительном анализе подгрупп выживших и умерших больных РГП выявлено уменьшение на 13,3% среди умерших исходного ТР «Активация врождённого иммунитета» (АВ). Кроме того, данный ТР в сочетании с ХТР «Декомпенсированный лейкопоэз» (Д) в подгруппе умерших исходно обнаружен на 11,9% случаев реже, чем среди выживших.
При сравнении подгрупп с исходными ТР «Угнетение иммунной системы» (ИД) и «Активация адаптивного иммунитета» (АА) отмечено увеличение количества больных в фазе сепсиса в первой подгруппе на 10,8%.
При сравнении показателей в зависимости от тяжести перитонита по МИП и ИБП установлено, что в подгруппе больных с МИП ≥ 30 баллов исходно было значимо меньше (p=0,011) больных с ТР «Активация врождённого иммунитета» (АВ) [29/86 (33,7±5,1%) больных], чем больных с ТР «Активация адаптивного иммунитета» (АА) [15/24 (62,5±9,9%) больных]; в подгруппе больных с ИБП ≥ 14 баллов исходно было значимо меньше (p=0,041) больных с ТР «Активация врождённого иммунитета» (АВ) [53/86 (61,6±5,2%) больных], чем больных с ТР «Угнетение иммунной системы» (ИД) [32/40 (80,0±6,3%) больных].
При анализе распределения исходных ТР иммунной системы в зависимости от тяжести ПОН и общего состояния больных выявлена тенденция увеличения (p=0,088) среднего балла по SAPS-II в подгруппе с ТР «Угнетение иммунной системы» (ИД) [30 (20,5; 35,5) баллов] в сравнении с подгруппой с ТР «Активация врождённого иммунитета» (АВ) [25 (17; 33) баллов].
При диагностике исходного типа ТР иммунной системы в зависимости от нозологической причины перитонита обнаружено, что при перфоративных гастродуоденальных язвах ТР «Угнетение иммунной системы» (ИД) встречался на 14,1% случаев больше [10/31 (32,3±8,4%) больных], чем при аппендикулярном перитоните [4/22 (18,2±8,2%) больных]. Кроме того, выявлено значимое уменьшение количества больных (p=0,037) с ТР «Активация врождённого иммунитета» (АВ) при перфорациях кишечника и послеоперационном перитоните [по 13/27 (48,1±9,6%) больных] по сравнению с острым аппендицитом [17/22 (77,3±8,9%) больных].
При анализе связи исходного ТР иммунной системы с различными показателями, в соответствии с одной задач исследования, установлена тенденция (r=0,14; p=0,085) к корреляции с тяжестью общего состояния по шкале SAPS-II.
При оценке состояния иммунной системы на основе определения показателей ТР и ХТР иммунной системы в динамике заболевания (таблица 2) выявлено 11 вариантов их сочетаний.
Таблица 2
Динамика сочетаний ТР/ХТР иммунной системы у больных РГП, абс. (%±S%)
|
Сочетания ТР/ХТР |
Дни с момента первичной операции |
||||||||
|
0 |
1 |
3 |
5 |
7 |
10 |
15 |
20 |
28 |
|
|
n=152 |
n=118 |
n=111 |
n=102 |
n=80 |
n=83 |
n=83 |
n=62 |
n=27 |
|
|
АВ/Д |
63 (41,4±4,0) |
61 (51,7±4,6) |
56 (50,5±4,7) |
39 (38,2±4,8) |
35 (43,8±5,5) |
39 (47,0±5,5) |
21 (25,3±4,8) |
10 (16,1±4,7) |
5 (18,5±7,5) |
|
АВ/НЛ |
23 (15,1±2,9) |
13 (11,0±2,9) |
17 (15,3±3,4) |
22 (21,6±4,1) |
18 (22,5±4,7) |
16 (19,3±4,3) |
15 (18,1±4,2) |
9 (14,5±4,5) |
4 (14,8±6,8) |
|
АВ/Н |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
1 (3,7±3,6) |
|
ИД/Д |
36 (23,7±3,4) |
27 (22,9±3,9) |
21 (18,9±3,7) |
19 (18,6±3,9) |
12 (15,0±4,0) |
9 (10,8±3,4) |
17 (20,5±4,4) |
15 (24,2±5,4) |
10 (37,0±9,3) |
|
ИД/АГ |
4 (2,6±1,3) |
0 |
0 |
0 |
0 |
1 (1,2±1,2) |
0 |
3 (4,8±2,7) |
2 (7,4±5,0) |
|
ИД/Н |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
1 (1,6±1,6) |
0 |
|
АА/НЛ |
19 (12,5±2,7) |
15 (12,7±3,1) |
14 (12,6±3,1) |
16 (15,7±3,6) |
12 (15,0±4,0) |
12 (14,5±3,9) |
10 (12,0±3,6) |
7 (11,3±4,0) |
2 (7,4±5,0) |
|
АА/АЛ |
5 (3,3±1,4) |
2 (1,7±1,2) |
0 |
3 (2,9±1,7) |
1 (1,3±1,3) |
1 (1,2±1,2) |
3 (3,6±2,0) |
3 (4,8±2,7) |
0 |
|
Т/НЛ |
1 (0,7±0,7) |
0 |
2 (1,8±1,3) |
2 (2,0±1,4) |
1 (1,3±1,3) |
2 (2,4±1,7) |
5 (6,0±2,6) |
3 (4,8±2,7) |
2 (7,4±5,0) |
|
Т/Н |
1 (0,7±0,7) |
0 |
1 (0,9±0,9) |
1 (1,0±1,0) |
1 (1,3±1,3) |
3 (3,6±2,0) |
11 (13,3±3,7) |
10 (16,1±4,7) |
1 (3,7±3,6) |
|
Т/АГ |
0 |
0 |
0 |
0 |
0 |
0 |
1 (1,2±1,2) |
1 (1,6±1,6) |
0 |
Наиболее клинически значимыми, на наш взгляд, являются 3 сочетания ТР/ХТР иммунной системы (рисунки 1-3): ТР «Активация врождённого иммунитета» (АВ) с ХТР «Декомпенсированный лейкопоэз» (Д), ТР «Угнетение иммунной системы» (ИД) с ХТР «Декомпенсированный лейкопоэз» (Д) и ТР «Ареактивность иммунной системы» (Т) с ХТР «Нормореакция» (Н).
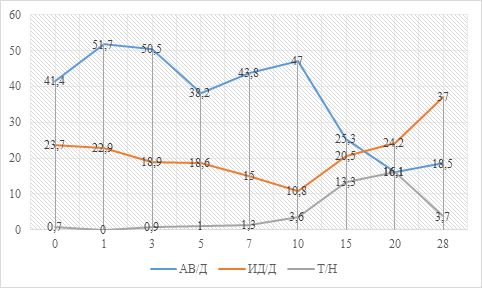
Рис. 1. Общая динамика клинически значимых вариантов сочетаний ТР/ХТР иммунной системы у больных РГП, % количества больных
Согласно данным таблицы 2 и рисунка 1, количество больных с сочетанием АВ/Д значимо уменьшилось (относительно данных исходно и на 1, 3, 5, 7 и 10-е сутки) на 15-е (p≤0,014) и 20-е сутки (p≤0,003).
Количество больных с сочетанием ИД/Д с 36/152 (23,7±3,4%) исходно, к 10-му дню достигло минимального значения 9/83 (10,8±3,4%) (p=0,017), вернулось к исходному уровню на 20-е сутки [15/62 (24,2±5,4%); p=0,032)], а на 28-е сутки увеличилось до 10/27 (37,0±9,3%).
Иная динамика выявлена относительно сочетания Т/Н. Количество таких больных исходно и до 10-х суток было от 0 до 3/83 (3,6±2,0%) на 10-е сутки, затем на 15-е сутки значимо увеличилось до 11/83 (13,3±3,7%) (p=0,026, относительно 10 суток), на 20-е сутки – до 10/62 (16,1±4,7%), вернувшись к 28-м суткам к исходному показателю [1/27 (3,7±3,6%)].
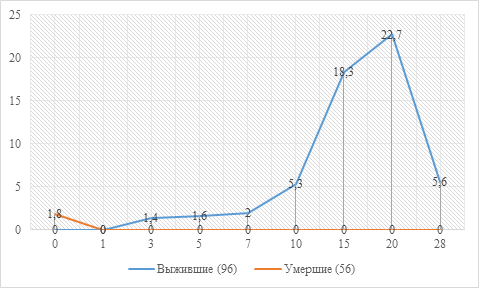
Рис. 2. Сравнительная характеристика динамики сочетания ТР «Ареактивность иммунной системы» (Т) с ХТР «Нормореакция» (Н) у больных РГП в зависимости от исхода заболевания, % количества больных
При сравнительном анализе динамики количества больных с сочетанием Т/Н в зависимости от исхода заболевания установлено, что вышеописанная динамика характерна только для подгруппы больных с благоприятным исходом (рисунок 2) (на 15-е сутки p=0,030; на 20-е сутки p=0,027). При этом максимальное количество больных с таким сочетанием ТР/ХТР [10/44 (22,7±6,3%)] в данной подгруппе наблюдалось на 20-е сутки.
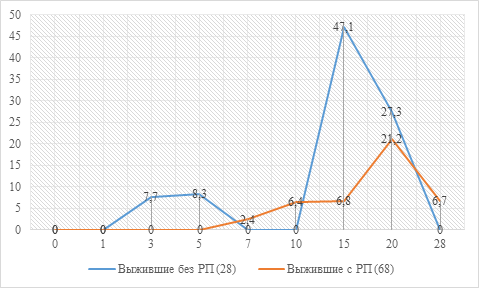
Рис. 3. Сравнительная характеристика динамики сочетания ТР «Ареактивность иммунной системы» (Т) с ХТР «Нормореакция» (Н) у больных РГП с благоприятным исходом заболевания в зависимости от метода ведения брюшной полости, % количества больных
Кроме того, обнаружена значимая зависимость динамики сочетания Т/Н у больных с благоприятным исходом заболевания в зависимости от метода ведения брюшной полости. В подгруппе больных с полузакрытым ведением брюшной полости «пик» данного сочетания ТР/ХТР приходится на 15-е сутки с момента выполнения первичной операции по поводу перитонита [8/17 (47,1±12,1%)], а при полуоткрытом ведении – на 20-е сутки [7/33 (21,2±7,1%)]. При этом на 15-е сутки различия по данному показателю в сравниваемых подгруппах являются значимыми (p<0,001).
Заключение
Таким образом, на основе анализа гемограммы исходно и в динамике заболевания у больных РГП выявляются различные «Типы реакции иммунной системы», «Характеристики типа реакции иммунной системы» и их сочетания. При этом в процессе лечения у больных РГП эти показатели многократно изменяются в зависимости от влияния многих факторов, что потенциально может быть использовано для прогноза осложнений и исхода заболевания, выявления наиболее уязвимой категории больных, в том числе требующей углублённого иммунологического исследования, планирования хирургической тактики, оптимизации лечебной программы, включая персонифицированную иммунокоррекцию.
Библиографическая ссылка
Борисов Р.Н., Бердников Д.С., Шрейдер Л.В., Здзитовецкая Н.Д., Чухломин Н.В., Будаев Г.С., Круглова О.С., Толстокорова Ю.А. КЛИНИЧЕСКОЕ ЗНАЧЕНИЕ ОЦЕНКИ ТИПОВ РЕАКЦИИ ИММУННОЙ СИСТЕМЫ ПРИ РАСПРОСТРАНЁННОМ ГНОЙНОМ ПЕРИТОНИТЕ // Современные проблемы науки и образования. 2019. № 3. ;URL: https://science-education.ru/en/article/view?id=28905 (дата обращения: 26.04.2026).



