Ультразвуковое исследование грудной клетки все активнее используется в диагностике заболеваний легких и плевры. Доступность и мобильность ультразвуковых сканеров, простота выполнения и безвредность метода позволяют применять его в клинической практике без существенных ограничений. Как правило, УЗИ используется для выявления плеврального выпота и примерного определения его объема, значительно реже – для диагностики воспалительных или опухолевых процессов в легких [1, 2].
Основным препятствием для визуализации патологии грудной полости является нормальная легочная ткань, полностью отражающая ультразвуковые волны [3]. Воздушное легкое имеет вид тонкой, подвижной при дыхании гиперэхогенной линии вдоль внутренней поверхности межреберий, названной в зарубежной литературе плевральной линией, хотя основной вклад в ее возникновение вносит отражение от воздуха в субплевральных альвеолах [4]. Париетальная плевра хорошо дифференцируется при плевральном выпоте как пристеночная тонкая гиперэхогенная линия. Висцеральная плевра в виде аналогичной тонкой эхогенной линии на поверхности легкого видна только при потере воздушности легочной ткани, когда ее не перекрывает интенсивный эхосигнал от воздуха [5].
Сам плевральный выпот со всеми находящимися в нем структурами представляет собой идеальную среду для ультразвукового сканирования. В большинстве случаев объектами исследования являются метастатические очаги на плевре, эхокартина которых хорошо изучена и неоднократно представлена в литературных источниках [5, 6]. Другим частым компонентом плеврального выпота являются фибриновые наложения на плевре, возникающие при серозно-фибринозных плевритах и имеющие достаточно разнообразную ультразвуковую семиотику [7]. Иногда они могут имитировать первичные или вторичные опухоли плевры, и для их дифференцировки может успешно применяться УЗИ с контрастированием, поскольку фибриновые массы не содержат сосудов, которые хорошо визуализируются в опухолях при данной методике исследования [8].
В практической работе мы встретились еще с одним объектом на плевре, который требовал дифференцировки от метастатического поражения. Это скопления нормальной жировой ткани в передних отделах плевральной полости, которые торакальные хирурги часто обнаруживают во время операций. Интраоперационно они не вызывают никаких диагностических проблем, но при трансторакальном УЗИ могут являться источником диагностических ошибок, в первую очередь гипердиагностики метастазов. Такие жировые элементы являются аналогами хорошо известных жировых подвесков (appendix epiploica) на ободочной кишке, но в отечественной и зарубежной медицинской литературе сведений об их ультразвуковой семиотике и дифференциальной диагностике с метастазами не найдено.
Цель исследования: с помощью оригинальной методики ультразвукового исследования переднего реберно-диафрагмального синуса и медиастинальной плевры при плевральном выпоте изучить эхосемиотику жировых подвесок и метастазов на плевре и разработать их дифференциальную диагностику.
Материал и методы исследования
На базе торакального хирургического отделения ГБУЗ НО «Городская клиническая больница № 5» г. Нижнего Новгорода в 2014–2016 гг. обследованы 114 пациентов, у которых при УЗИ грудной клетки на фоне плеврального выпота различной этиологии впервые выявлены очаговые образования на плевре. По данным комплексного клинико-инструментального исследования у 58 (50,9%) больных диагностирован экссудативный пара- или постпневмонический плеврит, у 31 (27,2%) – метастатический плеврит с первичной локализацией опухоли в легком, молочной железе или желудке, у 19 (16,6%) – гидроторакс вследствие хронической сердечной недостаточности, у 6 (5,3%) – при циррозе печени.
По морфологическому строению плевральные образования являлись жировыми подвесками или метастазами, в зависимости от чего выделены 2 группы больных. В первую группу включены 83 пациента с жировыми подвесками, из них 47 (56,6%) женщин и 36 (43,4%) мужчин в возрасте от 23 до 78 лет, средний возраст 42,5 года; во вторую – 31 пациент с метастазами, из них – 18 (58,1%) мужчин и 13 (41,9%) женщин в возрасте от 48 до 76 лет, средний возраст 58,7 года. Очаги верифицированы на основании комплексного клинико-инструментального обследования с цитологическим исследованием плеврального пунктата и динамического наблюдения, у 24 пациентов – по данным видеоторакоскопии с биопсией и у 3 больных с хронической сердечной недостаточностью – по данным аутопсии.
Трансторакальное УЗИ выполнено на ультразвуковых сканерах среднего класса производства Esaote (Италия) и Medison (Южная Корея) секторным (3,5 МГц) и конвексным (2–6 МГц) датчиками на абдоминальной программе сканирования. Обследование проводили в положении пациента стоя или сидя при межреберном сканировании, перемещая датчик от нижних межреберий к верхним. При осмотре задних отделов плевральной полости пациент клал руку на противоположное плечо, отводя лопатку вперед, а для исследования аксиллярной области поднимал руку за голову [9]. Плевральный выпот и листки плевры последовательно визуализировались по задней, боковой и передней поверхности грудной клетки с обязательным осмотром передних реберно-диафрагмальных синусов, прилежащих к ним отделов диафрагмальной плевры и медиастинальной плевры вдоль поверхности сердца по разработанной и запатентованной оригинальной методике.
В соответствии с ней выпот в переднем реберно-диафрагмальном плевральном синусе сначала сканировали продольно по парастернальной линии из межреберья над реберной дугой перпендикулярно грудной стенке. Для визуализации медиастинальной плевры вдоль правых отделов сердца плоскость сканирования направляли медиально за грудину. Затем смещали датчик вниз и устанавливали субкостально параллельно реберной дуге с краниальным наклоном. Покачивая датчик вверх-вниз, осматривали заполненное выпотом пространство синуса и листки плевры на его фоне [10]. Осмотр медиастинальной плевры слева выполняли сначала в продольной плоскости из IV и V межреберий по парастернальной линии, затем смещали датчик латерально до среднеключичной линии, направляя плоскость сканирования к сердцу и разворачивая датчик в стандартное четырехкамерное сечение для более полного осмотра поверхности верхушки и левого желудочка [11].
Изображение в виде отдельных кадров или кинопетли архивировалось на жесткий диск прибора или записывалось на видеомагнитофон и оцифровывалось компьютерной программой Pinnacle Studio Ultimate 12.1 с последующим изучением полученных видеофайлов на персональном компьютере.
Результаты исследования и их обсуждение
Жировые подвески представляют собой нормальные анатомические образования на плевре. Это обычная жировая ткань, расположенная интраплеврально в виде отдельных элементов или массивных скоплений (рис. 1). При отсутствии плеврального выпота они прижимаются воздушным легким к медиастинальной или диафрагмальной плевре и не дифференцируются из-за полного отражения ультразвуковых волн от воздуха в субплевральных альвеолах. Однако даже небольшое количество жидкости, окружавшей эти жировые образования, позволяло отслоить их от воздушной легочной ткани и сделать эхографически видимыми.
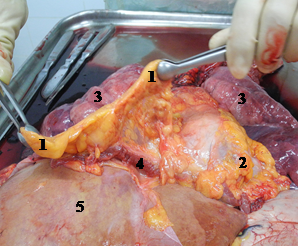
Рис. 1. Жировые подвески в переднем реберно-диафрагмальном плевральном синусе (1) и на медиастинальной плевре (2), легкие (3), правый купол диафрагмы (4), печень (5)
У всех пациентов очаговые образования на плевре обнаружены на фоне плеврального выпота, объем которого варьировал от 50 мл до 2,5 л. Для выявления жировых подвесок в переднем реберно-диафрагмальном плевральном синусе достаточно скопления в нем 20–30 мл жидкости, тогда как при поиске метастазов для эффективного осмотра всех листков плевры объем выпота должен быть не менее 800–1000 мл. Правосторонний плевральный выпот различного объема выявлен у 42 (50,6%) пациентов с жировыми подвесками и у 15 (48,4%) – с метастазами на плевре, левосторонний – у 25 (30,1%) и 12 (38,7%), двусторонний – у 16 (19,3%) и 4 (12,9%) больных соответственно.
В результате сравнительного анализа эхокартины жировых подвесок и метастазов на плевре разработаны критерии их дифференциальной диагностики.
1. Локализация. Все жировые подвески располагались в передних отделах плевральной полости, справа чаще, чем слева – у 48 (57,8%) и у 28 (33,8%) больных, двусторонние – у 7 (8,4%) пациентов. Сочетанная локализация в переднем реберно-диафрагмальном плевральном синусе и на медиастинальной плевре выявлена у 27 (32,5%) пациентов (из них у 14 – справа, у 9 – слева, у 4 – двусторонние), изолированное расположение только в синусе – у 33 (39,8%) пациентов (из них у 26 – справа, у 7 – слева), только на медиастинальной плевре – у 23 (27,7%) больных (из них у 8 – справа, у 12 – слева, у 3 – двусторонние). У 2 пациентов жировые подвески были выявлены дополнительно на костальной плевре по передней поверхности грудной стенки несколько выше уровня плеврального синуса. Избирательная локализация подвесок на плевре обусловлена, видимо, анатомическими особенностями накопления жировой ткани, подобно тому, как в брюшной полости жировые подвески концентрируются преимущественно на ободочной кишке.
Метастазы во всех случаях были множественными и лоцировались на двух и более листках плевры, чаще на диафрагмальной и костальной (у 25 и 20 больных соответственно), реже на висцеральной (у 11 больных). Расположение очагов на медиастинальной плевре установлено у 3 больных, в переднем плевральном синусе – у 1 пациента, однако во всех случаях, кроме них, метастазы были выявлены и на других листках плевры. Изолированных метастазов только на медиастинальной плевре или в переднем плевральном синусе, а также их сочетанного поражения без вовлечения других отделов плевры не отмечено.
2. Передаточная подвижность. Для жировых подвесков на плевре характерна выраженная передаточная смещаемость, обусловленная их мягкой консистенцией. У жировых элементов в переднем реберно-диафрагмальном синусе это выражалось в плавных, синхронных с дыханием качательных движениях вследствие дыхательного смещения диафрагмы, а у очагов на медиастинальной плевре – в резких толчкообразных колебаниях при сокращениях сердца. Плотные метастазы с низкой эластичностью жестко фиксированы на плевре и не имели передаточной смещаемости, даже при локализации на медиастинальной плевре по контуру сердца. Они смещались вместе с сердцем единым целым, не совершая собственных дополнительных колебательных движений.
3. Эхогенность и эхоструктура. Крупные жировые подвески (более 1–2 см) имели типичное для жировой ткани строение – среднюю эхогенность с множественными линейными гиперэхогенными включениями, создававшими неоднородную дольчатую структуру, подобную изображению паранефральной клетчатки. Мелкие дольки были более однородными и эхогенными, они чаще лоцировались на медиастинальной плевре по контуру сердца. Метастазы независимо от размеров имели однородное гипоэхогенное строение. Оценивая эхогенность любых очаговых образований на плевре, необходимо учитывать толщину предлежащего слоя жидкости, поскольку за ней неизбежен артефакт дистального псевдоусиления, который повышает эхогенность всех расположенных позади него структур.
4. Размеры и форма. У всех пациентов с сочетанной локализацией жировых подвесок на медиастинальной плевре и в переднем плевральном синусе наблюдались очаги различного размера и формы, что зависело от их расположения. Представленная ниже закономерность сохранялась и при изолированной локализации жировых элементов в этих местах плевральной полости. Жировые подвески на медиастинальной плевре по контуру сердца, как правило, имели округлую, овальную или треугольную форму и примерно одинаковые размеры – 10–15 мм в диаметре (рис. 2а). С увеличением размеров до 20–25 мм их форма становилась более вытянутой, эхоструктура приобретала выраженную дольчатость, увеличивалась передаточная смещаемость при сердцебиении. Жировые подвески в переднем плевральном синусе длиной до 5 см имели вертикально ориентированную вытянутую овальную или грушевидную форму с узким основанием в глубине синуса и краниальным расширением за его пределами (рис. 2б). Единичные жировые подвески большей длины (до 7–8 см при толщине до 1–1,5 см) приобретали характерную булавовидную или лентовидную форму, распространялись из плеврального синуса вверх и плавно смещались при дыхании. Подобную картину мы наблюдали у 12 пациентов, и она не вызвала диагностических трудностей. Метастазы имели округлую или уплощенную форму с широким основанием (рис. 3).
5. Количество. Жировые подвески на медиастинальной плевре в подавляющем большинстве были множественными, расположенными вплотную друг к другу, местами сливавшимися в единую структуру неравномерной толщины с выраженной передаточной смещаемостью при сердцебиении. Только у одного пациента отмечена единичная крупная жировая подвеска на боковой поверхности левого желудочка. Жировые подвески, исходившие из глубины переднего плеврального синуса, чаще были единичными (у 22 больных), реже – множественными (11 больных), и тогда они располагались по отдельности или в виде скоплений на разном уровне по переднему скату диафрагмы. Метастазы всегда были множественными, хаотично распределенными на разных листках плевры.
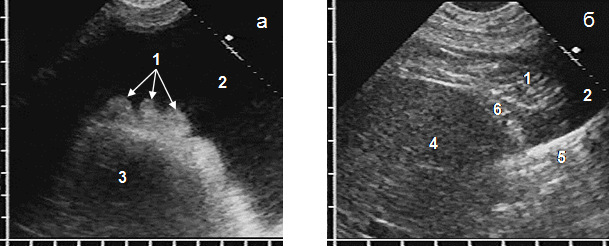
Рис. 2. Эхограммы жировых подвесок на медиастинальной плевре по контуру левых отделов сердца (а) и в правом переднем реберно-диафрагмальном синусе (б): жировые подвески (1), плевральный выпот (2), левый желудочек (3), печень (4), легкое (5), диафрагма (6)
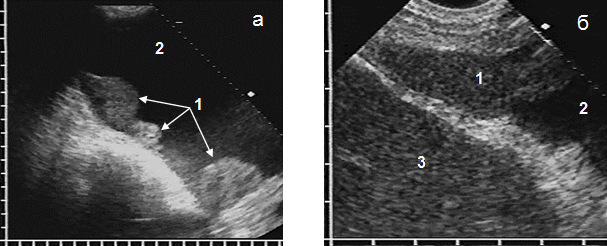
Рис. 3. Эхограммы метастазов на диафрагмальной и висцеральной плевре (а) и в правом переднем реберно-диафрагмальном синусе (б): метастаз (1), выпот (2), печень (3)
Выводы
УЗИ грудной клетки является доступным высокоинформативным радиологически безопасным методом дифференциальной диагностики жировых подвесок и метастазов на плевре. Для жировых подвесок характерны локализация в переднем плевральном синусе и/или на медиастинальной плевре по контуру сердца, выраженная передаточная смещаемость при дыхании или сердцебиении, дольчатая среднеэхогенная структура и вытянутая форма с узким основанием, особенно при локализации в переднем реберно-диафрагмальном синусе плевры. Для метастазов характерны различная локализация на двух и более листках плевры, чаще на костальной и диафрагмальной, жесткая фиксация на плевре без передаточной смещаемости, однородная гипоэхогенная структура, округлая или уплощенная форма с широким основанием. Разработанный нами симптомокомплекс позволит избежать диагностических ошибок, особенно гипердиагностики метастазов, и правильно и своевременно определять генез очаговых образований на плевре.



