Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
RECURRENCE OF THE UTERINE LEIOMYOMA IN WOMEN: FREQUENCY AND PROGNOSIS
Органосохраняющее лечение самого распространенного доброкачественного новообразования у женщин – лейомиомы (миомы) матки – на сегодняшний день приобрело широкое распространение во всем мире. Такая тактика вызвана омоложением самого заболевания, необходимостью для женщины реализовать репродуктивную функцию или просто желанием сохранить детородный орган, тем самым улучшив качество своей жизни. Уменьшение роста опухоли сегодня достигается разными методами – медикаментозными и хирургическими. Среди хирургических методов наибольшую популярность приобрела миомэктомия, которая выполняется в основном с помощью лапароскопии, гистероскопии или открытым лапаротомным доступом. По мнению многих авторов, удалением опухоли не устраняется ее причина, которая до сих пор не известна, а значит, всегда существует риск рецидива [1, 2]. По данным разных авторов, частота рецидивирования опухоли после миомэктомии колеблется от 4,9% и до 62,0% [3, 4] и зависит от множества факторов – возраста больной [3, 5], наследственности [6], количества миоматозных узлов [2, 6], размера матки [7, 8], хронических воспалительных гинекологических заболеваний [5, 9], некоторых соматических заболеваний [7, 8], назначения гормональных средств в предоперационном периоде (гонадотропин-рилизинг-гормон) [10]. Имеются сведения о том, что для рецидива миомы матки имеют значение зоны роста, оставшиеся в месте энуклеации узла и в окружающем миометрии [1]. По мнению большинства исследователей, роды после миомэктомии существенно снижают риск ее повторного роста [4, 8]. В Кыргызской республике официальные сведения о частоте заболеваемости миомой матки отмечаются лишь с 2011 г. и свидетельствуют о ее росте. В 2011 г. Республиканский медико-информационный центр Кыргызской республики отметил удельный вес заболеваемости миомой матки 14,1%, а в 2016 г. – 19,9%. Таким образом, в связи с широким распространением органосохраняющих методов лечения миомы матки вопросы частоты возникновения рецидива заболевания, прогностических факторов и сроков повторного роста опухоли представляются весьма актуальной проблемой.
Цель: определить частоту и выявить прогностические факторы повторного роста миомы после миомэктомии.
Материалы и методы исследования
Проведено ретроспективное изучение анамнеза женщин, обратившихся в КНЦРЧ впервые и повторно по поводу миомы матки за период 2010–2017 гг.
В качестве факторных рассматривался 21 признак: возраст, вес, семейное положение, наличие занятости, родов, абортов, самопроизвольных выкидышей, неразвивающихся беременностей, наличие кистозных образований придатков матки в анамнезе, хронические воспалительные заболевания органов малого таза, нарушения менструального цикла, псевдоэрозии шейки матки, перенесенные оперативные вмешательства на органах малого таза, заболевания мочевыделительной системы, заболевания органов дыхания, заболевания со стороны сердечно-сосудистой системы, желудочно-кишечного тракта, сосудов, заболевания эндокринной системы, заболевания крови, заболевания органов зрения.
Анамнестические данные были выделены из первичной учетно-отчетной документации (истории болезни гинекологического стационара 003-1/у) со слов женщин и по результатам обследования до проведения миомэктомии.
Всего в исследование вошли 146 историй болезней женщин, перенесших миомэктомию в КНЦРЧ, 15 из которых в течение последующих 7 лет была произведена гистерэктомия по поводу повторно развившейся симптомной миомы. Миомэктомия проводилась открытым лапаротомным доступом.
Статистическая обработка полученных данных. Для выявления влияния факторных признаков, связанных с риском рецидива, был использован метод построения многофакторных логистических регрессионных моделей [1]. Для логистической модели регрессии прогнозируемый признак является бинарным и принимает только два значения: «True» («случай» – 1, рецидив) и «False» («не случай» – 0, отсутствие рецидива). Для построения модели проводится логит-преобразование:
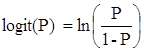 , (1)
, (1)
здесь P – вероятность «случая». Математическая модель может быть представлена уравнением:
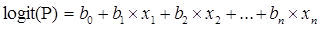 , (2)
, (2)
где xi – значение i-го (i=1, …, n) факторного признака, bi (i=1, …, n) – соответствующий коэффициент в модели. Для оценки адекватности модели использовался метод анализа кривых операционных характеристик (ROC – Receiver Operating Characteristic curve analysis) [11], при этом рассчитывались площадь под ROC-кривой (AUC – Area under the ROC curve) [1002] и ее 95%-ный доверительный интервал (95%-ный ДИ). Величина AUC может быть интерпретирована как вероятность того, что при анализе «случая» значение 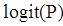 будет выше, чем для «не случая». Модель считается адекватной при статистически значимом отличии величины AUC от величины 0,5. При проведении анализа ROC-кривой выбирается оптимальное значение порога принятия/отвержения модели, для которого определяются ее чувствительность и специфичность (также проводился расчет их 95%-ного ДИ). Для оценки степени связи факторных признаков с результирующим рассчитывается значение показателя отношения шансов (ОШ, 95%-ный ДИ). ОШ (для данного факторного признака) дает отношение шансов
будет выше, чем для «не случая». Модель считается адекватной при статистически значимом отличии величины AUC от величины 0,5. При проведении анализа ROC-кривой выбирается оптимальное значение порога принятия/отвержения модели, для которого определяются ее чувствительность и специфичность (также проводился расчет их 95%-ного ДИ). Для оценки степени связи факторных признаков с результирующим рассчитывается значение показателя отношения шансов (ОШ, 95%-ный ДИ). ОШ (для данного факторного признака) дает отношение шансов 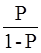 (где P – вероятность «случая») при изменении факторного признака на 1 единицу. При ОШ>1 риск «случая» увеличивается при увеличении значения факторного признака, при ОШ<1 риск «случая» снижается при увеличении значения факторного признака (если ОШ статистически значимо не отличается от 1, то нельзя сделать вывод о наличии связи факторного и результирующего признаков).
(где P – вероятность «случая») при изменении факторного признака на 1 единицу. При ОШ>1 риск «случая» увеличивается при увеличении значения факторного признака, при ОШ<1 риск «случая» снижается при увеличении значения факторного признака (если ОШ статистически значимо не отличается от 1, то нельзя сделать вывод о наличии связи факторного и результирующего признаков).
Результаты и их обсуждение
Из 1692 женщин, обратившихся в КНЦРЧ за исследуемый период по поводу миомы матки, требующей хирургического лечения, 146 была произведена органосохраняющая операция миомэктомия, что составило 8,6%.
Из 146 прооперированных больных лейомиома, требующая оперативного лечения, развилась повторно за период 7 лет у 15 женщин, что составило 10,3%.
При сравнении полученных результатов с литературными данными можно отметить заметную разницу в выявляемой авторами частоте рецидива: от 4,9% в течение 2 лет [3] до 62,0% в течение 5 лет после миомэктомии [4]. Полученные данные согласуются с клиническим руководством SOGC [8], в котором указано, что частота рецидива миомы матки составляет 15,0%, а 10,0% больных нуждаются в повторной операции в течение 5–10 лет. Учитывая, что подобное исследование впервые проведено в Кыргызской республике, можно предположить более высокий уровень частоты рецидива миомы матки, для определения которого необходимы дальнейшие проспективные исследования.
Средний возраст пациенток, вошедших в исследование, составил 36,7±5,5 лет. Средняя масса тела – 65,0±10,9 кг. Все вошедшие в исследование женщины были азиатской национальности.
Из 15 повторно обратившихся в клинику больных рецидив миомы матки, подлежащий оперативному лечению, был отмечен у 2 пациенток через 1 год после миомэктомии, у 5 пациенток – через 2 года, у 3 – через 4 года и у 5 – через 5 лет.
Минимальный период повторного роста опухоли, требующей оперативного лечения, составил 1 год, а максимальный – 5 лет.
Факторными признаками послужили данные осмотра и анамнеза больных перед проведением миомэктомии.
Из 146 пациенток 71,9% (n=105) состояли в браке, 36,3% (n=53) работали, у 56,8% (n=83) в анамнезе были самопроизвольные роды, у 42,5% (n=62) – артифициальные аборты, у 16,4% (n=24) – самопроизвольные выкидыши, у 4,1% (n=6) – замершие беременности и у 41,1% (n=60) в анамнезе беременностей не было.
Из гинекологических заболеваний у 21,2% (n=31) в анамнезе были диагностированы кистозные изменения яичников, 27,4% (n=40) страдали хроническими воспалительными заболеваниями органов малого таза, нарушения менструального цикла отмечали 4,1% (n=6) пациенток, эрозия и эктропион шейки матки отмечали 13,0% (n=19) женщин и 13,0% (n=19) сообщили о перенесенных гинекологических операциях на придатках.
Из соматических заболеваний при первичном обращении отмечены заболевания: желудочно-кишечного тракта в 16,4% (n=24), крови (железодефицитные анемии) в 14,4% (n=21), мочевыделительной системы в 9,6% (n=14), органов дыхания в 7,5% (n=11), системы кровообращения в 6,8% (n=10), эндокринной системы в 4,8% (n=7), органов зрения в 1,4% (n=2).
Прогностические факторы развития рецидива миомы матки представлены в таблице 1.
На первом этапе анализа из всех представленных в таблице признаков выявлены лишь два, которые связаны с риском рецидива: хронические воспалительные заболевания органов малого таза (ХВЗОМТ) и перенесенные оперативные вмешательства на придатках матки. Установлено, что при наличии ХВЗОМТ риск рецидива возрастает (p=0,02), ОШ=3,50 (95%-ный ДИ 1,18–10,4) по сравнению с отсутствием заболевания. Выявлено также повышение (p=0,046) риска рецидива при наличии перенесенных оперативных вмешательств, ОШ=3,02 (95%-ный ДИ 1,02–8,92) по сравнению с отсутствием операций.
Таблица 1
Прогностические факторы развития рецидива миомы матки (однофакторная логистическая модель регрессии)
|
Факторный признак |
Коэффициент модели, b±m |
Уровень значимости отличия коэффициента от 0, p |
Показатель отношения шансов, ОШ (95% ДИ) |
|
Возраст |
0,069±0,053 |
0,20 |
1,07 (0,96–1,19) |
|
Вес |
–0,035±0,029 |
0,23 |
0,97 (0,91–1,02) |
|
Семейное положение |
0,39±0,41 |
0,33 |
1,49 (0,47–3,29) |
|
Работает |
–0,015±0,58 |
0,80 |
0,86 (0,28–2,68) |
|
Роды в анамнезе |
–0,01±0,28 |
0,98 |
0,99 (0,57–1,73) |
|
Артифициальные аборты в анамнезе |
0,72±0,59 |
0,22 |
2,06 (0,65–6,56) |
|
Выкидыши в анамнезе |
0,32±0,52 |
0,53 |
1,38 (0,50–3,84) |
|
Замершие беременности в анамнезе |
0,56±1,13 |
0,62 |
1,76 (0,19–16,1) |
|
Кистозные образования придатков в анамнезе |
0,32±0,62 |
0,61 |
1,37 (0,41–4,66) |
|
Хронические воспалительные заболевания органов малого таза |
1,25±0,56 |
0,02* |
3,50 (1,18–10,4) |
|
Нарушения менструального цикла |
1,58±0,91 |
0,08 |
4,84 (0,81–29,1) |
|
Псевдоэрозии шейки матки |
0,59±0,70 |
0,40 |
1,80 (0,46–7,06) |
|
Перенесенные оперативные вмешательства на органах малого таза |
1,10±0,55 |
0,046* |
3,02 (1,02–8,92) |
|
Заболевания мочевыделительной системы |
–0,67±1,07 |
0,53 |
0,51 (0,06–4,17) |
|
Заболевания органов дыхания |
0,86±0,84 |
0,31 |
2,37 (0,45–12,3) |
|
Заболевания системы кровообращения |
0,52±0,82 |
0,53 |
1,67 (0,33–8,42) |
|
Заболевания желудочно-кишечного тракта |
–0,22±0,80 |
0,79 |
0,81 (0,17–3,84) |
|
Заболевания эндокринной системы |
0,40±1,12 |
0,72 |
1,49 (0,17–13,3) |
|
Заболевания крови |
–0,10±0,80 |
0,90 |
0,91 (0,19–4,34) |
|
Заболевания органов зрения |
–17,6±1000 |
0,99 |
– |
На втором этапе анализа была предпринята попытка выделения набора факторных признаков, связанных с риском рецидива, для чего был использован метод построения и анализа многофакторной модели логистической регрессии. Отбор наиболее значимых факторов (из 21 анализируемого признака) проводился с использованием метода пошагового включения/исключения переменных (Stepwise, при пороге включения p<0,1 и пороге исключения p>0,3). При проведении отбора было выделено 3 признака, тесно связанных с риском рецидива: наличие артифициальных абортов в анамнезе, ХВЗОМТ и перенесенные оперативные вмешательства на органах малого таза. На выделенном наборе признаков была построена трехфакторная модель прогнозирования риска рецидива, модель адекватна (χ2-квадрат=11,8 при 3 степенях свободы, p=0,008). На рисунке 1 представлена кривая операционных характеристик модели. Площадь под ROC-кривой модели AUC=0,73 (95%-ный ДИ 0,65–0,80), что свидетельствует о хорошем качестве модели и позволяет говорить о средней степени связи таких факторов, как артифициальные аборты в анамнезе, ВЗОМТ и перенесенные оперативные вмешательства на органах малого таза с риском рецидива.
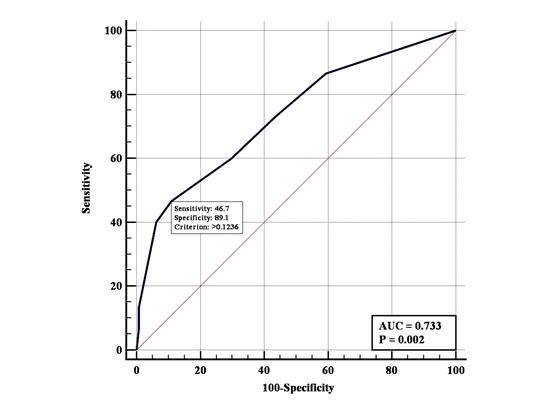
Рис. 1. ROC-кривая 3-факторной логистической модели прогнозирования риска рецидива
При проведении многофакторного анализа (табл. 2) выявлены три признака, тесно связанных с риском рецидива: наличие в анамнезе артифициальных абортов, ХВЗОМТ и гинекологических операций. Установлено, что при наличии ХВЗОМТ риск рецидива возрастает (p=0,01), ОШ=4,56 (95%-ный ДИ 1,3–15,6) по сравнению с отсутствием заболевания (при стандартизации по другим факторам риска). Выявлено повышение (p=0,05) риска рецидива при наличии перенесенных оперативных вмешательств на органах малого таза ОШ=3,0 (95%-ный ДИ 1,0–9,4) по сравнению с отсутствием операции (при стандартизации по другим факторам риска). Выявлена также тенденция к увеличению риска рецидива при наличии 2 и более абортов в анамнезе (p=0,08). При выборе оптимального порога принятия/отвержения чувствительность модели составила 46,7% (95%-ный ДИ 21,3–73,4%), специфичность модели – 89,1% (95%-ный ДИ 82,3–93,9%).
Таблица 2
Анализ факторов риска рецидивов (3-факторная логистическая модель регрессии)
|
Факторный признак |
Коэффициент модели, b±m |
Уровень значимости отличия коэффициента от 0, p |
Показатель отношения шансов, ОШ (95%-ный ДИ) |
|
Артифициальные аборты в анамнезе |
1,20±0,67 |
0,08 |
3,3 (0,9–12,5) |
|
Хронические воспалительные заболевания органов малого таза |
1,52±0,62 |
0,01* |
4,6 (1,3–15,6) |
|
Перенесенные оперативные вмешательства на органах малого таза |
1,11±0,57 |
0,05* |
3,0 (1,0–9,4) |
«Факторы риска не обязательно совпадают с прогностическими факторами, причем для одного и того же заболевания эти факторы могут быть совершенно разными» [12]. Выявленные в настоящем исследовании факторы можно отнести к менее значимым в отношении риска возникновения миомы матки, а в отношении прогноза ее рецидива их значимость возрастает. Полученные результаты согласуются лишь с незначительным количеством литературных данных. Так, некоторые авторы отмечают связь рецидивирования миомы с формированием послеоперационного спаечного процесса [9]. В работе Adebiyi G. Adesiyun [9] отмечено влияние воспалительных заболеваний органов малого таза на процесс формирования спаек у категории больных после миомэктомии. Исходя из этого можно предположить, что предшествующие ХВЗОМТ и оперативные вмешательства в малом тазу, способствующие развитию спаек, еще более усугубляют спаечный процесс после миомэктомии, как и после любого оперативного вмешательства, и поэтому являются прогностически неблагоприятными факторами.
В обзоре Radmila Sparic et al. [13] имеются сведения о том, что инфекция и травмы матки, которыми могут быть артифициальные аборты, стимулируют зоны роста опухоли. Неупорядоченный процесс заживления и образование спаечного процесса являются факторами риска образования самой миомы, не говоря уже о ее рецидиве после дополнительного оперативного вмешательства (миомэктомии). Имеются достаточно интересные сведения литературы, указывающие на связь использования талька в качестве раздражающего фактора с ростом миомы, а также на связь роста миомы с инфекционно-паразитарным заболеванием Шагаса [13]. Полученные в нашем исследовании данные о влиянии воспалительного процесса на рецидив миомы матки некоторым образом согласуются с результатами работы Э.В. Баширова c соавт. [14], в которой авторы указывают, что молекулярными механизмами развития рецидива могут быть долгая сохранность провоспалительного сдвига, ухудшение деструктивных процессов в травмированной ткани и развитие иммуносупрессии. Исследователи считают, что провоспалительный цитокиновый профиль является предиктором рецидива опухоли.
Выводы
1. По данным обращаемости в КНЦРЧ частота рецидива миомы матки, требующего повторного оперативного вмешательства, составила 10,3%.
2. Выделены 3 признака, тесно связанных с риском рецидива: ХВЗОМТ, перенесенные оперативные вмешательства на органах малого таза и артифициальные аборты в анамнезе. Площадь под ROC-кривой модели, построенной на этих признаках, AUC= 0,73 (95%-ный ДИ 0,65–0,80).
3. Установлено, что при наличии ВЗОМТ риск рецидива возрастает (p=0,01), ОШ=4,56 (95%-ный ДИ 1,3–15,6) по сравнению с отсутствием этих заболеваний. Риск рецидива повышается (p=0,05) при наличии в анамнезе оперативных вмешательств на органах малого таза ОШ=3,0 (95%-ный ДИ 1,0–9,4) по сравнению с отсутствием операций (при стандартизации по другим факторам риска).
Заключение
Необходимы дальнейшие исследования частоты возникновения и прогностических факторов рецидива миомы матки, учитывая широкое распространение органосохраняющих методов лечения на современном этапе.
Библиографическая ссылка
Третьякова Н.В., Рыскельдиева В.Т., Гурьянов В.Г. РЕЦИДИВ ЛЕЙОМИОМЫ МАТКИ У ЖЕНЩИН: ЧАСТОТА И ПРОГНОЗ // Современные проблемы науки и образования. 2018. № 5. ;URL: https://science-education.ru/en/article/view?id=28035 (дата обращения: 23.05.2026).
DOI: https://doi.org/10.17513/spno.28035



