Scientific journal
Modern problems of science and education
ISSN 2070-7428
"Перечень" ВАК
ИФ РИНЦ = 0,936
VARIABILITY OF HIV-ASSOCIATED TB IN THE EXAMPLE OF TUBERCULOMA BRAIN
Современное течение туберкулёза (ТБ) характеризуется широкой панорамой клинических и патоморфологических форм [1; 2], что отражает патоморфоз ТБ в ХХI веке [3; 4]. В наши дни патоморфозу ТБ способствуют множество факторов: биологические, экологические, эпидемиологические, медико-социальные, экономические и т.д. Особое значение придают биологическому фактору патоморфоза ТБ – ВИЧ-инфекции (ВИЧ) [5; 6]. Ко-инфекция ВИЧ и туберкулёз (ВИЧ/ТБ) поражает различные социальные слои населения, большую часть составляют социально дезадаптированные лица: без определенного места жительства, безработные, из мест лишения свободы, мигранты, страдающие алкогольной и наркотической зависимостью, в то же время они являются отягощенной группой по развитию сочетанной ко-инфекции ВИЧ/ТБ [7]. Достижение положительных результатов в лечении у дезадаптированных лиц затруднено из-за плохой приверженности как к противотуберкулезной терапии (ПТТ), так и к антиретровирусной (АРВТ). Неудачи в лечении у данной категории лиц приводят к психологическим проблемам, замыкая порочный круг, окончательно разрушая комплаентность в назначениях врача [8]. Кроме того, препараты при ПТТ и АРВТ являются очень токсичными для организма и вызывают массу побочных эффектов [9]. Одной из многих нерешенных задач в проблеме ВИЧ-ассоциированного туберкулёза является прогрессирование ТБ-процесса на фоне начала успешной антиретровирусной терапии – воспалительный синдром восстановления иммунной системы (ВСВИС) (immune reconstitution inflammatory syndrome - IRIS). Наиболее часто ВСВИС проявляется возникновением рецидивов или обострением туберкулеза на фоне АРВТ в первые 3-6 месяцев, несмотря на «положительную» возрастающую динамику восстановления CD4+ клеток и снижение вирусной нагрузки (ВН) в плазме, РНК ВИЧ, более чем на 1 log10 копий/мл [10]. Если ВСВИС возник на фоне проводимой терапии ПТП, то его называют «парадоксальным», если же ТБ возник впервые, то он является «выявляющимся или разоблачающим» синдромом восстановления иммунной системы, связанным с туберкулёзом. Частота встречаемости ВСВИС на фоне ВИЧ/ТБ ко-инфекции, по различным данным, составляет от 5 до 50% с возрастанием процента случаев при количестве CD4+ клеток < 200 кл/мкл в сочетании с высокой ВН до начала АРВТ. Кроме того, к факторам, предрасполагающим к развитию ВСВИС, относят врожденную предрасположенность и употребление психически активных веществ (ПАВ) [11].
Поражения центральной нервной системы (ЦНС) при ко-инфекции ВИЧ/ТБ остаются одними из наиболее трудно диагностируемых состояний, что объясняется чрезвычайным многообразием клинических и морфологических проявлений [12]. Клинические варианты течения сочетанных нозологий при поражении ЦНС разнообразны: от головной боли, когнитивных нарушений до развития неврологической симптоматики, что определяется морфологическими проявлениями на различных уровнях повреждения при ко-инфекции ВИЧ/ТБ [13].
Туберкулома головного мозга является редкой патологией при ко-инфекции ВИЧ/ТБ, клиническая и морфологическая картина зависит от стадии развития, может локализоваться в любом отделе ЦНС, а дифференциальный диагноз очень сложен в отношении опухолей, которые часто сопутствуют ВИЧ-инфекции.
Материалы и методы
Работа выполнялась в два этапа, с проведением медико-социального патоморфологического наблюдения. Для реализации медико-социального наблюдения произведена выборка медицинской документации больной Ч. в ГКУЗ «Волгоградский областной клинический противотуберкулезный диспансер», ГКУЗ «Волгоградский областной Центр по профилактике и борьбе со СПИД и инфекционными заболеваниями», в ФКУ «Главное бюро медико-социальной экспертизы по Волгоградской области». Патоморфологическое наблюдение осуществлялось в условиях ГБУЗ «Волгоградское областное патологоанатомическое бюро». Вскрытие проводили в ранние сроки после смерти больной (до 6 часов). Использовали макроскопическое описание и фотопротоколирование наблюдения. Образцы органов извлекали из трупа по общепринятым в патологической анатомии методикам, фиксировали в 10% растворе нейтрального забуференного формалина в течение 24-48 часов при комнатной температуре, обрабатывали по стандартной методике с дальнейшим обезвоживанием в батарее спиртов с изготовлением парафиновых блоков. Из парафиновых блоков были изготовлены гистологические срезы толщиной 3-5 мкм, окрашенные гематоксилином и эозином, по Цилю-Нильсену. Гистологические препараты изучали на световом микроскопе CarlZiess (Германия) c встроенной цифровой камерой.
Медико-социальное наблюдение
Пациентка Ч. 38 лет, по профессии кондитер, до болезни работала барменом, проживала в 3-комнатной квартире вместе с несовершеннолетней дочерью, сестрой и отцом пенсионером. Почувствовала себя плохо в декабре 2013 года: потеряла в массе более 10 кг, появился кашель и одышка. Лечилась самостоятельно, к врачам не обращалась. Резкое ухудшение состояния наступило в апреле 2014 года, нарастали симптомы интоксикации, появилась резкая слабость, недомогание, лихорадка до 40 °С, усилилась одышка и кашель. Каретой скорой медицинской помощи больная была доставлена в стационар, где при рентгенологическом исследовании был заподозрен туберкулёз легких. После консультации фтизиатра больную перевели в стационар противотуберкулёзного диспансера (ПТД) с диагнозом: диссеминированный туберкулёз лёгких в фазе распада и обсеменения. При исследовании мокроты на микобактерии туберкулёза (МБТ) микроскопическим и методом посева 3-кратно обнаружены МБТ (+). В ОАК отмечались анемия, лимфопения легкой степени, высокое СОЭ. Назначен I режим ПТТ. Больной был выполнен скрининг-тест для определения антител к ВИЧ, который впоследствии дал положительный результат. Больная была консультирована врачом-инфекционистом областного Центра по профилактике и борьбе со СПИД и инфекционными заболеваниями (ЦСПИД), установлен диагноз: ВИЧ-инфекция стадия IVБ, без приема АРВТ. При клинико-лабораторном исследовании выявлен лабораторный иммунодефицит со снижением количества CD4+ лимфоцитов до 224 кл/мкл и высокая вирусная нагрузка (ВН), больной был назначен курс АРВТ, от приема препаратов пациентка отказалась. ПТТ получала стационарно по апрель 2015 года, отмечалась положительная динамика в виде прекращения микобактериовыделения, с рассасыванием и уплотнением очагов в легких по данным рентген-исследований, затем продолжила амбулаторный курс ПТТ. В феврале 2015 года пациентка освидетельствована в специализированном по туберкулёзу бюро медико-социальной экспертизы, была установлена 2 группа инвалидности. С учётом низкого реабилитационного потенциала и сомнительного реабилитационного прогноза, больной была разработана индивидуальная программа реабилитации и абилитации инвалида (ИПРА) с рекомендациями начать прием АРВТ под контролем инфекциониста и продолжить лечение ТБ у фтизиатра, в сочетании с социальным сопровождением с учетом комплаенс-контроля. В декабре 2015 года с ухудшением общего состояния вновь госпитализирована в ПТД в тяжёлом состоянии, было начато лечение по III режиму ПТТ. В январе 2016 выявлена широкая лекарственная устойчивость МБТ с сохранением чувствительности к Pas, Cs, переведена на IV режим химиотерапии в интенсивной фазе. По настоянию врачебной комиссии ПТД, с учётом результатов клинико-лабораторных, иммунологических, вирусологических исследований, больная была консультирована инфекционистом ЦСПИД. У больной отмечено прогрессирование ВИЧ-инфекции: число CD4+ лимфоцитов снизилось до 58 кл/мкл с уменьшением иммунорегуляторного индекса CD4/CD8 до 0,09, выросла вирусная нагрузка до 454878 копий вируса. Больная начала прием АРВТ по схеме 3TC+ddI+EFV. Состояние больной улучшилось, но за постоянное нарушение больничного режима (самостоятельные уходы из стационара, прием алкоголя) в апреле 2016 года была выписана для амбулаторного долечивания. В июле 2016 года состояние больной ухудшилось, появились давящие головные боли, выраженная одышка, кашель, лихорадка до 38 °С. Больная госпитализирована в стационар ПТД, диагноз прежний, продолжала лечение по IV режиму ПТТ. В сентябре 2016 года при контроле лабораторных показателей иммунного статуса отмечено восстановление числа CD4+ до 204 кл/мкл со снижением ВН до <200 коп/мл. При консультации с инфекционистом была изменена схема приёма АРВТ на ZDV/3TC+, LPV/r. У больной выявлена неврологическая симптоматика в виде шаткости походки, нарастала интенсивность головной боли, по поводу чего выполнено нативное МРТ-исследование и с контрастным усилением. Выявлено объёмное образование округлой формы, размером 27х24х24 мм (фронтальный, сагиттальный, вертикальный), гетерогенной структуры, изоинтенсивное в Т1, гипоинтенсивное в T2 и Flair сигналах, с выраженным перифокальным отёком, локализующимся кпереди и медиально, с компрессией IV желудочка с четкими – нечеткими, неровными контурами. Из заключения: МР-картина соответствует объёмному образованию правой гемисферы мозжечка. Больная была проконсультирована нейрохирургом городской клинической больницы скорой медицинской помощи - показано хирургическое лечение. Пациентка от операции по поводу объёмного образования правой гемисферы мозжечка отказалась, продолжала лечение в стационаре ПТД. В декабре 2016 года переводилась для лечения в инфекционную больницу с диагнозом: ветряная оспа (varicella zoster). В январе 2017 года вновь поступила в стационар ПТД, состояние ухудшалось, прогрессировала мозговая симптоматика. В феврале 2017 года больная нуждалась в постоянном постороннем уходе и была признана инвалидом 1 группы. В марте 2017 года больная впала в кому, после чего наступила смерть.
Патоморфологическое наблюдение
При вскрытии черепной коробки отмечалось выраженное набухание и отёк головного мозга с дислокацией ствола в большое затылочное отверстие. Отмечалось уплощение извилин, растяжение заднего рога прозрачной жидкостью. В правой миндалине мозжечка обнаружено образование – туберкулома размером 4×3,5×3 см, серо-желтого цвета с участком деструкции (рис. 1). Микроскопически в оболочках мозга наблюдался отек, умеренное полнокровие. В веществе мозга обнаруживался перицеллюлярный отек, дистрофия нервных клеток, рассеянная инфильтрация мелкими лимфоцитами, массивные участки казеозного некроза с МБТ.
Лёгкие имели серо-синюшный цвет в результате венозного полнокровия, с белесоватыми тяжами, отмечались участки компенсаторной эмфиземы. В обоих легких обнаруживались патологические образования в виде очагов серо-желтого цвета в d от 0,5 до 2 см, четко отграниченные, с полостями деструкции до 1,5 см в d, в нижних долях выявлялась милиарная диссеминация узелками серого цвета (рис. 2). Микроскопически обнаруживались участки казеозного некроза без признаков продуктивного воспаления, что связано со сниженным T-клеточным иммунитетом при прогрессировании ВИЧ-инфекции [14], со слабой лимфоплазмоцитарной инфильтрацией, одни альвеолы были уменьшены, деформированы, другие увеличены с истонченными перегородками с наличием отечной жидкости.
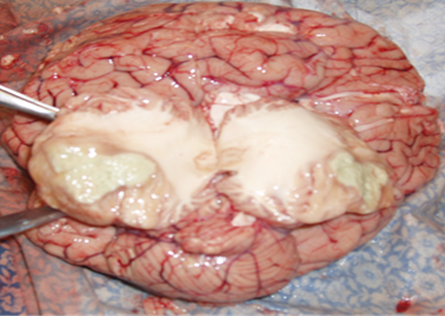
Рис. 1. Генерализованный туберкулёз, туберкулома правого полушария мозжечка, участки казеозного некроза с деструкцией. ВИЧ-инфекция стадия 4Б. Умершая Ч., 38 лет
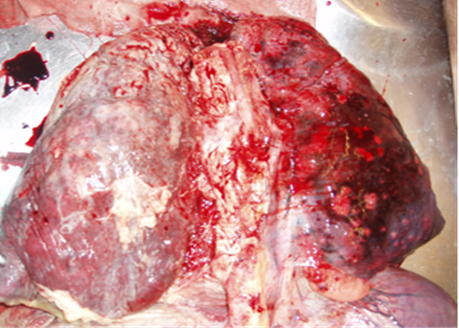
Рис. 2. Генерализованный туберкулёз, диссеминация в легких, плевральные спайки.
ВИЧ-инфекция стадия 4Б. Умершая Ч., 38 лет
Изменения в лимфатической системе носили диффузный характер с поражением внутригрудных, паратрахеальных, парааортальных лимфатических узлов. При разрезе дыхательных путей на уровне бифуркации обнаруживались увеличенные до 1,5 см бифуркационные лимфатические узлы синюшного цвета влажные, на разрезе с клиновидными серовато-желтого цвета вкраплениями. Периферические лимфатические узлы были увеличены размером 0,5-2,5 см, влажные подвижные с казеозным некрозом. Микроскопически изменения были в виде лимфоидного истощения, инволюции фолликулов, нередко обнаруживались фокусы казеозного некроза с небольшим количеством макрофагов, гигантских многоядерных клеток Пирогова-Лангханса, которые располагались эксцентрично, в центральных областях отмечалось разрастание ретикулярной фиброзной ткани (рис. 3).
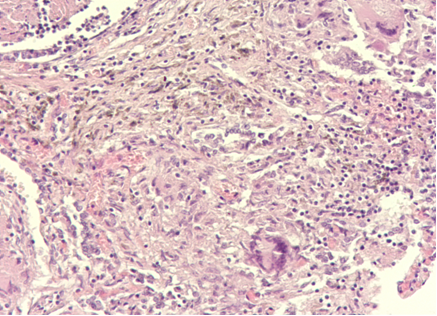
Рис. 3. Генерализованный туберкулёз, поражение периферических лимфатических узлов, участки детрита и гигантские клетки Пирогова-Лангханса. ВИЧ-инфекция стадия 4Б. Умершая Ч., 38 лет. Окраска гематоксилином и эозином. Ув. Х 400
Обсуждение полученных результатов
Выявленное в представленном клинико-морфологическом случае прогрессирование туберкулёза с генерализацией процесса на фоне ВИЧ-инфекции, с лимфогематогенной диссеминацией, с поражением легких и головного мозга, характеризует часто встречающийся исход ко-инфекции ВИЧ/ТБ, что сопоставимо с результатами вышеуказанных исследователей, занимающихся проблемой двойной инфекции. Кроме того, в нашем исследовании выявлены факторы (выраженный иммунодефицит CD4=58 кл/мкл, CD4/CD8 = 0,09, высокая вирусная нагрузка 454878 копий РНК ВИЧ до начала АРВТ; девиантное поведение с приемом алкоголя), которые, по мнению большинства исследователей, повышают вероятность развития IRIS у пациентов с выраженной иммуносупрессией на момент начала АРВТ и при приеме ПАВ, в том числе алкоголя [15].
Заключение
Таким образом, туберкулома правой гемисферы мозжечка привела к выраженному отеку и набуханию головного мозга с дислокацией ствола, что и явилось непосредственной причиной смерти пациента. Лимфогематогенная диссеминация и прогрессирование туберкулёза лёгких с поражением головного мозга при ко-инфекции ВИЧ/ТБ на фоне начала приёма АРВТ может рассматриваться как воспалительный синдромом восстановления иммунной системы с «парадоксальным» туберкулёзом. Представленный случай демонстрирует патоморфоз туберкулёза при ВИЧ-инфекции под воздействием различных факторов: биологических и медико-социальных в результате нерегулярного приёма препаратов и аддиктивного поведения больной в виде приема алкоголя.
Исследование выполнено при финансовой поддержке РФФИ и Администрации Волгоградской области, проект «Прогностическая модель медико-социальной реабилитации больных ВИЧ-инфекцией и туберкулезом (на примере Волгоградской области) № 17-16-34026.
Библиографическая ссылка
Быхалов Л.С., Туманов В.П., Соснин Д.С., Ибраимова Д.И., Зелимханов Ш.Р., Баймурзаева Г.К. ПАТОМОРФОЗ ВИЧ-АССОЦИИРОВАННОГО ТУБЕРКУЛЁЗА НА ПРИМЕРЕ ТУБЕРКУЛОМЫ ГОЛОВНОГО МОЗГА // Современные проблемы науки и образования. 2018. № 4. ;URL: https://science-education.ru/en/article/view?id=27973 (дата обращения: 13.05.2026).



